โรคต่อมธัยรอยด์ในสตรีตั้งครรภ์
รศ.พญ.สุชยา ลือวรรณ
การเปลี่ยนแปลงของการทำงานของต่อมธัยรอยด์ขณะตั้งครรภ์
การเปลี่ยนแปลงทางสรีรวิทยาในการตั้งครรภ์ปกติ มีผลทำให้การทำงานของต่อมธัยรอยด์เปลี่ยนแปลงไปมาก ที่สำคัญได้แก่ การเพิ่มขึ้นของ thyroxine binding globulin (TBG) ซึ่งเป็นผลสืบเนื่องมาจากการกระตุ้นของเอสโตรเจนที่สูงมากขึ้นระหว่างการตั้งครรภ์และมีการเปลี่ยนแปลงอื่นๆ เป็นผลตามมาอีกมาก ทั้งที่ถือว่าครรภ์ปกติอยู่สภาพธัยรอยด์ปกติ แต่ก็มีการเพิ่มขึ้นของ basal metabolic rate ขนาดของต่อมธัยรอยด์ และเพิ่มการจับไอโอดีนกัมมันตรังสี
การทำงานของต่อมธัยรอยด์ในคนตั้งครรภ์สรุปได้ดังนี้ (1)
-
- .ต่อมธัยรอยด์โตขึ้นเล็กน้อย แต่อยู่ในภาวะ euthyroid
- ระดับของ TSH มีการเปลี่ยนแปลงไม่ชัดเจน แต่ ในช่วงไตรมาสแรก TSH จะต่ำกว่าปกติ เนื่องจากฮอร์โมน hCG ที่ทำงานคล้ายคลึงกับธัยรอยด์ฮอร์โมนเพิ่มขึ้นทำให้การสร้างและหลั่ง TSH ลดลง ซึ่งจะมีผลมากในช่วงอายุครรภ์ 7-11 สัปดาห์ ค่าปกติของ TSH ในช่วงการตั้งครรภ์จะเปลี่ยนไปตามไตรมาส โดยที่ในไตรมาสแรก ค่าอยู่ระหว่าง 0.2-2.5 มิลลิยูนิต/ลิตร ในไตรมาสที่สองและเป็น 0.3-3.0 มิลลิยูนิต/ลิตร
- .TBG เพิ่มมากขึ้น ทำให้ระดับ total T3,T4 เพิ่มขึ้น ในช่วงอายุครรภ์ 4-8 สัปดาห์ แต่ free T3 และอยู่ในระดับปกติ หลัง 12-14 สัปดาห์ TBG ก็จะเพิ่มถึงระดับสูงคงที่ ซึ่ง T3,T4 ก็ขึ้นตามไปด้วยกัน
- T3 resin uptake (RT3U) ลดลงจากร้อยละ 25-35 เป็นร้อยละ 20-(คล้ายกับคนไม่ตั้งครรภ์ที่เป็นhypothyroidism สะท้อนถึงส่วน TBG ที่ยังว่างจากการถูกจับมีมากขึ้น)
- Free thyroxin index (FTI) ไม่มีการเปลี่ยนแปลงถึงแม้ TBG จะเพิ่มขึ้น
- .ต่อมจับสารไอโอดีนกัมมันตรังสีได้มากขึ้น
- .BMR ในครรภ์ปกติเพิ่มขึ้นประมาณร้อยละ 20
- T4 ผ่านรกได้น้อยแต่มีนัยสำคัญ แต่ T3 ไม่ผ่านรก
- TSH ถือว่าเป็นฮอร์โมนที่ไม่ผ่านรก
ภาวะพร่องธัยรอยด์ฮอร์โมนในสตรีตั้งครรภ์ (Hypothyroidism) (2-3)
hypothyroidism ในระหว่างการตั้งครรภ์พบได้ไม่บ่อย อุบัติการณ์ต่ำ ประมาณ 2-3 ต่อสตรีตั้งครรภ์ 1000 ราย อาจเป็นเพราะสตรีที่เป็น hypothyroidism จะมีภาวะมีบุตรยาก ซึ่งมักสัมพันธ์กับการไม่ตกไข่ สาเหตุที่พบบ่อยที่สุดของ primary hypothyroidism (พยาธิสภาพอยู่ที่ต่อมธัยรอยด์) คือ idiopathic hypothyroidism ซึ่งมีแอนติบอดีย์ต่อต่อมธัยรอยด์ ต่อมฝ่อลง ถ้าต่อมตอบสนองต่อการเพิ่ม TSH ด้วยการเกิดคอพอกเรียกว่า Harshimoto’s disease และภาวะขาดไอโอดีน สาเหตุอื่นที่พบรองลงไปคือ iatrogenic จากการผ่าตัดหรือได้รับไอโอดีนกัมมันตรังสี การใช้ยากลุ่ม amiodarone ยาต้านธัยรอยด์หรือ lithium เป็นต้น ในการดูแลรักษาจะแบ่งภาวะพร่องธัยรอยด์ออกเป็น 2 ชนิด คือ clinical หรือ overt hypothyroidism และ subclinical hypothyroidism
1 ภาวะพร่องธัยรอยด์ชนิดมีอาการ(Overt hypothyroidism, OH )
โดยมากเกิดจาก Hashimoto thyroiditis ร้อยละ 0.3-0.5 อาการที่พบบ่อยได้แก่ เหนื่อยง่าย อารมณ์ผันผวน ผิวหยาบและแห้ง ผมแห้ง เสียงแหบ น้ำหนักเพิ่ม กลืนลำบาก ขี้หนาว เบื่ออาหาร ท้องผูก วินิจฉัย ได้โดยการตรวจระดับ thyrotropin จะเพิ่มสูง (TSH>2.5 มิลลิยูนิต/ลิตร)และ thyroxin (FT4) ต่ำผิดปกติ การตรวจ thyroid autoantibodies titer ได้แก่ แอนติบอดีย์ ของ thyroid peroxidase (TPO) และ thyroglobulin (TG) (TPOAb and TGAb) จะช่วยยืนยันสาเหตุที่เกิดจาก autoimmune
2. ภาวะพร่องธัยรอยด์ไม่มีอาการ หรือ แอบแฝง (subclinical hypothyroidism, SCH)
พบได้ร้อยละ 1.5-4 วินิจฉัย จากระดับ TSH สูงแต่ FT4 ปกติ พบบ่อยขึ้นในรายเบาหวาน type I ทั้งที่ฮอร์โมนธัยรอยด์ก่อนการตั้งครรภ์ปกติ
ผลของการตั้งครรภ์ต่อโรค
โดยทั่วไปแล้วการตั้งครรภ์ไม่มีผลต่อการดำเนินโรค แต่อย่างไรก็ตามรายที่เป็น euthyroid แต่มีแอนติบอดีย์ต่อธัยรอยด์จะปรากฏอาการพร่องธัยรอยด์ชัดเจนได้ถึงร้อยละ 40
ผลของโรคต่อการตั้งครรภ์
พบภาวะแท้งได้ถึง ร้อยละ 60 ส่วนภาวะแทรกซ้อนทางสูติกรรมอื่น ๆ เช่น ความดันโลหิตสูงระหว่างตั้งครรภ์ รกลอกตัวก่อนกำหนด หรือ ตกเลือดหลังคลอด ก็อาจเกิดขึ้นได้ ทารกในครรภ์ จะ เพิ่มความเสี่ยงต่อการคลอดก่อนกำหนด ทารกน้ำหนักน้อย รวมถึงทารกตายคลอด ด้านสติปัญญา พบว่า ระดับความสามารถทางสติปัญญา (IQ) น้อยกว่าเด็กทั่วไป มีโอกาสเกิดปัญหาด้านพัฒนาการเรียนรู้สูงถึง 3 เท่า
Isolated Maternal Hypothyroxinemia
คือ ภาวะที่ ระดับ FT4 ต่ำ แต่ TSH ปกติ พบได้ ร้อยละ 1.3 ของสตรีตั้งครรภ์ จากรายงานของ Casey (2007) พบว่าภาวะนี้ไม่ส่งผลกระทบต่อการตั้งครรภ์และทารกในครรภ์ และไม่จำเป็นต้องตรวจคัดกรองในสตรีตั้งครรภ์
สรุปหลักการรักษา hypothyroidism ในสตรีตั้งครรภ์ อ้างอิงจาก The American Thyroid Association ปี 2011(3)
- ในรายที่เป็น Overt hypothyroidism หรือระดับ TSH สูงกว่าค่าปกติในแต่ละช่วงอายุครรภ์ และระดับ FT4 ต่ำกว่าปกติ หรือ TSH มากกว่า 10 มิลลิยูนิต/ลิตรเพียงอย่างเดียว และ Subclinical hypothyroidism ที่มี แอนติบอดีย์ต่อ Thyroid peroxidase(TPOAb) ควรจะให้การรักษาระหว่างการตั้งครรภ์ แต่ในรายที่ไม่มี TPOAb ยังไม่มีหลักฐานสนับสนุนเพียงพอถึงความจำเป็นในการรักษา
- ในรายที่เป็น Isolated hypothyroxinemia ไม่จำเป็นต้องรักษา
- ในรายที่มี TPOAb โดยที่ระดับฮอร์โมนปกติ และไม่ได้รับยา ควรตรวจติดตามระดับ TSH เฝ้าระวังการเกิด hypothyroidism
- ยาที่ใช้รักษาอยู่ในรูปแบบรับประทาน คือ levothyroxine(LT4) และไม่แนะนำให้ใช้ รูปแบบอื่น เช่น T3 หรือ desiccated thyroid
- SCH ที่ไม่ได้รับการรักษาระหว่างการตั้งครรภ์ ควรมีการตรวจติดตามระดับ TSH และ FT4 เป็นระยะ
เป้าหมายในการรักษา
ควบคุมให้ระดับ TSH อยู่ในเกณฑ์ดังนี้(4)
- ไตรมาสแรก 0.1-2.5 มิลลิยูนิต/ลิตร
- ไตรมาสที่สอง 0.2-3.0 มิลลิยูนิต/ลิตร
- ไตรมาสที่สาม 0.3-3.0 มิลลิยูนิต/ลิตร
การตรวจติดตาม
ตรวจวัดระดับ TSH และ FT4 ทุก 4 สัปดาห์ในช่วงครึ่งแรกของการตั้งครรภ์ จนกระทั่งถึง 16-20 สัปดาห์ และควรตรวจซ้ำอย่างน้อยหนึ่งครั้ง ในช่วง 26-32 สัปดาห์
- ในรายที่ได้รับการรักษามาตั้งแต่ก่อนตั้งครรภ์ ควรปรับเพิ่มขนาดยา LT4 ขึ้นอีกร้อยละ 25-30 ทันทีที่ทราบว่าตั้งครรภ์ เพราะร่างกายต้องการ T4 เพิ่มขึ้นเรื่อย ๆ ตั้งแต่ช่วงอายุครรภ์ 4-6 สัปดาห์ ไปจนถึง 16-20 สัปดาห์
- ก่อนตั้งครรภ์ควรควบคุมระดับ TSH ให้น้อยกว่า 2.5 มิลลิยูนิต/ลิตร
- หลังคลอด ควรปรับลดระดับยาลงมาให้ใกล้เคียงช่วงก่อนตั้งครรภ์ และตรวจวัดระดับ TSH ซ้ำหลังคลอด 6 สัปดาห์
- Hypothyroidism ที่ได้รับการรักษาและตรวจติดตามระดับ TSH และ FT4 อย่างเหมาะสมในระหว่างการตั้งครรภ์ ไม่จำเป็นต้องตรวจพิเศษอย่างอื่นๆ เพิ่มเติมทั้งในมารดาและทารกในครรภ์ ( เช่น ตรวจอัลตราซาวด์ประเมินทารกในครรภ์ ตรวจสุขภาพทารกในครรภ์ ด้วย nonstress test เป็นต้น)
- มีการศึกษา RCT เกี่ยวกับการให้ selenium เพื่อป้องกัน การเกิด postpartum thyroiditis ปัจจุบัน ยังไม่แนะนำให้ใช้ selenium ในสตรีตั้งครรภ์ ที่มี TPOAb + เนื่องจากยังไม่มีการศึกษาที่สนับสนุนเพียงพอถึงประโยชน์ของการรักษา
อนึ่งคอพอกธรรมดาในสตรีตั้งครรภ์ที่ไม่มีปัญหาฮอร์โมนบกพร่อง ไม่มีผลต่อการดำเนินการตั้งครรภ์ nodule เดี่ยวๆของต่อมธัยรอยด์ในคนอายุน้อยก็อาจเป็นมะเร็งได้ (ส่วนใหญ่เป็นมะเร็ง low grade ชนิด papillary หรือ follicular) ในสตรีที่ไม่ตั้งครรภ์จะทดสอบโดยการให้ไอโอดีนกัมมันตรังสี ถ้าเป็น nonfunctioning (cold) มีโอกาสเป็นมะเร็งสูงกว่า ในสตรีตั้งครรภ์ทดสอบได้โดยให้ T4 ขนาดสูงเพื่อลดขนาดของ nodule ถ้าลดขนาดได้ ให้ T4 ไปตลอดการตั้งครรภ์ ถ้าขนาดไม่ลดลงควรผ่าตัด
การให้ไอโอดีนเสริมในครรภ์ปกติ(3)
ในสตรีตั้งครรภ์และหลังคลอด จะมีความต้องการไอโอดีนเพิ่มขึ้นเนื่องจาก ระหว่างการตั้งครรภ์มีการสร้างธัยรอยด์ฮอร์โมนเพิ่มมากขึ้น การขับไอโอดีนออกทางไตเพิ่ม และต้องแบ่งให้ทารกในครรภ์ ส่วนหลังคลอด ทารกจะได้ไอโอดีนผ่านทางน้ำนมแม่ ถ้าขาดไอโอดีนย่างรุนแรง มีผลให้สร้างธัยรอยด์ฮอร์โมนลดลง เกิดคอพอกในมารดาและทารก และเพิ่มอัตราการแท้ง ทารกตายคลอดและภาวะทุพพลภาพของทารกในครรภ์ การขาดธัยรอยด์ในช่วงเดือนที่ 3-4 ของการตั้งครรภ์จะมีผลกระทบกับการพัฒนาของระบบประสาท และสติปัญญาของทารกหลังคลอด และทำให้เกิดภาวะพร่องธัยรอยด์โดยกำเนิด (congenital hypothyroidism) ทารกปัญญาอ่อน เป็นใบ้หูหนวก ได้ หลาย ๆ องค์กรจึงแนะนำให้เสริมไอโอดีนในสตรีตั้งครรภ์ ทั้งนี้
- WHO (2007) ได้กำหนดว่าในสตรีตั้งครรภ์ได้รับไอโอดีน ในปริมาณที่เหมาะสมจะมีค่าไอโอดีนในปัสสาวะ อยู่ระหว่าง 149-249 มคก./ล.
- The American Thyroid Association (2011) แนะนำให้สตรีตั้งครรภ์และให้นมบุตรควรได้รับไอโอดีนเสริม 250 มคก./วัน โดยได้รับจากอาหารที่รับประทาน ร่วมกับยาเสริมไอโอดีนในรูปของ potassium iodide ขนาด 150 มคก./วัน หรือในรูปของเกลือไอโอดีน
ในประทศไทย สถาบันวิจัยระบบสาธารณสุข (สวรส.) ได้สำรวจข้อมูลพบว่า โรคขาดสารไอโอดีน (Iodine Deficiency Disorder-IDD) ของไทยมีแนวโน้มเป็นปัญหามากขึ้น จากการสำรวจไอโอดีนในกลุ่มหญิงตั้งครรภ์เมื่อ พ.ศ.2552พบว่าร้อยละ 59 มีปัญหาการขาดสารไอโอดีน มีระดับไอโอดีนในปัสสาวะต่ำกว่า 150 มคก/ล. และจากการสำรวจระดับไอคิวของกลุ่มเด็ก 6000 คน จาก21 จังหวัดปี พ.ศ.2552 พบว่ามีไอคิวเฉลี่ย 91 จุด ซึ่งค่อนข้างต่ำเมื่อเทียบกับมาตรฐานไอคิวเฉลี่ยของสากลคือ 90-110 จุด องค์การเภสัชกรรมของประเทศไทย ได้ผลิตยาเสริมไอโอดีน ซึ่งมี 2 สูตรดังนี้
- TRIFERDINE 150 (ยาเม็ดผสมประกอบด้วย Iodine 0.15 มก.+Ferrous fumarate 185 มก. +Folic acid 0.4 มก.) ให้กินวันละ 1 เม็ด ตลอดการตั้งครรภ์และขณะเลี้ยงลูกด้วยนม
- Iodine GPO (Iodine เดี่ยว ขนาด 0.15 มก.) สำหรับหญิงตั้งครรภ์ที่เป็น Thalassemia ซึ่งมีข้อจำกัดเรื่องการได้รับธาตุเหล็ก ให้กินวันละ 1 เม็ด
คอพอกเป็นพิษในสตรีตั้งครรภ์ (Thyrotoxicosis) (3-6)
คอพอกเป็นพิษในสตรีตั้งครรภ์พบได้ราว 1:1000-1:2000 สถิติของโรงพยาบาลมหาราชนครเชียงใหม่ในปี 2553 พบโรคคอพอกเป็นพิษในสตรีตั้งครรภ์ร้อยละ 1.1 ของการคลอด สาเหตุของคอพอกเป็นพิษขณะตั้งครรภ์ ได้แก่ Graves’ disease เป็นสาเหตุที่พบได้บ่อยที่สุด เป็นโรคออโตอิมมูน thyroid stimulating immunoglobulin (TSI) เป็นแอนติบอดีย์จับกับ receptor ของ TSH และกระตุ้นต่อมธัยรอยด์ให้สังเคราะห์และหลั่งฮอร์โมน เพิ่มขึ้นและทำให้เกิดอาการของคอพอกเป็นพิษ ส่วน Plummer’s disease ในวัยเจริญพันธุ์ พบได้ค่อนข้างน้อยเพราะเกิดขึ้นใน nodular goiter ที่เป็นมายาวนาน สาเหตุอื่น ๆ เช่น การตั้งครรภ์แฝด ครรภ์ไข่ปลาอุก หรือมะเร็งเนื้อรก คอพอกเป็นพิษอาจเกิดจากการตั้งครรภ์เอง เรียกว่า Gestational hyperthyroidism หรือ Transient hyperthyroidism เกิดในช่วงแรกของการตั้งครรภ์ ระดับของ FT4 สูงอย่างเดียว โดยที่ TSH จะต่ำมาก โดยไม่ได้เกิดจาก autoimmunity พบได้ ร้อยละ 1-3 ของสตรีตั้งครรภ์ สัมพันธ์กับระดับของ hCG ที่สูงขึ้นระหว่างการตั้งครรภ์ อาจพบร่วมกับ hyeremesis gravidarum ซึ่งจะมีอาการคลื่นไส้ อาเจียนอย่างรุนแรง มากกว่าร้อยละ 5 จะมี น้ำหนักลด ขาดสารน้ำ และมีคีโตนในปัสสาวะ(ketonuria)
การวินิจฉัยคอพอกเป็นพิษระหว่างการตั้งครรภ์
การวินิจฉัยอาจยากขึ้นเพราะสตรีตั้งครรภ์ปกติอาจมีอาการและอาการแสดงแบบคอพอกเป็นพิษที่ไม่รุนแรงได้ หรือ Gestational hyperthyroidism เช่น
- การเพิ่มการไหลเวียนของเลือดบริเวณผิวหนังในระหว่างการตั้งครรภ์ ทำให้ทนร้อนไม่ค่อยได้ ผิวหนังอุ่น
- ชีพจรเร็วขึ้นเล็กน้อยในระหว่างครรภ์ปกติ
- การเปลี่ยนแปลงผลการทดสอบการทำงานของต่อมธัยรอยด์ ในครรภ์ปกติมีระดับธัยรอยด์ฮอร์โมนเพิ่มขึ้น, ต่อมจับไอโอดีนกัมมันตรังสีเพิ่มขึ้น
อาการแสดงของคอพอกเป็นพิษ เช่น น้ำหนักลด อาจถูกบดบังไว้ด้วยการเพิ่มน้ำหนักของการตั้งครรภ์ การเปลี่ยนแปลงทางตาของ Graves’ disease หรือ pretibial myxedema อาจช่วยได้ แต่อาจไม่จำเพาะต่อคอพอกเป็นพิษเสมอไป อาการแสดงที่ช่วยในการวินิจฉัยคอพอกเป็นพิษระหว่างการตั้งครรภ์ที่เกิดจาก Grave’s disease ออกจาก Gestational hyperthyroidism ได้แก่
- ชีพจรเร็วมากกว่าครรภ์ปกติ ชีพจรขณะพักมากกว่า 100 ครั้ง/นาทีหรือชีพจรเร็วขณะหลับ
- การมี onycholysis หรือปลายเล็บยกแยกขึ้นจากฐาน ตาโปน ต่อมธัยรอยด์โต (ครรภ์ปกติก็อาจโตได้บ้าง) ช่วยสนับสนุนคอพอกเป็นพิษ
- ไม่สามารถเพิ่มน้ำหนักได้อย่างครรภ์ปกติ
การตรวจการทำงานของต่อมธัยรอยด์
TSH < 0.1 มิลลิยูนิต/ลิตร และระดับ FT4 > 15 มค./ดล. บ่งชี้ว่าเป็นคอพอกเป็นพิษ หรือถ้าเป็น T3 thyrotoxicosis ผู้ป่วยจะมีคอพอก แต่เมื่อตรวจ FT4 แล้วปกติให้นึกถึงภาวะนี้ ในผู้ป่วยที่ไม่ขาด TBG เมื่อตรวจพบ RT3U ระหว่างตั้งครรภ์อยู่ในเกณฑ์ปกติของคนไม่ตั้งครรภ์ ก็บ่งชี้ว่าเป็นคอพอกเป็นพิษ free thyroxin index(FTI) ก็พอจะนำมาช่วยวินิจฉัยคอพอกเป็นพิษระหว่างการตั้งครรภ์ได้ อย่างไรก็ตามการเพิ่มของ TBG ระหว่างการตั้งครรภ์ ทำให้ค่า FTI ไม่แน่นอนนัก ไม่ถูกต้องเหมือนค่า FT4 จริงๆ การตรวจหา FT4 หรือ FT3 ให้การวินิจฉัยที่แน่นอนแต่เทคนิคการตรวจยุ่งยากกว่า
ผลของการตั้งครรภ์ต่อคอพอกเป็นพิษ
- การดำเนินโรคของคอพอกเป็นพิษระหว่างการตั้งครรภ์และหลังคลอดมีความสัมพันธ์กับการเปลี่ยนแปลงของระบบภูมิคุ้มกันของร่างกายระหว่างการตั้งครรภ์ ในระยะแรกของการตั้งครรภ์โรคอาจมีการกำเริบได้ แต่เมื่ออายุครรภ์มากขึ้นการดำเนินโรคมีแนวโน้มดีขึ้น น้อยมากที่จะมีอาการเลวลงขณะที่อายุครรภ์มากขึ้น มีรายงานว่าสามารถหยุดยาต้านธัยรอยด์ได้ในไตรมาสที่สามได้ถึงร้อยละ 40 แต่ในระยะหลังคลอดจะมีโอกาสโรคกำเริบสูงขึ้นชัดเจน มีหลักฐานบ่งชี้ว่าการตั้งครรภ์มีการกดระบบภูมิคุ้มกัน ทำให้ TSI ลดลงและอาการของโรคดีขึ้นหรือสงบลงระหว่างตั้งครรภ์
- การตั้งครรภ์ ทำให้การวินิจฉัยยากขึ้นเพราะค่าการทดสอบต่างๆของต่อมธัยรอยด์เปลี่ยนแปลงไป
- การตั้งครรภ์ส่งเสริมทำให้เกิดหัวใจล้มเหลวมากขึ้นในกลุ่มที่ควบคุมโรคไม่ดี หัวใจล้มเหลวเกิดจากผลระยะยาวของฮอร์โมนธัยรอยด์ต่อหัวใจ ซึ่งจะถูกซ้ำเติมด้วยความดันโลหิตสูงจากการตั้งครรภ์ ติดเชื้อ ซีด
ผลของโรคต่อการตั้งครรภ์
อาจมีผลทำให้เพิ่มอัตราเสี่ยงต่อภาวะความดันโลหิตสูงจากการตั้งครรภ์ถึงร้อยละ 11-17 ภาวะหัวใจวาย จนถึงเสียชีวิต ผลต่อทารกในครรภ์ จะเพิ่มความเสี่ยงต่อการคลอดก่อนกำหนด ทารกโตช้าในครรภ์ ทารกเสียชีวิตในครรภ์ และทารกน้ำหนักน้อยได้ในกลุ่มที่ควบคุมโรคได้ไม่ดี(8) ในรายที่ควบคุมได้ทารกในครรภ์ก็มีความเสี่ยงที่จะเกิดภาวะ thyrotoxicosis hypothyroidism หรือ goiter ได้
ผลกระทบต่อทารกในครรภ์หลังการรักษา ขึ้นกับ
- การควบคุมภาวะ hyperthyroidism ถ้าคุมไม่ได้ อาจทำให้เกิด transient centeral hypothyroidism
- การรักษาด้วยยาต้านธัยรอยด์ปริมาณมาก จะผ่านรกไปมีผลกดการทำงานของต่อมธัยรอยด์ทำให้เกิด fetal และ neonatal goitrous hypothyroidism
- ระดับ TSH receptor antibody (TRAb) ที่สูงมากในแม่ที่เป็น Grave’s disease จะผ่านรกไปกระตุ้นให้เกิด fetal และ neonatal goitrous hyperthyroidism ในรายที่รุนแรงอาจเกิดภาวะบวมน้ำ(hydrops)และทารกเสียชีวิตได้
- ในรายที่เคยได้ ไอโอดีนกัมมันตรังสี ทารกในครรภ์ยังมีความเสี่ยงต่อการเกิด fetal thyrotoxicosis ได้ จาก thyroid-stimulating antibodies ที่ผ่านทางรก(9)
การดูแลรักษา(3,7)
มารดาที่มีคอพอกเป็นพิษทุกรายควรได้รับการควบคุมให้อยู่ในสภาพธัยรอยด์ปกติ เนื่องจากคอพอกเป็นพิษมีผลเสียทั้งต่อมารดาและทารก โดยทั่วไปแนะนำว่าการควบคุมที่ดีควรให้อยู่ในภาวะ Hyperthyroid เล็กน้อย (ชีพจร 100-110 ครั้ง/นาที) ซึ่งถือว่าควบคุมโรคได้โดยใช้ยาต้านธัยรอยด์น้อยที่สุด
Gestational hyperthyroidism
การรักษาขึ้นกับความรุนแรงของโรค ในรายที่มี อาการแพ้ท้องอย่างรุนแรง(Hyperemesis gravidarum) ให้รักษาตามอาการ จากภาวะขาดน้ำ หรือความไม่สมดุลของเกลือแร่ต่าง ๆ แต่ไม่แนะนำให้ใช้ยาต้านธัยรอยด์ เพราะระดับ T4 จะกลับมาสู่ระดับปกติในช่วง 14-18 สัปดาห์
Grave’s disease
- ก่อนการตั้งครรภ์ ควรรักษาให้อยู่ในภาวะ euthyroid อาจรักษาด้วย ยาต้านธัยรอยด์หรือ ไอโอดีนกัมมันตรังสี หรือ ผ่าตัดรักษา
- ถ้ารักษาด้วย ไอโอดีนกัมมันตรังสี ควรคุมกำเนิดไว้อย่างน้อย 4 เดือนหลังการรักษา
- ในระหว่างการตั้งครรภ์ ไม่ควรรักษาด้วยไอโอดีนกัมมันตรังสี เพราะมีผลทำลายต่อมธัยรอยด์ทารก โดยเฉพาะในช่วงหลัง thyroid organogenesis คืออายุครรภ์ 10-11 สัปดาห์ แต่ถ้าก่อนหน้านั้น ไม่ค่อยมีผลต่อต่อมธัยรอยด์
- การผ่าตัดควรพิจารณาเฉพาะรายที่รักษาด้วยยาไม่ได้ผล
- การรักษาด้วยยาต้านธัยรอยด์: เป็นวิธีหลักของการรักษาคอพอกเป็นพิษ ยาต้านธัยรอยด์ที่ใช้กันส่วนมากเป็น thioamides ซึ่งออกฤทธิ์ยับยั้งการสังเคราะห์ธัยรอยด์ฮอร์โมน โดยการยับยั้ง iodine ของ tyrosine molecules ยับยั้งการสังเคราะห์แต่ไม่ยับยั้งการหลั่ง การตอบสนองต่อการรักษาด้วย thioamides จึงยังไม่เกิดขึ้นจนกว่าธัยรอยด์ฮอร์โมนที่สะสมไว้ใน colloid จะถูกใช้ไปก่อน การควบคุมจึงต้องใช้เวลาบ้างกว่าจะเห็นผล ขึ้นอยู่กับปริมาณการเก็บสะสมของฮอร์โมน โดยทั่วไปแล้ว อาการทางคลินิกมักจะดีขึ้นใน 1 สัปดาห์หลังเริ่มรักษา และเข้าสู่ภาวะ euthyroidism หลังเริ่มรักษา 5-8 สัปดาห์ ยาที่ใช้ได้แก่
Propylthiouracil (PTU)
เป็นยาต้านธัยรอยด์ที่นิยมใช้กันอย่างแพร่หลาย ผ่านรกร้อย ไม่มีรายงานของ embryopathy ต่างจาก methimazole(MMI) PTU มีข้อดีเหนือกว่า methimazole ในแง่ของการออกฤทธิ์คือ PTU ยังมีฤทธิ์ยับยั้งการเปลี่ยน T4 ไปเป็น T3ได้บางส่วน แต่ในปี 2009 FDA ของ สหรัฐอเมริกา ได้รายงานการเกิดพิษต่อตับ (hepatotoxicity) หลังจากใช้ PTU จึงมีการควบคุมการใช้ยาตัวนี้ระหว่างการตั้งครรภ์ ภาวะแทรกซ้อนอื่น ๆ ได้แก่ ผื่นแดงเล็กน้อย คัน หรือเป็น purpura พบได้ร้อยละ 3-5 อาจมีไข้เนื่องจากยา, คลื่นไส้ ซึ่งเกิดขึ้นได้ประมาณร้อยละ 2 ของผู้ที่ได้รับ PTU ฤทธิ์ข้างเคียงที่ไม่รุนแรงเหล่านี้มีแนวโน้มที่จะเกิดภายใน 4 สัปดาห์ของการรักษา ขนาดที่ใช้รักษา คือ 100-450 มก./วัน แบ่งให้ 3 เวลา
Methimazole (MMI)
ผ่านรกได้มากกว่า PTU มีความสัมพันธ์กับการเกิด aplasia cutis ในทารกด้วย และทำให้เกิดความพิการแต่กำเนิดอื่น ๆ เรียกว่า “MMI embryopathy” ซึ่งอาจพบ choanal หรือ esophageal atresia หรือ dysmothic facies ขนาดที่ใช้รักษา คือ 10-20 มก./วัน ให้วันละ 1 ครั้ง
ในกลุ่ม Thioamide อาจเกิด agranulocytosis ได้ร้อยละ 0.2 มักเกิดหลังรักษาไปได้ 4-8 สัปดาห์ จะต้องหยุดยา thioamide ทันที รายที่รุนแรงขั้นชีวิตพบได้น้อยกว่า 1:10,000 ก่อนที่จะเริ่มต้นการรักษาควรตรวจนับ leukocytes ก่อนเพราะร้อยละ 10 ของ Graves’ disease เป็น leukopenia อยู่ก่อนแล้ว การตรวจเม็ดเลือดขาวสัปดาห์ละครั้งระหว่างการรักษานี้ก็อาจไม่มีประโยชน์ เพราะเม็ดเลือดขาวอาจลดเร็วมาก
Propranolol
เป็น beta blocker ช่วยลดชีพจร แต่ไม่ลดฮอร์โมน เห็นผลเร็วกว่า PTU โดยเริ่มให้ปริมาณ 20-40 มก.ทุก 6-8 ชั่วโมง แต่อย่างไรก็ตามการใช้ยานี้เป็นเวลานาน อาจทำให้รกมีขนาดเล็ก ทารกโตช้าในครรภ์ ทนต่อการขาดออกซิเจนได้ไม่ดี และอาจทำให้ทารกแรกคลอดมีชีพจรช้า และน้ำตาลในเลือดต่ำ ใช้ควบคุมคอพอกเป็นพิษที่ต้องการเห็นผลเร็ว ก็มักต้องใช้ร่วมกันระหว่าง propranolol 40 มก.ทุก 6 ชั่วโมง กับ iodide ซึ่งยับยั้งการ หลั่งธัยรอยด์ฮอร์โมนซึ่งมักจะดีขึ้นใน 2-7 วัน iodide ออกฤทธิ์ยับยั้งการหลั่งและยับยั้งการ uptake ของ iodide เข้าสู่ต่อมธัยรอยด์อย่างเฉียบพลัน แต่ iodide มีผลเช่นเดียวกันนี้ต่อการทำงานของต่อมธัยรอยด์ทารกด้วย
สรุปการรักษา Grave’s disease ระหว่างการตั้งครรภ์ อ้างอิงจาก The American Thyroid Association ปี 2011 (3)
- ในรายที่ได้รับยาต้านธัยรอยด์ ให้รักษาด้วย PTU ในไตรมาสแรก หลังจากนั้นให้เปลี่ยนเป็น MMI ตลอดการตั้งครรภ์ ในช่วงที่ได้รับ PTU ควรตรวจติดตามการทำงานของตับเป็นระยะ
- ไม่แนะนำให้ใช้ PTU เพราะอาจเกิดพิษต่อตับได้ตลอดการตั้งครรภ์ อนุโลมให้ใช้ กรณีแพ้ MMI หรือ มีภาวะ thyroid storm
- ขนาดของยา ควรเริ่มด้วย PTU 50-300 มก./วัน หรือ MMI 5-15 มก./วัน
เป้าหมายการรักษา ให้ระดับ FT4 อยู่ระดับปกติหรือสูงกว่าเล็กน้อย
การตรวจติดตาม เจาะ FT4 และ TSH ทุก 2-4 สัปดาห์ในช่วงแรก หลังจากปรับยาได้ ให้ตรวจติดตาม ทุก4-6 สัปดาห์
- ไม่ควรให้ ยาต้านธัยรอยด์ ร่วมกับ LT4 เพราะจะทำให้เกิด fetal hypothyroidism จะมีที่ใช้ในกรณีที่มี fetal hyperthyroidism
- ตรวจหา TRAb ในช่วงอายุครรภ์ 20-24 สัปดาห์ ในรายที่เคยเป็นหรือกำลังเป็น Grave’s disease
- เฝ้าระวังภาวะแทรกซ้อนต่อทารกในครรภ์ โดยการตรวจอัลตราซาวด์ ร่วมกับการตรวจสุขภาพทารกในครรภ์(NST)ในรายที่ไม่สามารถควบคุมโรคได้ หรือ มีค่า TRAb สูงเกินกว่าค่าปกติ 3 เท่า เพื่อดูอัตราการเจริญเติบโต การเต้นของหัวใจ ปริมาณน้ำคร่ำ และคอพอกในทารก
- ถ้ามีลักษณะอาการที่บ่งชี้ว่าเป็น fetal hyperthyroidism จากการตรวจคลื่นเสียงความถี่สูงคือ หัวใจเต้นเร็วมากกว่า 170 ครั้งต่อนาที นานมากกว่า 10 นาที มีภาวะทารกโตช้าในครรภ์ มีก้อนที่คอทารก สงสัยคอพอก มีการเจริญเติบโตของอายุกระดูกมากกว่าปกติ อาการแสดงของภาวะหัวใจล้มเหลว หรือบวมน้ำ ควรตรวจวินิจฉัยทารกในครรภ์โดยการเจาะเลือดสายสะดือ (umbilical blood sampling) และให้การรักษาด้วยยาต้านธัยรอยด์ผ่านทางมารดา
ภาวะหลังคลอด
ตรวจติดตามฮอร์โมนธัยรอยด์เป็นระยะตั้งแต่ 6 สัปดาห์หลังคลอด เฝ้าระวัง Grave’s disease กำเริบ โดยต้องแยกกับ ระยะ hyperthyroid ใน postpartum thyroiditis
สามารถให้นมบุตรได้ ในมารดาที่ใช้ thioamides ปริมาณไม่สูง คือ MMI 20–30 มก./วัน และอาจให้ PTU ไม่เกิน 300 มก./วัน เสริมในรายที่ควบคุมยาก
การคุมกำเนิด วิธีไหนก็ได้ แต่ถ้าใช้ยาเม็ดคุมกำเนิดชนิดฮอร์โมนรวม เอสโตรเจนอาจมีผลรบกวนทดสอบการทำงานของต่อมธัยรอยด์คล้ายขณะตั้งครรภ์ จึงต้องระมัดระวังในการแปลผล
ภาวะธัยรอยด์วิกฤต (thyroid storm)
พบได้ร้อยละ 2 ของคอพอกเป็นพิษในคนตั้งครรภ์ เป็นอันตรายขั้นชีวิต มักเกิดขึ้นในรายคอพอกเป็นพิษที่ถูกละเลย หรือได้รับการรักษาไม่เพียงพอ และมีปัจจัยกระตุ้นเช่นการคลอด การผ่าตัดทำคลอดทางหน้าท้อง การติดเชื้อ อาจมีอาการไข้สูง (เช่น 106 ‘F) ชีพจรเร็ว อ่อนเพลียหมดแรง มีภาวะขาดน้ำรุนแรง อันตรายขั้นชีวิตประมาณร้อยละ 25 ทั้งๆ ที่ให้การรักษาอย่างดี แนวทางในการดูแลรักษามีดังนี้
- ดูแลรักษาในหอผู้ป่วยหนัก
- ให้สารน้ำอย่างเพียงพอ (5 ลิตร) และแก้ความสมดุลย์ของอีเลคโตรลัยท์
- ลดไข้ เช่น อาจให้ acetaminophen หลีกเลี่ยงการให้ salicylate เพราะจะไล่ฮอร์โมนธัยรอยด์จากโปรตีนในพลาสมา
- 4.ยับยั้งการสังเคราะห์ฮอร์โมนและยับยั้ง deiodination ของ T4 ไปเป็น T3 โดยรับประทานPTU 600-800 มิลลิกรัม ตามด้วย 150-200 มก.ทุก 4-6 ชั่วโมง ถ้ากินไม่ได้ให้ methimazole เหน็บทางทวาร
- ยับยั้งการปล่อย T3,T4 จากต่อมธัยรอยด์ โดยรับประทาน
- Supersaturated solution of potassium iodide (SSKI) 2-5 หยด ทุก 8 ชม. หรือ
- Sodium iodide 0.5-1.0 กรัม ทางหลอดเลือดดำ ทุก 8 ชม. หรือ
- Lugol 10 หยดทุก 8 ชม. ถ้ามีประวัติแพ้ไอโอดีน ให้ lithium carbonate 300 มก.ทุก 6 ชม.แทนไอโอไดด์
- ยับยั้งการเปลี่ยน ไปเป็น T3 โดย dexamethasone 2 มก. ทางหลอดเลือดดำ ทุก 6 ชม. 4 ครั้ง
- ควบคุม beta-adrenergicโดย propranolol (หรือ esmolol) รับประทาน 40 มก. ทุก 6 ชั่วโมง ถ้าจำเป็นก็สามารถให้ยาโดยการฉีด 1-2 มก. ทางหลอดเลือดดำทุก 5 นาที จนครบ 6 มก. จึงให้ต่อ 1-10 มก. ทุก 4 ชม.
- ขจัดปัจจัยกระตุ้น เช่น ลดความดันโลหิตสูงรุนแรง รักษาการติดเชื้อ และภาวะโลหิตจาง ในรายที่กระวนกระวายพักไม่ได้ ให้รับประทาน phenobarbital 30-60 มก. ทุก 6-8 ชม. ได้
ธัยรอยด์อักเสบหลังคลอด (postpartum thyroiditis)(10,11)
การกดภูมิคุ้มกันวิทยาระหว่างการตั้งครรภ์ อาจมีอิทธิพลต่อการดำเนินโรคออโตอิมมูนของต่อมธัยรอยด์ที่สงบอยู่ตลอดการตั้งครรภ์และเกิดอาการในระยะหลังคลอด ทั้งที่ไม่เคยมีอาการมาก่อนการตั้งครรภ์ ธัยรอยด์อักเสบหลังคลอด ซึ่งมี destructive lymphocytic thyroiditis การขาดไอโอดีนก็มีส่วนเกี่ยวข้องด้วย พบได้ถึงร้อยละ 5-10 ในรายที่ระดับธัยรอยด์ฮอร์โมนปกติในไตรมาสแรกแต่มี thyroid autoantibodies จะเกิด postpartum thyroiditis ได้ถึงร้อยละ 50 และอาจพบได้ถึงร้อยละ 25 ของรายที่เป็นเบาหวาน type I ซึ่งมีได้ทั้ง hyperthyroidism หรือ hypothyroidism อาการจะคล้ายคลึงกับภาวะซึมเศร้าหลังคลอด ซึ่งแบ่งเป็น 2 ระยะ
- ระยะ thyrotoxicosisthyroid microsomal autoantibodies ได้ร้อยละ 7-10 พบบ่อยขึ้นในรายโรคเนื้อเยื่อเกี่ยวพัน ตรวจพบคอพอกขนาดเล็ก ไม่เจ็บ อ่อนเพลีย และใจสั่น ส่วนใหญ่รักษาตามอาการ โดยให้กลุ่ม beta blocker (Propanolol 10-20 มก 4 มื้อต่อวัน) ไม่ต้องให้ยาต้านธัยรอยด์ พบว่า 2 ใน 3 จะกลับมาเป็นปกติ มีเพียง 1 ใน 3 ที่จะเข้าสู่ระยะ hypothyroidism เมื่ออาการดีขึ้นควรตรวจติดตาม TSH ทุก 2 เดือนจนครบ 1 ปีหลังคลอดเพื่อเฝ้าระวังภาวะพร่องธัยรอยด์
- ระยะ hypothyroidism พบได้ช่วง 4-8 เดือน หลังคลอด ประมาณร้อยละ 2-5 มีการพร่องของธัยรอยด์ มีคอพอกชัดเจน อ่อนเพลียง่าย เหม่อลอย ไม่มีสมาธิ รักษาด้วยธัยรอยด์ฮอร์โมน(thyroxine) 25-75 มคก./วัน นาน 6-12 เดือน อาจเกิดภาวะพร่องธัยรอยด์ถาวรได้ประมาณ 1 ใน 3 ส่วนใหญ่หายไปได้เอง หลังจากนั้นควรตรวจติดตามระดับ TSH ทุกปี
ก้อนที่ต่อมธัยรอยด์(thyroid nodule)(3)
พบได้ร้อยละ 20 โดยเกิดจากหลายสาเหตุ ควรซักประวัติครอบครัวว่ามีใครเคยเป็นมาก่อนหรือไม่ หรือเป็น familial medullary thyr oid carcinoma multiple endocrine neoplasia type 2 (MEN 2), familial papillary thyroid carcinoma, and familial polyposis coli เป็นต้น
การตรวจด้วยคลื่นเสียงความถี่สูง ดูขนาดและของเหลวภายใน ถ้าขนาดมากกว่า 1 ซม.ควรตรวจด้วย Fine needle aspiration หรือ FNA ต่อ ร่วมกับตรวจ TFT ในรายที่เป็นมะเร็ง ค่า TFT จะปกติได้ โดยสรุปแนวทาการดูแลรักษาดังแสดงในรูปที่ 1
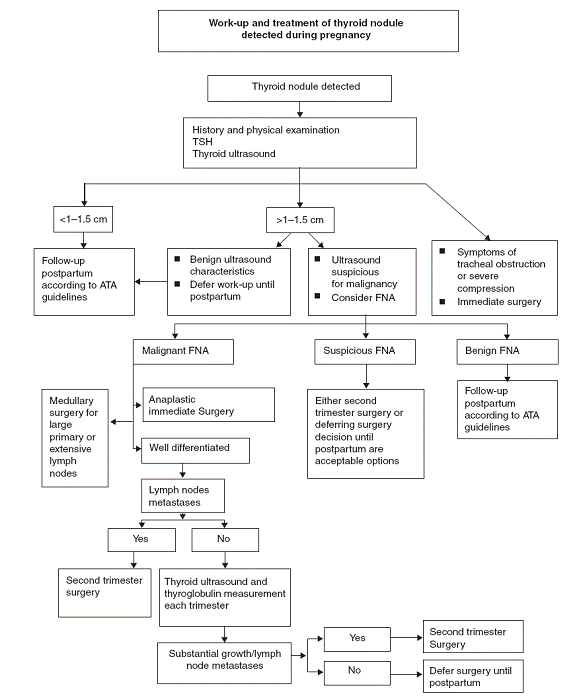
รูปที่ 1 แนวทางการดูแล สืบค้น และรักษาก้อนที่ต่อมธัยรอยด์ในสตรีตั้งครรภ์(3)
เอกสารอ้างอิง
- Cunningham FG, Leveno KJ, Bloom SL, Hauth JC, Rouse DJ, Spong CY. Williams Obstetrics 23rd ed. McGraw-Hill : New York, 2010: 1126.
- Committee on Patient Safety and Quality Improvement, Committee on Professional Liability. ACOG Committee Opinion No. 381: Subclinical hypothyroidism in pregnancy. Obstet Gynecol 2007; 110:959.
- Stagnaro-Green A, Abalovich M, Alexander E, et al. Guidelines of the American Thyroid Association for the diagnosis and management of thyroid disease during pregnancy and postpartum. Thyroid 2011; 21:1081.
- Stricker R, Echenard M, Eberhart R, et al. Evaluation of maternal thyroid function during pregnancy: the importance of using gestational age-specific reference intervals. Eur J Endocrinol 2007; 157:509.
- .American College of Obstetricians and Gynecologists.. ACOG Practice Bulletin. Clinical management guidelines for obstetrician-gynecologists. Number 37, August 2002. Thyroid disease in pregnancy. Obstet Gynecol 2002; 100:387
- Laurberg P, Bournaud C, Karmisholt J, Orgiazzi J. Management of Graves’ hyperthyroidism in pregnancy: focus on both maternal and foetal thyroid function, and caution against surgical thyroidectomy in pregnancy. Eur J Endocrinol. 2009;160:1.
- Negro R, Mestman JH. Thyroid disease in pregnancy. Best Pract Res Clin Endocrinol Metab. 2011;25:927
- Luewan S, Chakkabut P, Tongsong T. Outcomes of pregnancy complicated with hyperthyroidism: a cohort study. Arch Gynecol Obstet 2011 Feb;283(2):243-7.
- Srisupundit K, Sirichotiyakul S, Tongprasert F, Luewan S, Tongsong T. Fetal therapy in fetal thyrotoxicosis: a case report. Fetal Diagn Ther 2008;23(2):114-6.
- Stagnaro-Green A. Postpartum thyroiditis. Best Pract Res Clin Endocrinol Metab 2004 Jun;18(2):303-16.
- .Abalovich M, Amino N, Barbour LA, Cobin RH, De Groot LJ, Glinoer D, et al. Management of thyroid dysfunction during pregnancy and postpartum: an Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab 2007 Aug;92(8 Suppl):S1-47.

