วัคซีนสำหรับสตรีตั้งครรภ์
(Vaccination in pregnancy)
อ. พญ. ศิรินาถ ศิริเลิศ
บทนำ
การให้วัคซีนเป็นการกระตุ้นการสร้างภูมิคุ้มกันเพื่อป้องกันการติดเชื้อ สำหรับสตรีตั้งครรภ์การให้วัคซีนถือว่ามีความสำคัญ เนื่องจากสตรีตั้งครรภ์มีภูมิคุ้มกันต่ำลงจึงเสี่ยงต่อการติดเชื้อต่าง ๆ มากขึ้น นอกจากประโยชน์ในสตรีตั้งครรภ์ วัคซีนยังมีประโยชน์ต่อทารกที่ได้รับภูมิคุ้มกันที่มารดาสร้างขึ้นและส่งผ่านทางรก ทำให้ได้รับการปกป้องไปจนกระทั่งหลังคลอดก่อนทารกจะได้รับวัคซีนตามช่วงวัย แต่วัคซีนที่จะให้ในสตรีตั้งครรภ์ต้องมีความปลอดภัยต่อการตั้งครรภ์ สตรีตั้งครรภ์ และพัฒนาการของทารกในครรภ์ ดังนั้นสตรีตั้งครรภ์และสตรีวัยเจริญพันธุ์ควรได้รับคำแนะนำการได้รับวัคซีนอย่างเหมาะสมเพื่อความปลอดภัยและประสิทธิภาพในการป้องกันการติดเชื้อสูงสุด
ระบบภูมิคุ้มกันของสตรีตั้งครรภ์
ระบบภูมิคุ้มกันของสตรีตั้งครรภ์มีการเปลี่ยนแปลงตามช่วงของการตั้งครรภ์(1) แต่โดยรวมระบบภูมิคุ้มกันของร่างกายจะถูกกดเพื่อป้องกันปฏิกิริยาต่อต้านทารกในครรภ์(1-5) โดยเพิ่มการทำงานของ T-helper 2 ซึ่งทำหน้าที่ต้านการอักเสบ (anti-inflammatory)(2, 5-7) ทำให้ติดเชื้อง่ายขึ้น และอาการจากการติดเชื้อรุนแรงขึ้น
สตรีตั้งครรภ์ควรหลีกเลี่ยงการเดินทางไปยังสถานที่ที่มีการระบาดของโรค ดูแลสุขอนามัยของตนเองและสิ่งแวดล้อม และฉีดวัคซีนให้ผู้ที่อาศัยร่วมกันกับสตรีตั้งครรภ์หากยังได้รับวัคซีนไม่ครบ เพื่อลดความเสี่ยงของการรับเชื้อ
ปฏิกิริยาทางภูมิคุ้มกันต่อวัคซีนในสตรีตั้งครรภ์
การกดภูมิคุ้มกันของสตรีตั้งครรภ์อาจส่งผลให้สร้างแอนติบอดีจากการฉีดวัคซีนได้ไม่ดีเพียงพอ แต่จากการศึกษาพบว่าสตรีตั้งครรภ์สามารถสร้างแอนติบอดีได้ไม่แตกต่างจากสตรีทั่วไป(8, 9)
ประสิทธิภาพการส่งต่อภูมิคุ้มกันไปสู่ทารกขึ้นกับความเข้มข้นของแอนติบอดีของมารดา ชนิดของแอนติบอดี (ชนิด IgG โดยเฉพาะ IgG1 สามารถส่งผ่านได้ดี ส่วน IgM, IgA และ IgE ไม่สามารถส่งผ่านทางรกได้) และอายุครรภ์ขณะได้รับวัคซีน โดยความเข้มข้นของ IgG ในทารกจะต่ำกว่าความเข้มข้นในมารดาในช่วงครึ่งแรกของการตั้งครรภ์ จากนั้นจะค่อย ๆ เพิ่มขึ้นจนมีความเข้มข้นประมาณร้อยละ 50 ของมารดาขณะอายุครรภ์ 28-32 สัปดาห์ และจะเท่ากับมารดาขณะอายุครรภ์ 36 สัปดาห์ เมื่อทารกครบกำหนดระดับความเข้มข้นของ IgG จะมากกว่ามารดา(10)
วัคซีนที่แนะนำสำหรับสตรีวัยเจริญพันธุ์
สตรีวัยเจริญพันธุ์ทุกรายควรได้รับการซักประวัติวัคซีนในวัยเด็กเพื่อพิจารณาความเสี่ยงและวางแผนการให้วัคซีน
หากได้รับวัคซีนตามเกณฑ์ของสมาคมโรคติดเชื้อเด็กแห่งประเทศไทย ปี พ.ศ. 2563(11) เมื่ออายุครบ 12 ปี จะได้รับวัคซีน คือ วัคซีนป้องกันวัณโรค (BCG) วัคซีนป้องกันไวรัสตับอักเสบบี (HBV) วัคซีนป้องกันคอตีบ บาดทะยัก ไอกรนชนิดทั้งเซลล์ (DTwP) วัคซีนป้องกันฮีโมฟีลุสอินฟลูเอนเซ ชนิดบี (Hib) วัคซีนป้องกันโปลิโอชนิดกิน (OPV) วัคซีนป้องกันไวรัสโรต้า (rotavirus vaccine) วัคซีนป้องกันคางทูม หัด และหัดเยอรมัน (MMR) วัคซีนป้องกันไข้สมองอักเสบเจอี (live JE) วัคซีนป้องกันไข้หวัดใหญ่ (influenza) วัคซีนป้องกันมะเร็งปากมดลูก (HPV)
นอกจากนี้ยังมีวัคซีนอื่น ๆ ที่อาจให้เสริมหรือทดแทนได้ คือ วัคซีนรวมของคอตีบ บาดทะยัก ไอกรน ชนิดไร้เซลล์ (DTaP, Tdap หรือ TdaP) – ตับอักเสบบี (HBV) – โปลิโอชนิดฉีด (IPV) – ฮีโมฟีลุสอินฟลูเอนเซ ชนิดบี (Hib) วัคซีนป้องกันนิวโมคอคคัสชนิดคอนจูเกต (PCV) วัคซีนป้องกันไข้สมองอักเสบเจอี (inactivated JE) วัคซีนป้องกันไวรัสตับอักเสบเอ (HAV) วัคซีนป้องกันอีสุกอีใส (VZV) หรือวัคซีนรวมคางทูม หัด หัดเยอรมัน อีสุกอีใส (MMRV) วัคซีนป้องกันไข้เลือดออก (DEN) วัคซีนป้องกันพิษสุนัขบ้า (rabies)
การได้รับวัคซีนในวัยเด็กอาจแตกต่างกันไปขึ้นกับคำแนะนำการให้วัคซีนขององค์กรต่าง ๆ ณ ขณะนั้นและการเข้าถึงวัคซีนของแต่ละคน(12) ดังนั้นการให้วัคซีนในผู้ใหญ่ในกรณีที่ยังไม่ได้รับวัคซีนในวัยเด็กหรือเพื่อกระตุ้นภูมิคุ้มกันจำเป็นต้องพิจารณาให้ในสตรีวัยเจริญพันธุ์ร่วมด้วย โดยคำแนะนำจะแตกต่างกันระหว่างกรณีที่มีสุขภาพแข็งแรงและกรณีมีโรคประจำตัว ในที่นี้จะขอกล่าวถึงเฉพาะผู้ที่อายุ 20 ปีขึ้นไปและมีสุขภาพแข็งแรง คำแนะนำจากกองโรคป้องกันด้วยวัคซีน กรมควบคุมโรค ปี 2562(12) แนะนำให้ได้รับวัคซีนดังนี้
-
- วัคซีนป้องกันไข้หวัดใหญ่ (influenza vaccine) ปีละ 1 ครั้งในฤดูกาลที่มีการระบาดของโรค
- วัคซีนป้องกันบาดทะยัก คอตีบ ไอกรน (tetanus, diphtheria, and pertussis: Tdap vaccine) หรือวัคซีนป้องกันบาดทะยัก คอตีบ (Td vaccine) กระตุ้นทุก 10 ปี
- วัคซีนป้องกันคางทูม หัด หัดเยอรมัน (mump, measles, rubella: MMR vaccine) 1-2 เข็มตามความเสี่ยง
- วัคซีนป้องกันไวรัสตับอักเสบบี (hepatitis B vaccine) 3 เข็ม
- วัคซีนป้องกันไวรัสตับอักเสบเอ (hepatitis A vaccine) 2 เข็ม
- วัคซีนป้องกันอีสุกอีใส (varicella vaccine) 2 เข็ม
- วัคซีนป้องกันมะเร็งปากมดลูก (human papillomavirus: HPV vaccine) 2-3 เข็มตามอายุที่เริ่มได้รับวัคซีน
- วัคซีนป้องกันไข้สมองอักเสบ (live attenuated Japanese encephalitis) 1 เข็ม
สตรีวัยเจริญพันธุ์ควรได้รับวัคซีนดังกล่าวนี้ให้ครบก่อนตั้งครรภ์(13) โดยเฉพาะวัคซีนชนิดเชื้อเป็น (live attenuated vaccine) เช่น วัคซีนป้องกันคางทูม หัด หัดเยอรมัน (MMR vaccine) และวัคซีนป้องกันอีสุกอีใส (varicella vaccine) เนื่องจากเป็นวัคซีนที่ไม่ควรฉีดในขณะตั้งครรภ์และการติดเชื้อระหว่างตั้งครรภ์จะส่งผลเสียรุนแรงต่อสตรีตั้งครรภ์และทารก
ก่อนฉีดวัคซีนชนิดเชื้อเป็นในสตรีวัยเจริญพันธุ์ ควรทำการซักประวัติเรื่องการตั้งครรภ์และแผนการตั้งครรภ์ภายใน 4 สัปดาห์หลังฉีดวัคซีน แต่ไม่แนะนำให้ตรวจการตั้งครรภ์ก่อนฉีดวัคซีนในสตรีวัยเจริญพันธุ์ทุกรายเป็นกิจวัตร และการให้วัคซีนเหล่านี้ในสตรีวัยเจริญพันธุ์ ควรแนะนำให้คุมกำเนิดต่อไปอย่างน้อย 28 วัน หลังแต่ละเข็มของวัคซีนที่ได้รับ ยกเว้นวัคซีนป้องกันอีสุกอีใสที่ทาง FDA แนะนำให้คุมกำเนิด 3 เดือน(14) แต่คำแนะนำที่เกี่ยวข้องกับการให้วัคซีน คือ Advisory Committee on Immunization Practices (ACIP) และองค์กรหลักทางสูติศาสตร์และนรีเวชวิทยาของสหรัฐอเมริกา (American College of Obstetricians and Gynecologists: ACOG) ยังคงแนะนำให้คุมกำเนิดต่อ 1 เดือน(13, 15) อย่างไรก็ตามหากตั้งครรภ์ในช่วงดังกล่าวก็ยังไม่มีรายงานความผิดปกติเกิดขึ้น(16)
การตรวจระดับภูมิคุ้มกันก่อนตั้งครรภ์
การซักประวัติและตรวจเพื่อยืนยันการมีภูมิคุ้มกันต่อโรคต่าง ๆ ที่ส่งผลต่อการตั้งครรภ์ เช่น หัดเยอรมัน ซึ่งเป็นการติดเชื้อที่ส่งผลเสียรุนแรงต่อการตั้งครรภ์และทารกในครรภ์ โดยที่วัคซีนไม่สามารถให้ได้ในขณะตั้งครรภ์ถือเป็นมาตรฐานที่ควรปฏิบัติในการตรวจสตรีวัยเจริญพันธุ์(17) การตรวจสอบประวัติว่าได้รับวัคซีนครบโดยได้รับวัคซีนหัดเยอรมันอย่างน้อย 1 เข็ม หรือมีการตรวจพบภูมิคุ้มกันต่อหัดเยอรมันจะช่วยลดความเสี่ยงที่อาจเกิดขณะตั้งครรภ์ลงได้ หากประวัติวัคซีนไม่ชัดเจน การตรวจภูมิคุ้มกันต่อหัดและหัดเยอรมันจะถือเป็นการตรวจพื้นฐานสำหรับการตรวจก่อนการตั้งครรภ์ ดังนั้นการซักประวัติร่วมกับการตรวจระดับภูมิคุ้มกันในกรณีประวัติไม่ชัดเจนจึงถือเป็นแนวทางปฏิบัติที่สำคัญอย่างหนึ่งของการตรวจวางแผนครอบครัว(13)
ภูมิคุ้มกันต่อหัด (measles antibody) หากตรวจไม่พบหรือภูมิคุ้มกันยังมีปริมาณไม่เพียงพอ แนะนำให้ฉีดวัคซีนก่อน 1-2 ครั้งตามความเสี่ยง(18) (กลุ่มเสี่ยงที่ควรได้รับวัคซีน 2 เข็มคือบุคลากรทางการแพทย์ นักศึกษา นักท่องเที่ยวต่างชาติ)
ภูมิคุ้มกันต่อหัดเยอรมัน (rubella antibody) หากตรวจไม่พบหรือภูมิคุ้มกันยังมีปริมาณไม่เพียงพอสำหรับสตรีวัยเจริญพันธุ์ที่ได้รับวัคซีนมาแล้ว 1-2 เข็ม แนะนำให้ฉีดวัคซีนอีก 1 เข็มก่อน (รวมไม่เกิน 3 เข็ม) ในกรณีนี้ ไม่จำเป็นต้องตรวจภูมิคุ้มกันซ้ำก่อนตั้งครรภ์(17) สำหรับกรณีที่มีภูมิคุ้มกันเพียงพอแล้ว ไม่จำเป็นต้องตรวจซ้ำก่อนการตั้งครรภ์ครั้งต่อ ๆ ไป
ภูมิคุ้มกันต่ออีสุกอีใส (varicella antibody) หากตรวจไม่พบหรือภูมิคุ้มกันยังมีปริมาณไม่เพียงพอ(19) แนะนำให้ฉีดวัคซีน 2 เข็มห่างกัน 4-8 สัปดาห์(15)
หลังจากฉีดวัคซีนทั้ง 3 ชนิดข้างต้น แนะนำให้คุมกำเนิดต่อไปก่อนอย่างน้อย 28 วัน (หรือ 3 เดือนสำหรับวัคซีนอีสุกอีใส) หลังฉีดวัคซีนแต่ละเข็ม
วัคซีนที่ควรให้ในสตรีตั้งครรภ์
วัคซีนที่เหมาะสมที่จะให้ในสตรีตั้งครรภ์ มีเกณฑ์ในการคัดเลือกคือ เป็นวัคซีนที่ช่วยป้องกันการติดเชื้อที่สตรีตั้งครรภ์มีโอกาสติดเชื้อได้ง่าย การติดเชื้อส่งผลเสียต่อมารดาหรือทารก และวัคซีนต้องไม่ส่งผลเสียต่อการตั้งครรภ์(20, 21) แต่อย่างไรก็ตามการศึกษาการใช้วัคซีนต่าง ๆ ในสตรีตั้งครรภ์ก็ยังมีข้อมูลไม่มากนัก ระหว่างตั้งครรภ์จึงควรเลือกใช้วัคซีนอย่างเหมาะสม สำหรับวัคซีนที่ไม่สามารถให้ได้ในขณะตั้งครรภ์หรือวัคซีนที่ยังไม่ได้ให้ในสตรีตั้งครรภ์รายนั้น ๆ ควรจะถูกบันทึกและวางแผนที่จะให้ในช่วงหลังคลอด(12, 13, 15, 17)
ชนิดของวัคซีนที่ปลอดภัย ไม่พบหลักฐานว่าส่งผลเสียต่อการตั้งครรภ์และทารกในครรภ์ คือ
-
- วัคซีนชนิดเชื้อตาย (inactivated vaccine)
- วัคซีนชนิดท็อกซอยด์ (toxoid)
- อิมมูโกลบูลิน (immunoglobulin)
วัคซีนป้องกันบาดทะยัก คอตีบ ไอกรน (tetanus, diphtheria, and pertussis vaccine: Tdap)
และ วัคซีนป้องกันไข้หวัดใหญ่ชนิดเชื้อตาย (inactivated influenza vaccine) เป็นวัคซีนที่เป็นที่ยอมรับและแนะนำให้ใช้ในสตรีตั้งครรภ์ทุกราย(20-23) เนื่องจากมีความปลอดภัยสูง ไม่ส่งผลเสียต่อการตั้งครรภ์ ไม่ก่อให้เกิดการแท้ง(24-27) และภูมิคุ้มกันที่สตรีตั้งครรภ์สร้างจากการได้รับวัคซีนเหล่านี้สามารถส่งผ่านรกไปยังทารกในครรภ์ และช่วยปกป้องทารกในช่วงหลังคลอดได้(20, 21, 28)
1. วัคซีนป้องกันบาดทะยัก คอตีบ ไอกรน (tetanus, diphtheria, and pertussis vaccine: Tdap)
ทารกอายุน้อยกว่า 3 เดือนถือเป็นกลุ่มที่มีความเสี่ยงสูงต่อการเจ็บป่วยรุนแรงจากไอกรน(29, 30) และร้อยละ 50 ทารกจะได้รับเชื้อมาจากผู้ดูแลในครอบครัว(31, 32) ดังนั้นการฉีดวัคซีนให้มารดาระหว่างตั้งครรภ์ และการที่สมาชิกในครอบครัวมีภูมิคุ้มกันต่อไอกรนจะลดความเสี่ยงการติดเชื้อในทารกลงได้(33, 34) นอกจากนี้การฉีดวัคซีนในสตรีตั้งครรภ์ในช่วงไตรมาสที่ 3 จะกระตุ้นให้สร้างและส่งต่อภูมิคุ้มกันที่สามารถปกป้องทารกในช่วง 2-3 เดือนแรกหลังคลอดได้(29) เนื่องจากทารกจะได้รับวัคซีนเมื่ออายุ 6-8 สัปดาห์(11) ในช่วงก่อนที่ทารกจะได้รับวัคซีน ภูมิคุ้มกันจะมาจากมารดาส่งผ่านรกในขณะตั้งครรภ์และผ่านน้ำนมในช่วงหลังคลอดเท่านั้น
ไม่มีรายงานผลเสียของวัคซีน Tdap ต่อการตั้งครรภ์ ต่อสตรีตั้งครรภ์ และต่อทารก จึงมีความปลอดภัยสูงที่จะใช้ระหว่างตั้งครรภ์(24) โดยมีคำแนะนำในการให้วัคซีน ดังนี้
สตรีตั้งครรภ์ที่ไม่เคยได้รับวัคซีน ได้รับไม่ครบ 3 เข็ม หรือไม่ทราบประวัติวัคซีน
แนะนำให้ฉีดวัคซีนใหม่ทั้ง 3 เข็ม โดยฉีดเป็น Td ที่ 0, 4 สัปดาห์และ 6-12 เดือน เริ่มฉีดในช่วงไตรมาสที่ 2-3 และเพื่อป้องกันไอกรน (pertussis) แนะนำให้เปลี่ยน 1 ใน 3 เข็มของ Td เป็น Tdap ในช่วงอายุครรภ์ 27-36 สัปดาห์(35, 36)
สตรีตั้งครรภ์ที่ได้รับวัคซีนครบ 3 เข็มก่อนตั้งครรภ์
แนะนำให้ Tdap 1 เข็มในช่วง 27-36 สัปดาห์(36, 37) ให้ซ้ำในทุก ๆ การตั้งครรภ์ แม้การตั้งครรภ์จะห่างกันไม่ถึง 1 ปีก็ตาม(35, 36) เนื่องจากการตรวจปริมาณแอนติบอดีในเลือดสายสะดือทารกที่คลอดจากสตรีตั้งครรภ์ที่ได้รับ Tdap ในช่วงก่อนตั้งครรภ์ถึงแม้จะไม่เกิน 2 ปี พบว่าภูมิคุ้มกันส่งไปให้ทารกได้ในปริมาณที่ไม่เพียงพอสำหรับการปกป้องทารก(38)
ในกรณีที่ไม่มี Tdap การให้ Td จะให้ในกรณี(12)
-
-
-
- ได้รับ Td เข็มสุดท้ายนาน 10 ปีขึ้นไป
- ได้รับ Td เข็มสุดท้ายนาน 5 ปีขึ้นไป ร่วมกับมีบาดแผลที่เสี่ยงต่อบาดทะยัก
-
-
เนื่องจากวัคซีนจะกระตุ้นให้สตรีตั้งครรภ์สร้างภูมิคุ้มกันได้สูงสุดที่ประมาณ 2-4 สัปดาห์(35) หลังจากได้รับวัคซีน ดังนั้นวัคซีนที่ต้องการให้สร้างและส่งต่อภูมิคุ้มกันให้ทารก เช่น Tdap จึงควรให้ในช่วงต้นของไตรมาสที่ 3 เพื่อให้สตรีตั้งครรภ์สามารถสร้างภูมิคุ้มกันและส่งต่อให้ทารกได้สูงสุดในช่วงก่อนคลอด(9) การศึกษาที่สนับสนุนการให้วัคซีนในช่วงต้นของไตรมาส 3 พบว่าสตรีตั้งครรภ์ที่ฉีดวัคซีนในช่วงต้นของไตรมาสที่ 3 (27-32 สัปดาห์) พบระดับแอนติบอดีในเลือดสายสะดือทารกสูงกว่ากลุ่มที่ฉีดวัคซีนในช่วงท้ายของไตรมาสที่ 3 (32-36 สัปดาห์) (39, 40) แต่อย่างไรก็ตามการศึกษาเรื่องช่วงเวลาสำหรับการฉีดวัคซีนที่ให้ประสิทธิภาพสูงสุดยังมีความแตกต่างกัน(41, 42) โดยประสิทธิภาพในการปกป้องทารกจะลดลงในสตรีตั้งครรภ์ที่ได้รับ Tdap ในช่วงก่อนคลอดไม่นาน(34) แต่สำหรับสตรีตั้งครรภ์ที่ได้รับ Tdap ในช่วงก่อนอายุครรภ์ 27-36 สัปดาห์ อาจเนื่องจากมีบาดแผลที่เสี่ยงต่อบาดทะยักหรือมีการระบาดของไอกรน ในกรณีนี้สตรีตั้งครรภ์ไม่จำเป็นต้องได้รับ Tdap ซ้ำในช่วงอายุครรภ์ 27-36 สัปดาห์(36)
สตรีตั้งครรภ์ที่ไม่ได้รับ Tdap ระหว่างตั้งครรภ์ แนะนำให้ฉีด Tdap ในช่วงหลังคลอดก่อนออกจากโรงพยาบาล(11, 12, 35, 36) เพื่อป้องกันการติดเชื้อไปสู่ทารกทางอ้อม และส่งผ่านภูมิคุ้มกันผ่านน้ำนมไปสู่ลูก แต่การให้วัคซีนหลังคลอดต้องใช้เวลาในการกระตุ้นภูมิคุ้มกันจึงไม่สามารถปกป้องทารกได้ตั้งแต่แรกคลอด
สมาชิกในครอบครัวหรือผู้ดูแลทารก (อายุน้อยกว่า 12 เดือน) ควรได้รับวัคซีน Tdap จนครบมาก่อน หากได้รับไม่ครบ แนะนำให้ฉีดวัคซีนเพื่อเป็นการปกป้องทารกทางอ้อม สำหรับการให้วัคซีน Tdap เพื่อกระตุ้น ไม่แนะนำสำหรับสมาชิกในครอบครัวที่เคยได้รับวัคซีนครบมาก่อน(12, 35, 36)
2. วัคซีนป้องกันไข้หวัดใหญ่ชนิดเชื้อตาย (inactivated influenza vaccine)
วัคซีนป้องกันไข้หวัดใหญ่จะให้เพื่อสร้างภูมิคุ้มกันป้องกันทั้งสตรีตั้งครรภ์และทารก ดังนั้นจึงควรให้ในช่วงที่มีการระบาดของโรคโดยไม่คำนึงถึงอายุครรภ์หากสตรีตั้งครรภ์มีความเสี่ยงสูงที่จะได้รับเชื้อ(22, 43) แต่หากการได้รับวัคซีนสามารถเลื่อนออกไปได้ เช่น การระบาดอยู่ในวงจำกัด ไม่รุนแรง สามารถพิจารณาเลื่อนไปฉีดวัคซีนที่ไตรมาส 2 ได้(12) เพื่อลดความกังวลเรื่องความเสี่ยงที่อาจเกิดขึ้นในไตรมาสแรกได้ตามธรรมชาติ เช่น ภาวะแท้ง ทารกที่ผิดปกติ
การให้วัคซีนป้องกันไข้หวัดใหญ่นี้หวังประโยชน์เพื่อป้องกันการติดเชื้อในสตรีตั้งครรภ์เป็นหลัก(44) แต่อย่างไรก็ตามภูมิคุ้มกันสามารถส่งไปถึงทารก(45) ได้มากเพียงพอถึงร้อยละ 85 ของทารกที่มารดาได้รับวัคซีนระหว่างตั้งครรภ์(46)
วัคซีนที่สามารถให้ในสตรีตั้งครรภ์ได้ เมื่อมีข้อบ่งชี้
การให้วัคซีนเพื่อป้องกันการติดเชื้ออื่น ๆ ในสตรีตั้งครรภ์ จะพิจารณาจากความเสี่ยงของสตรีตั้งครรภ์(20) เช่น โรคประจำตัว ความเสี่ยงในการสัมผัสเชื้อ การเดินทางไปยังแหล่งที่มีการระบาดของโรค เป็นต้น การติดเชื้อนั้นส่งผลเสียต่อการตั้งครรภ์อย่างชัดเจน และวัคซีนนั้นไม่มีรายงานผลเสียต่อการตั้งครรภ์ สตรีตั้งครรภ์ และทารก ดังนั้นการพิจารณาให้วัคซีนจะพิจารณาให้เมื่อมีข้อบ่งชี้ในสตรีตั้งครรภ์เป็นราย ๆ ไป(47)
วัคซีนในกลุ่มนี้มีประโยชน์ทั้งเพื่อป้องกันก่อนสัมผัสเชื้อ (pre-exposure prophylaxis) และป้องกันหลังจากสัมผัสเชื้อ (post-exposure prophylaxis) โดยวัคซีนที่สามารถให้ได้มีดังนี้
- วัคซีนป้องกันนิวโมคอคคัส (pneumococcal vaccine) แนะนำให้ในผู้ป่วยที่มีโรคเรื้อรัง เช่น โรคหัวใจ โรคปอด โรคตับ โรคไต เบาหวาน ผู้ป่วยที่ตัดม้าม และผู้ป่วยที่มีภูมิต้านทานต่ำ เช่น ติดเชื้อเอชไอวี มะเร็ง ได้รับยากดภูมิคุ้มกัน เป็นต้น(48) ในผู้ป่วยกลุ่มดังกล่าวควรได้รับวัคซีนตั้งแต่ก่อนตั้งครรภ์ แต่หากยังไม่ได้รับวัคซีนมาก่อน แนะนำให้วัคซีนในช่วงไตรมาส 2-3(49) เนื่องจากการศึกษาผลข้างเคียงของวัคซีนต่อการตั้งครรภ์ยังไม่มากเพียงพอ(50) และประโยชน์ในแง่ของการลดการติดเชื้อในทารกยังไม่ชัดเจน(51) จึงไม่ได้แนะนำให้ใช้กับสตรีตั้งครรภ์ทุกราย
- วัคซีนป้องกันฮีโมฟีลุสอินฟลูเอนเซ ชนิดบี (haemophilus Influenzae Type B: Hib vaccine) แนะนำให้ในผู้ป่วยที่มีโรคเรื้อรัง เช่น ลูคีเมีย ผู้ป่วยที่ตัดม้าม ผู้ติดเชื้อเอชไอวี และไม่เคยได้รับ Hib vaccine ในช่วงวัยเด็กมาก่อน(48) การให้วัคซีนนี้มีการศึกษาว่ามีความปลอดภัยในช่วงไตรมาสที่ 3(9) แต่ไม่ได้แนะนำให้ใช้กับสตรีตั้งครรภ์ทุกราย
- วัคซีนป้องกันไข้กาฬหลังแอ่น (meningococcal vaccine) แนะนำให้ในผู้อาศัยในแหล่งที่มีการระบาดของโรค ผู้ติดเชื้อเอชไอวี ผู้ป่วยที่ตัดม้าม เป็นต้น(48) การศึกษาผลข้างเคียงของวัคซีนต่อการตั้งครรภ์ยังไม่มากเพียงพอ(52) จึงไม่ได้แนะนำให้ใช้กับสตรีตั้งครรภ์ทุกราย
- วัคซีนป้องกันไวรัสตับอักเสบบี (hepatitis B vaccine) เป็นวัคซีนที่ปลอดภัย สามารถให้ได้ระหว่างการตั้งครรภ์ ในสตรีตั้งครรภ์ที่ได้รับวัคซีนมาแล้วและจะต้องได้รับเข็มต่อไประหว่างการตั้งครรภ์สามารถให้วัคซีนต่อตามตารางได้ และวัคซีนนี้จะมีข้อบ่งชี้ในสตรีตั้งครรภ์ที่มีความเสี่ยงสูง(53, 54) คือ สตรีตั้งครรภ์ที่ตรวจไม่พบภูมิคุ้มกัน (anti-HBs: negative) ที่มีสามีติดเชื้อไวรัสตับอักเสบบี มีคู่นอนหลายคน ใช้ยาเสพติดเข้าเส้น ติดเชื้อเอชไอวีหรือโรคติดต่อทางเพศสัมพันธ์อื่น ๆ เป็นต้น แต่การตรวจหาภูมิคุ้มกัน (anti-HBs) ในสตรีตั้งครรภ์ทุกรายเพื่อให้วัคซีนในรายที่ยังไม่มีภูมิคุ้มกันไม่มีความจำเป็น เนื่องจากการตรวจหาการติดเชื้อไวรัสตับอักเสบบี (HBsAg) ถือปฏิบัติเป็นกิจวัตรในการฝากครรภ์ครั้งแรก(53, 55) และหากพบการติดเชื้อสามารถให้การดูแลเพื่อลดการติดต่อจากแม่สู่ลูกได้อย่างมีประสิทธิภาพ(54, 56)
- วัคซีนป้องกันไวรัสตับอักเสบเอ (hepatitis A vaccine) การติดเชื้อไวรัสตับอักเสบเอในสตรีตั้งครรภ์อาจส่งผลให้เกิดการคลอดก่อนกำหนด(57) และทารกในครรภ์มีรายงานการตรวจพบ meconium peritonitis, ascites, polyhydramnios(58) แต่อย่างไรก็ตามการศึกษาผลข้างเคียงของวัคซีนต่อการตั้งครรภ์ยังมีไม่มากพอ(59, 60) จึงแนะนำให้เพื่อป้องกันในผู้อาศัยหรือเสี่ยงต่อการสัมผัสกับสิ่งแวดล้อมที่มีสุขอนามัยไม่ดี ผู้ป่วยที่เสี่ยงต่อการมีอาการรุนแรง เช่น โรคตับเรื้อรัง ติดเชื้อเอชไอวี เป็นต้น(53, 61) แต่หากสตรีตั้งครรภ์สัมผัสกับไวรัสตับอักเสบเอระหว่างการตั้งครรภ์ แนะนำให้ฉีดทั้งวัคซีนป้องกันไวรัสตับอักเสบเอและอิมมูโนโกลบูลิน
- วัคซีนป้องกันพิษสุนัขบ้า (rabies vaccine) กรณีสัมผัสเชื้อระหว่างการตั้งครรภ์สามารถใช้ได้อย่างปลอดภัย โดยอาจให้อิมมูโนโกลบูลินร่วมด้วย(62) สำหรับกรณีใช้เพื่อป้องกันการติดเชื้อแนะนำเฉพาะผู้เสี่ยงสูงต่อการสัมผัสเชื้อ
- วัคซีนอื่น ๆ เช่น วัคซีนป้องกันไข้เหลือง (yellow fever vaccine) วัคซีนป้องกันโปลิโอ (poliovirus vaccine) วัคซีนป้องกันไข้ไทฟอยด์ (typhoid vaccine) วัคซีนป้องกันไข้สมองอักเสบที่เกิดจากไวรัสเจอี (Japanese encephalitis vaccine)(48)
- วัคซีนที่ควรหลีกเลี่ยงในระหว่างตั้งครรภ์แต่สามารถให้ได้ในสถานการณ์จำเพาะ คือ วัคซีนป้องกันฝีดาษ (smallpox)(63) และวัคซีนป้องกันแอนแทรกซ์ (anthrax vaccine)(64) ซึ่งสามารถให้ได้หากสตรีตั้งครรภ์รายนั้นสัมผัสเชื้อ
วัคซีนที่ไม่ควรให้ในสตรีตั้งครรภ์
วัคซีนชนิดเชื้อเป็นสร้างจากเชื้อโรคที่ถูกทำให้อ่อนกำลังลง โดยทั่วไปวัคซีนชนิดนี้ไม่ส่งผลเสียต่อผู้ใหญ่หรือเด็กหลังคลอด แต่ทารกในครรภ์จัดอยู่ในกลุ่มเสี่ยงที่หากได้รับวัคซีนที่มีเชื้อโรคอยู่ถึงแม้จะอ่อนกำลังลง ก็ยังมีความเสี่ยงที่จะติดเชื้อจากวัคซีนได้(65) ถึงแม้จะยังไม่มีหลักฐานหรือการศึกษาที่พบผลเสียต่อมารดาและทารกที่ได้รับวัคซีนกลุ่มนี้อย่างชัดเจน แต่อาจเกิดการติดเชื้อที่ไม่แสดงอาการ (subclinical infection) ได้ โดยทั่วไปการตั้งครรภ์จะถือเป็นข้อบ่งห้ามในการฉีดวัคซีนกลุ่มนี้(65, 66) แต่หากสตรีตั้งครรภ์รายใดมีความเสี่ยงต่อการติดเชื้อที่จะส่งผลเสียรุนแรง การพิจารณาให้วัคซีนโดยขึ้นกับวิจารณญาณของแพทย์โรคติดเชื้อสามารถทำได้เป็นราย ๆ ไป(66)
1. วัคซีนป้องกันคางทูม หัด และหัดเยอรมัน (MMR Vaccine)
เป็นวัคซีนชนิดเชื้อเป็น จึงไม่ควรให้ในสตรีตั้งครรภ์ แต่การติดเชื้อนี้ส่งผลเสียรุนแรงต่อการตั้งครรภ์ ดังนั้นการมีภูมิคุ้มก่อนการตั้งครรภ์จะส่งผลดีต่อการตั้งครรภ์(17, 19, 48)
หากสตรีตั้งครรภ์ไม่มีภูมิคุ้มกันและสัมผัสเชื้อแนะนำให้อิมมูโนโกลบูลินภายใน 6 วันหลังจากสัมผัสเชื้อ(17, 18) โดยแนะนำให้ทางหลอดเลือดมากกว่าฉีดเข้ากล้ามเนื่องจากระดับของแอนติบอดีจะมากเพียงพอต่อการปกป้องทารก(17)
ความเสี่ยงจากการฉีดวัคซีนนี้ในสตรีตั้งครรภ์เป็นความเสี่ยงตามทฤษฎีเนื่องจากเป็นวัคซีนชนิดเชื้อเป็น แต่จากรายงานไม่พบความผิดปกติทั้งความผิดปกติของทารกที่สัมพันธ์กับการติดเชื้อหัดเยอรมัน (หูหนวก ต้อกระจก ผิดปกติของหัวใจ กระดูก การเจริญเติบโต พัฒนาการของสมอง) และความผิดปกติของการตั้งครรภ์(16, 17) ดังนั้นการได้รับวัคซีนขณะตั้งครรภ์ไม่ถือเป็นข้อบ่งชี้ให้ยุติการตั้งครรภ์(17, 67)
โดยวัคซีนสามารถให้ได้อย่างปลอดภัยในช่วงหลังคลอดและให้นมบุตร ดังนั้นหากสตรีตั้งครรภ์ยังไม่มีภูมิคุ้มกันแนะนำให้วัคซีนในช่วงหลังคลอดก่อนออกจากโรงพยาบาล(48)
2. วัคซีนอีสุกอีใส (varicella vaccine)
เป็นวัคซีนชนิดเชื้อเป็น จึงไม่ควรให้ในสตรีตั้งครรภ์ แต่การติดเชื้อนี้จะก่อให้เกิดความพิการของทารก (congenital varicella syndrome) ได้ร้อยละ 1-2 และอาการของสตรีตั้งครรภ์มักมีความรุนแรง ดังนั้นการมีภูมิคุ้มก่อนการตั้งครรภ์จะส่งผลดีต่อการตั้งครรภ์(68)
หากสตรีตั้งครรภ์ไม่มีภูมิคุ้มกันและสัมผัสเชื้อแนะนำให้อิมมูโนโกลบูลิน และแนะนำให้ฉีดวัคซีนหลังคลอดโดยห่างจากอิมมูโนโกลบูลินอย่างน้อย 5 เดือน
ความเสี่ยงจากการฉีดวัคซีนนี้ในสตรีตั้งครรภ์เป็นความเสี่ยงตามทฤษฎีเนื่องจากเป็นวัคซีนชนิดเชื้อเป็น แต่จากรายงานพบความผิดปกติเพียงเล็กน้อยไม่ต่างจากประชากรทั่วไป(15, 68) ดังนั้นการได้รับวัคซีนขณะตั้งครรภ์ไม่ถือเป็นข้อบ่งชี้ให้ยุติการตั้งครรภ์(15)
วัคซีนสามารถให้ได้ในช่วงหลังคลอดและให้นมบุตร เนื่องจากไม่พบ DNA ของเชื้อในน้ำนมและไม่พบความผิดปกติของทารก แต่การศึกษายังไม่มากเพียงพอ(69)
3. วัคซีนป้องกันมะเร็งปากมดลูก (HPV Vaccine)
เป็นวัคซีนชนิดเชื้อตาย ปัจจุบันวัคซีนป้องกันเชื้อ HPV มีทั้งแบบป้องกัน 2 สายพันธุ์ (bivalent: 16, 18) ป้องกัน 4 สายพันธุ์ (quadrivalent: 6, 11, 16, 18) และป้องกัน 9 สายพันธุ์ (nonavalent: 6, 11, 16, 18, 31, 33, 45, 52, 58)
แม้จะเป็นวัคซีนชนิดเชื้อตายแต่การศึกษาการใช้วัคซีนนี้ในสตรีตั้งครรภ์ยังมีไม่เพียงพอ(70) ดังนั้นหากสตรีตั้งครรภ์ได้รับวัคซีนมาก่อนและเข็มต่อไปจะต้องได้รับในช่วงตั้งครรภ์แนะนำให้เลื่อนออกไปฉีดหลังคลอดแทน(71) แต่เนื่องจากยังไม่มีรายงานความผิดปกติที่เกิดขึ้นทั้งต่อมารดา ทารก และการตั้งครรภ์ที่ชัดเจน หากสตรีตั้งครรภ์ได้รับวัคซีนนี้แนะนำให้ตั้งครรภ์ต่อตามปกติ(72)
วัคซีนอื่น ๆ ที่ไม่ควรให้ในสตรีตั้งครรภ์
-
- วัคซีนป้องกันไข้หวัดใหญ่ชนิดเชื้อเป็น (live attenuated influenza vaccine)(73)
- วัคซีนป้องกันวัณโรค (Bacillus Calmette Guerin: BCG vaccine)(74)
- วัคซีนป้องกันงูสวัด (zoster Vaccine)(75)
ก่อนฉีดวัคซีนในสตรีวัยเจริญพันธุ์ทุกครั้งโดยเฉพาะวัคซีนกลุ่มนี้ แนะนำให้ซักประวัติเพื่อประเมินการตั้งครรภ์หรือแผนการตั้งครรภ์ในอีก 4 สัปดาห์และตรวจยืนยันการตั้งครรภ์หากไม่สามารถประเมินการตั้งครรภ์จากการซักประวัติได้ แต่ไม่แนะนำให้ตรวจการตั้งครรภ์ก่อนฉีดวัคซีนเป็นกิจวัตร แต่หากให้วัคซีนกลุ่มนี้ไปแล้ว โดยไม่ทราบว่าตั้งครรภ์หรือตั้งครรภ์ระหว่าง 4 สัปดาห์หลังได้รับวัคซีน สตรีตั้งครรภ์ควรได้รับข้อมูลความเสี่ยงที่อาจเกิดขึ้นได้ แต่ไม่มีข้อบ่งชี้ของการยุติการตั้งครรภ์เนื่องจากยังไม่มีรายงานความผิดปกติที่ชัดเจนในสตรีตั้งครรภ์ที่ได้รับวัคซีน(12, 48)
ตารางที่ 1 วัคซีนที่ควรให้ สามารถให้ได้ และไม่ควรให้ในสตรีตั้งครรภ์
| ประเภทของวัคซีน | วัคซีน | ชนิดของวัคซีน | ช่วงเวลาที่เหมาะสมในการให้วัคซีน | เหตุผลสนับสนุน |
|---|---|---|---|---|
| วัคซีนที่ควรให้ | บาดทะยัก คอตีบ ไอกรน (Tdap) | เชื้อตายและท็อกซอยด์ | 27-36 สัปดาห์ (ช่วง 27-30 สัปดาห์ให้ประสิทธิภาพสูงสุด) | ป้องกันการติดเชื้อในสตรีตั้งครรภ์และสร้างภูมิคุ้มกันส่งให้ทารกตั้งแต่ในครรภ์ |
| ไข้หวัดใหญ่ชนิดเชื้อตาย (inactivated influenza vaccine) | เชื้อตาย | เมื่อตั้งครรภ์ในช่วงที่มีการระบาดของโรค โดยไม่คำนึงถึงอายุครรภ์ (แนะนำให้ในไตรมาส 2-3) | ป้องกันการติดเชื้อซึ่งส่งผลรุนแรงต่อสตรีตั้งครรภ์และทารก | |
| วัคซีนที่สามารถให้ได้เมื่อมีข้อบ่งชี้ | นิวโมคอคคัส (pneumococcal vaccine) | เชื้อตาย | ไตรมาส 2-3 (หากไม่เคยได้รับวัคซีนมาก่อนตั้งครรภ์) | ให้เฉพาะกลุ่มเสี่ยงคือ ผู้ป่วยที่มีโรคเรื้อรัง ตัดม้าม มีภูมิคุ้มกันต่ำ |
| ฮีโมฟีลุสอินฟลูเอนเซ ชนิดบี (haemophilus influenzae type b: Hib vaccine) | เชื้อตาย | ไตรมาส 3 (หากไม่เคยได้รับวัคซีนมาก่อนตั้งครรภ์) | ให้เฉพาะกลุ่มเสี่ยงคือ ผู้ป่วยที่มีโรคเรื้อรัง ตัดม้าม มีภูมิคุ้มกันต่ำ | |
| ไข้กาฬหลังแอ่น (meningococcal vaccine) | เชื้อตาย | –
การศึกษายังไม่มากเพียงพอ |
ให้เฉพาะกลุ่มเสี่ยงคือ ผู้อาศัยในแหล่งที่มีการระบาดของโรค ตัดม้าม ติดเชื้อเอชไอวี | |
| ไวรัสตับอักเสบบี (hepatitis B vaccine) | เชื้อตาย | ตลอดการตั้งครรภ์ (หากตรวจไม่พบภูมิคุ้มกัน anti-HBs: negative) | ให้วัคซีนต่อได้หากเริ่มได้รับวัคซีนมาก่อนตั้งครรภ์ และให้ในกลุ่มเสี่ยงคือ สามีติดเชื้อ คู่นอนหลายคน ใช้ยาเสพติด ติดเชื้อทางเพศสัมพันธ์อื่น ๆ | |
| ไวรัสตับอักเสบเอ (hepatitis A vaccine) | เชื้อตาย | กรณีสัมผัสเชื้อระหว่างการตั้งครรภ์ แนะนำให้ทั้งวัคซีนและอิมมูโนโกลบูลิน | ให้เฉพาะกลุ่มเสี่ยงคือ ผู้สัมผัสกับสิ่งแวดล้อมที่สุขอนามัยไม่ดี และผู้ป่วยที่เสี่ยงอาการรุนแรง เช่น โรคตับ ติดเชื้อเอชไอวี | |
| พิษสุนัขบ้า (rabies vaccine) | เชื้อตาย | กรณีสัมผัสเชื้อระหว่างการตั้งครรภ์ แนะนำให้ทั้งวัคซีนและอิมมูโนโกลบูลิน | ไม่แนะนำในกรณีป้องกันก่อนสัมผัสเชื้อ (pre-exposure prophylaxis) | |
| วัคซีนที่ไม่ควรให้ | คางทูม หัด และหัดเยอรมัน (MMR vaccine) | เชื้อเป็น | ให้ก่อนตั้งครรภ์ (อย่างน้อย 28 วัน) หรือหลังคลอด
(กรณีไม่มีภูมิคุ้มกันและสัมผัสเชื้อ แนะนำให้อิมมูโนโกลบูลิน) |
มีความเสี่ยงตามทฤษฎีเนื่องจากเป็นวัคซีนชนิดเชื้อเป็น แต่การได้รับวัคซีนไม่เป็นข้อบ่งชี้ให้ยุติการตั้งครรภ์ |
| อีสุกอีใส (varicella vaccine) | เชื้อเป็น | ให้ก่อนตั้งครรภ์ (อย่างน้อย 28 วัน) หรือหลังคลอด
(กรณีไม่มีภูมิคุ้มกันและสัมผัสเชื้อ แนะนำให้อิมมูโนโกลบูลิน) |
มีความเสี่ยงตามทฤษฎีเนื่องจากเป็นวัคซีนชนิดเชื้อเป็น แต่การได้รับวัคซีนไม่เป็นข้อบ่งชี้ให้ยุติการตั้งครรภ์ | |
| มะเร็งปากมดลูก (HPV vaccine) | เชื้อตาย | หลังคลอด
(กรณีได้รับวัคซีนมาก่อนและเข็มต่อไปจะต้องได้รับในช่วงตั้งครรภ์แนะนำให้เลื่อนออกไปฉีดหลังคลอด) |
แม้จะเป็นวัคซีนชนิดเชื้อตายแต่การศึกษาการใช้วัคซีนนี้ในสตรีตั้งครรภ์ยังมีไม่เพียงพอ แต่ยังไม่มีรายงานความผิดปกติที่ชัดเจน การได้รับวัคซีนจึงไม่เป็นข้อบ่งชี้ให้ยุติการตั้งครรภ์ |
ที่มา: สร้างตารางโดย พญ.ศิรินาถ ศิริเลิศ หน่วยเวชศาสตร์มารดาและทารก ภาควิชาสูติศาสตร์และนรีเวชวิทยา คณะแพทยศาสตร์ มหาวิทยาลัยเชียงใหม่
วัคซีนที่ควรให้ในช่วงหลังคลอด
ช่วงตั้งครรภ์ เป็นช่วงที่ดีที่จะประเมินประวัติการได้รับวัคซีน สำหรับวัคซีนที่ไม่สามารถให้ได้ในขณะตั้งครรภ์ ควรจะถูกบันทึกและวางแผนที่จะให้ในช่วงหลังคลอด
ในช่วงหลังคลอดสามารถให้วัคซีนได้ทั้งวัคซีนชนิดเชื้อเป็นและเชื้อตาย โดยการให้นมบุตรไม่เป็นข้อบ่งห้ามในการให้วัคซีน(48, 76) ยกเว้น วัคซีนป้องกันฝีดาษและวัคซีนป้องกันไข้เหลืองเนื่องจากมีรายงานการส่งต่อเชื้อผ่านน้ำนมไปยังทารกได้(77, 78)
วัคซีนที่ควรให้ก่อนออกจากโรงพยาบาลคือวัคซีนป้องกันคางทูม หัด หัดเยอรมัน วัคซีนป้องกันอีสุกอีใส(18, 20, 21) และหากระหว่างตั้งครรภ์ไม่ได้รับวัคซีนป้องกันบาดทะยัก คอตีบ ไอกรน (Tdap vaccine) แนะนำให้ในช่วงหลังคลอด เพื่อป้องกันการติดเชื้อในมารดาซึ่งสามารถติดต่อไปยังทารกและเพื่อส่งภูมิคุ้มกันผ่านน้ำนมไปยังทารก(9, 23)
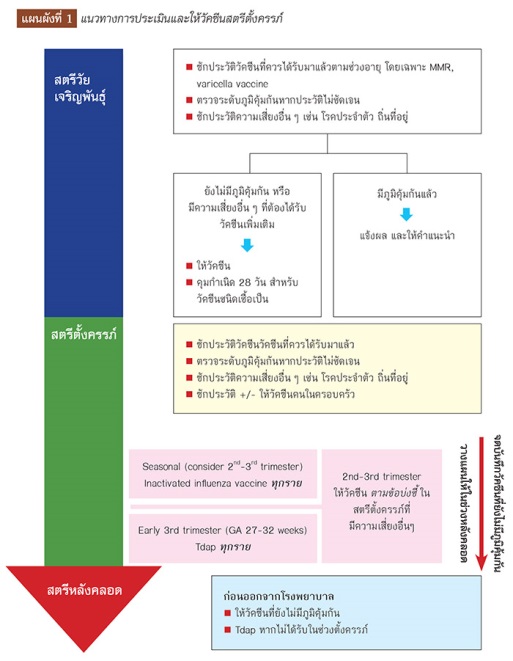
ที่มา: จัดทำโดย พญ.ศิรินาถ ศิริเลิศ หน่วยเวชศาสตร์มารดาและทารก ภาควิชาสูติศาสตร์และนรีเวชวิทยา คณะแพทยศาสตร์ มหาวิทยาลัยเชียงใหม่
บทสรุป
สตรีตั้งครรภ์ทุกรายควรได้รับการซักประวัติการได้รับวัคซีนเพื่อประเมินความเสี่ยงและวัคซีนที่ควรให้ระหว่างตั้งครรภ์ โดยวัคซีนที่สตรีตั้งครรภ์ทุกรายควรได้รับคือวัคซีนป้องกันบาดทะยัก คอตีบ ไอกรน (Tdap) ในช่วงต้นของไตรมาส 3 และวัคซีนป้องกันไข้หวัดใหญ่ชนิดเชื้อตาย (inactivated influenza vaccine) ในช่วงที่มีการระบาดของโรค สำหรับวัคซีนอื่น ๆ พิจารณาให้โดยประเมินจากความเสี่ยงของสตรีตั้งครรภ์แต่ละราย และควรหลีกเลี่ยงวัคซีนชนิดเชื้อเป็น (live attenuated vaccine) และวัคซีนที่ยังมีการศึกษาไม่เพียงพอหากประโยชน์ที่จะได้รับจากวัคซีนไม่คุ้มค่ากับความเสี่ยงต่อการตั้งครรภ์
เอกสารอ้างอิง
1. Förger F, Villiger PM. Immunological adaptations in pregnancy that modulate rheumatoid arthritis disease activity. Nat Rev Rheumatol. 2020;16:113-22.
2. Chaouat G, Dubanchet S, Ledée N. Cytokines: Important for implantation? J Assist Reprod Genet. 2007;24:491-505.
3. Robertson SA, Care AS, Moldenhauer LM. Regulatory T cells in embryo implantation and the immune response to pregnancy. J Clin Invest. 2018;128:4224-35.
4. Arck PC, Hecher K. Fetomaternal immune cross-talk and its consequences for maternal and offspring’s health. Nat Med. 2013;19:548-56.
5. Billingham RE, Brent L, Medawar PB. Actively acquired tolerance of foreign cells. Nature. 1953;172:603-6.
6. Robertson SA, Sharkey DJ. Seminal fluid and fertility in women. Fertil Steril. 2016;106:511-9.
7. Saito S, Shima T, Nakashima A, Inada K, Yoshino O. Role of Paternal Antigen-Specific Treg Cells in Successful Implantation. Am J Reprod Immunol. 2016;75:310-6.
8. Gonik B, Fasano N, Foster S. The obstetrician-gynecologist’s role in adult immunization. Am J Obstet Gynecol. 2002;187:984-8.
9. Chu HY, Englund JA. Maternal immunization. Birth Defects Res. 2017;109:379-86.
10. DeSesso JM, Williams AL, Ahuja A, Bowman CJ, Hurtt ME. The placenta, transfer of immunoglobulins, and safety assessment of biopharmaceuticals in pregnancy. Crit Rev Toxicol. 2012;42:185-210.
11. สมาคมโรคติดเชื้อในเด็กแห่งประเทศไทย. ตารางการให้วัคซีนในเด็กไทย แนะนำโดย สมาคมโรคติดเชื้อในเด็กแห่งประเทศไทย 2563 [Available from: https://www.pidst.or.th/A694.html.
12. กระทรวงสาธารณสุข กก. ตำราวัคซีนและการสร้างเสริมภูมิคุ้มกันโรค ปี 2562 [Available from: https://ddc.moph.go.th/uploads/publish/938420191209023015.pdf.
13. Prepregnancy counseling: Committee Opinion No. 762. Fertil Steril. 2019;111:32-42.
14. Medicine UNLo. Varicella virus vaccine live injection [updated September 15, 2020. Available from: https://dailymed.nlm.nih.gov/dailymed/drugInfo.cfm?setid=524cf052-e90e-4595-af0a-608edbe9bd31#S17.
15. Marin M, Güris D, Chaves SS, Schmid S, Seward JF. Prevention of varicella: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep. 2007;56:1-40.
16. Keller-Stanislawski B, Englund JA, Kang G, et al. Safety of immunization during pregnancy: a review of the evidence of selected inactivated and live attenuated vaccines. Vaccine. 2014;32:7057-64.
17. McLean HQ, Fiebelkorn AP, Temte JL, Wallace GS. Prevention of measles, rubella, congenital rubella syndrome, and mumps, 2013: summary recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep. 2013;62:1-34.
18. American College of Obstetricians and Gynecologists’ Immunization ID, and Public Health Preparedness Expert Work Group with Linda O’Neal Eckert, MD and Laura E. Riley, MD in collaboration with Alisa Kachikis, MD and the University of Washington. Practice Advisory: Management of Pregnant and Reproductive-Aged Women during a Measles Outbreak Reaffirmed September 2020 [Available from: https://www.acog.org/clinical/clinical-guidance/practice-advisory/articles/2019/04/management-of-pregnant-and-reproductive-aged-women-during-a-measles-outbreak.
19. Centers for Disease Control and Prevention. National Center for Immunization and Respiratory Diseases DoVD. Measles (Rubeola): For healthcare professional. [updated November 5, 2020. Available from: https://www.cdc.gov/measles/hcp/index.html.
20. ACOG Committee Opinion No. 741: Maternal Immunization. Obstet Gynecol. 2018;131:e214-e7.
21. ACOG Committee Opinion No. 772: Immunization Implementation Strategies for Obstetrician-Gynecologists. Obstet Gynecol. 2019;133:e254-e9.
22. ACOG Committee Opinion No. 732: Influenza Vaccination During Pregnancy. Obstet Gynecol. 2018;131:e109-e14.
23. ACOG Committee Opinion No. 521: Update on immunization and pregnancy: tetanus, diphtheria, and pertussis vaccination. Obstet Gynecol. 2012;119:690-1.
24. McMillan M, Clarke M, Parrella A, Fell DB, Amirthalingam G, Marshall HS. Safety of Tetanus, Diphtheria, and Pertussis Vaccination During Pregnancy: A Systematic Review. Obstet Gynecol. 2017;129:560-73.
25. Sukumaran L, McCarthy NL, Kharbanda EO, et al. Infant Hospitalizations and Mortality After Maternal Vaccination. Pediatrics. 2018;141.
26. Becerra-Culqui TA, Getahun D, Chiu V, Sy LS, Tseng HF. Prenatal Tetanus, Diphtheria, Acellular Pertussis Vaccination and Autism Spectrum Disorder. Pediatrics. 2018;142.
27. Kerr SM, Van Bennekom CM, Mitchell AA. Tetanus, diphtheria, and pertussis vaccine (Tdap) in pregnancy and risk of major birth defects in the offspring. Birth Defects Res. 2020;112:393-403.
28. Pickering LK, Baker CJ, Freed GL, et al. Immunization programs for infants, children, adolescents, and adults: clinical practice guidelines by the Infectious Diseases Society of America. Clin Infect Dis. 2009;49:817-40.
29. Forsyth K, Plotkin S, Tan T, Wirsing von König CH. Strategies to decrease pertussis transmission to infants. Pediatrics. 2015;135:e1475-82.
30. Gerbie MV, Tan TQ. Pertussis disease in new mothers: effect on young infants and strategies for prevention. Obstet Gynecol. 2009;113:399-401.
31. Bisgard KM, Pascual FB, Ehresmann KR, et al. Infant pertussis: who was the source? Pediatr Infect Dis J. 2004;23:985-9.
32. Wendelboe AM, Njamkepo E, Bourillon A, et al. Transmission of Bordetella pertussis to young infants. Pediatr Infect Dis J. 2007;26:293-9.
33. Romanin V, Acosta AM, Juarez MDV, et al. Maternal Vaccination in Argentina: Tetanus, Diphtheria, and Acellular Pertussis Vaccine Effectiveness During Pregnancy in Preventing Pertussis in Infants <2 Months of Age. Clin Infect Dis. 2020;70:380-7.
34. Amirthalingam G, Andrews N, Campbell H, et al. Effectiveness of maternal pertussis vaccination in England: an observational study. Lancet. 2014;384:1521-8.
35. Committee Opinion No. 718: Update on Immunization and Pregnancy: Tetanus, Diphtheria, and Pertussis Vaccination. Obstet Gynecol. 2017;130:e153-e7.
36. Liang JL, Tiwari T, Moro P, et al. Prevention of Pertussis, Tetanus, and Diphtheria with Vaccines in the United States: Recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep. 2018;67:1-44.
37. Halperin BA, Morris A, Mackinnon-Cameron D, et al. Kinetics of the antibody response to tetanus-diphtheria-acellular pertussis vaccine in women of childbearing age and postpartum women. Clin Infect Dis. 2011;53:885-92.
38. Healy CM, Rench MA, Baker CJ. Importance of timing of maternal combined tetanus, diphtheria, and acellular pertussis (Tdap) immunization and protection of young infants. Clin Infect Dis. 2013;56:539-44.
39. Abu Raya B, Srugo I, Kessel A, et al. The effect of timing of maternal tetanus, diphtheria, and acellular pertussis (Tdap) immunization during pregnancy on newborn pertussis antibody levels – a prospective study. Vaccine. 2014;32:5787-93.
40. Healy CM, Rench MA, Swaim LS, et al. Association Between Third-Trimester Tdap Immunization and Neonatal Pertussis Antibody Concentration. JAMA. 2018;320:1464-70.
41. Abraham C, Pichichero M, Eisenberg J, Singh S. Third-Trimester Maternal Vaccination Against Pertussis and Pertussis Antibody Concentrations. Obstet Gynecol. 2018;131:364-9.
42. Eberhardt CS, Blanchard-Rohner G, Lemaître B, et al. Maternal Immunization Earlier in Pregnancy Maximizes Antibody Transfer and Expected Infant Seropositivity Against Pertussis. Clin Infect Dis. 2016;62:829-36.
43. Grohskopf LA, Alyanak E, Broder KR, et al. Prevention and Control of Seasonal Influenza with Vaccines: Recommendations of the Advisory Committee on Immunization Practices – United States, 2020-21 Influenza Season. MMWR Recomm Rep. 2020;69:1-24.
44. Kumar A, Meldgaard TS, Bertholet S. Novel Platforms for the Development of a Universal Influenza Vaccine. Front Immunol. 2018;9:600.
45. Galvao TF, Silva MT, Zimmermann IR, Lopes LA, Bernardo EF, Pereira MG. Influenza vaccination in pregnant women: a systematic review. ISRN Prev Med. 2013;2013:879493.
46. Blanchard-Rohner G, Meier S, Bel M, et al. Influenza vaccination given at least 2 weeks before delivery to pregnant women facilitates transmission of seroprotective influenza-specific antibodies to the newborn. Pediatr Infect Dis J. 2013;32:1374-80.
47. Kim DK, Hunter P. Advisory Committee on Immunization Practices Recommended Immunization Schedule for Adults Aged 19 Years or Older – United States, 2019. MMWR Morb Mortal Wkly Rep. 2019;68:115-8.
48. Freedman MS, Hunter P, Ault K, Kroger A. Advisory Committee on Immunization Practices Recommended Immunization Schedule for Adults Aged 19 Years or Older – United States, 2020. MMWR Morb Mortal Wkly Rep. 2020;69:133-5.
49. Quiambao BP, Nohynek HM, Käyhty H, et al. Immunogenicity and reactogenicity of 23-valent pneumococcal polysaccharide vaccine among pregnant Filipino women and placental transfer of antibodies. Vaccine. 2007;25:4470-7.
50. Prevention of pneumococcal disease: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep. 1997;46:1-24.
51. Chaithongwongwatthana S, Yamasmit W, Limpongsanurak S, Lumbiganon P, Tolosa JE. Pneumococcal vaccination during pregnancy for preventing infant infection. Cochrane Database Syst Rev. 2015;1:Cd004903.
52. Cohn AC, MacNeil JR, Clark TA, et al. Prevention and control of meningococcal disease: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep. 2013;62:1-28.
53. ACOG Practice Bulletin No. 86: Viral hepatitis in pregnancy. Obstet Gynecol. 2007;110:941-56.
54. Terrault NA, Bzowej NH, Chang KM, Hwang JP, Jonas MM, Murad MH. AASLD guidelines for treatment of chronic hepatitis B. Hepatology. 2016;63:261-83.
55. WHO Guidelines Approved by the Guidelines Review Committee. Guidelines for the Prevention, Care and Treatment of Persons with Chronic Hepatitis B Infection. Geneva: World Health Organization Copyright (c) World Health Organization 2015.; 2015.
56. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection. J Hepatol. 2017;67:370-98.
57. Elinav E, Ben-Dov IZ, Shapira Y, et al. Acute hepatitis A infection in pregnancy is associated with high rates of gestational complications and preterm labor. Gastroenterology. 2006;130:1129-34.
58. McDuffie RS, Jr., Bader T. Fetal meconium peritonitis after maternal hepatitis A. Am J Obstet Gynecol. 1999;180:1031-2.
59. Moro PL, Museru OI, Niu M, Lewis P, Broder K. Reports to the Vaccine Adverse Event Reporting System after hepatitis A and hepatitis AB vaccines in pregnant women. Am J Obstet Gynecol. 2014;210:561.e1-6.
60. Groom HC, Smith N, Irving SA, et al. Uptake and safety of hepatitis A vaccination during pregnancy: A Vaccine Safety Datalink study. Vaccine. 2019;37:6648-55.
61. Nelson NP, Weng MK, Hofmeister MG, et al. Prevention of Hepatitis A Virus Infection in the United States: Recommendations of the Advisory Committee on Immunization Practices, 2020. MMWR Recomm Rep. 2020;69:1-38.
62. Sudarshan MK, Giri MS, Mahendra BJ, et al. Assessing the safety of post-exposure rabies immunization in pregnancy. Hum Vaccin. 2007;3:87-9.
63. Suarez VR, Hankins GD. Smallpox and pregnancy: from eradicated disease to bioterrorist threat. Obstet Gynecol. 2002;100:87-93.
64. Bower WA, Schiffer J, Atmar RL, et al. Use of Anthrax Vaccine in the United States: Recommendations of the Advisory Committee on Immunization Practices, 2019. MMWR Recomm Rep. 2019;68:1-14.
65. Psarris A, Sindos M, Daskalakis G, et al. Immunizations during pregnancy: How, when and why. Eur J Obstet Gynecol Reprod Biol. 2019;240:29-35.
66. Swamy GK, Heine RP. Vaccinations for pregnant women. Obstet Gynecol. 2015;125:212-26.
67. Revised ACIP recommendation for avoiding pregnancy after receiving a rubella-containing vaccine. MMWR Morb Mortal Wkly Rep. 2001;50:1117.
68. Wilson E, Goss MA, Marin M, et al. Varicella vaccine exposure during pregnancy: data from 10 Years of the pregnancy registry. J Infect Dis. 2008;197 Suppl 2:S178-84.
69. Bohlke K, Galil K, Jackson LA, et al. Postpartum varicella vaccination: is the vaccine virus excreted in breast milk? Obstet Gynecol. 2003;102:970-7.
70. Oshman LD, Davis AM. Human Papillomavirus Vaccination for Adults: Updated Recommendations of the Advisory Committee on Immunization Practices (ACIP). JAMA. 2020;323:468-9.
71. Petrosky E, Bocchini JA, Jr., Hariri S, et al. Use of 9-valent human papillomavirus (HPV) vaccine: updated HPV vaccination recommendations of the advisory committee on immunization practices. MMWR Morb Mortal Wkly Rep. 2015;64:300-4.
72. Markowitz LE, Dunne EF, Saraiya M, Lawson HW, Chesson H, Unger ER. Quadrivalent Human Papillomavirus Vaccine: Recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep. 2007;56:1-24.
73. Moro PL, Broder K, Zheteyeva Y, et al. Adverse events in pregnant women following administration of trivalent inactivated influenza vaccine and live attenuated influenza vaccine in the Vaccine Adverse Event Reporting System, 1990-2009. Am J Obstet Gynecol. 2011;204:146.e1-7.
74. The role of BCG vaccine in the prevention and control of tuberculosis in the United States. A joint statement by the Advisory Council for the Elimination of Tuberculosis and the Advisory Committee on Immunization Practices. MMWR Recomm Rep. 1996;45:1-18.
75. Dooling KL, Guo A, Patel M, et al. Recommendations of the Advisory Committee on Immunization Practices for Use of Herpes Zoster Vaccines. MMWR Morb Mortal Wkly Rep. 2018;67:103-8.
76. Sachs HC. The transfer of drugs and therapeutics into human breast milk: an update on selected topics. Pediatrics. 2013;132:e796-809.
77. Staples JE, Bocchini JA, Jr., Rubin L, Fischer M. Yellow Fever Vaccine Booster Doses: Recommendations of the Advisory Committee on Immunization Practices, 2015. MMWR Morb Mortal Wkly Rep. 2015;64:647-50.
78. Transmission of yellow fever vaccine virus through breast-feeding – Brazil, 2009. MMWR Morb Mortal Wkly Rep. 2010;59:130-2.

