การตรวจคัดกรองมะเร็งปากมดลูกสำหรับสตรีไทย
(Cervical cancer screening for Thais)
อ.พญ.ชลัยธร นันทสุภา
ศ.นพ.จตุพล ศรีสมบูรณ์
บทนำ
ในระยะเวลาสองปีที่ผ่านมา ได้มีการปรับปรุงแนวทางการคัดกรองมะเร็งปากมดลูก และการดูแลรักษาผลการคัดกรองมะเร็งปากมดลูกที่ผิดปกติ ซึ่งส่วนใหญ่ปรับปรุงจากความรู้ที่เพิ่มมากขึ้น ทั้งในส่วนของธรรมชาติของการติดเชื้อ human papilloma virus (HPV) การดำเนินโรคเป็นมะเร็งปากมดลูก อุบัติการณ์ของการเกิดโรคและอัตราการเสียชีวิตจากโรคมะเร็งปากมดลูกในแต่ละกลุ่มอายุ รวมถึงการศึกษาเปรียบเทียบสมรรถนะการคัดกรองมะเร็งปากมดลูกด้วยวิธีต่าง ๆ จากความเปลี่ยนแปลงในแนวทางการตรวจคัดกรองมะเร็งปากมดลูกของสมาคมมะเร็งอเมริกัน (American Cancer Society, ACS) ฉบับ ค.ศ. 2020(1) และการดูแลรักษาผลการตรวจคัดกรองมะเร็งปากมดลูกที่ผิดปกติของสมาคมคอลโปสโคปีและพยาธิวิทยาปากมดลูกอเมริกัน (American Society of Colposcopy and Cervical Pathology, ASCCP) ฉบับ ค.ศ. 2019(2) ที่ได้มีการกล่าวถึงที่มาที่ไปโดยละเอียดในบทก่อนหน้า ประเทศไทยก็ได้มีการปรับปรุงแนวทางการตรวจคัดกรองมะเร็งปากมดลูก และการดูแลรักษาผลการตรวจคัดกรองที่ผิดปกติ ให้เหมาะสมตามบริบทด้านโครงสร้างพื้นฐาน (infrastructure) ของการให้บริการทางสาธารณสุข ทรัพยากร ความพร้อมของการตรวจทางห้องปฏิบัติการและเซลล์วิทยาภายในประเทศ โดย ราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย (The Royal Thai College of Obstetricians and Gynaecologists, RTCOG) สมาคมมะเร็งนรีเวชไทย ร่วมกับชมรมคอลโปสโคปีและพยาธิสภาพปากมดลูกแห่งประเทศไทย ได้จัดทำเรียบเรียงแนวทางการตรวจคัดกรองมะเร็งปากมดลูกขึ้น ฉบับปรับปรุงล่าสุดอนุมัติเมื่อปีค.ศ. 2020 ซึ่งจะได้นำมาสรุปลงในบทความนี้
การพิจารณาการตรวจคัดกรองมะเร็งปากมดลูกในแต่ละภูมิภาค
สิ่งที่ควรพิจารณาในการตรวจคัดกรองมะเร็งปากมดลูกในแต่ละภูมิภาค ได้แก่ การตรวจหารอยโรคก่อนมะเร็งให้ได้มากที่สุด ความคุ้มค่าของการใช้ทรัพยากร ความสะดวกในการปฏิบัติและการแปลผล และลดภยันตรายจากการรักษาเกินความจำเป็น (maximize benefits & minimize harms)(3)
การที่จะสามารถตรวจหารอยโรคก่อนมะเร็งให้ได้มากที่สุด จำเป็นต้องทราบความชุกของโรค อัตราการเกิดผลลบลวง (false negative) ของวิธีการตรวจคัดกรอง และความเสี่ยงต่อโรคมะเร็งปากมดลูกของสตรีในพื้นที่นั้น ๆ
การพิจารณาความคุ้มค่าของการใช้ทรัพยากร จำเป็นต้องทราบ ประสิทธิผลของการตรวจคัดกรองวิธีต่าง ๆ ค่าใช้จ่ายที่เกิดขึ้นจริง รวมถึงอัตราการเกิดผลบวกลวง (false positive) ซึ่งอาจนำไปสู่การรักษาเกินความจำเป็น (overtreatment)
วิธีการตรวจคัดกรองมะเร็งปากมดลูกในประเทศไทย
วิธีการตรวจคัดกรองมะเร็งปากมดลูกที่มีให้บริการในประเทศไทยในปัจจุบันนี้ มี 3 วิธี(4) ได้แก่
1. การตรวจหาเชื้อ HPV (HPV testing)
ปัจจุบันมีทั้งแบบที่มีการระบุสายพันธุ์จำเพาะของเชื้อ high-risk HPV โดยเฉพาะ HPV 16 และ HPV 18 และแบบที่ตรวจหาเชื้อ HPV โดยไม่มีการระบุสายพันธุ์จำเพาะ
1.1 การตรวจ HPV testing เบื้องต้นอย่างเดียว (primary HPV testing)
1.2 การตรวจ HPV testing ร่วมกับการตรวจ cervical cytology (Co-testing)
2. การตรวจเซลล์วิทยาของปากมดลูก (cervical cytology)
มี 2 วิธี ได้แก่ การตรวจแบบดั้งเดิม (conventional cytology หรือ Papanicolaou smear) และการตรวจแบบ liquid-based cytology
3. การตรวจปากมดลูกด้วยน้ำส้มสายชูร่วมกับการจี้ปากมดลูกด้วยความเย็น (visual inspection with acetic acid, VIA)
เป็นการตรวจโดยใช้สารละลาย acetic acid เจือจาง ร้อยละ 3-5 ชโลมลงบนปากมดลูกนาน 1-2 นาที แล้วสังเกตการเปลี่ยนแปลงของการเกิดฝ้าขาวบนเยื่อบุปากมดลูก (acetowhite) การตรวจวิธีนี้ควรทำโดยบุคลากรที่ได้รับการฝึกอบรมทางด้านนี้มา และเหมาะสมเฉพาะในรายที่เห็น squamo-columnar junction (SCJ) ครบชัดเจนเท่านั้น การตรวจคัดกรองวิธีนี้เป็นทางเลือกหนึ่ง ในกระบวนการตรวจคัดกรองมะเร็งปากมดลูกสำหรับพื้นที่ที่มีทรัพยากรจำกัด (low-resource settings)(4)
เปรียบเทียบการคัดกรองมะเร็งปากมดลูกตามคำแนะนำของ RTCOG และของ ACS
สิ่งที่แตกต่างกันระหว่างการตรวจคัดกรองมะเร็งปากมดลูกในประเทศไทย และสหรัฐอเมริกา(1) ได้แก่ อายุที่เริ่มตรวจ รูปแบบการตรวจ และ ความถี่ในการคัดกรอง ดังสรุปไว้ในตารางที่ 1
ตารางที่ 1 เปรียบเทียบคำแนะนำการตรวจคัดกรองมะเร็งปากมดลูกของ ราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย (RTCOG) สมาคมมะเร็งนรีเวชไทย ร่วมกับชมรมคอลโปสโคปีและพยาธิสภาพปากมดลูกแห่งประเทศไทย ค.ศ. 2020 กับ ACS ฉบับค.ศ. 2020
| อายุ | คำแนะนำของ RTCOG ค.ศ. 2020 | คำแนะนำของ ACS ค.ศ. 2020 |
| น้อยกว่า 25 ปี | – ไม่แนะนำให้ตรวจคัดกรอง* | – ไม่ตรวจคัดกรอง |
| 25-65 ปี | – เริ่มตรวจคัดกรองที่อายุ 25 ปี (เมื่อมีเพศสัมพันธ์แล้ว) หรือ 30 ปี (เมื่อยังไม่มีเพศสัมพันธ์) ด้วยวิธีใด ๆ ต่อไปนี้
– Primary HPV testing หรือ Co-testing ทุก 5 ปี – Cytology อย่างเดียว ทุก 2 ปี** |
– เริ่มตรวจคัดกรองที่อายุ 25 ปี ด้วยวิธีใดๆต่อไปนี้
– Primary HPV testing ทุก 5 ปี (แนะนำ) – Co-testing ทุก 5 ปี หรือ cytology อย่างเดียว ทุก 3 ปี (ยอมรับได้) ในกรณีที่ไม่มี HPV tests ที่ FDA รับรองให้ใช้สำหรับ primary HPV testing* |
| 30-45 ปี | – ในพื้นที่ที่การดำเนินการตรวจคัดกรองโดยเซลล์วิทยา/HPV testing ไม่สามารถเชื่อมโยงกับการรักษาได้อย่างมีประสิทธิผล และ/หรือมีความครอบคลุมต่ำกว่าเป้าหมาย ให้ตรวจคัดกรองโดยวิธี VIA และรักษาโดยวิธีจี้เย็น ทุก 5 ปี*** | – ไม่มีคำแนะนำการตรวจคัดกรองด้วยวิธีนี้ |
| > 65 ปี | – หยุดตรวจคัดกรองได้ถ้าผลตรวจ คัดกรองก่อนหน้านี้ปกติติดต่อกันในช่วง 10 ปีที่ผ่านมา- สตรีที่ยังคงมีเพศสัมพันธ์หรือ มีคู่นอนหลายคน ควรตรวจคัดกรองต่อไปตามปกติ |
– หยุดตรวจคัดกรองได้ ถ้าผลตรวจ คัดกรองก่อนหน้านี้ปกติติดต่อกันในช่วง 10 ปีที่ผ่านมาโดยการตรวจล่าสุดอยู่ในช่วง 3-5 ปีที่ผ่านมา- สตรีที่ไม่มีผลการตรวจ คัดกรองก่อนหน้านี้อย่างเป็นลายลักษณ์อักษรควรตรวจคัดกรองต่อไปจนกว่าจะถึงเกณฑ์ของการหยุดตรวจคัดกรอง |
| หลังตัดมดลูกและปากมดลูก | – สตรีที่ตัดมดลูกพร้อมกับปากมดลูกออกแล้วและไม่มีประวัติเป็น cervical intraepithelial neoplasia (CIN) หรือมะเร็งปากมดลูก ไม่จำเป็นต้องตรวจคัดกรอง | – ถ้าไม่มีปากมดลูกและไม่มีประวัติเป็น CIN2+ ในช่วง 25 ปีที่ผ่านมา ไม่ควรตรวจ คัดกรอง |
* ยกเว้นในสตรีที่มีความเสี่ยงสูง เช่น ติดเชื้อเอชไอวี มีคู่นอนหลายคน เป็นโรคติดเชื้อทางเพศสัมพันธ์
** ความถี่ในการตรวจคัดกรองอาจปรับเปลี่ยนได้ตามความเหมาะสมของบริบทในแต่ละพื้นที่ เช่น อาจทำการตรวจคัดกรองทุก 1 ปี ในพื้นที่ที่มีความชุกของโรคมะเร็งปากมดลูกสูง หรือในพื้นที่ที่มีอัตราผลลบลวง (false negative) สูงในการตรวจ cervical cytology หรือในสตรีที่มีความเสี่ยงสูงต่อการเป็นมะเร็งปากมดลูก
***ควรทำในรายที่เห็น squamo-columnar junction (SCJ) ครบชัดเจนเท่านั้น
ที่มา: สร้างตารางโดย ชลัยธร นันทสุภา หน่วยมะเร็งวิทยานรีเวช ภาควิชาสูติศาสตร์และนรีเวชวิทยา คณะแพทยศาสตร์ มหาวิทยาลัยเชียงใหม่
ผลการตรวจคัดกรองที่ปกติ
หมายถึง การไม่พบการติดเชื้อ high-risk HPV และผลตรวจทางเซลล์วิทยาปกติ ซึ่งต้องประกอบด้วย satisfactory for evaluation (มี endocervical/transformation zone component และ การแปลผลว่า negative for intraepithelial lesion or malignancy)
แม้ในช่วงที่เว้นจากการตรวจคัดกรองมะเร็งปากมดลูก แต่สตรีไทยยังควรมารับการตรวจภายในเพื่อหาโรคทางนรีเวชอื่น ๆ เป็นประจำทุกปี
การตรวจคัดกรองมะเร็งปากมดลูกในข้อพิจารณาพิเศษ
จากคำแนะนำสากล รวมถึงประเทศไทย สตรีที่เคยได้รับวัคซีนป้องกันมะเร็งปากมดลูกแล้ว ยังต้องรับการตรวจคัดกรองมะเร็งปากมดลูกเช่นเดียวกับสตรีทั่วไป(1, 4, 5) แต่ในสตรีที่มีความเสี่ยงสูงต่อการเกิดมะเร็งปากมดลูก หรือสตรีที่เคยได้รับการวินิจฉัยรอยโรคก่อนมะเร็ง หรือ มะเร็งปากมดลูกมาแล้วนั้น ยังคงมีความเสี่ยงสูงต่อการคงอยู่หรือกลับเป็นซ้ำของโรค ควรได้รับการตรวจติดตามเป็นพิเศษ ดังนี้
1. สตรีที่มีภาวะภูมิคุ้มกันบกพร่อง
ควรได้รับการตรวจคัดกรองด้วยวิธีการตรวจเซลล์วิทยาของปากมดลูก (cervical cytology) ทุก 1 ปี และควรเริ่มตรวจคัดกรองภายในปีแรกหลังจากมีเพศสัมพันธ์ เมื่ออายุ 30 ปีขึ้นไป แนะนำให้ตรวจคัดกรองด้วยวิธี co-testing ต่อทุก 3 ปี(2) คำจำกัดความของสตรีที่มีภูมิคุ้มกันบกพร่องที่ควรได้รับการตรวจคัดกรองมะเร็งปากมดลูกเป็นกรณีพิเศษนั้น นอกจากสตรีที่ติดเชื้อ HIV แล้ว ยังรวมถึง สตรีกลุ่มที่ได้รับการปลูกถ่ายอวัยวะ ปลูกถ่ายไขกระดูก และโรคภูมิคุ้มกันต้านเนื้อเยื่อตนเอง (autoimmune disease) ที่ต้องได้รับยากดภูมิคุ้มกัน (immunosuppressive treatment) เช่น โรค systemic lupus erythematosus (SLE) โรคข้ออักเสบรูมาตอยท์ (rheumatoid arthritis) และโรคลำไส้แปรปรวน (irritable bowel syndrome)(6)
2. สตรีที่เคยได้รับการรักษารอยโรคก่อนมะเร็ง (CIN2-3/ Adenocarcinoma in situ: AIS) หรือมะเร็งปากมดลูก
ควรได้รับการตรวจติดตามอย่างต่อเนื่อง จนครบ 25 ปี เนื่องจากยังมีความเสี่ยงต่อการคงอยู่ หรือกลับเป็นซ้ำของโรค(2)
การดูแลสำหรับผลตรวจคัดกรองเบื้องต้นที่ผิดปกติตามคำแนะนำของราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย (RTCOG)
ASCCP ฉบับ ค.ศ. 2019(2) ได้เปลี่ยนแปลงแนวทางการดูแลรักษาจากปีค.ศ. 2012(7) ที่มีการนำผลการตรวจคัดกรอง หรือประวัติการรักษาในอดีตมาประกอบการพิจารณาร่วมกับผลการตรวจในปัจจุบัน และการดูแลรักษาในแต่ละครั้งนั้นจะพิจารณาตามความเสี่ยงต่อการมีรอยโรค CIN3+ เป็นหลัก โดยแม้ผลการตรวจคัดกรองในปัจจุบันจะเหมือนกัน แต่ความเสี่ยงของการมีรอยโรค CIN3+ อาจแตกต่างกันแต่ละบุคคล ขึ้นกับประวัติในอดีต นำไปสู่การได้รับการดูแลรักษาต่อที่แตกต่างกัน อย่างไรก็ตามสำหรับประเทศไทยนั้น โดยส่วนใหญ่ยังมีแนวทางการดูแลรักษาใกล้เคียงกับ ASCCP ฉบับ ค.ศ. 2012(7) เนื่องจากในประเทศไทยยังมิได้ใช้ HPV testing เป็น primary HPV screening นอกจากนี้ ในหลายพื้นที่ยังมีข้อจำกัดในแง่ของการตรวจทางห้องปฏิบัติการและค่าใช้จ่าย การนำประวัติในอดีตด้านการตรวจ HPV testing ก็ยังมีน้อย อย่างไรก็ตาม ราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย ได้อนุมัติการออกแนวทางปฏิบัติ เรื่อง การดูแลสตรีที่ผลการตรวจคัดกรองมะเร็งปากมดลูกผิดปกติ ในปี พ.ศ. 2563 ขึ้น โดยมีการพิจารณาดูแลรักษาผลการตรวจคัดกรองที่ผิดปกติเบื้องต้น จำแนกตามวิธีการตรวจคัดกรองมะเร็งปากมดลูกในประเทศไทย 3 วิธี ดังนี้(4, 8, 9)
1. ความผิดปกติจากวิธีการตรวจหาเชื้อ HPV (HPV testing)
1.1 Primary HPV testing คือการตรวจพบการติดเชื้อ high-risk HPV แนะนำให้พิจารณาตามผลการตรวจ HPV 16/18 partial genotyping
ก) ตรวจพบ HPV 16 หรือ 18 แนะนำให้ส่งตรวจปากมดลูกด้วยกล้องส่องตรวจช่องคลอด (colposcopy)
ข) ตรวจพบ HPV สายพันธุ์อื่น ๆ ที่มิใช่ HPV 16 หรือ 18 แนะนำให้ทำการตรวจ cervical cytology (reflex cytology) ต่อไป(10) ถ้าผลการตรวจ cervical cytology ปกติ แนะนำให้ตรวจติดตามด้วย co-testing ที่ 1 ปี แต่ถ้าผลการตรวจ cervical cytology ผิดปกติรุนแรงมากกว่าหรือเท่ากับ ASC-US แนะนำให้ตรวจ colposcopy
1.2 HPV testing ร่วมกับการตรวจ cervical cytology (Co-testing) สามารถพบความผิดปกติได้ 5 รูปแบบ ได้แก่
ก) ตรวจพบการติดเชื้อ high-risk HPV แต่ตรวจ cervical cytology ไม่พบความผิดปกติ อาจเลือกการดูแลรักษาต่อได้ 2 แนวทาง ได้แก่
ก1) ตรวจ HPV 16/18 partial genotyping โดยหากพบเชื้อ HPV 16 หรือ 18 ให้ส่งตรวจ colposcopy แต่ถ้าไม่พบเชื้อ HPV 16 หรือ 18 แนะนำให้ตรวจติดตามด้วย co-testing ที่ 1 ปี
ก2) ตรวจติดตาม co-testing ซ้ำในอีก 12 เดือน หากผลผิดปกติอย่างใดอย่างหนึ่ง แนะนำให้ส่งตรวจ colposcopy แต่หากผลการตรวจไม่พบความผิดปกติในทั้ง 2 วิธี ให้ตรวจ co-testing อีกครั้งเมื่อครบ 1 ปี(10)
ข) ผลการตรวจ cervical cytology ไม่พบเซลล์ผิดปกติ แต่เป็น unsatisfactory for evaluation ให้พิจารณาการรักษาตามผลตรวจ HPV ที่ได้ เช่น หากพบ HPV 16 หรือ HPV 18 ให้ส่งตรวจ colposcopy หากพบ HPV สายพันธุ์อื่น ๆ ที่มิใช่ HPV 16 หรือ 18 อาจส่งตรวจ colposcopy หรือทำการตรวจ cervical cytology ซ้ำใน 8-16 สัปดาห์(2)
ค) ตรวจไม่พบ high-risk HPV แต่ผลการตรวจ cervical cytology เป็น ASC-US แนะนำให้ตรวจ co-testing อีกครั้งที่ 3 ปี หากผลการตรวจผิดปกติอย่างใดอย่างหนึ่งให้ส่งตรวจ colposcopy แต่หากผลการตรวจไม่พบความผิดปกติทั้ง 2 วิธี แนะนำให้ตรวจคัดกรองอีกครั้งเมื่อครบ 5 ปี
ง) ตรวจพบการติดเชื้อ high-risk HPV ร่วมกับ cervical cytology เป็น ASC-US และ ให้ส่งตรวจ colposcopy
จ) ผลการตรวจ cervical cytology ผิดปกติรุนแรงมากกว่า ASC-US แนะนำให้ส่งตรวจ colposcopy โดยไม่คำนึงถึงผลการตรวจ HPV testing ยกเว้น ผล low grade squamous intraepithelium neoplasia (LSIL) ที่ตรวจไม่พบ high risk-HPV ควรตรวจติดตามด้วย co-testing ที่ 1 ปี
2. ความผิดปกติจากวิธีการตรวจเซลล์วิทยาของปากมดลูก (cervical cytology)
2.1) ผลการตรวจ cervical cytology ไม่พบเซลล์ผิดปกติ (negative for intraepithelial lesion or malignancy, NILM) แต่ไม่มี endocervical/transformation zone component หมายความว่าเซลล์ที่เก็บมาอาจไม่ได้เก็บในตำแหน่งที่เหมาะสมบริเวณ transformation zone
ก) ในสตรีอายุน้อยกว่า 30 ปี แนะนำให้ตรวจ cervical cytology อีกครั้งที่ 2 ปี
ข) ในสตรีอายุ 30 ปีขี้นไป แนะนำให้ทำการส่งตรวจ HPV testing เพิ่มเติมและให้การดูแลรักษาตามผลที่ได้ เช่น หากไม่พบ high-risk HPV ให้ตรวจซ้ำที่ 5 ปี หากพบ HPV 16 หรือ HPV 18 ให้ส่งตรวจ colposcopy ในกรณีที่ไม่สามารถส่งตรวจ HPV testing ได้ แนะนำให้ตรวจ cervical cytology อีกครั้งที่ 2 ปี
ค) ในสตรีตั้งครรภ์ทุกอายุ แนะนำให้นัดตรวจซ้ำหลังคลอด 6 สัปดาห์
ง) สตรีกลุ่มเสี่ยง ให้นัดตรวจซ้ำเร็วขึ้นที่ 6 เดือน ได้แก่ สตรีที่มีลักษณะดังต่อไปนี้
- มีประวัติ cervical epithelial cell abnormalities
- มีประวัติเคยตรวจพบ high-risk HPV ภายใน 12 เดือนที่ผ่านมา
- ในขณะที่ตรวจ ผู้ตรวจไม่เห็นปากมดลูกชัดเจน หรือไม่สามารถเก็บสิ่งส่งตรวจจากปากมดลูกได้ดี
- มีภาวะภูมิคุ้มกันบกพร่อง
- ไม่เคยได้รับการตรวจคัดกรองมาก่อน
จ) ในกรณีที่พบเลือด หรือการอักเสบ หรือมี air-drying artifact ให้ตรวจซ้ำใน 1 ปี
2.2) ผลการตรวจเป็น “unsatisfactory for evaluation”
ก) หากเกิดจากการมีจำนวน squamous cell น้อยกว่าที่กำหนดไว้ใน Bethesda System 2014 ว่าเพียงพอต่อการแปลผล (น้อยกว่า 8,000-12,000 เซลล์ จาก conventional Pap smear หรือ น้อยกว่า 5,000 เซลล์ จาก liquid-based preparation)(11) ควรทำการตรวจซ้ำใน 8-16 สัปดาห์
ข) หากเกิดจากคุณภาพของเซลล์ไม่เหมาะสมในการตรวจ เช่น มีการอักเสบติดเชื้อ ให้ทำการรักษาตามสาเหตุ แล้วตรวจซ้ำใน 8-16 สัปดาห์ ถ้าผลจากการตรวจซ้ำยังคงเป็น unsatisfactory smear จากเลือด การอักเสบ หรือ มีลักษณะของเนื้อเยื่อตาย (necrosis) ให้ส่งตรวจ colposcopy
2.3) ผลการตรวจ cervical cytology พบเซลล์ผิดปกติเป็น ASC-US
การดูแลรักษามีทางเลือก 3 แนวทาง โดยเลือกพิจารณาตามความเหมาะสมกับศักยภาพของสถานพยาบาล ความวิตกกังวลเรื่องมะเร็ง และเศรษฐานะของผู้ป่วย(10, 12-14)
ก) ตรวจ HPV testing (reflex HPV testing) ในประเทศไทยการตรวจหาเชื้อ HPV ยังมีราคาสูงและไม่รวมอยู่ในสิทธิ์การรักษาประกันสุขภาพถ้วนหน้า อาจพิจารณาในสตรีที่มีเศรษฐานะเหมาะสม และมีห้องปฏิบัติการรองรับ ถ้าผลการตรวจไม่พบ high-risk HPV ให้นัดตรวจ co-testing ซ้ำที่ 3 ปี ถ้าผลตรวจพบ high-risk HPV ให้ส่งตรวจ colposcopy
หมายเหตุ ในสตรีที่อายุน้อยกว่า 25 ปี ถ้าผลการตรวจไม่พบเชื้อ high-risk HPV ให้ตรวจตามปกติ คือ cervical cytology ที่ 3 ปี แต่ถ้าตรวจพบ high-risk HPV ให้ตรวจ cervical cytology ซ้ำที่ 12 และ 24 เดือน โดยจะส่งตรวจ colposcopy เมื่อผล cervical cytology ที่ 12 เดือนผิดปกติรุนแรงขึ้นเป็นมากกว่าหรือเท่ากับ ASC-H หรือ ผลตรวจที่ 24 เดือนผิดปกติรุนแรงกว่าหรือเท่ากับ ASC-US ถ้าผลตรวจที่ 12 และ 24 เดือนเป็นปกติทั้ง 2 ครั้ง ให้ตรวจตามปกติ
ข) ส่งตรวจ colposcopy แนวทางนี้อาจพิจารณาในสถาบันที่มีความพร้อมในการตรวจ ในสตรีที่มีความวิตกกังวล มีความเสี่ยงสูงต่อการเป็นมะเร็งปากมดลูก ในพื้นที่ที่มีความชุกของรอยโรคก่อนมะเร็งปากมดลูกสูง หรือเสี่ยงต่อการไม่กลับมารับการตรวจติดตาม ถ้าผลการตรวจปกติให้นัดตรวจ cervical cytology ซ้ำที่ 12 เดือน
หมายเหตุ ไม่แนะนำให้ดูแลรักษาด้วยวิธีนี้ในสตรีที่อายุน้อยกว่า 25 ปี ยกเว้นว่ามีความเสี่ยงสูง เช่น มีภูมิคุ้มกันบกพร่อง
ค) ตรวจติดตามโดย cervical cytology ที่ 6 และ 12 เดือน(15) แนวทางนี้เหมาะสมในสตรีที่สามารถกลับมารับการตรวจติดตามได้ และไม่มีความวิตกกังวล ถ้าผลการตรวจซ้ำปกติทั้ง 2 ครั้ง สามารถนัดตรวจคัดกรองตามปกติ ถ้าผลการตรวจซ้ำผิดปกติรุนแรงกว่าหรือเท่ากับ ASC-US ให้ส่งตรวจcolposcopy
2.4) ผลการตรวจ cervical cytology พบเซลล์ผิดปกติเป็น LSIL
แนะนำให้ส่งตรวจ colposcopy
หมายเหตุ ในสตรีที่อายุน้อยกว่า 25 ปี แนะนำให้ตรวจ cervical cytology ที่ 12 และ 24 เดือน โดยจะส่งตรวจ colposcopy เมื่อผล cervical cytology ที่ 12 เดือนผิดปกติรุนแรงกว่าหรือเท่ากับ ASC-H หรือ ผลที่ 24 เดือนผิดปกติเทียบเท่าหรือรุนแรงกว่า ASC-US ถ้าผลตรวจที่ 12 และ 24 เดือนเป็นปกติทั้ง 2 ครั้ง ให้ตรวจ cervical cytology ที่ 3 ปี
ในสตรีวัยหมดระดูกลุ่มความเสี่ยงต่ำ อาจพิจารณาตรวจ HPV testing หรือตรวจติดตามด้วย cervical cytology ที่ 6 และ 12 เดือน(7) ถ้าผล cervical cytology ที่ 6 หรือ 12 เดือนผิดปกติรุนแรงกว่าหรือเท่ากับ ASC-US หรือตรวจพบ high-risk HPV ให้ส่งตรวจ colposcopy ถ้าผลตรวจ cervical cytology ซ้ำที่ 6 และ 12 เดือนปกติติดต่อกัน 2 ครั้งให้นัดตรวจคัดกรองตามปกติได้
2.5) ผลการตรวจ cervical cytology พบเซลล์ผิดปกติเป็น ASC-H
แนะนำให้ส่งตรวจ colposcopy ร่วมกับทำ endocervical sampling (ECS) ยกเว้น สตรีตั้งครรภ์ห้ามทำ ECS(7)
2.6) ผลการตรวจ cervical cytology พบเซลล์ผิดปกติเป็น HSIL
แนะนำให้ส่งตรวจ colposcopy ทุกราย จากนั้น มีการดูแลต่อ 2 แนวทาง(16, 17) ได้แก่ การตรวจชิ้นเนื้อจากการทำ colposcopic-directed biopsy (CDB) ก่อนพิจารณาการรักษาต่อ หรือการรักษาเลย (see and treat approach) ด้วยการตัดปากมดลูกออกเป็นรูปกรวยด้วยห่วงลวดไฟฟ้า (loop electrosurgical excision procedure: LEEP/ large loop excision of the transformation zone: LLETZ) เมื่อตรวจด้วย colposcopy แล้วไม่สงสัยมะเร็ง วิธีนี้ไม่แนะนำในสตรีอายุน้อยกว่า 25 ปี และสตรีตั้งครรภ์
2.7) ผลการตรวจ cervical cytology พบเซลล์ผิดปกติเป็น Atypical glandular cells (AGC)
เซลล์ที่ผิดปกติแบบนี้ อาจเกิดจากติ่งเนื้อธรรมดา (polyp) หรือเนื้อเยื่อที่ผิดปกติจากบริเวณปากมดลูก เยื่อบุโพรงมดลูก ท่อนำไข่ รังไข่ หรือจากอวัยวะอื่นๆ เช่น ลำไส้ใหญ่ เป็นต้น(18) การดูแลเบื้องต้นขึ้นกับชนิดของ AGC
ก) AGC of endometrial origin (AGC-EM) สตรีกลุ่มนี้มีโอกาสพบโอกาสพบมะเร็งเยื่อบุโพรงมดลูกประมาณร้อยละ 4-64 รอยโรค HSIL หรือ AIS ประมาณร้อยละ 0.3-13 และมะเร็งปากมดลูกได้ประมาณร้อยละ 0-4(19-23) ดังนั้น จึงแนะนำให้ทำ endometrial sampling (ES) และ ECS และตรวจ colposcopy
ข) AGC of endocervical origin (AGC-EC) สตรีกลุ่มนี้มีโอกาสพบ HSIL และ AIS ประมาณร้อยละ 9-13 มะเร็งปากมดลูกประมาณร้อยละ 6-10 และมะเร็งเยื่อบุโพรงมดลูกประมาณร้อยละ 0.8-7(20, 22, 23) ดังนั้นจึงแนะนำให้ตรวจ colposcopy และทำ ECS ร่วมกับพิจารณาทำ ES ในสตรีอายุ 35 ปีขึ้นไป หรือในสตรีที่มีความเสี่ยงต่อมะเร็งเยื่อบุโพรงมดลูก
ค) AGC favor neoplasia (AGC-FN) หรือ AIS สตรีกลุ่มนี้มีโอกาสพบ HSIL และ AIS ประมาณร้อยละ 8-22 พบมะเร็งปากมดลูกประมาณร้อยละ 3-66 และพบมะเร็งเยื่อบุโพรงมดลูกประมาณร้อยละ 0-39(19-23) ดังนั้นจึงแนะนำให้ตรวจ colposcopy และทำ ECS ร่วมกับพิจารณาทำ ES ในสตรีอายุ 35 ปีขึ้นไป หรือในสตรีที่มีความเสี่ยงต่อมะเร็งเยื่อบุโพรงมดลูก ถ้าตรวจแล้วไม่พบรอยโรค ควรตัดปากมดลูกเป็นรูปกรวย (LEEP/LLETZ) เพื่อการวินิจฉัย
ง) AGC not otherwise specified (AGC-NOS) สตรีกลุ่มนี้มีโอกาสพบ HSIL และ AIS ประมาณร้อยละ 3-13 พบมะเร็งปากมดลูกประมาณร้อยละ 2.2-8 และพบมะเร็งเยื่อบุโพรงมดลูกประมาณร้อยละ 0-12(19-23) ดังนั้นจึงแนะนำให้ตรวจ colposcopy และทำ ECS ร่วมกับพิจารณาทำ ES ในสตรีอายุ 35 ปีขึ้นไป หรือในสตรีที่มีความเสี่ยงต่อมะเร็งเยื่อบุโพรงมดลูก ถ้าตรวจแล้วไม่พบรอยโรค อาจทำการตรวจติดตามด้วย co-testing ที่ 12 และ 24 เดือน หรือตรวจด้วย cervical cytology ที่ 6, 12, 18 และ 24 เดือน
หมายเหตุ ถ้าตรวจไม่พบรอยโรคในเยื่อบุปากมดลูกหรือเยื่อบุโพรงมดลูก ควรตรวจเพิ่มเติมเพื่อหาความผิดปกติของรังไข่ ท่อนำไข่ หรืออวัยวะอื่น ๆ ในช่องท้องเพิ่มเติมเพื่อการวินิจฉัย เช่น การตรวจอัลตราซาวด์
2.8 ผลการตรวจ cervical cytology พบ benign glandular changes, endometrial cells
ควรทำการตรวจวินิจฉัยโรคในเยื่อบุโพรงมดลูกเพิ่มเติม เช่น การทำ ES หรือ hysteroscopy เฉพาะในสตรีวัยหมดระดูหรืออายุ 50 ปีขึ้นไป
3. ความผิดปกติจากวิธีการตรวจปากมดลูกด้วยน้ำส้มสายชู (visual inspection with acetic acid, VIA)(4, 24-27)
3.1) กรณีที่เห็น SCJ ไม่ครบโดยรอบ ให้ส่งต่อผู้ป่วยไป รพช. หรือ รพท. หรือ รพศ. ที่เป็นเครือข่ายเพื่อทำการตรวจคัดกรองด้วยวิธีอื่นต่อไป
3.2) หากพบรอยโรคเป็นฝ้าขาวขอบชัดและเข้าเกณฑ์ของการจี้เย็น(28) ผู้ตรวจสามารถทำการรักษาด้วยการจี้เย็นได้ทันที และตรวจติดตามด้วยวิธี VIA ซ้ำที่ 1, 3, และ 5 ปี ตามลำดับ ถ้าพบความผิดปกติเกิดขึ้นซ้ำให้ส่งต่อผู้ป่วยไปโรงพยาบาลเครือข่ายเพื่อการตรวจวินิจฉัยและรักษาต่อไป
3.3) หากรอยโรคสงสัยมะเร็งปากมดลูก ให้ส่งต่อผู้ป่วยไปยังโรงพยาบาลเครือข่ายที่มีศักยภาพเพื่อการตรวจวินิจฉัยและรักษาต่อไป
สรุป
ราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย (RTCOG) สมาคมมะเร็งนรีเวชไทย ร่วมกับชมรมคอลโปสโคปีและพยาธิสภาพปากมดลูกแห่งประเทศไทย ได้จัดทำแนวทางในการตรวจคัดกรองมะเร็งปากมดลูก และการดูแลรักษาผลการตรวจคัดกรองมะเร็งปากมดลูกที่ผิดปกติ โดยได้มีการปรับปรุงให้มีความเหมาะสมกับ โครงสร้างพื้นฐานของการให้บริการทางสาธารณสุข ความพร้อมของการตรวจทางห้องปฏิบัติการภายในประเทศ บทความนี้ส่วนใหญ่เรียบเรียงและดัดแปลงมาจาก แนวทางเวชปฏิบัติของราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทยฉบับ ค.ศ. 2020 และได้มีการเปรียบเทียบข้อเหมือน ข้อแตกต่างระหว่างแนวเวชปฏิบัติในประเทศและต่างประเทศ รวมถึงได้สรุปแนวทางการดูแลผลการตรวจคัดกรองที่ผิดปกติสำหรับสูตินรีแพทย์ทั่วไป ดังที่สรุปไว้ในแผนภูมิที่ 1-3
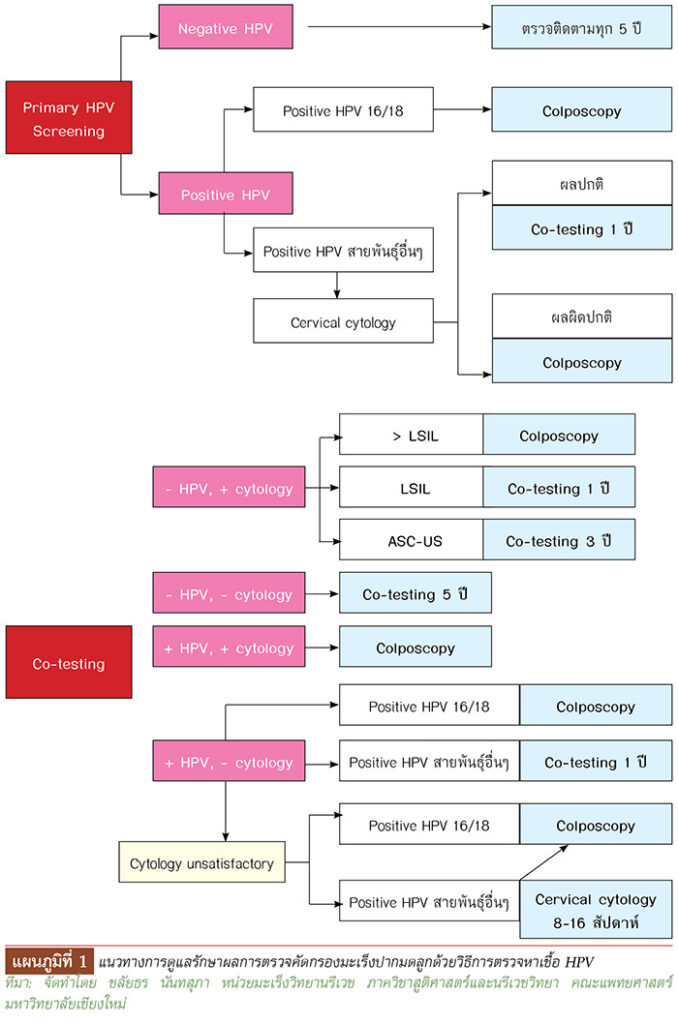
แผนภูมิที่ 1 แนวทางการดูแลรักษาผลการตรวจคัดกรองมะเร็งปากมดลูกด้วยวิธีการตรวจหาเชื้อ HPV
ที่มา: จัดทำโดย ชลัยธร นันทสุภา หน่วยมะเร็งวิทยานรีเวช ภาควิชาสูติศาสตร์และนรีเวชวิทยา คณะแพทยศาสตร์ มหาวิทยาลัยเชียงใหม่
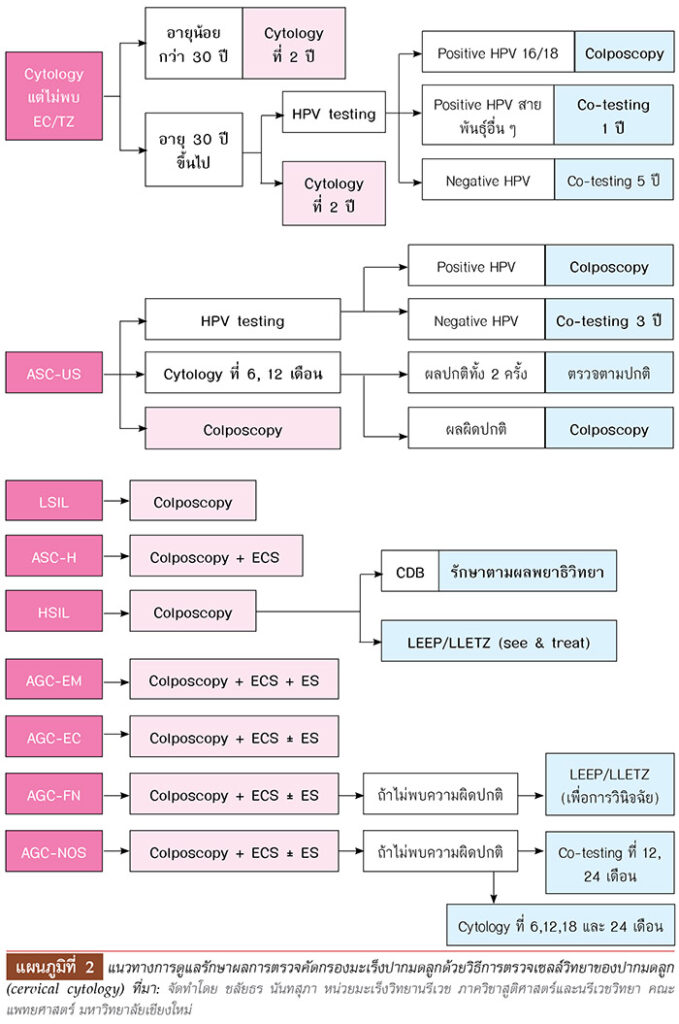
แผนภูมิที่ 2 แนวทางการดูแลรักษาผลการตรวจคัดกรองมะเร็งปากมดลูกด้วยวิธีการตรวจเซลล์วิทยาของปากมดลูก (cervical cytology) ที่มา: จัดทำโดย ชลัยธร นันทสุภา หน่วยมะเร็งวิทยานรีเวช ภาควิชาสูติศาสตร์และนรีเวชวิทยา คณะแพทยศาสตร์ มหาวิทยาลัยเชียงใหม่
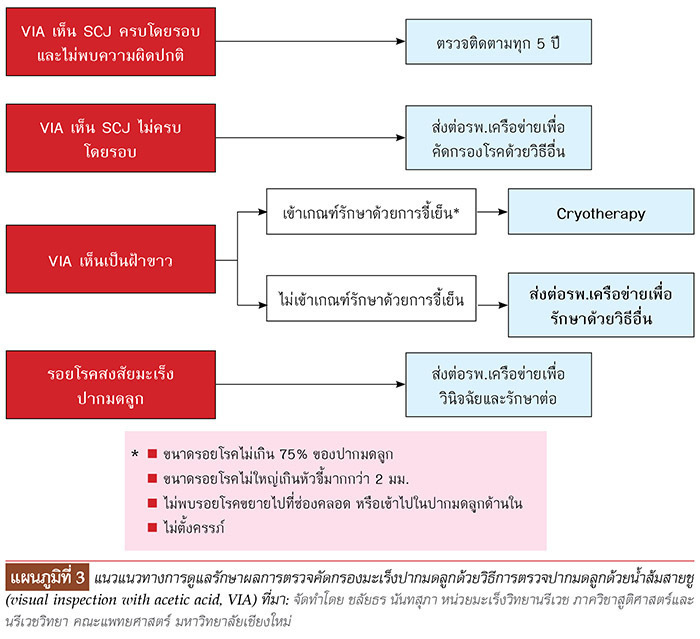
แผนภูมิที่ 3 แนวทางการดูแลรักษาผลการตรวจคัดกรองมะเร็งปากมดลูกด้วยวิธีการตรวจปากมดลูกด้วยน้ำส้มสายชู (visual inspection with acetic acid, VIA) ที่มา: จัดทำโดย ชลัยธร นันทสุภา หน่วยมะเร็งวิทยานรีเวช ภาควิชาสูติศาสตร์และนรีเวชวิทยา คณะแพทยศาสตร์ มหาวิทยาลัยเชียงใหม่
เอกสารอ้างอิง
1. Fontham ETH, Wolf AMD, Church TR, et al. Cervical cancer screening for individuals at average risk: 2020 guideline update from the American Cancer Society. CA Cancer J Clin. 2020.
2. Perkins RB, Guido RS, Castle PE, et al. 2019 ASCCP Risk-Based Management Consensus Guidelines for Abnormal Cervical Cancer Screening Tests and Cancer Precursors. J Low Genit Tract Dis. 2020;24:102-31.
3. Sawaya GF, Huchko MJ. Cervical Cancer Screening. Med Clin North Am. 2017;101:743-53.
4. ปิยวัฒน์ เลาวหุตานนท์ อช, วีรวุฒิ อิ่มสำราญ. แนวทางการตรวจคัดกรอง วินิจฉัยและรักษาโรคมะเร็งปากมดลูก. กรุงเทพฯ: กลุ่มงานสนับสนุนวิชาการ สถาบันมะเร็งแห่งชาติ; 2561.
5. Practice Bulletin No. 168 Summary: Cervical Cancer Screening and Prevention. Obstet Gynecol. 2016;128(4):923-5.
6. Moscicki AB, Flowers L, Huchko MJ, et al. Guidelines for Cervical Cancer Screening in Immunosuppressed Women Without HIV Infection. J Low Genit Tract Dis. 2019;23:87-101.
7. Massad LS, Einstein MH, Huh WK, et al. 2012 updated consensus guidelines for the management of abnormal cervical cancer screening tests and cancer precursors. Obstet Gynecol. 2013;121:829-46.
8. Castle PE, Stoler MH, Wright TC, Jr., et al. Performance of carcinogenic human papillomavirus (HPV) testing and HPV16 or HPV18 genotyping for cervical cancer screening of women aged 25 years and older: a subanalysis of the ATHENA study. Lancet Oncol. 2011;12:880-90.
9. Gage JC, Schiffman M, Katki HA, et al. Reassurance against future risk of precancer and cancer conferred by a negative human papillomavirus test. J Natl Cancer Inst. 2014;106(8):dju153.
10. Saslow D, Solomon D, Lawson HW, et al. American Cancer Society, American Society for Colposcopy and Cervical Pathology, and American Society for Clinical Pathology screening guidelines for the prevention and early detection of cervical cancer. CA Cancer J Clin. 2012;62:147-72.
11. Solomon D, Davey D, Kurman R, et al. The 2001 Bethesda System: terminology for reporting results of cervical cytology. JAMA. 2002;287:2114-9.
12. Stoler MH, Schiffman M. Interobserver reproducibility of cervical cytologic and histologic interpretations: realistic estimates from the ASCUS-LSIL Triage Study. JAMA. 2001;285:1500-5.
13. A-LTS G. Results of a randomized trial on the management of cytology interpretations of atypical squamous cells of undetermined significance. Am J Obstet Gynecol. 2003;188:1383-92.
14. Wright TC, Jr., Massad LS, Dunton CJ, et al. 2006 consensus guidelines for the management of women with abnormal cervical cancer screening tests. Am J Obstet Gynecol. 2007;197:346-55.
15. Massad LS, Einstein MH, Huh WK, et al. 2012 updated consensus guidelines for the management of abnormal cervical cancer screening tests and cancer precursors. Obstet Gynecol. 2013;121:829-46.
16. Charoenkwan K, Srisomboon J, Siriaunkgul S, et al. A “See and Treat” approach for high grade squamous intraepithelial lesion on cervical cytology. J Med Assoc Thai. 2004;87:865-8.
17. Numnum TM, Kirby TO, Leath CA, 3rd, et al. A prospective evaluation of “see and treat” in women with HSIL Pap smear results: is this an appropriate strategy? J Low Genit Tract Dis. 2005;9:2-6.
18. Zhao C, Florea A, Onisko A, et al. Histologic follow-up results in 662 patients with Pap test findings of atypical glandular cells: results from a large academic womens hospital laboratory employing sensitive screening methods. Gynecol Oncol. 2009;114:383-9.
19. Sawangsang P, Sae-Teng C, Suprasert P, et al. Clinical significance of atypical glandular cells on Pap smears: experience from a region with a high incidence of cervical cancer. J Obstet Gynaecol Res. 2011;37:496-500.
20. Chatchotikawong U, Ruengkhachorn I, Laiwejpithaya S. Factors predicting pathologic significance among women with atypical glandular cells on liquid-based cytology. Int J Gynaecol Obstet. 2012;119:30-4.
21. Watcharanon W, Luanratanakorn S, Kleebkaow P, et al. High-grade Cervical Histopathology in Women with Atypical Glandular Cell Cytology. Asian Pac J Cancer Prev. 2016;17:135-8.
22. Jang TK, Park JY, Kim DY, et al. Histologic Correlation and Clinical Significance of Atypical Glandular Cells on Cervical Pap Tests: Analysis of 540 Cases at a Single Institution. Cancer Invest. 2019;37:8-15.
23. Toyoda S, Kawaguchi R, Kobayashi H. Clinicopathological Characteristics of Atypical Glandular Cells Determined by Cervical Cytology in Japan: Survey of Gynecologic Oncology Data from the Obstetrical Gynecological Society of Kinki District, Japan. Acta Cytol. 2019;63:361-70.
24. Mandelblatt JS, Lawrence WF, Gaffikin L, et al. Costs and benefits of different strategies to screen for cervical cancer in less-developed countries. J Natl Cancer Inst. 2002;94:1469-83.
25. Goldie SJ, Gaffikin L, Goldhaber-Fiebert JD, et al. Cost-effectiveness of cervical-cancer screening in five developing countries. N Engl J Med. 2005;353:2158-68.
26. Sauvaget C, Fayette JM, Muwonge R, et al. Accuracy of visual inspection with acetic acid for cervical cancer screening. Int J Gynaecol Obstet. 2011;113:14-24.
27. วสันต์ ลีนะสมิต พห, กิตติพงศ์ แซ่เจ็ง, บุญฤทธิ์ สุขรัตน์, และคณะฯ การควบคุมมะเร็งปากมดลูกที่ครอบคลุม: แนวทางการปฏิบัติที่สำคัญ: สำนักอนามัยเจริญพันธุ์ กรมอนามัย กระทรวงสาธารณสุข; 2559.
28. WHO N, T. Moran. Prevention of cervical cancer through screening using visual inspection with acetic acid (VIA) and treatment with cryotherapy. Geneva: World Health Organization; 2012.

