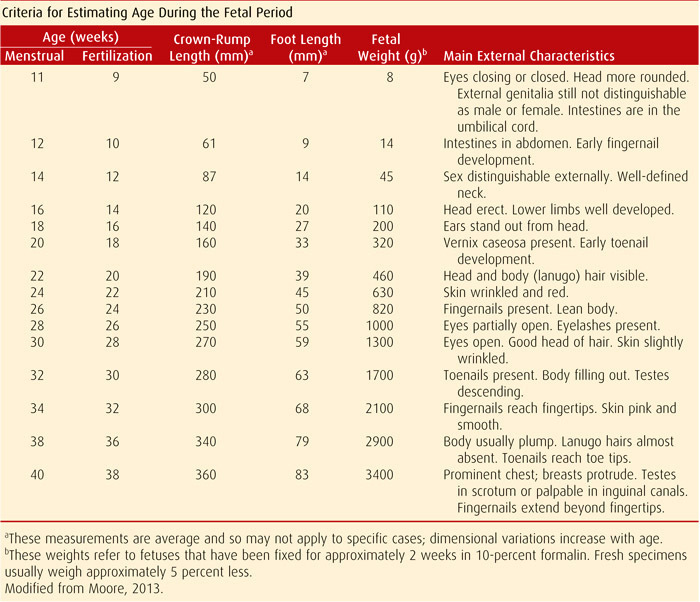
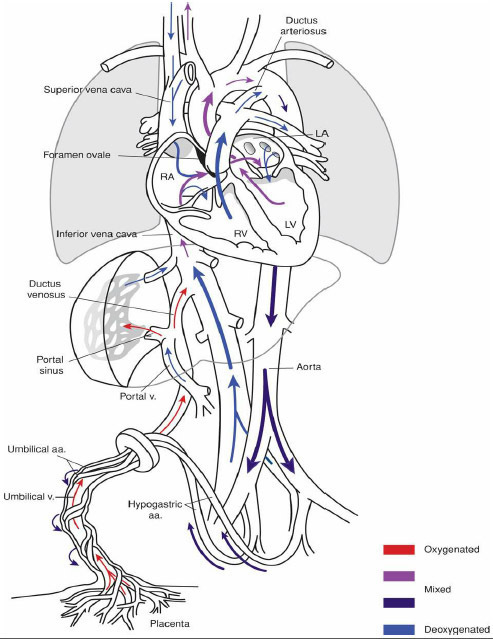
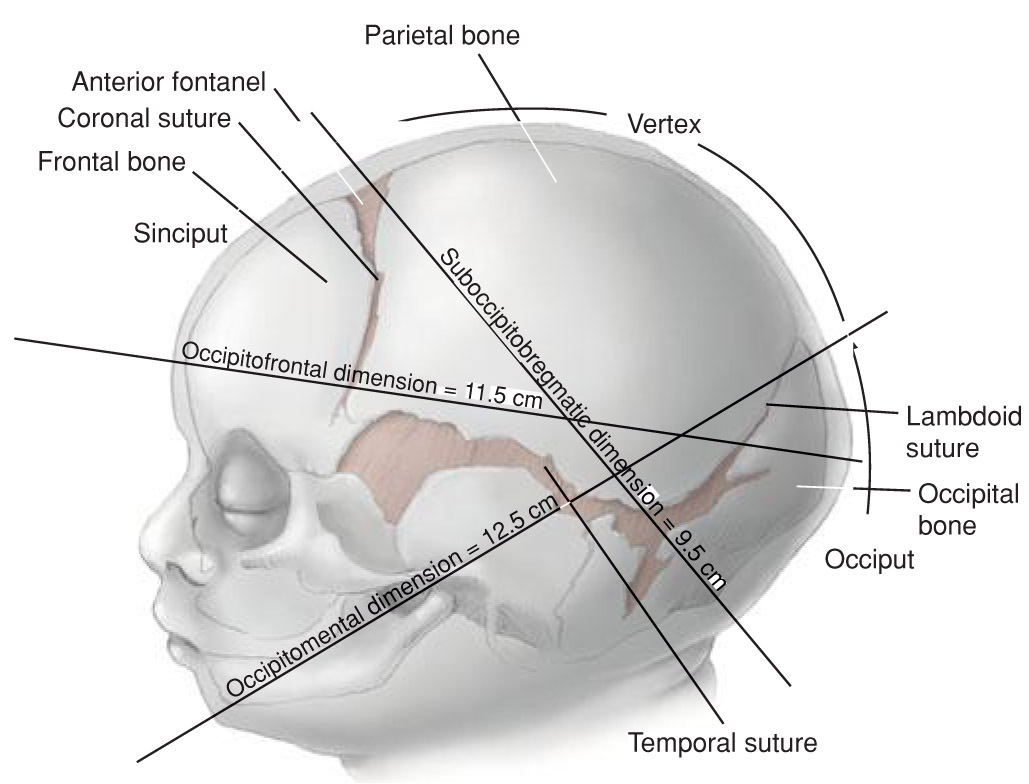
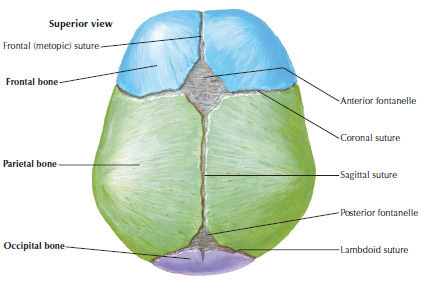
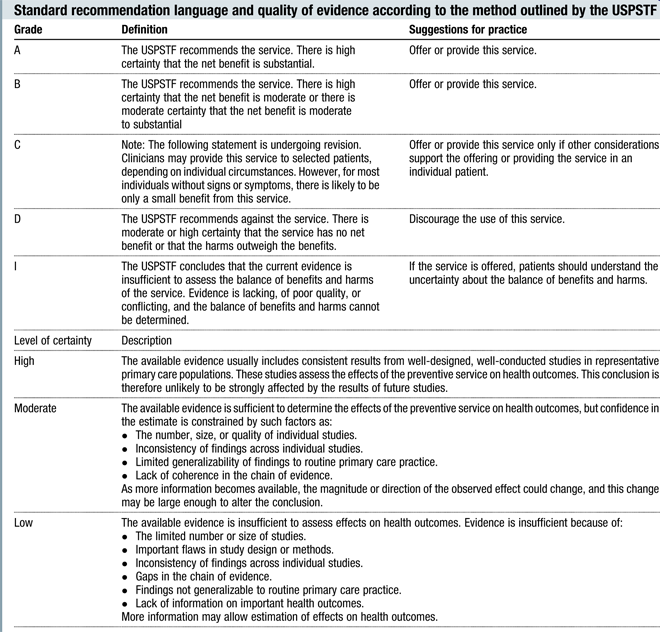
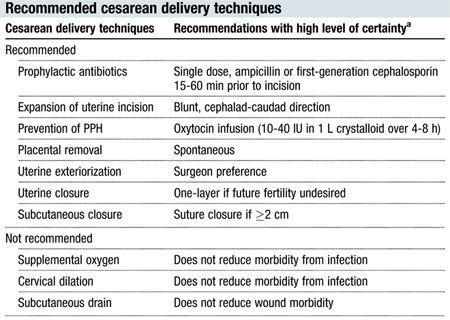
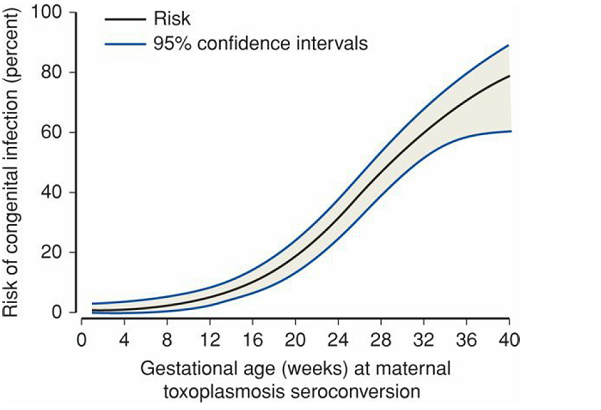
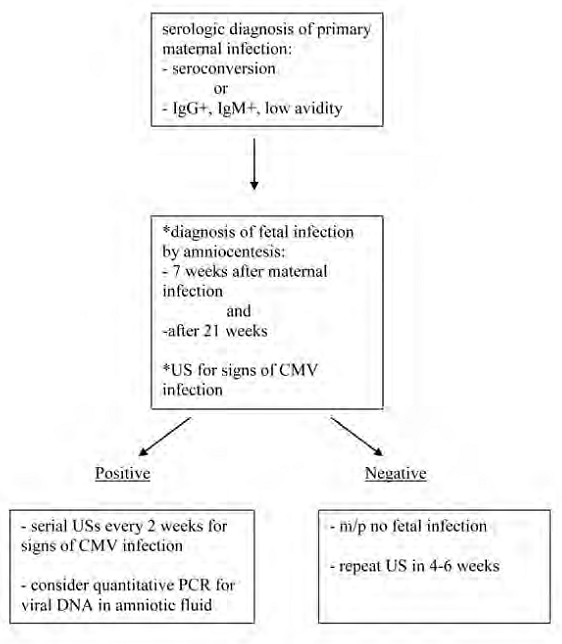
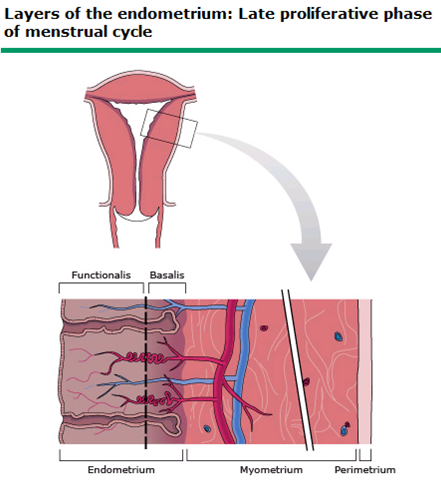
การบริหารกล้ามเนื้ออุ้งเชิงกราน (Pelvic Floor Muscle Training)
การบริหารกล้ามเนื้ออุ้งเชิงกราน (Pelvic Floor Muscle Training)
พญ. นภวรี จันทรวงศ์
อาจารย์ที่ปรึกษา พญ. อรวี ฉินทกานันท์
อาการปัสสาวะเล็ด (Urinary incontinence) ตามนิยามของ International Continence Society (ICS) หมายถึง ภาวะใดๆที่มีปัสสาวะเล็ดราด โดยควบคุมไม่ได้1,2 พบได้ในผู้หญิงมากกว่าผู้ชาย โดยมีความชุกระหว่าง 9 ถึง 72 เปอร์เซนต์ ระหว่างช่วงอายุ 17 ถึง 79 ปี1 อาการปัสสาวะเล็ดนั้นแบ่งได้เป็นหลายประเภท ซึ่งประเภทที่เป็นอาการสำคัญที่นำผู้ป่วยมาพบแพทย์บ่อยที่สุดคือ Stress Urinary Incontinence คือ อาการปัสสาวะเล็ดราดออกมาโดยควบคุมไม่ได้ ขณะออกแรง ไอ หรือจาม1,3,4 การที่มีปัสสาวะเล็ดนั้นเป็นปัญหาก่อให้เกิดผลเสียต่อคุณภาพชีวิตของผู้ป่วยในการดำเนินชีวิตประจำวัน และการออกสังคม1-4 และยังส่งผลต่อสุขภาพของผู้ป่วย เพราะการใช้ชีวิตประจำวัน หรือการออกกำลังกายนั้น เป็นปัจจัยสำคัญในการป้องกันกระดูกพรุน โรคอ้วน เบาหวาน ความดันโลหิตสูง โรคหลอดเลือดหัวใจ มะเร็งเต้านม มะเร็งลำไส้ โรคซึมเศร้าและวิตกกังวล1
อาการปัสสาวะเล็ด สามารถรักษาได้หลายวิธี ได้แก่ การรักษาเชิงพฤติกรรม การบริหารกล้ามเนื้ออุ้งเชิงกราน การรักษาโดยการใส่ห่วงช่วยพยุง การรักษาโดยการใช้ยา และการผ่าตัด5 ในบทความนี้จะกล่าวถึง การบริหารกล้ามเนื้ออุ้งเชิงกราน จากการศึกษาพบว่า มีร้อยละ 84 ของผู้ป่วยที่มีอาการปัสสาวะเล็ดสามารถรักษาหายได้ด้วยการบริหารกล้ามเนื้ออุ้งเชิงกราน1-4
การบริหารกล้ามเนื้ออุ้งเชิงกรานนั้นนอกจากจะใช้รักษาอาการปัสสาวะเล็ดแล้ว ยังมีการศึกษาว่า มีประโยชน์ในการรักษาภาวะอุ้งเชิงกรานหย่อนได้3,6-13 ภาวะอุ้งเชิงกรานหย่อน คือการเสียความแข็งแรงของการพยุงอวัยวะในอุ้งเชิงกราน ทำให้เกิดการเคลื่อนต่ำลงมาของอวัยวะอุ้งเชิงกรานจากตำแหน่งปกติ พบได้ประมาณร้อยละ 40-50 จากประชากรทั้งหมด8 จากการศึกษาพบว่าการบริหารกล้ามเนื้ออุ้งเชิงกรานช่วยลดการหย่อนของอุ้งเชิงกรานในระดับเล็กน้อยถึงปานกลางได้ โดยสามารถลดทั้งการหย่อนทางโครงสร้างและอาการแสดง6,7,9-13
กล้ามเนื้ออุ้งเชิงกรานประกอบไปด้วย
1. Pelvic diaphragm
- Coccygeus
- Levetor ani ซึ่งประกอบไปด้วยกล้ามเนื้อ 3 มัด คือ pubococcygeus, puborectalis, iliococcygeus
2. Urogenithral diaphragm หรือ Perineal membrane ประกอบด้วย
- Deep transverse perineal muscle
- Compressor urethrae
- Urethrovaginal sphincter
- Sphincter urethrae muscle
3. Urethral and anal sphincter muscle
ในภาวะการกลั้นปกติเกิดจากมีการหดรัดตัวของกล้ามเนื้ออุ้งเชิงกรานทุกมัดพร้อมกัน ซึ่งจะทำให้เกิดการเคลื่อนตัวเข้าข้างใน (inward movement) และ การปิดของรูเปิดอุ้งเชิงกราน (Closure around pelvic openings) ดังนั้นผลของการบริหารกล้ามเนื้ออุ้งเชิงกราน คือการปิดกั้นท่อปัสสาวะ จะทำให้เพิ่มแรงดันในท่อปัสสาวะ ซึ่งจะสามารถป้องกันการเล็ดของปัสสาวะที่เกิดจากการเพิ่มของความดันในช่องท้องได้1
ในปีค.ศ.1948 Dr. Arnold Henry Kegel สูตินรีแพทย์ชาวอเมริกัน ได้คิดค้นการรักษาอาการปัสสาวะเล็ดโดยไม่ต้องผ่าตัด โดยในตอนแรก Dr. Kegel ได้คิดการรักษาเพื่อรักษาอาการปัสสาวะเล็ดของหญิงตั้งครรภ์หลังคลอดบุตร โดยการบริหารกล้ามเนื้ออุ้มเชิงกราน Dr. Kegel อธิบายไว้ว่าการบริหารกล้ามเนื้อ pubococcygeus สามารถลดปัญหาของการปัสสาวะในสตรีหลังคลอดบุตรได้ อีกทั้ง Dr. Kegel ยังคิดค้น Perineometer ใช้สำหรับวัดประเมิน vaginal pressure14,15


รูปที่ 1– ภาพ Dr. Arnold H. Kegel และ perineometer
ข้อบ่งชี้ในการบริหารกล้ามเนื้ออุ้งเชิงกราน
- ระบบกล้ามเนื้อที่ทำหน้าที่พยุงช่องท้องทำงานไม่สัมพันธ์กัน
- ตำแหน่งของอวัยวะในอุ้งเชิงกรานเปลี่ยนแปลงไป ได้แก่ การเคลื่อนต่ำของช่องคลอด (vaginal descent) กระเพาะปัสสาวะหย่อน (cystocele) ลำไส้ใหญ่หย่อน (rectocele)
- อาการปัสสาวะ อุจจาระเล็ด/ ราด
- Disorder of emptying : อาการท้องผูก (constipation) ปัสสาวะไม่ออก (urinary retention)
- สมรรถภาพทางเพศถดถอย เช่น relaxed vagina, vaginismus
- กระดูกโอบอุ้งเชิงกราน (pelvic girdle) มีความไม่มั่นคง: sacroiliac joint, lumbosacral joint
- อุ้งเชิงกรานไม่สมมาตร : pelvic scoliosis
วิธีบริหารกล้ามเนื้ออุ้งเชิงกราน (Pelvic Floor Muscle Training หรือ Kegel exercise)
การบริหารกล้ามเนื้ออุ้งเชิงกราน อย่างถูกวิธีนั้นประกอบไปด้วย 2 องค์ประกอบ คือ การขมิบรอบๆรูเปิดของอวัยวะอุ้งเชิงกราน (squeeze around the pelvic openings) และ การขมิบให้กล้ามเนื้ออุ้งเชิงกรานยกขึ้นและเข้าข้างใน (inward lift) โดยมีขั้นตอนดังต่อไปนี้16-18
- อันดับแรก ต้องระบุกล้ามเนื้อที่จะขมิบให้ถูกต้อง โดยวิธี คือ การทดลองขมิบขณะที่ปัสสาวะ หากสามารถขมิบให้ปัสสาวะหยุดไหลได้ ถือว่าขมิบกล้ามเนื้อได้ถูกมัด ให้ขมิบลักษณะนี้เพียงไม่กี่ครั้งเท่านั้นในช่วงที่เรียนรู้ หลังจากนั้นสามารถขมิบกล้ามเนื้อได้ในทุกอิริยาบท ไม่จำเป็นและไม่ควรทำขณะปัสสาวะ เพราะจะทำให้เกิดกระเพาะปัสสาวะอักเสบได้
- หลังจากขมิบได้ถูกกล้ามเนื้อแล้ว ให้พยายามขมิบค้างไว้นานที่สุดเท่าที่ทำได้ แล้วคลาย หลังจากนั้นให้เพิ่มระยะเวลาให้ขมิบนานขึ้นสามารถขมิบได้นาน 8 ถึง 10 วินาทีต่อครั้ง โดยให้ขมิบ 8 ถึง 12 ครั้งต่อ 1 ชุด และ ปฏิบัติให้ได้ 3 ชุด ต่อ วัน และควรปฏิบัติอย่างน้อย 3 ถึง 4 วันต่อสัปดาห์ เป็นระยะเวลานาน 15 ถึง 20 สัปดาห์ เมื่อปฏิบัติตามวิธีดังกล่าวได้แล้ว สามารถเพิ่มความแรงและระยะเวลาขมิบให้มากขึ้นได้
- หากต้องการให้กล้ามเนื้ออุ้งเชิงกรานมีความแข็งแรงต่อไปในระยะยาว ควรปฏิบัติตามวิธีดังกล่าวอย่างต่อเนื่อง
นอกจากนั้นยังมีอุปกรณ์ที่ใช้ช่วยในการฝึกฝนกล้ามเนื้ออุ้งเชิงกราน เช่น vaginal cones19-23 โดยมีหลายแนวทางในการฝึก แต่วิธีที่แนะนำโดยทั่วไปคือ เริ่มใช้ cone อันที่น้ำหนักมากที่สุดที่สามารถกลั้นไว้ได้เป็นเวลา 1 นาที โดยมีการใช้การหดรัดตัวของ PFM (The active weight) โดยปฏิบัตินานครั้งละ 15 นาที วันละ 2 ครั้ง ซึ่งผู้ป่วยสามารถปฏิบัติเองที่บ้านได้21,23
Biofeedback
Biofeedback คือการใช้คอมพิวเตอร์บันทึกการทำงาน การหดรัดตัว การคลายตัว และความแข็งแรงของกล้ามเนื้อ โดยคอมพิวเตอร์จะบันทึกออกมาเป็นกราฟ24 Biofeedback จะช่วยระบุกล้ามเนื้อโดยจะแสดงความเปลี่ยนแปลงออกมาบนกราฟเมื่อมีการขมิบกล้ามเนื้อได้ถูกต้อง จึงช่วยให้ฝึกฝนเฉพาะกล้ามเนื้อที่ต้องการ24,25 วิธีการทำ Biofeedback ทำได้โดยติด sensor patchที่ผิวหนังบริเวณรูทวาร หรือ ในช่องคลอด หรือ ในรูทวาร โดย sensor จะเชื่อมต่อกับคอมพิวเตอร์ที่แสดงกราฟการหดรัดตัวของกล้ามเนื้อ ระยะเวลาการตรวจแต่ละครั้งอยู่ที่ 20-30 นาที 1-2 ครั้งต่อเดือน แต่ในช่วงแรกของการฝึกอาจจะต้องมาถี่กว่านั้น หากต้องการผลการรักษาที่ดีที่สุด ควรจะได้รับการทำ Biofeedback เป็นระยะเวลา 6 เดือนขึ้นไป24
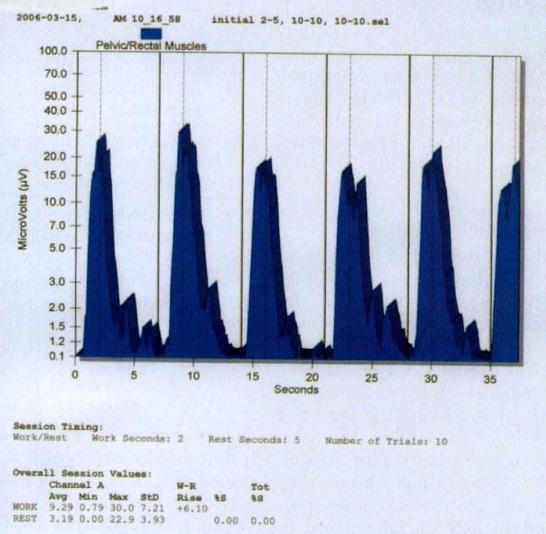
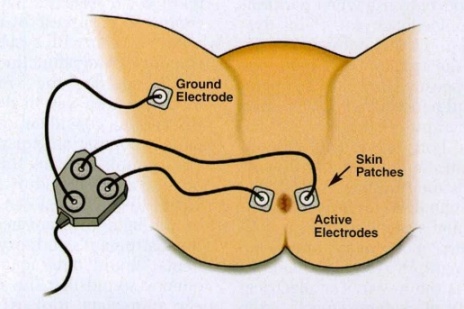
รูปที่ 2– Biofeedback
Alternative exercises4
1. Abdominal muscle training
การบริหารกล้ามเนื้อหน้าท้อง อาจจะมีประโยชน์ในการสร้างความแข็งแรงของกล้ามเนื้ออุ้งเชิงกรานได้
2. Paula method
เชื่อว่ารูเปิดในร่างกายของมนุษย์นั้นทำงานร่วมกัน ดังนั้น Paula method คือการที่มีการออกกำลังกายของปาก ตา และจมูก จะทำให้มีการหดรัดตัวและสร้างความแข็งแรงของกล้ามเนื้ออุ้งเชิงกราน
3. Pilates exercise
การทำ Pilates exercise เป็นการออกกำลังกายร่วมกันระหว่างการหายใจ และกล้ามเนื้ออุ้งเชิงกราน โดยที่จริงแล้วกล้ามเนื้ออุ้งเชิงกรานได้รับการฝึกฝนโดยอ้อมจากการออกกำลังกายชนิดนี้
4. Yoga
เป็นการออกกำลังกายประกอบกับการทำสมาธิ ที่ประกอบไปด้วย stretching, breathing, balance, และ strengthening และในบางครั้งมีการหดรัดของหูรูดทวารหนัก และ กล้ามเนื้ออุ้งเชิงกราน ร่วมด้วย
5. Tai Chi
Tai Chi หรือ ไทเก๊ก เป็นการออกกำลังกายของชาวจีน ในการออกกำลังกายมีการหดรัดของหูรูดทวารหนักร่วมด้วย
6. Breathing exercise
การกลั้นหายใจจะเพิ่มแรงดันในช่องท้อง ซึ่งจะทำให้เกิดการเคลื่อนลงต่ำ และอ่อนแรงของกล้ามเนื้ออุ้งเชิงกราน ดังนั้นเชื่อว่าการบริหารการหายใจโดย คลายกระบังลม จะลดความดันในช่องท้อง และอาจกระตุ้นกล้ามเนื้อหน้าท้อง และกล้ามเนื้ออุ้งเชิงกราน
7. Posture correction
การอยู่ในท่าทางที่ผิด จะทำให้เกิดอาการเจ็บปวดและ กล้ามเนื้ออุ้งเชิงกรานที่ผิดปกติ
8. General fitness training
การออกกำลังกายจะมีการหดตัวของกล้ามเนื้ออุ้งเชิงกรานร่วมด้วย ส่งผลให้การเกิดการเล็ด/ ราดลดลง
จากการศึกษายังไม่พบหลักฐานใดที่พบว่าวิธีดังกล่าวนี้ มีประสิทธิภาพในการรักษาอาการปัสสาวะเล็ดมากกว่าการบริหารกล้ามเนื้ออุ้งเชิงกราน และมี 84 เปอร์เซนต์ของผู้ป่วยที่มีอาการปัสสาวะเล็ดสามารถรักษาหายได้ด้วยการบริหารกล้ามเนื้ออุ้งเชิงกราน4
จากที่ผู้ป่วยฝึกบริหารกล้ามเนื้ออุ้งเชิงกรานเองที่บ้านนั้น จึงควรมีการตรวจติดตามด้วยแพทย์เป็นระยะ โดยจะตรวจติดตามที่ระยะเวลา 3 เดือน เพื่อประเมินว่าฝึกกล้ามเนื้อได้ถูกกล้ามเนื้อ และประเมินความแข็งแรงของกล้ามเนื้ออุ้งเชิงกราน
วิธีการประเมิน PFM Function and Strength1 แบ่งได้เป็น
- วิธีการวัดความสามารถในการหดรัดตัว ( Clinical observation, vaginal palpation, ultrasound, MRI, electromyography [EMG] )
- วิธีการประเมินความแข็งแรง ( manual muscle test by vaginal palpation, manometry, dynamometry, cones)
วิธีการดังกล่าวนี้ เป็นการวัดในหลายด้านของ PFM ได้แก่ activity, anterior and cephalad movement, squeeze pressure, electrical activity โดยที่ทุกวิธีhave their place in physical therapist evaluation แต่ก็ยังมีข้อจำกัด
วิธีการวัดความสามารถในการหดรัดตัว
- Clinical observation
ในปี 1948 ตามที่ Kegel ได้อธิบายการหดรัดตัวของ PFM ที่ถูกต้อง คือ squeeze รอบรูเปิดของ urethra vagina และ anus สังเกตุเห็นบริเวณฝีเย็บมี inward lift โดยวิธีการสังเกตุนี้จะสังเกตุได้เพียง superficial perineal muscles แต่ levator ani muscles ก็ตอบสนองไปในทางเดียวกัน เนื่องจากมีการหดตัวร่วมกันกับ superficial perineal muscles - Vaginal palpation
เป็นเทคนิคที่ใช้กันมากในปัจจุบัน และเป็นวิธีที่ Kegel ใช้ในการประเมิน PFM function โดยทำการสอดนิ้วมือ 1 นิ้วไปที่ 1/3 ของช่องคลอดส่วนล่าง และให้ผู้ป่วย lift inward และ squeeze นิ้วของผู้ตรวจ ซึ่งวิธีนี้ใช้เพื่อสอนให้ผู้ป่วยฝึกบริหารกล้ามเนื้ออุ้งเชิงกราน และเพื่อประเมินว่าผู้ป่วยทำถูกหรือไม่
ส่วนการประเมิน PFM strength ได้นำ perineometer มาใช้ในการประเมินความสามารถ PFM ในการสร้าง vaginal squeeze pressure - Ultrasound และ MRI
ยังไม่มีข้อสรุปที่ชัดเจน แต่ในปัจจุบัน Ultrasound ได้ถูกนำมาใช้มากขึ้นในการวัดความสามารถในการหดรัดตัวของ PFM เนื่องจากค่าใช้จ่ายในการตรวจด้วย ultrasound ราคาต่ำลง - Electromyography [EMG]
เป็นการวัด electrical activity ของกล้ามเนื้อ ซึ่งเป็นการแสดงถึงกระแสการส่งออกของ motorneurons โดยตรงทั้งการหดรัดตัวของกล้ามเนื้ออุ้งเชิงกรานแบบตั้งใจ และ เป็นreflex โดยการวัดกล้ามเนื้ออุ้งเชิงกรานนั้นควรใช้เป็น intramuscular electrodes (needle or wire) เนื่องจากเป็นกล้ามเนื้อที่เล็กและอยู่ลึกในร่างกาย แต่ในทางปฏิบัติแล้วมักจะใช้ surface electrodes ที่อยู่บน vaginal probe เนื่องจากบริเวณอุ้งเชิงกรานนั้นมีความไวสูง และการใช้ needle electrodes ต้องอาศัยทักษะที่ดีในการตรวจ
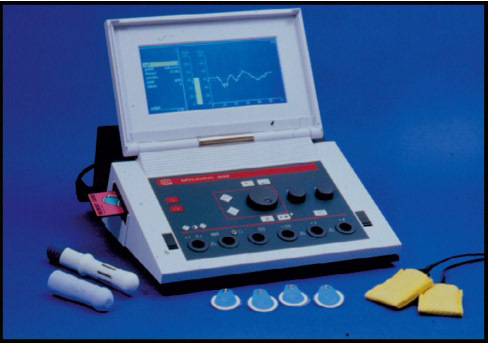
รูปที่ 3– Electromyography for pelvic floor muscle evaluation
วิธีการประเมินความแข็งแรง
– Manual muscle testing
เป็นการวัดประเมินความแข็งแรงของ PFM โดยการคลำ เช่นเดียวกับการทำ vaginal palpitation ซึ่งมีการประเมินออกมาเป็นคะแนนโดยใช้ modified Oxford Grading System2,26 สามารถประเมินได้ในขณะตรวจ vaginal palpation และไม่จำเป็นต้องใช้เครื่องมือใดๆ แต่เนื่องจากเป็นการประเมินโดยบุคคล จึงทำให้เกิดความคลาดเคลื่อนของผลการประเมินได้
ตารางที่ 1- Grading of pelvic floor muscle strength (Modified Oxford Scale)
{tabulizer:style[gr.alterora.elemental_1_blue_green.css]}
| Grade | Description |
| 0/5 | No discernible pelvic floor muscle contraction |
| 1/5 | A flicker or pulsing under the examining finger; a weak contraction |
| 2/5 | A weak contraction; an increase in tension in the muscle without any discernible lift or squeeze |
| 3/5 | A moderate contraction; characterized by a degree of lifting of the posterior vaginal wall and squeezing on the base of the finger with in-drawing of the perineum. A grade 3 or higher contraction in generally discernible on visual perineal inspection. |
| 4/5 | A good pelvic floor muscle contraction producing elevation of the posterior vaginal wall against resistance and in-drawing of the perineum. If 2 fingers (index and middle) are placed laterally or vertically in the vagina and separated, a grade 4 contraction can squeeze them together against resistance. |
| 5/5 | A strong contraction of the pelvic floor muscle; strong resistance can be given against elevation of the posterior vaginal wall and approximation of the index and middle fingers as for grade 4/5 |
– Manometry
เป็นการประเมินความแข็งแรงของ PFM โดยการวัดแรงดันแรงดัน เป็น mmHg หรือ cmH2O โดยจะใช้ vaginal pressure device เชื่อมต่อกับ manometer (the perineometer) หรือ specialized balloon catheter เชื่อมต่อกับ a fiberoptic microtip and strain-gauge pressure transducer โดยวาง probe ไว้ที่ 1/3 lower vagina หรือ 3.5 cm ด้านในจาก introitus จะได้แรงดันที่สูงที่สุด

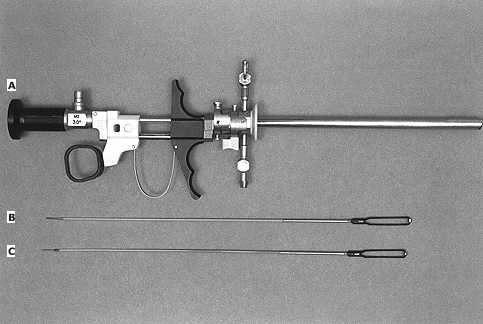
รูปที่ 4.1– Perineometer

รูปที่ 4.2– Vaginal squeeze pressure measured with a vaginal balloon connected to a microtip pressure transducer
– Dynamometers
Dynamometer ใช้วัดกำลังของกล้ามเนื้อในทาง dorsoventral (ในหน่วย นิวตัน) จนถึงปัจจุบันยังไม่มีหลักฐานสนับสนุนในการใช้เครื่องมือชนิดนี้ ข้อด้อยของเครื่องมือชนิดนี้คือ สามารถวัดได้เพียงการบีบรัด แต่ไม่ได้วัดการยก และการใช้ Dynamometer วัดจะได้รับผลกระทบจากแรงดันในช่องท้อง หรือ การหดรัดของกล้ามเนื้อมัดอื่นๆ ได้

รูปที่ 5– Vaginal dynamometer.
– Vaginal weights/cones
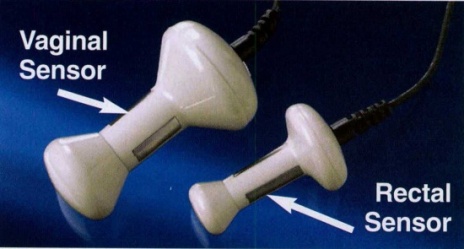
Vaginal cones นั้นสามารถใช้เป็นได้ทั้งเครื่องมือในการวัดประเมิน และเป็นเครื่องมือที่ใช้ในการฝึกฝนด้วย แต่เดิมนั้น Cones ชุดจะประกอบไปด้วย Cones ที่มีน้ำหนักแตกต่างกัน 9 ชิ้น น้ำหนักตั้งแต่ 20 ถึง 100 กรัม โดยแต่ละชิ้นมีปริมาตรเท่ากัน แต่ในปัจจุบัน 1 ชุดจะประกอบไปด้วย Cones 3 และ 5 ชิ้น โดยมีขนาดและรูปร่างที่แตกต่างกัน
ใช้ประเมิน Resting PFM strength หรือ Passive PFM strength คือ น้ำหนักที่มากที่สุดที่สามารถกลั้นไว้ได้เป็นเวลา 1 นาทีโดยไม่มีการหดรัดตัวของ PFM โดยตั้งใจ ส่วน Active PFM strengthคือ น้ำหนักที่มากที่สุดที่สามารถกลั้นไว้ได้เป็นเวลา 1 นาทีโดยมีการหดรัดตัวของ PFM โดยตั้งใจ แต่ก็ไม่ทราบว่ากล้ามเนื้อที่ใช้เพื่อกลั้น Cones ไว้คือกล้ามเนื้ออะไร และจากการศึกษายังไม่ทราบแน่ชัดว่าการกลั้น Cones ไว้จะสัมพันธ์กันการหดรัดตัวของ PFM ดังนั้นการใช้ Cones จะต้องใช้อย่างระมัดระวัง และต้องมีการศึกษาเพิ่มเติมอีกต่อไป

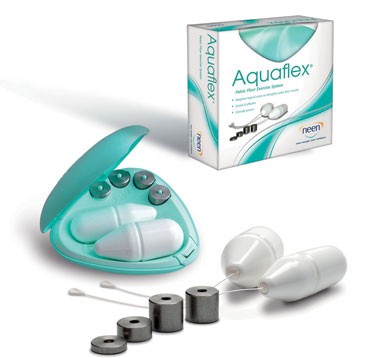
รูปที่ 6– Different sizes and shapes of vaginal cones
จากการศึกษาพบว่าไม่วิธีใดที่สามารถวัดได้ทั้งหน้าที่การทำงานของกล้ามเนื้อ (การยกของกล้ามเนื้อ และแรงในการบีบรัดตัว) เนื่องจากวิธีส่วนใหญ่นั้นจะได้รับผลกระทบจากการตัดสินใจของผู้ให้การประเมิน และแต่ละวิธีก็ยังมีข้อจำกัดในแต่ละวิธีอยู่เช่นกัน1
สรุป
อาการปัสสาวะเล็ดและอุ้งเชิงกรานหย่อนเป็นภาวะที่พบได้บ่อย โดยในภาวะที่อาการไม่รุนแรงโดยส่วนใหญ่แล้วสามารถรักษาให้อาการลดลงหรือหายไปได้ด้วยการบริหารกล้ามเนื้ออุ้งเชิงกราน ในปัจจุบันได้มีการคิดค้นการบริหารร่างกายวิธีต่างเพื่อฝึกกล้ามเนื้ออุ้งเชิงกรานให้แข็งแรง แต่ยังไม่พบหลักฐานใดที่พบว่าวิธีดังกล่าวนี้ มีประสิทธิภาพในการรักษาอาการปัสสาวะเล็ดมากกว่าการบริหารกล้ามเนื้ออุ้งเชิงกราน และร่วมกับ Biofeedback จะช่วยให้การฝึกกล้ามเนื้ออุ้งเชิงกรานสามารถทำได้อย่างมีประสิทธิภาพมากขึ้น ส่วนการประเมินความแข็งแรงของกล้ามเนื้ออุ้งเชิงกรานนั้นยังไม่พบวิธีใดที่สามารถประเมินได้อย่างครอบคลุม ยังจำเป็นต้องมีการศึกษาเพิ่มเติมต่อไป
References
- Bo K, Sherburn M. Evaluation of female pelvic-floor muscle function and strength. Physical therapy. Mar 2005;85(3):269-282.
- Wein AJ. Re: Pelvic floor exercise for urinary incontinence: a systematic literature review. The Journal of urology. Apr 2012;187(4):1353-1354.
- Bo K. Pelvic floor muscle training in treatment of female stress urinary incontinence, pelvic organ prolapse and sexual dysfunction. World journal of urology. Aug 2012;30(4):437-443.
- Bo K, Herbert RD. There is not yet strong evidence that exercise regimens other than pelvic floor muscle training can reduce stress urinary incontinence in women: a systematic review. Journal of physiotherapy. Sep 2013;59(3):159-168.
- Virkud A. Management of stress urinary incontinence. Best practice & research. Clinical obstetrics & gynaecology. Apr 2011;25(2):205-216.
- Bernardes BT, Resende AP, Stupp L, et al. Efficacy of pelvic floor muscle training and hypopressive exercises for treating pelvic organ prolapse in women: randomized controlled trial. Sao Paulo medical journal = Revista paulista de medicina. 2012;130(1):5-9.
- Bo K. Can pelvic floor muscle training prevent and treat pelvic organ prolapse? Acta obstetricia et gynecologica Scandinavica. 2006;85(3):263-268.
- Bulletins–Gynecology ACoP. ACOG Practice Bulletin No. 85: Pelvic organ prolapse. Obstetrics and gynecology. Sep 2007;110(3):717-729.
- Culligan PJ. Nonsurgical management of pelvic organ prolapse. Obstetrics and gynecology. Apr 2012;119(4):852-860.
- Doaee M, Moradi-Lakeh M, Nourmohammadi A, Razavi-Ratki SK, Nojomi M. Management of pelvic organ prolapse and quality of life: a systematic review and meta-analysis. International urogynecology journal. Feb 2014;25(2):153-163.
- Giarenis I, Robinson D. Prevention and management of pelvic organ prolapse. F1000prime reports. 2014;6:77.
- Hagen S, Stark D. Conservative prevention and management of pelvic organ prolapse in women. The Cochrane database of systematic reviews. 2011(12):CD003882.
- Hagen S, Stark D, Glazener C, Sinclair L, Ramsay I. A randomized controlled trial of pelvic floor muscle training for stages I and II pelvic organ prolapse. International urogynecology journal and pelvic floor dysfunction. Jan 2009;20(1):45-51.
- Miklos JR, Moore R. Postoperative cosmetic expectations for patients considering labiaplasty surgery: our experience with 550 patients. Surg Technol Int. 2011;1:170-174.
- Nancy. The History of Kegels. 2013; http://www.nationalincontinence.com/blog/the-history-of-kegels/.
- Patient information: Pelvic floor muscle exercises (Beyond the Basics). 2014.
- Treatment and prevention of urinary incontinence in women. 2014.
- An overview of the epidemiology, risk factors, clinical manifestations, and management of pelvic organ prolapse in women. 2014.
- Cammu H, Van Nylen M. Pelvic floor exercises versus vaginal weight cones in genuine stress incontinence. European journal of obstetrics, gynecology, and reproductive biology. Mar 1998;77(1):89-93.
- Dellas A, Drewe J. Conservative therapy of female genuine stress incontinence with vaginal cones. European journal of obstetrics, gynecology, and reproductive biology. Oct 1995;62(2):213-215.
- Herbison GP, Dean N. Weighted vaginal cones for urinary incontinence. The Cochrane database of systematic reviews. 2013;7:CD002114.
- Kato K, Kondo A. Clinical value of vaginal cones for the management of female stress incontinence. International urogynecology journal and pelvic floor dysfunction. 1997;8(5):314-317.
- Perkins J. Vaginal weights for assessment and training of the pelvic floor. Journal of wound, ostomy, and continence nursing : official publication of The Wound, Ostomy and Continence Nurses Society / WOCN. Jul 1998;25(4):206-216.
- Newman DK. Pelvic floor muscle rehabilitation using biofeedback. Urologic nursing. Jul-Aug 2014;34(4):193-202.
- Prichard D, Bharucha AE. Management of pelvic floor disorders: biofeedback and more. Current treatment options in gastroenterology. Dec 2014;12(4):456-467.
- Wieslander CK. Clinical approach and office evaluation of the patient with pelvic floor dysfunction. Obstetrics and gynecology clinics of North America. Sep 2009;36(3):445-462.