วัคซีน HPV และ การตรวจหาเชื้อไวรัส HPV ด้วยตนเอง
Human Papillomavirus Vaccination and HPV Self-Sampling
นพ.ณัฐพล พบลาภ
อาจารย์ที่ปรึกษา อ.พญ.รัฐิญา เพียรพิเศษ
บทนำ
Human Papilloma Virus (HPV) เป็นเชื้อไวรัส ที่ก่อให้เกิดรอยโรคบริเวณอวัยวะสืบพันธุ์ และช่องปากและลำคอ สามารถติดได้ทั้งในเพศชายและเพศหญิง จากการศึกษาพบว่า หากมีการติดเชื้อไวรัส HPV สายพันธุ์ที่มีความเสี่ยงสูง โดยเฉพาะอย่างยิ่ง สายพันธุ์ 16 และ 18 โดยที่ร่างกายไม่สามารถกำจัดออกไปได้ (persistent HPV infection) จะนำไปสู่การเกิดมะเร็งปากมดลูกในอนาคตได้ ในทำนองเดียวกัน เชื้อไวรัส HPV ยังเป็นปัจจัยสำคัญที่ทำให้เกิดมะเร็งทวารหนัก (anal cancer), มะเร็งช่องปากและลำคอ (oropharyngeal cancer), มะเร็งปากช่องคลอดและมะเร็งช่องคลอด (vulvar and vaginal cancer) และมะเร็งอวัยวะเพศชาย (penile cancer) นอกจากนี้ เชื้อ HPV สายพันธุ์ 6 และ 11 ยังสามารถทำให้เกิดหูดที่อวัยวะเพศ (anogenital wart) ได้ถึงร้อยละ 90
สถิติการเกิดมะเร็งปากมดลูกอ้างอิงจาก GLOBOCAN ค.ศ. 2022 มีอุบัติการณ์ ถึง 662,301คนต่อปี และมีอัตราการเสียชีวิตอยู่ที่ 348,874 คนต่อปี โดยในประเทศไทย พบอุบัติการณ์ อยู่ที่ 8,662 คนต่อปี คิดเป็นร้อยละ 9.3 ของมะเร็งในหญิง และมีอัตราการเสียชีวิตอยู่ที่ 4,576 คนต่อปี เรียกได้ว่าทุกๆ 2 ชั่วโมง จะมีหญิงที่เสียชีวิตจากมะเร็งปากมดลูก 1 คน
เนื่องจากมีข้อมูลบ่งชี้ชัดเจนว่า มะเร็งปากมดลูกเกิดจากการติดเชื้อไวรัส HPV ชนิดความเสี่ยงสูง เป็นเวลานาน จึงได้มีการศึกษามากมาย เพื่อหาวิธีป้องกันการเกิดมะเร็งชนิดนี้ โดยการป้องกันที่ได้รับการยอมรับว่าสามารถช่วยลดอุบัติการณ์การเกิดมะเร็งปากมดลูกได้อย่างมีประสิทธิภาพก็คือ การฉีดวัคซีน HPV และการตรวจคัดกรองเชื้อ HPV โดยคาดว่าการป้องกันดังกล่าว จะช่วยลดอุบัติการณ์ และลดอัตราการเสียชีวิตจากมะเร็งปากมดลูกลงได้อย่างมาก นำมาสู่การวางกลยุทธของ องค์การอนามัยโลก ในปี ค.ศ. 2018 ที่ผ่านมา มีเป้าหมายจะลดอุบัติการณ์ การเกิดมะเร็งปากมดลูกลงให้เหลือต่ำกว่า 4 ราย ต่อหญิง 100,000 คน โดยให้เด็กผู้หญิงที่อายุต่ำกว่า 15 ปี ต้องได้รับ vaccine อย่างน้อยร้อยละ 90 ให้หญิงวัย 35 และ 45 ปี ได้รับการคัดกรองมะเร็งปากมดลูกด้วยการตรวจหาเชื้อ HPV อย่างน้อยร้อยละ 70 และให้หญิงที่ตรวจพบความผิดปกติของปากมดลูก ได้รับการรักษา อย่างน้อยร้อยละ 90
ชนิดของวัคซีน HPV
วัคซีน HPV ที่มีในปัจจุบัน มี 3 ชนิด คือ ชนิดสองสายพันธุ์ (bivalent), สี่สายพันธุ์ (quadrivalent) และ เก้าสายพันธุ์ (nonavalent)
- Bivalent (Cervarix/Cecolin) ป้องกัน HPV สายพันธุ์ 16 และ 18
- Quadrivalent (Gardasil) ป้องกัน HPV สายพันธุ์ 6, 11, 16 และ 18
- Nonavalent (Gardasil-9) ป้องกัน HPV สายพันธุ์ 6, 11, 16, 18, 31, 33, 45, 52 และ 58
ซึ่งวัคซีนทั้งหมดได้รับการออกแบบมาเพื่อป้องกันการติดเชื้อ HPV ในระยะเริ่มแรกและรอยโรคที่เกี่ยวข้องกับ HPV ที่เกิดในภายหลัง (HPV-associated lesions)1,2
ใครบ้างที่ควรได้รับ vaccine และควรได้รับเมื่อใด
ตามคำแนะนำของ American College of Obstetricians and Gynecologists (ACOG) ค.ศ. 20203 แนะนำให้ฉีดวัคซีน HPV ทั้งในผู้ชายและผู้หญิง โดยแนะนำในช่วงกลุ่มอายุ 9-26 ปี (มีการฉีดเป็นวัคซีนพื้นฐานที่อายุ 11-12 ปี แต่อาจเริ่มฉีดได้ตั้งแต่อายุ 9 ปีในบางรายที่มีความเสี่ยงต่อการรับเชื้อสูง) สำหรับผู้ที่มีอายุมากกว่า 26 ปีไปจนถึงอายุ 45 ปี แนะนำให้มีตัดสินใจร่วมกับแพทย์ผู้ดูแล ถึงประสิทธิภาพ ผลข้างเคียง และความคุ้มค่า และในคำแนะนำล่าสุด ของศูนย์ควบคุมโรคติดต่อสหรัฐอเมริกา (CDC) ค.ศ. 20234 ก็ไปในแนวทางเดียวกัน
สำหรับคำแนะนำเกี่ยวกับการฉีดวัคซีน HPV ของราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทยแนะนำไว้ดังนี้
- กลุ่มเป้าหมายหลักที่แนะนำให้ฉีดวัคซีน คือ เด็กหญิงอายุ 11-12 ปี โดยฉีด 2 เข็ม ห่างกัน 6-12 เดือน
- กลุ่มอื่นที่แนะนำให้ฉีดวัคซีน คือ
- หญิงและชาย ช่วงอายุ 9-26 ปี โดยฉีด 3 เข็มที่ 0, 1-2, และ 6 เดือน (หากอายุน้อยกว่า 15 ปี ให้ฉีด 2 เข็ม ห่างกัน 6-12 เดือนได้ ยกเว้นมีภาวะภูมิคุ้มกันต่ำต้องฉีดให้ครบ 3 เข็ม)
- หญิงและชายที่มีภาวะภูมิคุ้มกันต่ำ เช่น ติดเชื้อ Human Immunodeficiency Virus (HIV)
- หญิงที่เคยมีผลเซลล์วิทยาปากมดลูก (PAP smear) หรือ ผลตรวจเชื้อ HPV (HPV testing) ผิดปกติ หรือ เคยเป็นรอยโรคระยะก่อนมะเร็งปากมากมดลูก หรือเคยเป็นหูดหงอนไก่มาก่อน
- กลุ่มหญิงอายุ 26-45 ปี ให้พิจารณาการฉีดวัคซีนเป็นรายๆ ไป โดยตัดสินใจร่วมกับบุคลากรทางการแพทย์ หลังจากได้รับข้อมูลเกี่ยวกับความเสี่ยงการติดเชื้อ HPV และประโยชน์ของการฉีดวัคซีน
ในประเทศไทยมีการกำหนดการให้วัคซีนตามแผนงานสร้างเสริมภูมิคุ้มกันโรคของกระทรวงสาธารณสุขปี พ.ศ 2567 โดยจะให้ฉีดวัคซีน HPV เข็มที่ 1 และ 2 ในนักเรียนหญิงชั้นประถมศึกษาปีที่ 5 โดยให้ฉีดแต่ละเข็มห่างกันอย่างน้อย 6 เดือน และกรณีเด็กที่ไม่ได้อยู่ในระบบการศึกษาให้ฉีดที่อายุ
11-12 ปี
เหตุผลที่เลือกช่วงอายุตามคำแนะนำต่างๆข้างต้น เพราะระยะเวลาที่เหมาะสมที่จะทำให้วัคซีนมีประสิทธิภาพสูงสุดคือ การฉีดวัคซีนก่อนการมีเพศสัมพันธ์ครั้งแรก และหากมีการติดเชื้อ HPV แล้วจะไม่มีการนำวัคซีนมาเพื่อใช้ในรักษาหรือช่วยเร่งการกำจัดเชื้อ HPV อย่างไรก็ตามการที่เคยมีผล PAP smear หรือ HPV testing ผิดปกติ, การเคยเป็นหูดหงอนไก่มาก่อนไม่ได้เป็นข้อห้ามในการฉีดวัคซีน 5,6
ควรเลือกฉีดวัคซีนชนิดไหนดี
การพิจารณาชนิดวัคซีนที่จะฉีดนั้น ขึ้นอยู่กับการเข้าถึงของวัคซีนในแต่ละพื้นที่รวมถึงปัจจัยเรื่องของค่าใช้จ่ายในการฉีดวัคซีนก็มีความสำคัญในการพิจารณา อย่างไรก็ตาม หากตัดปัจจัยเรื่องการเข้าถึงและค่าใช้จ่ายออกไป คำแนะนำในปัจจุบันแนะนำให้ฉีดเป็นชนิด 9 สายพันธุ์ ด้วยเหตุผลที่สามารถครอบคลุมชนิดของเชื้อ HPV ได้มากกว่า รวมถึงได้ประโยชน์จากภูมิคุ้มกันระดับชุมชน (herd immunity) จากการได้รับวัคซีนทั้งในผู้ชายและผู้หญิง และจากการศึกษาปัจจุบันพบว่าวัคซีนชนิด 9 สายพันธุ์ ช่วยลดอัตราการเกิดของมะเร็งในผู้ชายมากขึ้นด้วย7
การประเมินและเตรียมความพร้อมก่อนฉีดวัคซีน
สามารถฉีดวัคซีนโดยไม่ต้องเตรียมความพร้อมใดๆ เป็นพิเศษ ไม่ต้องตรวจการตั้งครรภ์ และไม่มีความจำเป็นต้องทำการตรวจ HPV testing หรือภูมิคุ้มกัน ก่อนการได้รับวัคซีน8
กลุ่มประชากรที่ต้องได้รับการพิจารณาเป็นพิเศษ
- หญิงตั้งครรภ์ และหญิงให้นมบุตร
ไม่แนะนำให้ฉีดวัคซีน HPV หากทราบว่ากำลังตั้งครรภ์ เนื่องจากยังมีข้อจำกัดเกี่ยวกับข้อมูลการศึกษาด้านความปลอดภัย แต่หากทราบว่าตั้งครรภ์หลังจากเริ่มฉีดไปแล้วสามารถตั้งครรภ์ต่อไปได้
เนื่องจากการศึกษาปัจจุบันพบว่า การได้รับวัคซีนช่วงตั้งครรภ์ไม่ได้เพิ่มความเสี่ยงต่อ การเกิดภาวะแทรกซ้อนระหว่างตั้งครรภ์ และความผิดปกติของทารกแต่อย่างใด เพื่อให้เกิดความมั่นใจและคลายกังวลของหญิงตั้งครรภ์ แต่วัคซีนที่ต้องฉีดเข็มต่อไปให้เลื่อนไปฉีดหลังคลอด ซึ่งมีการศึกษาว่าวัคซีนมีความปลอดภัยมากพอต่อหญิงที่กำลังให้นมบุตรอยู่ ดังนั้นหญิงหลังคลอดและกำลังให้นมบุตรสามารถได้รับวัคซีนได้เหมือนคนทั่วไป7,8
- หญิงที่มีประวัติติดเชื้อ HPV หรือมีรอยโรคที่สัมพันธ์กับเชื้อ HPV
หญิงที่เคยมีประวัติหูดที่อวัยวะเพศ, มีผลการตรวจคัดกรอง HPV เป็นบวก หรือผลเซลล์วิทยาของปากมดลูก ช่องคลอด ปากช่องคลอดและทวารหนักมีความผิดปกติ ซึ่งบ่งชี้ว่ามีการติดเชื้อ HPV มาแล้ว การฉีดวัคซีน HPV จะยังคงมีประโยชน์ในการป้องกันการติดเชื้อ HPV สายพันธุ์ที่ยังไม่เคยติดมาก่อน จึงยังแนะนำให้มีการฉีดวัคซีนในคำแนะนำข้างต้นในแต่ล่ะชวงอายุดังที่กล่าวไป8,9
อย่างไรก็ตามการฉีดวัคซีนไม่ได้มีส่วนในการรักษาในการติดเชื้อ HPV ก่อนหน้าและประสิทธิภาพของวัคซีนจะไม่ได้เท่ากับหญิงที่ยังไม่เคยได้รับเชื้อมาก่อน ดังนั้น แพทย์ควรให้คำแนะนำนี้ก่อนฉีดวัคซีนด้วย
- บุคลากรทางการแพทย์
สมาคมคอลโปสโคปีและพยาธิวิทยาของปากมดลูกแห่งประเทศสหรัฐอเมริกาหรือ American Society for Colposcopy and Cervical Pathology (ASCCP) กล่าวไว้ว่า บุคลากรทางการแพทย์ขณะปฏิบัติงานรักษารอยโรคที่เกดิจากเชื้อ HPV ไม่ว่าจะเป็นการตัด หรือ จี้ทำลายรอยโรค อาจได้รับเชื้อ HPV จากการที่มีละอองฝอยฟุ้งกระจายได้ สำหรับความเสี่ยงยังไม่เป็นที่แน่ชัด คำแนะนำปัจจุบันบุคลากรทางการแพทย์ควรได้รับวัคซีน HPV เป็นวัคซีนพื้นฐาน ซึ่งบุคคลากรทางการแพทย์นี้รวมถึงแพทย์ผู้รักษา พยาบาล และเจ้าหน้าที่ผู้เกี่ยวข้องที่ต้องสัมผัสผู้ป่วยด้วย10
- ผู้ที่มีภาวะภูมิคุ้มกันบกพร่อง
กลุ่มคนที่มีภาวะภูมิคุ้มกันบกพร่อง11 อันได้แก่ผู้ติดเชื้อ HIV และมี CD4 น้อยกว่า 200 cells/mL,
ผู้ป่วยเปลี่ยนถ่ายอวัยวะ, รับประทานยากดภูมิ, โรคภูมิตุ้มกันต่อต้านตนเอง (autoimmune disease), กลุ่มเม็ดเลือดขาวทำงานบกพร่อง (Complete or partial T-lymphocyte defects) และ B-lymphocyte antibody deficiencies
ตามแนวทางเวชปฏิบัติของราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย12 แนะนำให้คนกลุ่มนี้ได้รับวัคซีน HPV จำนวน 3 เข็ม ที่ 0, 1-2 และ 6 เดือน (เนื่องมาจากประสิทธิภาพของวัคซีนอาจไม่เท่ากับคนทั่วไป) และในกลุ่มนี้แม้ว่าอายุมากกว่า 26 ปีก็ยังแนะนำให้ฉีดวัคซีน HPV อยู่ถ้าก่อนหน้านี้ไม่เคยได้รับวัคซีน
ประสิทธิภาพและการตอบสนองของภูมิคุ้มกัน
ประสิทธิภาพในการสร้างแอนติบอดีค่อนข้างสูงทั้งในวัคซีนชนิด nonavalent, quadrivalent และ bivalent โดยในภาพรวมอัตรา seroconversion rate อยู่ที่ร้อยละ 93-100 ในผู้หญิงและร้อยละ 99-100 ในผู้ชาย1,13-16 และระดับ titer ของภูมิคุ้มกันจะขึ้นสูงในผู้ที่มีอายุน้อยเทียบกับอายุมาก ในปัจจุบันยังไม่ทราบว่าระดับ titer ที่เหมาะสมว่าเท่าใด จึงเพียงพอต่อการป้องกันการติดเชื้อ HPV (minimum threshold titer) แต่พบความสัมพันธ์ว่าเมื่อระดับภูมิคุ้มกันขึ้นไม่ว่าจะมากหรือน้อยเมื่อติดตามไปพบว่าความเสี่ยงในการติดเชื้อของ HPV จีโนไทป์ชนิดนั้นๆ จะลดลง17,18 และเมื่อเปรียบเทียบระดับภูมิคุ้มกันของการฉีดวัคซีนกับการติดเชื้อโดยธรรมชาติพบว่าระดับภูมิคุ้มกันที่ขึ้นจากการฉีดวัคซีนสูงกว่าการติดเชื้อโดยธรรมชาติ
เมื่อมีข้อจำกัดและสามารถฉีดวัคซีนได้เพียง 1 เข็ม (Single dose of HPV vaccine)
มีการทบทวนวรรณกรรมอย่างเป็นระบบ ใน ค.ศ. 2019 – 2022 เกี่ยวกับ การได้รับวัคซีนHPV 1 เข็ม โดยเทียบระหว่างกลุ่มที่ได้รับวัคซีนเพียง 1 เข็มกับกลุ่มที่ไม่ได้รับวัคซีน, ได้รับวัคซีน 2 และ 3 เข็ม เฝ้าติดตามอุบัติการณ์ในการตรวจพบ HPV สายพันธุ์ 16 และ18 ที่คงอยู่มากกว่า 6 เดือน พบว่ากลุ่มที่ได้รับวัคซีนเพียง 1 เข็มเทียบกับกลุ่มที่ไม่ได้รับวัคซีนเลย อุบัติการณ์การตรวจพบเชื้อ HPV ลดลงอย่างมีนัยสำคัญทางสถิติ และให้ผลที่สอดคล้องกันเมื่อตามดูอุบัติการณ์ที่ 12 เดือน19
และเมื่อเปรียบเทียบระหว่างกลุ่มที่ได้รับวัคซีนเพียง 1 เข็มกับกลุ่มที่ได้รับวัคซีน 2 เข็ม พบว่าอุบัติการณ์ในการตรวจพบ HPV สายพันธุ์ 16 และ18 ที่คงอยู่มากกว่า 6 และ 12 เดือน ไม่ได้มีความแตกต่างกันอย่างมีนัยสำคัญทางสถิติ รวมไปถึงการเกิดรอยโรคระยะก่อนมะเร็ง (CIN2+) ก็พบว่าสอดคล้องไปในแนวทางเดียวกันคือไม่ได้มีความแตกต่างกันของอุบัติการณ์การเกิด แต่เมื่อดูผลในแง่ของ การสร้างระดับภูมิคุ้มกัน (immunogenicity) พบว่าเมื่อเปรียบเทียบกลุ่มที่ได้รับวัคซีน 2 เข็มกับ 1 เข็ม ใน ระดับภูมิคุ้มกัน ของกลุ่มที่ได้รับวัคซีน 2 เข็มจะมีระดับที่สูงกว่า จึงแนะนำว่า ถ้าไม่ได้มีข้อจำกัดในแง่ค่าใช้จ่ายและการเข้าถึงควรได้รับฉีดวัคซีนให้ครบ แต่ถ้ามีข้อจำกัด การได้รับวัคซีนเพียง 1 เข็มก็ดีกว่าไม่ได้รับวัคซีนเลย และนอกจากประโยชน์ด้านการลดอุบัติการณ์รอยโรคก่อนมะเร็งแล้ว การได้รับวัคซีนเพียง 1 เข็ม ยังมีประโยชน์ในเรื่องของการลดอัตราการเกิดหูดที่อวัยวะเพศได้ด้วย เมื่อเทียบกับกลุ่มที่
ไม่เคยได้รับวัคซีน
ความปลอดภัยของวัคซีน HPV
วัคซีน HPV ทุกชนิดมีข้อมูลรับรองเกี่ยวกับความปลอดภัยที่ได้รับจากการศึกษาทดลองทางคลินิกขนาดใหญ่ และยังไม่มีข้อมูลถึงภาวะแทรกซ้อนรุนแรงภายหลังจากการได้รับอนุญาตและนำมาใช้ทางคลินิก วัคซีนทั้งหมดที่ผลิตขึ้นนั้นได้ใช้ส่วนประกอบที่คล้ายกับ viral capsid โดยที่ไม่มีสารพันธุกรรมของไวรัส และผลิตขึ้นในระบบชีวภาพที่มีการควบคุมและมีประวัติการใช้งานที่ปลอดภัยอย่างชัดเจน20 คณะกรรมการขององค์การอนามัยโลก (WHO)21 ระบุว่าเมื่อเปรียบเทียบความเสี่ยง กับประโยชน์ของวัคซีนพบว่าอยู่ในเกณฑ์ที่เหมาะสม และหลักฐานปัจจุบันไม่พบความเกี่ยวข้องว่าการฉัดวัคซีน HPV จะส่งผลเสียต่อภาวะเจริญพันธุ์ 22,23
สำหรับผลข้างเคียงที่พบบ่อย ได้แก่ อาการปวดศีรษะ คลื่นไส้ อาเจียน รู้สึกอ่อนเพลีย บางรายงาน24 พบอาการเวียนศีรษะและเป็นลมหมดสติ รวมไปถึงมีส่วนน้อยที่มีอาการกล้ามเนื้ออ่อนแรง แต่ไม่พบว่าเพิ่มความเสี่ยงต่อการเกิด Guillain-Barré Syndrome เมื่อเปรียบเทียบระหว่างกลุ่มที่ได้รับวัคซีนป้องกันโรคชนิดอื่นๆในกลุ่มอายุเดียวกัน25
พฤติกรรมที่เปลี่ยนไปหลังฉีดวัคซีน HPV
หลายคนมีความกังวลเกี่ยวกับการมีพฤติกรรมทางเพศที่ไม่เหมาะสมหลังจากฉีดวัคซีน HPV มีหลายการศึกษา26,27 พยายามแสดงให้เห็นว่าการฉีดวัคซีน HPV ไม่ได้เพิ่มความเสี่ยงในการมีเพศสัมพันธ์ที่ไม่ปลอดภัย อ้างอิงการศึกษาหนึ่ง28 ที่ทำในเด็กอายุ 11-12 ปี 493 คนมีประวัติการฉีดวัคซีนอย่างน้อย 1 เข็ม และ 905 คนไม่เคยได้รับการฉีดวัคซีน โดยติดตามอัตราการตั้งครรภ์ การติดเชื้อคลาไมเดีย (Chlamydia trachomatis) และอัตราการเข้ารับการปรึกษาเรื่องการคุมกำเนิด เมื่อปรับตัวกวนในเรื่องปัจจัยพื้นฐานทางสุขภาพ เชื้อชาติและสถานภาพ พบว่าการฉีดวัคซีน HPV ไม่ได้ส่งผลต่ออัตราการเพิ่มขึ้นของพฤติกรรมทางเพศที่ไม่เหมาะสม
กลยุทธ์ในการเพิ่มการได้รับวัคซีน HPV
จากการสำรวจโดยใช้แบบสอบถามผู้ปกครองถึงเหตุผลที่ไม่สนใจในการฉีดวัคซีน HPV ให้กับบุตรหลานตนเองตั้งแต่วัยเด็ก พบ 5 เหตุผลสำคัญดังนี้
- ยังมีความกังวลเกี่ยวกับความปลอดภัยของวัคซีน HPV
- ยังไม่เห็นถึงความจำเป็นและไม่ได้มีผู้แนะนำให้ฉีด
- ยังขาดความรู้ความเข้าใจเกี่ยวกับวัคซีน และตัวโรคที่เกิดจากเชื้อไวรัส HPV
- ไม่คิดว่าบุตรหลานตนเองจะมีกิจกรรมทางเพศในวัยนี้
- ขาดโอกาสในการเข้าถึงวัคซีน ในที่นี้รวมถึงสิทธิ์การรักษา และค่าใช้จ่ายในการฉีดวัคซีน
ได้มีการแก้ปัญหาเหล่านี้โดยยึดหลักการดำเนินงานโดยยึดชุมชนเป็นฐาน (Community based Intervention: CBI) เพื่อเพิ่มการเข้าถึงวัคซีน รวมถึงเน้นย้ำความสำคัญต่อประชาชน และแพทย์ที่ลงตรวจให้มีการแนะนำทั้งเชิงรับและเชิงรุก รวมไปถึงกลยุทธ์ทางการตลาดด้านราคาและการส่งสริมการขายให้มากขึ้น บางประเทศแก้ปัญหาโดยการจัดเป็นวัคซีนพื้นฐาน (national vaccine program) เช่น สหราชอาณาจักร, เดนมาร์ก, ออสเตรเลีย เป็นต้น29-31
ในประเทศไทยได้ใช้กลยุทธดำเนินงานในรูปแบบวัคซีนในสถานศึกษา (school-based vaccination) โดยดำเนินงานผ่านสถาบันการศึกษา ล่าสุดเมื่อ พ.ศ. 2566 ที่ผ่านมา หลังจากพึ่งผ่านพ้นวิกฤติ covid-19 ที่ทำให้วัคซีน HPV ขาดและการเข้าถึงวัคซีนน้อยลงอย่างมีนัยสำคัญ จึงได้ออกแนวทางการให้บริการวัคซีนป้องกันการติดเชื้อไวรัส HPV ตามนโยบายเร่งรัด 100 วันของกระทรวงสาธารณสุขโดยเน้นกลุ่มเป้าหมายหญิงไทยอายุ 11-20 ปี ที่ยังไม่ได้รับวัคซีนครบ 2 เข็ม ดำเนินงานใน 76 จังหวัดและกรุงเทพมหานคร เป้าหมายคือ การฉีดวัคซีน HPV ให้ได้อย่างน้อย 1 ล้านโดสใน 100 วัน
มะเร็งปากมดลูก ตรวจพบเร็ว รักษาได้ ด้วย HPV self-sampling
HPV เป็นเรื่องของทุกคน คนโสดหรือไม่เคยมีเพศสัมพันธ์ก็มีโอกาสติดเชื้อ HPV จากการสัมผัสสิ่งต่างๆ ที่มีเชื้อได้ ดังนั้น เพื่อเพิ่มการเข้าถึงการคัดกรอง ลดความเขินอายของผู้รับบริการ ลดภาระต่อผู้ให้บริการ ปัจจุบัน จึงได้มีการแนะนำ ให้ประชาชนตรวจคัดกรองมะเร็งปากมดลูกด้วยตนเอง ด้วยวิธี HPV self-sampling
ตามแนวทางการเก็บสิ่งส่งตรวจด้วยตนเองของสถาบันมะเร็งแห่งชาติ (National Cancer Institute) กรมการแพทย์และกระทรวงสาธารณสุข แนะนำวิธีการเก็บสิ่งส่งตรวจด้วยตนเองดังนี้32
- ล้างมือให้สะอาด / สเปรย์แอลกอฮอล์ก่อนการเก็บตัวอย่างทุกครั้ง
- ฉีกซองไม้เก็บตัวอย่าง จับตรงส่วนของขีดสีดำระวังอย่าสัมผัสโดนส่วนของสำลีปลายไม้เก็บตัวอย่าง และห้ามนำไม้เก็บตัวย่างไปจุ่มในขวดน้ำยาก่อนเก็บตัวอย่าง
- ยืนหรือนั่งในท่าที่สบาย ใช้ไม้เก็บตัวอย่างสอดเข้าไปในช่องคลอด ลึกประมาณ 2 นิ้วหรือ 5 เซนติเมตร จากนั้นหมุนไม้เก็บตัวอย่างในทิศทางเดียวกันให้สำลีที่ปลายไม้เก็บตัวอย่างสัมผัสกับผนังของช่องคลอด จับเวลาประมาณ 10-30 วินาที แล้วดึงไม้ออก
- เปิดฝาหลอดเก็บตัวอย่าง ในขณะที่ยังคงถือไม้เก็บตัวอย่างไว้ (ไม่ควรวางไม้เก็บตัวอย่างไว้ที่พื้นเพราะอาจจะเกิดการปนเปื้อนได้) ระวังอย่าให้น้ำยาในหลอดหก
- จุ่มไม้เก็บตัวอย่างลงในหลอดน้ำยาเก็บตัวอย่างให้ขีดสีดำกลางไม้ตรงกับขอบของหลอดน้ำยาแล้วทำการหักส่วนเกินของไม้เก็บตัวอย่างทิ้ง
- ปิดฝาหลอดน้ำยาเก็บอย่างให้สนิทพร้อมเขียนชื่อ-นามสกุลที่ข้างหลอด
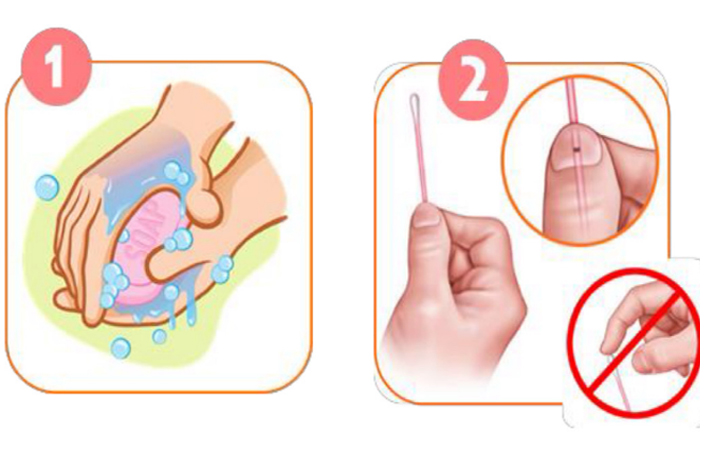
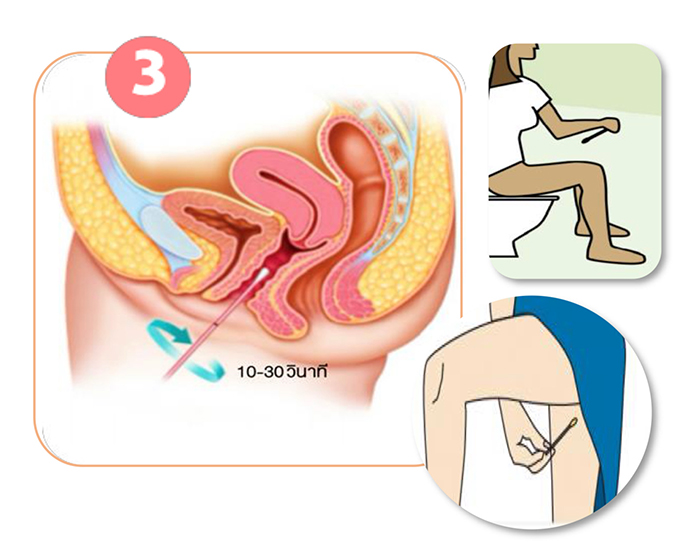
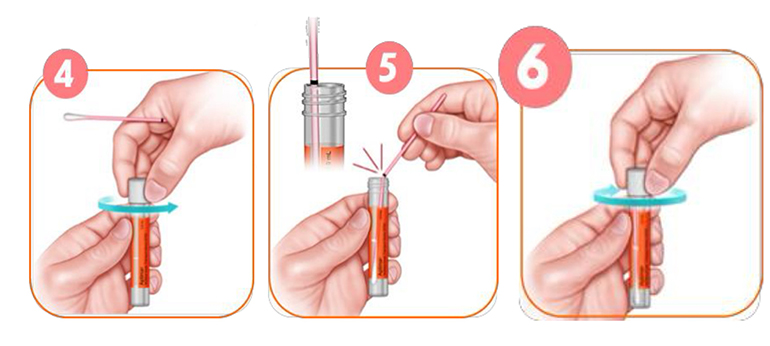
ภาพที่ 1: วิธีการเก็บสิ่งส่งตรวจ HPV self-sampling ด้วยตนเอง สถาบันมะเร็งแห่งชาติ
เมื่อไหร่จึงควรตรวจ
ไม่ใช่ทุกคนที่มีเชื้อ HPV จะกลายเป็นมะเร็งปากมดลูกเสมอไป ถ้าระบบภูมิคุ้มกันของร่างกายทำงานได้ดี จะสามารถกำจัดเชื้อได้เองได้ถึงร้อยละ 90 ภายในระยะเวลา 1-2 ปี ฉะนั้นการจะกลายเป็นระดับผิดปกติที่มากขึ้นหรือเป็นมะเร็งนั้นจะต้องมีการคงอยู่ของเชื้อ (persistent infection) และระยะกว่าที่จะกลายเป็นมะเร็งนั้นใช้ระยะถึง 5-15 ปี ด้วยการดำเนินโรคที่ช้า จึงเป็นที่มาให้เรามีโอการในการคัดกรองและตรวจพบระยะก่อนมะเร็งได้มากกว่ามะเร็งชนิดอื่นๆ
แนวทางในการตรวจคัดกรองมะเร็งปากมดลูกในปัจจุบันแนะนำให้มีการตรวจคัดกรองด้วย HPV testing เป็นหลักและการตรวจคัดกรองโดยใช้การตรวจแบบเซลล์วิทยามีบทบาทน้อยลง โดยทั่วไปจะเริ่มคัดกรองที่อายุ 25 ปี ไปจนถึงอายุ 65 ปี ดังคำแนะนำการตรวจคัดกรองมะเร็งปากมดลูก อ้างอิงตามราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย พ.ศ. 2563
| การตรวจเซลล์วิทยา (PAP smear หรือ liquid based cytology) |
HPV DNA testing | ||
| ร่วมกับการตรวจเซลล์วิทยา (co-testing) | Primary HPV testing |
||
| อายุที่เริ่มตรวจ | 25 ปี ในสตรีที่มีเพศสัมพันธ์แล้ว หรือ 30 ปี ในสตรีที่ไม่เคยมีเพศสัมพันธ์ |
25 ปี ในสตรีที่มีเพศสัมพันธ์แล้ว หรือ 30 ปี ในสตรีที่ไม่เคยมีเพศสัมพันธ์ | 25 ปี ในสตรีที่มีเพศสัมพันธ์แล้ว หรือ 30 ปี ในสตรีที่ไม่เคยมีเพศสัมพันธ์ |
| ความถี่ในการตรวจ | ทุก 2 ปี | ทุก 5 ปี | ทุก 5 ปี |
| อายุที่หยุดตรวจ | มากกว่า 65 ปี ถ้าผลตรวจไม่พบความผิดปกติติดต่อกัน 5 ครั้ง | มากกว่า 65 ปี ถ้าผลตรวจไม่พบความผิดปกติติดต่อกัน 2 ครั้ง | มากกว่า 65 ปี ถ้าผลตรวจไม่พบความผิดปกติติดต่อกัน 2 ครั้ง |
*สตรีที่อายุน้อยกว่า 25 ปี ไม่แนะนำให้ตรวจคัดกรอง ยกเว้นในสตรีที่มีความเสี่ยงสูง เช่น ติดเชื้อเฮชไอวี มีคู่นอนหลายคน เป็นโรคติดเชื้อทางเพศสัมพันธ์ เป็นต้น
**สตรีที่ตัดมดลูกพร้อมกับปากมดลูกออกแล้วและไม่มีประวัติเป็น CIN หรือมะเร็งปากมดลูก ไม่จำเป็นต้องตรวจคัดกรอง.
ตารางที่ 1: ดัดแปลงจากคำแนะนำการตรวจคัดกรองมะเร็งปากมดลูก ราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย พ.ศ. 2563
ความน่าเชื่อถือของการตรวจด้วยตนเอง
การที่ผลตรวจจะน่าเชื่อถือหรือไม่นั้น นอกจากวิธีการเก็บสิ่งส่งตรวจที่ควรทำอย่างถูกต้องแล้วชุดอุปกรณ์ที่ใช้ในการเก็บสิ่งส่งตรวจก็มีความสำคัญเช่นกันและควรได้รับการรับรองก่อนนำมาใช้ตรวจ โดยปัจจุบันมี 2 องค์กรที่ออกมารับรองชุดอุปกรณ์การการตรวจคือ WHO และ FDA ในข้อบ่งชี้ primary HPV testing
- Cobas รับรองโดย FDA (ตรวจหาเชื้อ HPV กลุ่มความเสี่ยงสูง 12 สายพันธุ์ และ รายงานผลสายพันธุ์ 16 และ 18 แยกต่างหาก)
- BD Onclarity รับรองโดย FDA (ตรวจหาเชื้อ HPV ความเสี่ยงสูง 14 สายพันธุ์ โดยรายงานแยก 6 สายพันธุ์ คือ สายพันธุ์ 16, 18, 31, 45, 51, and 52 และรายงานเป็นกลุ่ม สายพันธุ์ที่เหลือ ได้แก่ สายพันธุ์ 33,58,35,39,68,56,59,66
- Cepheid Xpert HPV รับรองโดย WHO (ตรวจหาเชื้อ HPV กลุ่มความเสี่ยงสูง 11 สายพันธุ์ และ รายงานผลสายพันธุ์ 16 และ 18/45 แยก)
- Qiagen care รับรองโดย WHO (ตรวจหาเชื้อ HPV กลุ่มความเสี่ยงสูง 14 สายพันธุ์)
สำหรับคำแนะนำ ของ WHO ค.ศ. 2022 (strong recommendation) แนะนำให้ใช้การตรวจหาเชื้อ HPV ด้วยตนเอง เป็นทางเลือกเสริมในการตรวจคัดกรองมะเร็งปากมดลูกในกลุ่มอายุ 30-60 ปี
มีข้อกังวลว่าการให้ประชาชนตรวจเองกับการตรวจโดยบุคลากรทางการแพทย์ โอกาสในการตรวจพบเชื้อ HPV มีความแตกต่างกันมากน้อยเพียงใด ข้อดีของการเก็บตัวอย่างโดยบุคลากรทางการแพทย์ คือจะสามารถตรวจดูลักษณะช่องคลอด ปากช่องคลอด ปากมดลูก รวมถึงลักษณะสารคัดหลั่งต่างๆ และเก็บสิ่งส่งตรวจจากตรงบริเวณปากมดลูกได้มากกว่า แต่ด้วยข้อจำกัดของการตรวจหาเชื้อ HPV ด้วยตนเอง คือผู้ตรวจจะไม่สามารถมองเห็นความผิดปกติดังกล่าวได้ บางคนไม่กล้าใส่อุปกรณ์การตรวจเข้าไปลึก ฉะนั้นมีโอกาสที่จะได้สิ่งส่งตรวจจากปากมดลูกน้อยลง โดยอาจได้สิ่งส่งตรวจจากบริเวณช่องคลอดด้านบน ด้านล่างหรือแค่บริเวณปากช่องคลอดมาแทน
การศึกษา33 พบว่าการเก็บสิ่งส่งตรวจจากปากมดลูก ช่องคลอดส่วนบนและส่วนล่าง หรือปากช่องคลอดโอกาสในการตรวจพบ CIN2+ (sensitivity) มีความแตกต่างกันโดยจะลดหลั่นไปตามความห่างจากปากมดลูก แต่ในภาพรวมโอกาสในการตรวจพบยังมากกว่าร้อยละ 90 และความแตกต่างของการตรวจพบ CIN2+ ในแต่ละบริเวณมีความแตกต่างกันน้อยมาก (น้อยกว่าร้อยละ 10 และไม่มีนัยสำคัญทางสถิติ)34
อย่างไรก็ตามคำแนะนำในปัจจุบัน แนะนำว่า ควรเก็บให้ถูกต้องและลึกมากพอเพื่อเพิ่ม ความไว และความจำเพาะต่อโรค
วิธีการตรวจจากสิ่งส่งตรวจปัจจุบันมี 2 วิธีคือการตรวจแบบ signal amplification (SA) และ polymerase chain reaction (PCR) สำหรับการตรวจหาเชื้อ HPV ด้วยตนเอง แนะนำให้ทำการตรวจแบบ PCR มากกว่า signal amplification เนื่องจากจะเพิ่มโอกาสการตรวจพบเชื้อ ส่วนการเก็บสิ่งส่งตรวจโดยใช้ swabs, brushes หรือ tampons ให้ผลลัพธ์ไม่ต่างกัน34
บทสรุป
การส่งเสริมการฉีดวัคซีนป้องกันเชื้อไวรัส HPV และการตรวจคัดกรองด้วยตนเองถือเป็นกลไกสำคัญในการป้องกันและการตรวจพบมะเร็งปากมดลูกระยะเริ่มต้น การนำโครงการฉีดวัคซีนป้องกันไวรัส HPV มาใช้อย่างแพร่หลายได้ลดการติดเชื้อ HPV หูดหงอนไก่ และรอยโรคก่อนเป็นมะเร็งปากมดลูกได้อย่างมีนัยสำคัญ ส่งผลให้อุบัติการณ์มะเร็งปากมดลูกลดลง
นอกจากนี้ การบูรณาการการตรวจคัดกรอง HPV ด้วยตนเองเข้าไปในโครงการคัดกรองมะเร็งปากมดลูกยังเป็นการเพิ่มอัตราการเข้ารับการคัดกรอง โดยเฉพาะในกลุ่มผู้ด้อยโอกาส ผู้ที่มีความเขินอาย และผู้ที่เข้าถึงบริการสาธารณสุขได้ยาก
แม้จะมีความก้าวหน้าเหล่านี้ แต่ก็ยังมีความท้าทายในแง่การสร้างความเท่าเทียมในการเข้าถึงการฉีดวัคซีนและการคัดกรอง HPV การรับมือกับความกังวลใจเรื่องวัคซีน และการปรับใช้โครงการตรวจ HPV ด้วยตนเองในสภาพแวดล้อมทางการแพทย์ที่หลากหลาย จำเป็นต้องมีความพยายามอย่างต่อเนื่องในการให้การศึกษา การรณรงค์ และการจัดสรรทรัพยากรเพื่อเอาชนะอุปสรรคเหล่านี้ เพื่อที่เราจะสามารถก้าวสู่เป้าหมายในการขจัดมะเร็งปากมดลูกให้หมดไปจากปัญหาสาธารณสุขได้
เอกสารอ้างอิง
- Gardasil 9 (Human papillomavirus 9-valent vaccine, recombinant). US FDA approved product information. Whitehouse Station, NJ: Merck & Co, Inc; June 2020.
- Trimble CL, Morrow MP, Kraynyak KA, et al. Safety, efficacy, and immunogenicity of VGX-3100, a therapeutic synthetic DNA vaccine targeting human papillomavirus 16 and 18 E6 and E7 proteins for cervical intraepithelial neoplasia 2/3: a randomised, double-blind, placebo-controlled phase 2b trial. Lancet. 2015;386:2078.
- American College of Obstetricians and Gynecologists’ Committee on adolescent Health Care, American College of Obstetricians and Gynecologists’ Immunization, Infectious Disease, and Public Health Preparedness Expert Work Group. Human Papillomavirus Vaccination: ACOG Committee Opinion, Number 809. Obstet Gynecol. 2020;136:e15. Reaffirmed 2023.
- Human Papillomavirus vaccines: World Health Organization position paper, December 2022. Available from: https://www.who.int/teams/immunization-vaccines-and-biologicals/policies/position-papers/human-papillomavirus-(hpv). Accessed January 10, 2024.
- Egemen D, Katki HA, Chaturvedi AK, et al. Variation in Human Papillomavirus Vaccination Effectiveness in the US by Age at Vaccination. JAMA Netw Open 2022; 5:e2238041.
- Chambers C, Deeks SL, Sutradhar R, et al. Vaccine Effectiveness Against 12-Month Incident and Persistent Anal Human Papillomavirus Infection Among Gay, Bisexual, and Other Men Who Have Sex With Men. J Infect Dis. 2023;228:89.
- Petrosky E, Bocchini JA Jr, Hariri S, et al. Use of 9-valent human papillomavirus (HPV) vaccine: updated HPV vaccination recommendations of the advisory committee on immunization practices. MMWR Morb Mortal Wkly Rep 2015; 64:300
- Markowitz LE, Dunne EF, Saraiya M, et al. Human papillomavirus vaccination: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep 2014; 63:1.
- Murthy N, Wodi AP, McNally VV, et al. Advisory Committee on Immunization Practices Recommended Immunization Schedule for Adults Aged 19 Years or Older – United States, 2024. MMWR Morb Mortal Wkly Rep. 2024;73:11.
- Harrison R, Huh W. Occupational Exposure to Human Papillomavirus and Vaccination for Health Care Workers. Obstet Gynecol. 2020;136:663.
- Rubin LG, Levin MJ, Ljungman P, et al. 2013 IDSA clinical practice guideline for vaccination of the immunocompromised host. Clin Infect Dis. 2014;58:309.
- แนวทางเวชปฏิบัติของราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย. การป้องกันมะเร็งปากมดลูกปฐมภูมิ RTCOG Clinical practice guideline. Primary prevention of cervical cancer [อินเตอร์เน็ต]. ราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย. พ.ศ. 2563. [เข้าถึงเมื่อ 11 มี.ค. 2567].
- GlaxoSmithKline Vaccine HPV-007 Study Group, Romanowski B, de Borba PC, et al. Sustained efficacy and immunogenicity of the human papillomavirus (HPV)-16/18 AS04-adjuvanted vaccine: analysis of a randomised placebo-controlled trial up to 6.4 years. Lancet. 2009;374:1975.
- Vesikari T, Brodszki N, van Damme P, et al. A Randomized, Double-Blind, Phase III Study of the Immunogenicity and Safety of a 9-Valent Human Papillomavirus L1 Virus-Like Particle Vaccine (V503) Versus Gardasil® in 9-15-Year-Old Girls. Pediatr Infect Dis J. 2015;34:992.
- Petäjä T, Keränen H, Karppa T, et al. Immunogenicity and safety of human papillomavirus (HPV)-16/18 AS04-adjuvanted vaccine in healthy boys aged 10-18 years. J Adolesc Health. 2009;44:33.
- Reisinger KS, Block SL, Lazcano-Ponce E, et al. Safety and persistent immunogenicity of a quadrivalent human papillomavirus types 6, 11, 16, 18 L1 virus-like particle vaccine in preadolescents and adolescents: a randomized controlled trial. Pediatr Infect Dis J. 2007;26:201.
- Lin SW, Ghosh A, Porras C, et al. HPV16 seropositivity and subsequent HPV16 infection risk in a naturally infected population: comparison of serological assays. PLoS One. 2013;8:e53067.
- Safaeian M, Porras C, Schiffman M, et al. Epidemiological study of antiHPV16/18 seropositivity and subsequent risk of HPV16 and -18 infections. J Natl Cancer Inst. 2010;102:1653.
- Updated systematic review on the immunogenicity and efficacy of a single dose of HPV vaccine. Available from: https://cdn-auth-cms.who.int/media/docs/defaultsource/immunization/position_paper_documents/ human-papillomavirus-(hpv)/systematic-review-of-1-dose-of-hpv-vaccinec14d7ee3-e409-4a1a-afd9-c3e7e0dd2bd9.pdf. Accessed March 14, 2023.
- Frazer IH, Cox JT, Mayeaux EJ Jr, et al. Advances in prevention of cervical cancer and other human papillomavirus-related diseases. Pediatr Infect Dis J 2006; 25:S65.
- World Health Organization. Global Advisory Committee on Vaccine Safety. Safety of HPV vaccines. July 2017. Available from: https://www.who.int/groups/globaladvisory-committee-on-vaccine-safety/topics/human-papillomavirus-vaccines/safety. Accessed on March 14, 2024.
- Torella M, Marrapodi MM, Ronsini C, et al. Risk of Premature Ovarian Insufficiency after Human Papilloma Virus Vaccination: A PRISMA Systematic Review and Meta-Analysis of Current Evidence. Vaccines (Basel). 2023; 11.
- Schmuhl NB, Mooney KE, Zhang X, et al. No association between HPV vaccination and infertility in U.S. females 18-33 years old. Vaccine. 2020;38:4038.
- Centers for Disease Control and Prevention (CDC). Syncope after vaccination—United States, January 2005-July 2007. MMWR Morb Mortal Wkly Rep. 2008; 57:457.
- Slade BA, Leidel L, Vellozzi C, et al. Postlicensure safety surveillance for quadrivalent human papillomavirus recombinant vaccine. JAMA. 2009; 302:750.
- Schuler CL, Reiter PL, Smith JS, Brewer NT. Human papillomavirus vaccine and behavioral disinhibition. Sex Transm Infect. 2011; 87:349.
- Marlow LA, Forster AS, Wardle J, Waller J. Mothers’ and adolescents’ beliefs about risk compensation following HPV vaccination. J Adolesc Health. 2009; 44:446.
- Bednarczyk RA, Davis R, Ault K, et al. Sexual activity-related outcomes after human papillomavirus vaccination of 11- to 12-year-olds. Pediatrics. 2012; 130:798.
- National HPV vaccination program register. Coverage Data. Australia. Available from: http://www.hpvregister.org.au/research/coverage-data. Accessed March 10, 2024).
- Vaccine uptake guidance and the latest coverage data. Public Health England. Available from: https://www.gov.uk/government/collections/vaccine-uptake. Accessed March 10, 2024.
- Widgren K, Simonsen J, Valentiner-Branth P, Mølbak K. Uptake of the human papillomavirus-vaccination within the free-of-charge childhood vaccination programme in Denmark. Vaccine. 2011; 29:9663.
- แนวทางการเก็บสิ่งส่งตรวจด้วยตนเองของสถาบันมะเร็งแห่งชาติ (National Cancer Institute). กรมการแพทย์และกระทรวงสาธารณสุข [อินเตอร์เน็ต] สถาบันมะเร็งแห่งชาติ (National Cancer Institute). เข้าถึงเมื่อ 11 มี.ค. 2567.
- Li T, Chen S, Li X, et al. The features of high-risk human papillomavirus infection in different female genital sites and impacts on HPV-based cervical cancer screening. Virol J. 2023; 20(1):116.
- Sy F, Greuel M, Winkler V, et al. Accuracy of HPV testing on self-collected and clinician-collected samples for different screening strategies in African settings: A systematic review and meta-analysis. Gynecol Oncol. 2022; 166(2):358-368.

