Ovarian germ cell neoplasms
Ovarian germ cell neoplasms
พ.ญ. ชลรส เจริญรัตน์
อาจารย์ที่ปรึกษา ผ.ศ. พ.ญ. จารุวรรณ แซ่เต็ง
Ovarian germ cell neoplasm(OGCNs) derived มาจาก primordial germ cells ของ ovary ซึ่งอาจจะเป็น benign หรือ malignant ก็ได้ คิดเป็น 20-25% ของเนื้องอกรังไข่ทั้งหมด และพบว่า 3% เป็น malignancy , ในประเทศ Asia พบ incidence ประมาณ 15%
เนื้องอกชนิดนี้มักพบในช่วงอายุ 10-30 ปี โดยเฉพาะอย่างยิ่งในช่วง 20 ปีแรกของชีวิต เกือบ 70% ของเนื้องอกรังไข่เป็น germ cell origin และพบว่าประมาณ 1 ใน 3 เป็น malignant(1, 2)
Classification(3)
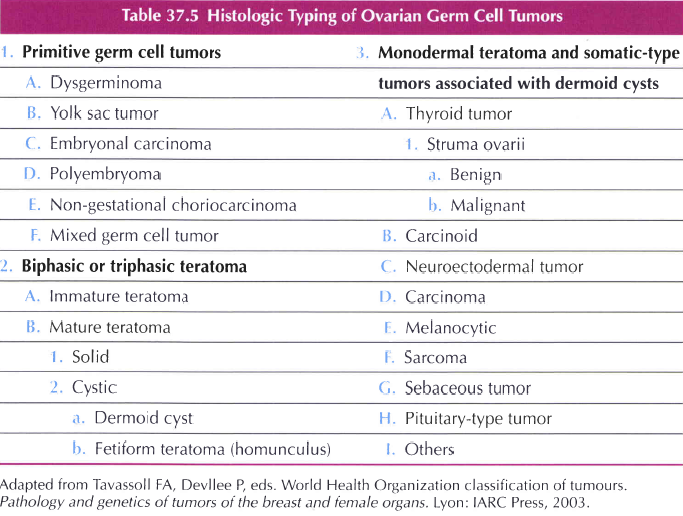
Benign cystic mature teratoma เป็น OGCNs ที่พบมากที่สุด แต่ว่าอาจพบ somatic malignant neoplasm develop ใน dermoid ได้ (termed mature cystic teratoma with malignant degeneration)
Malignant OGCNs (MOGCNs) ชนิด dysgerminoma, immature teratoma, yolk sac tumors, mixed germ cell neoplasm คิดเป็น 90% ของ case ทั้งหมด ส่วน pure embryonal carcinomas, nongestational choriocarcinoma และ pure polyembryomas พบได้ rare(4) โดย dysgerminoma เป็น most common malignant germ cell tumor คิดเป็นสัดส่วน 30-40% ของ MOGCNs ทั้งหมด ซึ่ง MOGCNs แต่ละชนิดจะมีการหลั่ง markers ที่แตกต่างกันดังตาราง(5) ซึ่งมีประโยชน์ช่วยในการวินิจฉัย monitor disease และใช้ในการ follow up after treatment
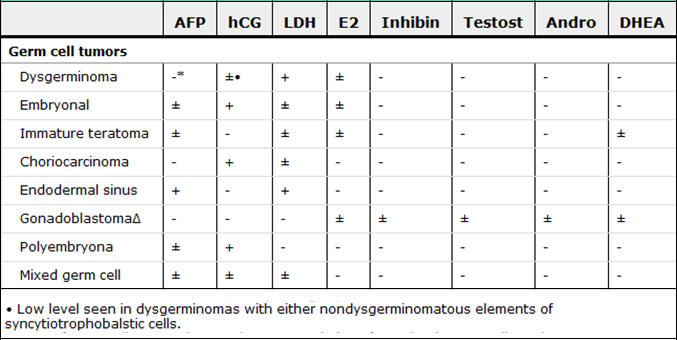
Clinical Features overview
Character ที่ค่อนข้างต่างกับ epithelial ovarian tumor คือ ก้อนจะโตเร็ว ทำให้ส่วนใหญ่มักพบผู้ป่วยตั้งแต่ early stage เนื่องจากทำให้เกิดอาการ subacute pelvic pain ซึ่งเกิดจาก capsular distension, hemorrhagic หรือ necrosis นอกจากนี้ผู้ป่วยอาจมาด้วย pressure symptom on the bladder หรือ rectum, menstrual irregularities หรือ symptoms of pregnancy (เกิดจาก hCG production) , acute pain จาก torsion หรือ rupture ใน case ที่ advances คนไข้อาจมาด้วย abdominal distension จาก ascites(3) โดยอาการที่พบบ่อยสุดได้แก้ abdominal pain and abdominal mass คิดเป็น 85% ของ case รองลงมาได้แก่ fever and vaginal bleeding (10%)(5)
Diagnosis overview
Definite diagnosis คือ histology จากชิ้นเนื้อที่ได้จากการผ่าตัด แต่ถ้าหากพบ adnexal mass on pelvic imaging ร่วมกับ tumor markers (serum hCG, AFP และ LDH)ที่สัมพันธ์กับ germ cell tumors rising ก็สามารถบอกการวินิจฉัยได้ค่อนข้าง strong ก่อนทำการผ่าตัด
Serum tumor markers มีประโยชน์ คือ 1. Diagnostic clue to the presence of an OGCN 2. Monitoring the response to chemotherapy and for subsequent posttreatment follow-up
ส่วน benign cystic mature teratoma อาจวินิจฉัยได้เบื้องต้นจาก ultrasound โดยมีรายว่า specificity สูงถึง 98-100% (6) (7)แต่อย่างไรก็ตามถึงเป็น benign การทำ cystectomy ก็ยังแนะนำให้ทำอยู่(5)
Karyotype ควรทำก่อนทำการผ่าตัดใน premenarcheal girls ทุกราย โดยเฉพาะ case ที่สงสัย dysgerminoma เนื่องจาก tumor ชนิดนี้มักเกิดใน dysgenetic gonads(8, 9)
ชนิดของ Ovarian germ cell neoplasm
1. Teratomas
แบ่งได้เป็น 2 กลุ่มหลักๆคือ mature (cystic or solid) และ immature teratoma
1.1 Mature teratoma (Dermoid cyst) ผู้ป่วยมัก asymptomatic ส่วนใหญ่เป็นชนิด benign ส่วนประกอบด้วย mature tissue of ectoderm(eg. skin,hair,sebaceous glands), mesoderm (eg. Muscle) และ endoderm origin (eg. GI) (10) ดังนั้น Macroscopic appearance จะเป็น multicystic mass ที่มี hair, teeth, and/or skin ร่วมกับ sebaceous, thick and of the foul-smelling material ,bilateral พบ 10% A solid prominence (Rokitansky’s protuberance) จะอยู่ที่ junction ระหว่าง teratoma และ normal ovarian tissue ซึ่งจะมี greatest cellular variety มากที่สุด มีความสำคัญคือ อาจจะพบ immature/ malignant component ซึ่ง malignant transformation พบได้ < 2% ของ Dermoid cyst. risk การรักษา mature teratoma คือ ovarian cystectomy หรือกรณีมีบุตรเพียงพอแล้วการทำ Salphingo-oophorectomy ก็เป็น acceptable treatment
1.2 Immature teratoma (Malignant teratoma,teratoblastoma or embryonal teratoma) histology จะมี 3 germ cell layers โดยมี varying amount of immature tissue. pure immature พบ <1% ของovarian cancer แต่เป็น second most common ของ MOGNs และคิดเป็น 10-20% ของ ovarian malignancies ที่พบในผู้หญิงอายุน้อยกว่า 20 ปี(1) เป็น OGCN เพียงชนิดเดียวที่มี Histologic grading (range : I (well differentiated) – III (poorly differentiate)) โดยแบ่งตามสัดส่วนของ immature neural element ใน Histologic tissue ซึ่ง grade จะเป็น indicator of risk for extraovarian spread (5) tumor markers มัก negative ยกเว้นเป็น mixed germ cell tumor
2. Dysgerminoma
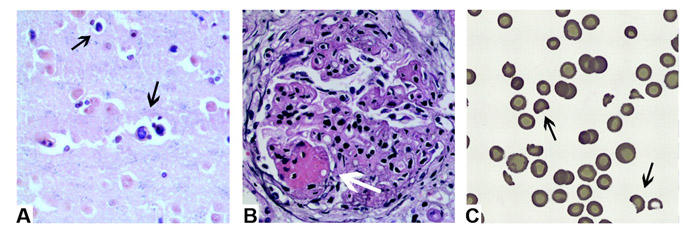
เป็น most common malignant OGNs คิดเป็น 30-40% ของ MOGNS ทั้งหมด ซึ่งพบมากถึง 5-10% ของ ovarian cancers ทั้งหมด ที่พบในผู้หญิงอายุน้อยกว่า 20 ปี. 75% ของ dysgerminoma พบระหว่างช่วงอายุ 10-30 ปี และเป็น ovarian malignancies ที่ associated with pregnancy ถึง 20-30% นอกจากนี้พบว่า 65% ของ dysgerminoma at diagnosis เป็น stage I(1, 2) มีเพียง 25% เท่านั้นที่เป็น metastatic disease at diagnosis โดยมักแพร่กระจายผ่าน lymphatic system ลักษณะทาง histology คือ abnormal proliferations of the basic germ cell โดยจะเห็นเป็น large round, ovoid, or polygonal cells ปริมาณมาก ,clear, very pale-staining cytoplasm, large and irregular nuclei and prominent nucleoli (called fried eggs)(3, 5) อีกลักษณะหนึ่งคือ arrangement of the elements in lobules separated by fibrous septa ซึ่งมี lymphocytes, plasma cells and granulomatous with epithelioid cells and multinucleated giant cells ถึงแม้ dysgerminoma จะเป็น malignant แต่มีเพียง 1 ใน 3 เท่านั้นที่ aggressive behavior ลักษณะทาง gross คือ lobulated mass, cut surface เป็นแบบ firm ,pale tan to gray-brown in color. พบ bilateral ได้ 10-15% ( MOGCNs อื่นๆ พบ bilateral ได้ rare) หากการรักษาเป็นแบบ preserved contralateral ovary โอกาสที่ ovary ข้างที่เหลือจะกลายเป็น dysgerminoma อยู่ที่ 5-10% ใน 2 ปี(1) ผู้ป่วยมัก present อาการด้วย ท้องโตขึ้นและมีการปวดเนื่องจาก complication ของก้อน นอกจากนี้ผู้ป่วยอาจมาด้วย precocious puberty ,virilization ซึ่งเป็นผลมาจาก syncytiotrophoblast giant cells tumor markers ที่เกี่ยวข้องได้แก่ LDH (ส่วน hCG พบว่า rising ประมาณ 3-5%ของ dysgerminoma ทั้งหมด)
พบว่ามีประมาณ 5% ของ dysgerminomas พบใน phenotypic women ที่มี abnormal gonad ซึ่ง โดยหากมี gonadoblastomas (benign ovarian tumor ประกอบด้วย germ cells and sex cord stroma) in patient with gonad dysgenesis จะมีโอกาสมากกว่า 50% ที่จะ develop เป็น ovarian malignancies(11) ดังนั้นหากพบว่ามี Y chromosome in karyotype แนะนำให้ remove both ovaries
3. Endodermal sinus tumors (EST)
หรือที่นิยมเรียกว่า yolk sac carcinomas เนื่องจาก tumor ชนิดนี้ derived มาจาก primitive yolk sac เป็น third most common MOGNs โดย median age อยู่ที่ 16-18 ปี และ 1 ใน 3 เป็น premenarcheal girl(1, 2) ลักษณะgross คือ soft grayish-brown, cystic จาก degeneration or necrosis. EST เป็น unilateral 100% ดังนั้นจึงเป็นข้อห้ามในการ biopsy opposite ovary นอกจากนี้อาจสัมพันธ์กับ gonadal dysgenesis ดังนั้นจึงควรทำ karyotyping in premenacheal girl ก่อนทำการผ่าตัด(2)
ลักษณะทาง microscopic คือ cystic space line ด้วย layer of flattend or irregular endothelium into which project a glomerulus-like tuft with a central vessel core (Schiller-Duval bodies) ส่วนใหญ่ของ EST จะมีการหลั่ง AFP อาจพบว่ามี LDH elevate ได้ในบางราย(12)
4. Rare germ cell tumors of the ovary
4.1 Embryonal carcinoma
เป็น extremely rare tumor แตกต่างกับ choriocarcinoma คือ ไม่มี syncytiotrophoblastic and cytotrophoblastic cells มักพบในผู้ป่วยอายุน้อย โดย mean age คือ 14 ปี tumor markers ที่ associate ได้แก่ AFP, hCG นอกจากนี้ยังสามารถ secrete estrogen ได้ ซึ่งทำให้มีอาการ precocious pseudopuberty or irregular bleeding
4.2 Choriocarcinoma of the Ovary (Non-gestational choriocarcinoma)
เป็น rare tumor (incidence 1 : 369,000,000) เกิดจาก extraembryonic differentiation of malignant germ cells ซึ่งลักษณะทาง histology จะเหมือนกับ primary gestational carcinoma ซึ่งต้องแยกโดย DNA analysis (คือถ้ามี paternal DNA แสดงว่าเป็น placental origin)(13) tumor ชนิดนี้ secrete hCG ถ้ามีปริมาณสูงมาก จะทำให้มีอาการ isosexual precocity ได้ถึง 50% ก่อน menarche(14)เช่นเดียวกับ Gestational choriocarcinoma ที่มักจะมี hematogenous metastasis ไปตามอวัยวะต่างๆ
4.3 Polyembryoma
เป็น extremely rare aggressive tumor ประกอบด้วย embryoid bodies และมี structure of early embryonic differentiation มักพบใน premenarche และ present ด้วย sign of pseudopuberty with elevate AFP and hCG(1)
5. Mixed Germ Cell Tumors
ประกอบด้วย ≥ 2 ชนิดของ ovarian germ cell neoplasm incidence คือ 5.3% ของ malignant OGCNs ทั้งหมด(15) โดย most common component คือ dysgerminoma (80%) รองลงมาได้แก่ EST (70%) ,immature teratoma (53%) ตามลำดับ(16) โดย combination ที่พบบ่อยสุดคือ dysgerminoma และ EST ซึ่ง markers ที่ secrete ออกมาจะขึ้นกับ components
Pattern of spreading
Malignant OGCNs สามารถ spread ผ่าน lymphatics, bloodstream, and peritoneal surface dissemination , lymph node metastasis พบมากสุดใน dysgerminoma (28%) รองลงมาได้แก่ mixed germ cell tumors(16%) และ malignant teratoma (8%) ตามลำดับ(17)
Staging
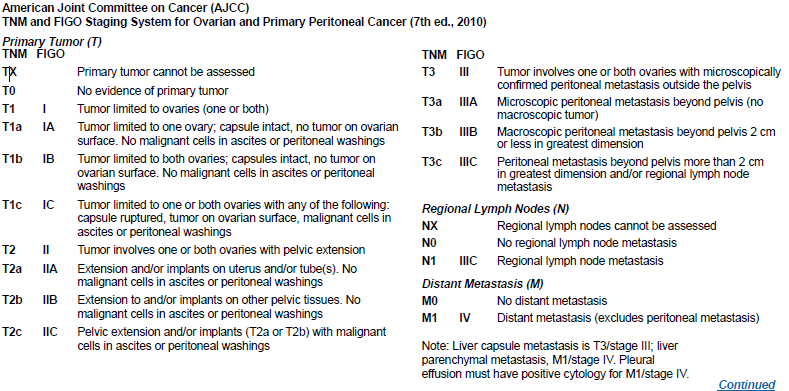
ปัจจุบันตาม guideline NCCN Clinical Practice Guidelines in Oncology ยังคงอ้างอิงตาม FIGO staging System 7th ed., 2010(18)
Workup อ้างอิงตาม NNCN ในรายที่มาด้วย pelvic mass(18)

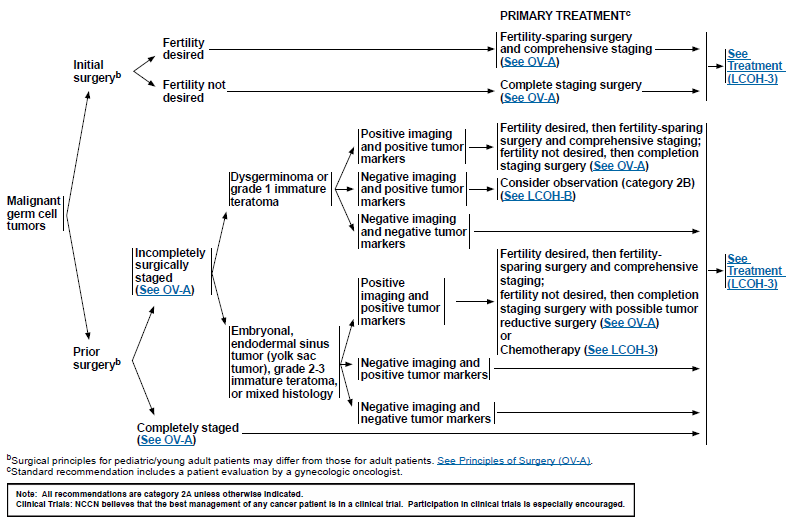
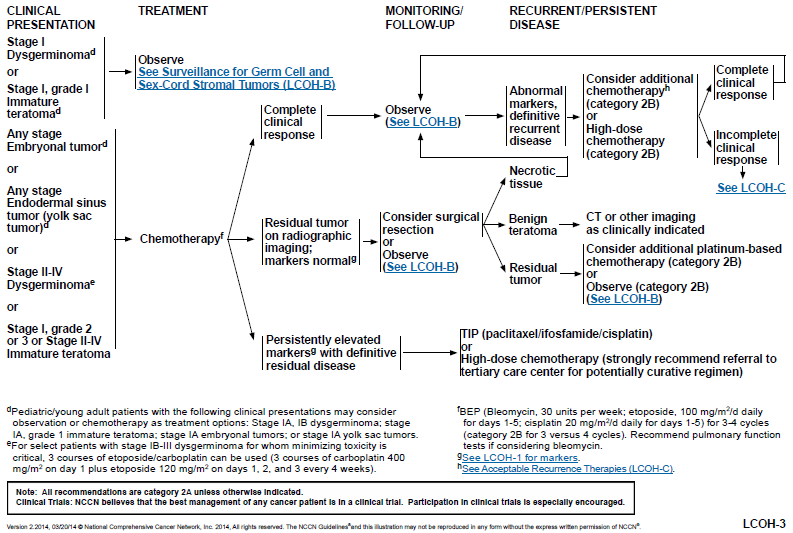
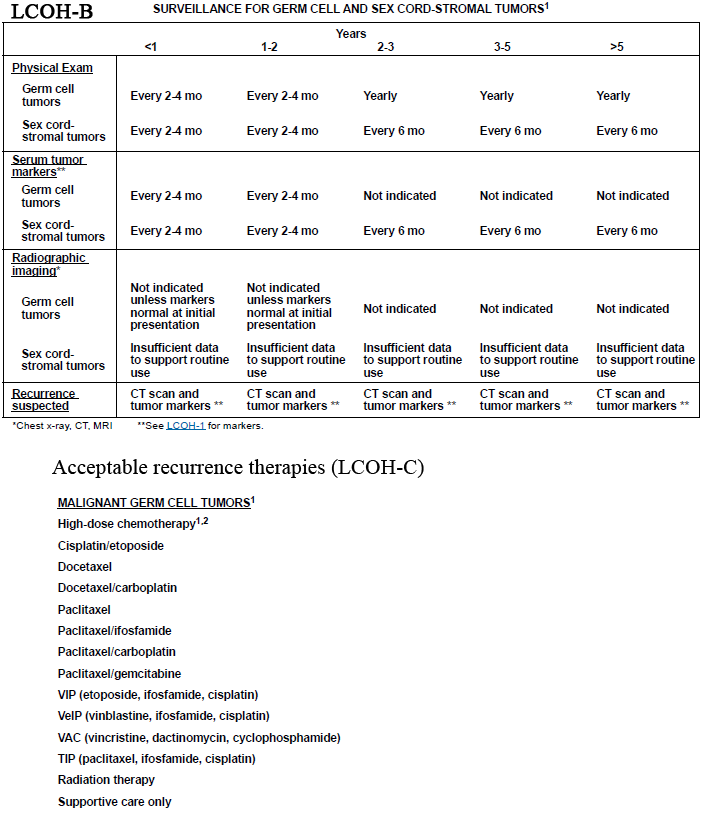
Treatment and surveillance germ cell tumors(18, 19)
ในกรณีที่ผู้ป่วย complete childbearing ควรทำ complete surgical staging แต่เนื่องจาก MOGCNs มักพบในคนอายุน้อยที่ยังต้องการมีบุตร จึงแนะนำการรักษาแบบ fertility-sparing surgery and comprehensive staging โดยมีคำแนะนำคือ (1) Intact removal of the tumor (2) sparing of the fallopian tube if not adherent to the tumor (3) procurement of cytologic washing or harvesting of ascites fluid (4) examination and palpation of the omentum with removal suspicious lesion (5) examination and palpation of the ileac and aortocaval nodes with biopsy of abnormal areas(20) โดยการทำ unilateral oophorectomy พิจารณาทำใน dysgerminoma(nonmetastasis) และ immature teratoma (3) แต่ถ้าหาพิจารณาจาก NCCN guideline จะแนะนำให้ทำเป็น unilateral salpingo-oophorectomy with comprehensive staging(18) เนื่องจากมี rich lymphovasucular connect ระหว่าง ipsilateral fallopian tube กับ ovary(19) หากกรณี contralateral ovary ลักษณะ gross ปกติ ไม่ควร routine biopsy เนื่องจากทำให้เกิด peritoneal adhesion ซึ่ง impair infertility อีกทั้ง 90-95% ของ MOGCNs สามารถ curable หลังได้ postoperative systemic chemotherapy(21) ซึ่ง standard regimen คือ BEP (bleomycin,etoposide, and cisplatin) ถึงแม้ว่า platinum-based chemotherapy อาจทำให้เกิด temporary ovarian dysfunction or failure ได้ แต่ส่วนใหญ่จะกลับมาเป็นปกติและสามารถมีบุตรได้ recommend ให้ full doses of all component drugs ตาม scheduled time (ภายใน 7-10 วันหลัง surgery) โดยไม่ควร ลด dose หรือ delay next cycle ถ้าหากมี myelosuppression ใน previous cycle ควรให้ GCSF during subsequent cycles(19)
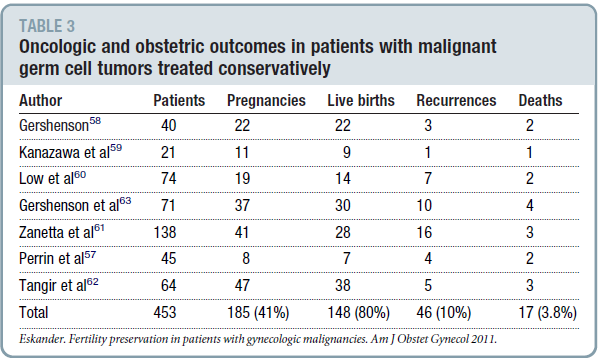
มี 7 articles ศึกษาเกี่ยวกับ obstetrics outcome ผลที่ได้ดังตาราง จะเห็นได้ว่า หลังการรักษาแบบ conservation ผู้ป่วยทั้งหมด 453 คน ตั้งครรภ์ 185 คน คิดเป็น 41% มี total live births 80% โดยมี recurrence เพียงแค่ 46 คน (10%) death 17 คน (3.8%) (22)
Initial cytoreduction for advanced disease
ถึงแม้ว่า MOGNs จะ sensitive ต่อ platinum-based chemotherapy , tumor volume ยังคงเป็น most important prognostic factor for outcome โดยมี evidence จากหลายงานวิจัยว่า optimally debulked disease (all areas of residual disease less than 2 cm) จะมี higher complete remission rate จาก chemotherapy และมี long-term outcome ที่ดีกว่า แต่อย่างไรก็ตามแพทย์ผู้ผ่าตัดควรคำนึงถึง benefits เทียบกับ risks ในการทำ aggressive cytoreductive maneuvers เนื่องจาก MOGNs เป็น chemosensitive tumor โดยเฉพาะ dysgerminomas ที่มีรายงานว่า 80% ของ advanced disease ที่ยังมี residual disease หลัง cytoreduction เป็นกลุ่ม long-term survivors (19)
หลังจาก primary surgery recommend ให้ postoperative chemotherapy ทั้งใน early stage และ more advanced OGCNs เป็น BEP regimen 3-4 courses ยกเว้น stage I grade I immature teratoma และ stage IA dysgerminoma(23) จากข้อมูลปัจจุบันอาจจะพิจารณาใช้เป็น carboplatin/etoposide/bleomycin ในคนที่มี preexisting neuropathy or renal disease(24, 25)
สำหรับผู้ป่วยที่ได้รับ BEP 4 cycles มีคำแนะนำให้งด bleomycin หลังจาก cycle 3 (Total cumulative dose 270 IU) เพื่อเลี่ยง lung toxicity (พบว่า Total dose > 300IU สัมพันธ์กับการเพิ่มขึ้นของ lung toxicity ในผู้ป่วยที่ได้ BEP ใน testicular germ cell tumor)(26)
กรณี advanced stage OGCNs เรื่อง optimal number of chemotherapy ยังไม่เป็นที่แน่ชัด ส่วนใหญ่แนะนำให้ 4-6 cycles
Prognostic factors
Prognostic factors ที่สำคัญที่สุดคือ histological type และ stage โดย dysgerminoma จะมี prognosis ดีที่สุด โดย cure rate >95% ถึงแม้ใน advanced disease(27) มีการศึกษา five-year overall survival rate ใน various MOGNs histiotypes treated with platinum-based chemotherapy พบว่า 100% for stage I,85% stage II, 79% stage III และ 71% stage IV นอกจาก stage แล้ว ในการศึกษานี้พบว่าถ้าผู้ป่วยมี normal AFP และ beta-hCG at initial ปกติจะมี one-year survival ดีกว่ากลุ่มที่มี rasing markers at diagnosis (28)
Immature teratoma grading ก็เป็น prognostic factors ที่สำคัญเช่นกัน โดย grade I และ II จะมี 5-year survival เท่ากับ 87% และ 81 % ตามลำดับ เมื่อเทียบกับ grade III ที่ลดลงเหลือเพียง 25% (p<0.01)(29)
ใน yolk sac tumors ; stage, AFP serum half life (<10 days), ascites at presentation และ size of residual tumor ก็ reported ว่าเป็น prognosis factor เช่นกัน(30, 31)
Posttreatment surveillance
90% recurrence มักเกิดภายใน 2 ปี หลังได้รับการ complete therapy (Dysgerminomas อาจ recur ได้ช้าถึง 10 หลัง Tretment ) , NCCN guideline และ the Society of Gynecologic Oncology (SGO) ไม่ได้แนะนำให้ทำ routine radiographic surveillance หลังจาก treatment โดย SGO จะแนะนำให้ทำทุก 2-4 เดือน ใน 2 ปีแรกหลังการรักษา กรณีถ้าผู้ป่วย ไม่มี tumor markers initially elevated
Late effects of chemotherapy
Gonadal function
ถึงแม้ว่า platinum-based chemotherapy เป็น risk factor ที่ทำให้ ovarian dysfunction หรือ failure ได้ แต่มีการศึกษาว่าส่วนใหญ่ผู้ป่วยที่ได้รับ BEP regimen 3-4 courses of standard dose จะกลับมามี normal ovarian function , ตั้งครรภ์และมีบุตรได้ รวมถึง ยังไม่มี evidence ว่าการรักษาดังกล่าวจะมีผลต่อ early pregnancy loss หรือ congenital malformation of fetus (27)
Secondary malignancies
Etoposide เชื่อว่าอาจทำให้เกิด treatment-related leukemia ได้ โดยเป็น dose-related พบว่า incidence leukemia มีเพียง <0.5% กรณีได้ typical 3-4 courses of BEP (accumulative dose <2000 mg/m2) เทียบกับ กลุ่มที่ได้มากกว่า 2000 mg/m2 (incidence 5%)
ถึงแม้ว่า etoposide อาจทำให้เกิด secondary malignancies ได้ เมื่อเทียบ risk-benefit และ ก็ยัง recommend ให้มี etoposide in regimen อยู่(32)
References
- Scully R, Young R, Clement P. Tumor of the ovary, maldeveloped gonads, fallopian tube, and broad ligament. 3 ed. Washington, DC: Armed Forces Institute of Pathology; 1998.
- Berek J, Friedlander M, Hacker N. Epithelial ovarian, fallopian tube and peritoneal cancer. 5 ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2009.
- Berek J, Longacre T, Friedlander M. Ovarian, Fallopian Tube, and Peritoneal Cancer. 15 ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2012.
- Tewari K, Cappuccini F, Disaia PJ, Berman ML, Manetta A, Kohler MF. Malignant germ cell tumors of the ovary. Obstet Gynecol. 2000;95(1):128-33.
- Ovarian germ cell neoplasms: Pathology, clinical manifestaions, and diagnosis [Internet]. UPTODATE. 2014.
- Tongsong T, Luewan S, Phadungkiatwattana P, Neeyalavira V, Wanapirak C, Khunamornpong S, et al. Pattern recognition using transabdominal ultrasound to diagnose ovarian mature cystic teratoma. Int J Gynaecol Obstet. 2008;103(2):99-104.
- Patel MD, Feldstein VA, Lipson SD, Chen DC, Filly RA. Cystic teratomas of the ovary: diagnostic value of sonography. AJR Am J Roentgenol. 1998;171(4):1061-5.
- Obata NH, Nakashima N, Kawai M, Kikkawa F, Mamba S, Tomoda Y. Gonadoblastoma with dysgerminoma in one ovary and gonadoblastoma with dysgerminoma and yolk sac tumor in the contralateral ovary in a girl with 46XX karyotype. Gynecol Oncol. 1995;58(1):124-8.
- Imai A, Furui T, Tamaya T. Gynecologic tumors and symptoms in childhood and adolescence; 10-years’ experience. Int J Gynaecol Obstet. 1994;45(3):227-34.
- DiSaia P, Creasman W. Germ cell, stromal and other ovarian tumors: Mosby-Elsevier; 2007.
- Bremer GL, Land JA, Tiebosch A, van der Putten HW. Five different histological subtypes of germ cell malignancies in an XY female. Gynecol Oncol. 1993;50(2):247-8.
- Kawai M, Kano T, Kikkawa F, Morikawa Y, Oguchi H, Nakashima N, et al. Seven tumor markers in benign and malignant germ cell tumors of the ovary. Gynecol Oncol. 1992;45(3):248-53.
- Fisher RA, Newlands ES, Jeffreys AJ, Boxer GM, Begent RH, Rustin GJ, et al. Gestational and nongestational trophoblastic tumors distinguished by DNA analysis. Cancer. 1992;69(3):839-45.
- Oliva E, Andrada E, Pezzica E, Prat J. Ovarian carcinomas with choriocarcinomatous differentiation. Cancer. 1993;72(8):2441-6.
- Smith HO, Berwick M, Verschraegen CF, Wiggins C, Lansing L, Muller CY, et al. Incidence and survival rates for female malignant germ cell tumors. Obstet Gynecol. 2006;107(5):1075-85.
- Chapman DC, Grover R, Schwartz PE. Conservative management of an ovarian polyembryoma. Obstet Gynecol. 1994;83(5 Pt 2):879-82.
- Kumar S, Shah JP, Bryant CS, Imudia AN, Cote ML, Ali-Fehmi R, et al. The prevalence and prognostic impact of lymph node metastasis in malignant germ cell tumors of the ovary. Gynecol Oncol. 2008;110(2):125-32.
- NCCN Guidelines Ovarian cancer including fallopian tube cancer and promary peritoneal cancer [Internet]. NCCN. 2014.
- Treatment of malignant germ cell tumors of the ovary [Internet]. uptodate. 2013.
- Billmire DF. Malignant germ cell tumors in childhood. Semin Pediatr Surg. 2006;15(1):30-6.
- Perrin LC, Low J, Nicklin JL, Ward BG, Crandon AJ. Fertility and ovarian function after conservative surgery for germ cell tumours of the ovary. Aust N Z J Obstet Gynaecol. 1999;39(2):243-5.
- Eskander RN, Randall LM, Berman ML, Tewari KS, Disaia PJ, Bristow RE. Fertility preserving options in patients with gynecologic malignancies. Am J Obstet Gynecol. 2011;205(2):103-10.
- Dark GG, Bower M, Newlands ES, Paradinas F, Rustin GJ. Surveillance policy for stage I ovarian germ cell tumors. J Clin Oncol. 1997;15(2):620-4.
- Dimopoulos MA, Papadopoulou M, Andreopoulou E, Papadimitriou C, Pavlidis N, Aravantinos G, et al. Favorable outcome of ovarian germ cell malignancies treated with cisplatin or carboplatin-based chemotherapy: a Hellenic Cooperative Oncology Group study. Gynecol Oncol. 1998;70(1):70-4.
- Mann JR, Raafat F, Robinson K, Imeson J, Gornall P, Sokal M, et al. The United Kingdom Children’s Cancer Study Group’s second germ cell tumor study: carboplatin, etoposide, and bleomycin are effective treatment for children with malignant extracranial germ cell tumors, with acceptable toxicity. J Clin Oncol. 2000;18(22):3809-18.
- O’Sullivan JM, Huddart RA, Norman AR, Nicholls J, Dearnaley DP, Horwich A. Predicting the risk of bleomycin lung toxicity in patients with germ-cell tumours. Ann Oncol. 2003;14(1):91-6.
- Parkinson CA, Hatcher HM, Earl HM, Ajithkumar TV. Multidisciplinary management of malignant ovarian germ cell tumours. Gynecol Oncol. 2011;121(3):625-36.
- Murugaesu N, Schmid P, Dancey G, Agarwal R, Holden L, McNeish I, et al. Malignant ovarian germ cell tumors: identification of novel prognostic markers and long-term outcome after multimodality treatment. J Clin Oncol. 2006;24(30):4862-6.
- Li H, Hong W, Zhang R, Wu L, Liu L, Zhang W. Retrospective analysis of 67 consecutive cases of pure ovarian immature teratoma. Chin Med J (Engl). 2002;115(10):1496-500.
- Nawa A, Obata N, Kikkawa F, Kawai M, Nagasaka T, Goto S, et al. Prognostic factors of patients with yolk sac tumors of the ovary. Am J Obstet Gynecol. 2001;184(6):1182-8.
- de La Motte Rouge T, Pautier P, Rey A, Duvillard P, Kerbrat P, Troalen F, et al. Prognostic factors in women treated for ovarian yolk sac tumour: a retrospective analysis of 84 cases. Eur J Cancer. 2011;47(2):175-82.
- Pedersen-Bjergaard J, Daugaard G, Hansen SW, Philip P, Larsen SO, Rørth M. Increased risk of myelodysplasia and leukaemia after etoposide, cisplatin, and bleomycin for germ-cell tumours. Lancet. 1991;338(8763):359-63.