Farewell OB GYN CMU 2023 “Y2K Party”
Farewell OB GYN CMU 2023 “Y2K Party”
งานเลี้ยงส่งแพทย์ประจำบ้าน/แพทย์ใช้ทุน resident 3 ใน ธีม “Y2K Party”
Farewell OB GYN CMU 2023 “Y2K Party”
งานเลี้ยงส่งแพทย์ประจำบ้าน/แพทย์ใช้ทุน resident 3 ใน ธีม “Y2K Party”
การตั้งครรภ์แฝด คือการตั้งครรภ์ที่มีทารกในครรภ์มากกว่าหนึ่งคนขึ้นไป การตั้งครรภ์แฝดเพิ่มความเสี่ยงในการเกิดภาวะแทรกซ้อนมากขึ้นทั้งในมารดาและทารก ยกเว้นภาวะแทรกซ้อนของการตั้งครรภ์เกินกำหนดและภาวะทารกในครรภ์ตัวโต โดยอัตราเสี่ยงจะเพิ่มมากขึ้นตามจำนวนของทารกในครรภ์ อัตราการเสียชีวิตของทารกในครรภ์แฝดเพิ่มมากขึ้น 4 เท่า เมื่อเทียบกับครรภ์เดี่ยว และ 12 เท่าในครรภ์แฝดสาม 1 ภาวะแทรกซ้อนที่พบได้ในมารดา ได้แก่ ความเสี่ยงในการเกิดภาวะครรภ์เป็นพิษ ภาวะตกเลือดหลังคลอด และเสียชีวิตได้ พบว่ามีความเสี่ยงเพิ่มขึ้น 2 เท่า เทียบกับครรภ์เดี่ยว 2
1. Monozygotic (Identical twin)
เกิดจากการผสมของไข่ 1 ใบ และ อสุจิ 1 ตัว แต่เกิดการแบ่งตัวได้เป็นทารก 2 คน
2. Dizygotic (Fraternal twin)
เกิดจากการผสมของไข่ 2 ใบ และ อสุจิ 2 ตัว เกิดเป็นทารก 2 คน พบว่าทารกที่มีเพศต่างกันโดยส่วนมากแล้วจะเกิดจาก dizygotic twin
การบอก chorionicity และ amnionicity เป็นสิ่งสำคัญในครรภ์แฝด เนื่องจากครรภ์แฝดชนิด monochorionic twins จะมีความเสี่ยงในการเกิดภาวะแทรกซ้อนระหว่างตั้งครรภ์ได้สูงกว่าชนิด dichorionic twins การตรวจอัลตราซาวน์เพื่อดูเยื่อกั้นระหว่างถุงการตั้งครรภ์จะสามารถวินิจฉัยได้ดีที่สุดในช่วงอายุครรภ์ 11-13+6 สัปดาห์ หากการอัลตราซาวน์ทางหน้าท้องไม่สามารถระบุเยื่อกั้นระหว่างถุงการตั้งครรภ์ได้ แนะนำให้ทำอัลตราซาวน์ทางช่องคลอด หรือส่งตัวผู้ป่วยไปพบกับแพทย์ผู้เชี่ยวชาญเฉพาะทางเพื่อตรวจเพิ่มเติม หากไม่สามารถระบุได้ ควรตรวจติดตามผู้ป่วยแบบ monochorionic twins เพื่อป้องกันภาวะแทรกซ้อนที่พบได้มากกว่า
หากอัลตราซาวน์พบว่ามีสายสะดือพันกันระหว่างแฝดสองคน ช่วยบ่งบอกว่าเป็น monochorionic twins
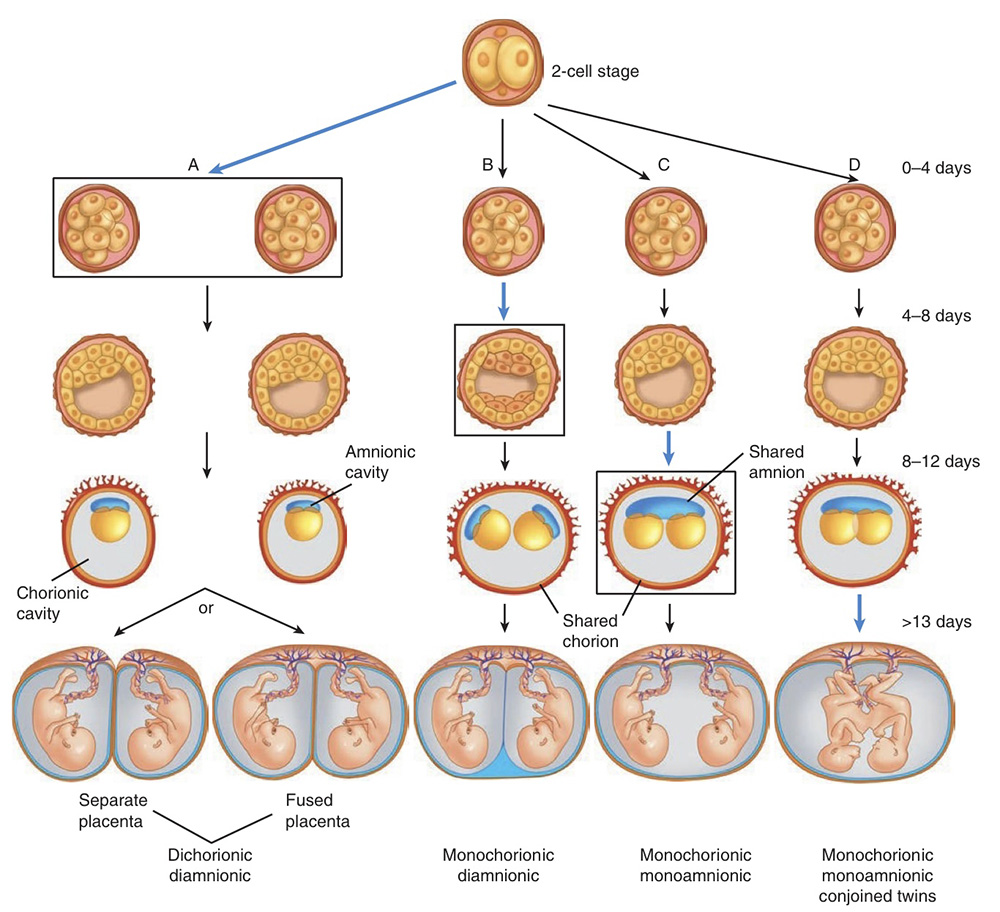
รูปที่ 1 แสดงถึงระยะเวลาที่เกิดการแบ่งตัวของ embryo
(ที่มา: Cunningham FG, Leveno KJ, Dashe JS, Hoffman BL, Spong CY, Casey BM. Editors. Williams Obstetrics, 26e. New York, NY: McGraw Hill; 2022.)
1. เทคโนโลยีเจริญพันธ์ (Infertility therapy)
การกระตุ้นให้เกิดการตกไข่ด้วยการใช้ยา clomiphene citrate หรือฮอร์โมน FSH, hCG ทำให้เกิดการตกไข่หลายใบพร้อมๆกัน หรือในขั้นตอนการย้ายตัวอ่อนที่เลือกย้ายหลายตัวอ่อนเข้าฝังบริเวณโพรงมดลูก 3
2. อายุมารดาที่มากขึ้น (Advance maternal age)
ปริมาณฮอร์โมน FSH จะเพิ่มมากขึ้นตามอายุ เพื่อกระตุ้นการตกไข่ให้ดียิ่งขึ้น พบว่าปริมาณฮอร์โมน FSH ที่เพิ่มสูงมากขึ้นมีความสัมพันธ์กับ dizygotic twinning 3
3. เชื้อชาติ (Race)
อุบัติการณ์การเกิดครรภ์แฝดในกลุ่มคนผิวสีดำสูงกว่าผิวขาว ซึ่งอาจสัมพันธ์กับความแปรปรวนของปริมาณฮอร์โมน FSH ในแต่ละเชื้อชาติ 4
4. กรรมพันธุ์ (Heredity)
พบว่าในรายที่ฝ่ายหญิงมีประวัติครรภ์แฝดในครอบครัว ทำให้เพิ่มโอกาสในการเกิด dizygotic twins ได้มากขึ้น 3
5. น้ำหนักและส่วนสูงของมารดา (Maternal weight and height)
พบว่าในผู้หญิงที่มีน้ำหนักตัวมาก (BMI ≥ 30 kg/m2) และสูง (Height ≥ 164 cm.) มีโอกาสที่จะเกิด dizygotic twins ได้มากกว่าผู้หญิงที่เตี้ยร้อยละ 23-30 5, 6
Superfecundation
การที่มีไข่ตก 2 ใบ ในรอบเดือนเดียวกัน และเกิดการปฏิสนธิทั้ง 2 ใบ อาจเป็นอสุจิจากคนละคนได้ เกิดขึ้นเป็นครรภ์แฝด เรียกว่า heteropaternity
Superfetation
การที่มีไข่ตก 1 ใบ ปฏิสนธิและได้ฝังตัวในโพรงมดลูกแล้ว มีไข่ตกเพิ่มอีก 1 ใบ ในรอบเดือนถัดมา และเกิดการปฏิสนธิอีกครั้ง ทำให้เกิดเป็นครรภ์แฝดขึ้น
1. การตรวจความสูงของระดับมดลูก (Fundal height) แล้วมีขนาดโตกว่าอายุครรภ์
2. คลำพบรยางค์ของทารกมากกว่าหนึ่งคน
3. คลำพบศีรษะของทารกได้มากกว่าหนึ่งคน
4. ตรวจพบเสียงหัวใจเต้นแตกต่างกัน 2 บริเวณ
1. Twin peak sign (Lambda sign)
ลักษณะของเยื่อกั้นระหว่างทารกในแฝดชนิด dichorionic twins บริเวณที่รกทั้งสองคนมาอยู่ติดกัน เห็นเป็นลักษณะสามเหลี่ยมยื่นเข้าไปในเยื่อกั้นระหว่างทารกและด้านในคือส่วนของเนื้อรก บริเวณเยื่อกั้นทารกจะประกอบด้วย chorion 2 ชั้น และ amnion 2 ชั้น การวัดความหนาของเยื่อกั้นระหว่างทารกได้หนามากกว่าเท่ากับ 2 มิลลิเมตร 7 มีแนวโน้มที่จะเป็นการตั้งครรภ์แฝดแบบ dichorionic twins
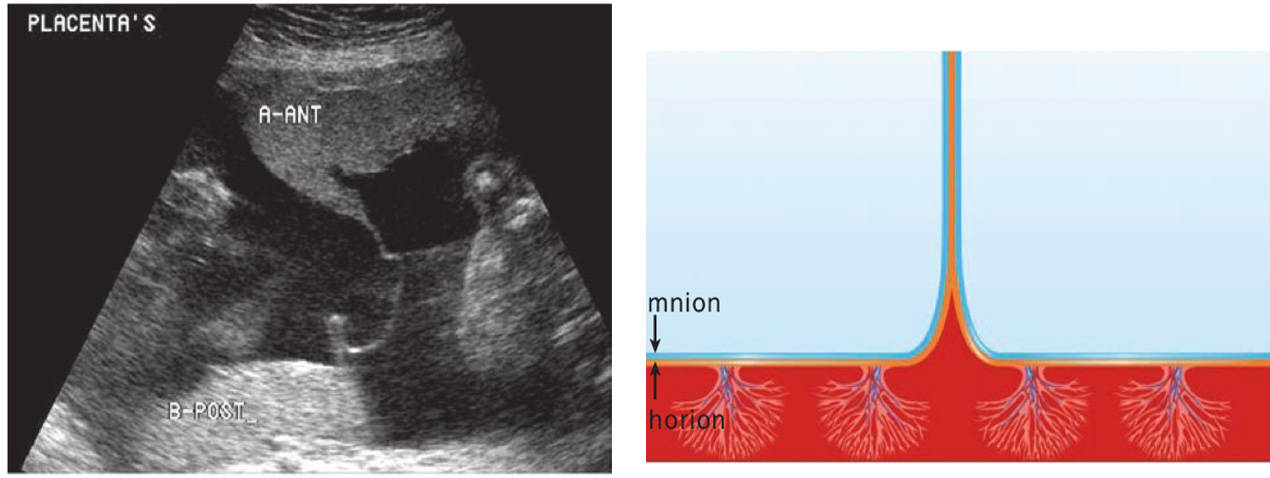
รูปที่ 2 ภาพอัลตราซาวน์และรูปแสดงลักษณะของ Lambda sign เห็น Chorion เป็นรูปสามเหลี่ยมยื่นเข้าไปบริเวณเยื่อกั้นระหว่างถุงน้ำ (ที่มา: Cunningham FG, Leveno KJ, Dashe JS, Hoffman BL, Spong CY, Casey BM. Editors. Williams Obstetrics, 26e. New York, NY: McGraw Hill; 2022.)
2. T sign
ลักษณะของเยื่อกั้นระหว่างทารกในแฝดชนิด monochorionic diamniotic twins เห็นเป็นเส้นบางๆกั้นระหว่างแฝด 2 คน เกิดจาก amnion ของแฝดทั้งสองคนมาเชื่อมติดกัน โดยทั่วไปแล้วจะใช้ค่าความหนาของเยื่อกั้นน้อยกว่า 2 มิลลิเมตร
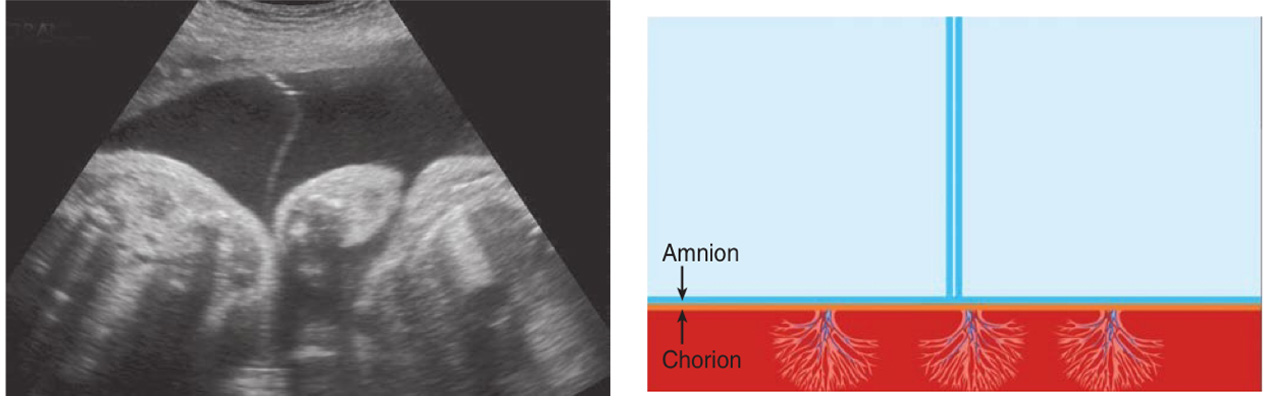
รูปที่ 3 ภาพอัลตราซาวน์และรูปแสดงลักษณะของ T sign คือ Amnion เป็นเส้นบางๆกั้นระหว่างถุงน้ำ (ที่มา: Cunningham FG, Leveno KJ, Dashe JS, Hoffman BL, Spong CY, Casey BM. Editors. Williams Obstetrics, 26e. New York, NY: McGraw Hill; 2022.)
การตรวจรกหลังคลอดสามารถบอก zygosity และ Chorionicity ได้เช่นกัน จากการดูจำนวนรก จำนวน chorion และ amnion
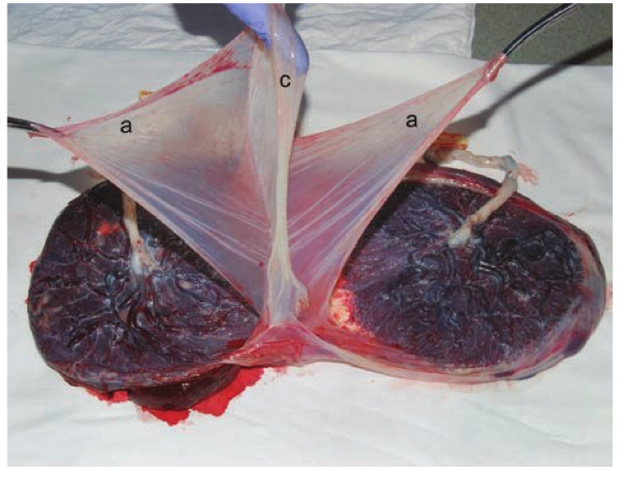
รูปที่ 4 แสดงลักษณะของ dichorionic diamniotic เห็นเป็น chorion คั่นกลางระหว่าง amnion 2 ชั้น
(ที่มา: Cunningham FG, Leveno KJ, Dashe JS, Hoffman BL, Spong CY, Casey BM. Editors. Williams Obstetrics, 26e. New York, NY: McGraw Hill; 2022.)
Spontaneous abortion and vanishing fetus
ครรภ์แฝดมีโอกาสเกิดการแท้งสูงกว่าครรภ์เดี่ยว และพบว่า monochorionic twins มีอัตราการแท้งสูงกว่า dichorionic twins ในบางรายพบว่าสามารถเกิดการแท้งเพียงคนเดียวได้ โดยอีกคนสามารถตั้งครรภ์ต่อไปได้ โดยหากเกิดขึ้นในไตรมาสแรก ทารกอีกคนที่แท้งไป อาจจะสลายหายไปได้ เรียกว่า vanishing fetus สามารถพบได้ร้อยละ 10-40 ของครรภ์แฝด8
Congenital anomaly
อุบัติการณ์ในการเกิดความพิการแต่กำเนิดในการตั้งครรภ์แฝดสูงกว่าการตั้งครรภ์ปกติ ในครรภ์แฝดพบได้ 406 ต่อ 10,000 และในครรภ์เดี่ยวพบได้ 238 ต่อ 10,000 และพบว่าใน monochorionic twins มีโอกาสเกิดความผิดปกติได้สูงกว่า dichorionic twin มากถึงสองเท่าตัว 9
Low birth weight
ทารกในครรภ์แฝดมีแนวโน้มที่จะมีน้ำหนักตัวน้อยกว่าทารกครรภ์เดี่ยว สาเหตุมาจาก ทารกเจริญเติบโตช้าในครรภ์ และการคลอดก่อนกำหนด
Hypertension
ความเสี่ยงในการเกิดความดันโลหิตสูงขณะตั้งครรภ์และภาวะครรภ์เป็นพิษเพิ่มมากขึ้นในครรภ์แฝด เนื่องจากมีระดับของ sFlt-1 (soluble Fms-like tyrosine kinase-1) ซึ่งเป็น antiangiogenic factors เพิ่มสูงขึ้น และ PIGF (placental growth factor) ลดลง 10
Preterm birth
พบว่าอัตราการคลอดก่อนกำหนดในครรภ์แฝดพบได้ร้อยละ 60 และร้อยละ 98 ในครรภ์แฝดสาม 11
พบได้ร้อยละ 10-15 ใน monochorionic twins สาเหตุเกิดจากความผิดปกติของการถ่ายเทเลือดให้กันระหว่างแฝด ผ่านเชื่อมต่อของเส้นเลือด artery – vein anastomoses ทำให้มีการถ่ายเทเลือดจากเส้นเลือดแดงของแฝดผู้ให้ (donor) ไปยังเส้นเลือดดำของแฝดผู้รับ (recipient) แฝดผู้ให้จะซีด ตัวเล็ก ปริมาณเลือดในร่างกายลดลง เลือดที่มาเลี้ยงไตจึงลดลงตามไปด้วย ปัสสาวะจึงลดลง น้ำคร่ำน้อยลง (oligohydramnios) ส่วนแฝดผู้รับจะตัวแดงเนื่องจากมีปริมาณเลือดในร่างกายมาก ปัสสาวะมากขึ้น จึงมีน้ำคร่ำมาก (polyhydramnios) และเกิดภาวะหัวใจล้มเหลว บวมน้ำได้
การตรวจคัดกรอง (Screening) ภาวะ TTTS
ควรเริ่มตรวจติดตามอัลตราซาวน์ทุก 2 สัปดาห์ใน monochorionic twins เริ่มที่อายุครรภ์ 16 สัปดาห์ หากเริ่มพบความแตกต่างของปริมาณน้ำคร่ำ แต่ยังไม่เข้าเกณฑ์วินิจฉัยให้ตรวจติดตามทุก 1 สัปดาห์ 12
การแบ่งระดับความรุนแรงของ TTTS ตาม Quintero staging 13
Stage I : มีความแตกต่างของปริมาณน้ำคร่ำ ในแฝดผู้รับมีน้ำคร่ำมาก (polyhydramnios) พบมี DVP (deep vertical pocket) > 8 ซม. แฝดผู้ให้มีน้ำคร่ำน้อย (oligohydramnios) มี DVP < 2 ซม. และยังเห็นกระเพาะปัสสาวะของแฝดผู้ให้อยู่
Stage II : ไม่เห็นกระเพาะปัสสาวะของแฝดผู้ให้
Stage III : พบความผิดปกติของ doppler artery ของ umbilical artery, ductus venosus, umbilical vein
Stage IV : ทารกคนใดคนหนึ่งบวมน้ำ
Stage V : ทารกคนใดคนหนึ่งเสียชีวิต
การพยากรณ์โรคขึ้นกับ Quintero stage และอายุครรภ์ที่ตรวจพบความผิดปกติ
Stage I สามารถเลือกการรักษาแบบประคับประคอง (expectant management) ตรวจติดตามและเฝ้าระวัง
หรือการใช้เลเซอร์จี้ทำลายบริเวณเส้นเลือดที่เชื่อมต่อกัน (laser ablation)
Stage II – IV สามารถเลือกใช้ได้หลายวิธี วิธีรักษาที่ดีที่สุดคือการรักษาด้วยการใช้เลเซอร์จี้ทำลายบริเวณเส้นเลือดทื่เชื่อมต่อกัน 14 โดยพบว่ามีอุบัติการณ์การเกิดซ้ำร้อยละ 14 15
การเจาะระบายน้ำคร่ำ (amnioreduction) ควรทำหลังจากอายุครรภ์ 26 สัปดาห์ 14
selective fetocide ควรทำก่อนอายุครรภ์ 20 สัปดาห์ โดยใช้ radiofrequency ablation, fetoscopic ligation, coagulation with laser
สาเหตุเกิดจากการมี arteriovenous anastomoses จากเส้นเลือดเส้นเล็ก เกิดการถ่ายเทเลือดแบบทางเดียวจากแฝดผู้ให้ไปยังแฝดผู้รับในปริมาณเล็กน้อยแต่เรื้อรัง TAPS สามารถเกิดขึ้นได้ในทุกอายุครรภ์ หรือเกิดตามหลังการทำ laser ablation ในการรักษา TTTS โดยพบได้ร้อยละ 13 และพบว่ามักเกิดขึ้นภายใน 5 สัปดาห์หลังทำ laser ablation 15
การวินิจฉัย (Diagnosis)
การวินิจฉัยขณะตั้งครรภ์ ใช้การอัลตราซาวน์ดู MCA-PSV หากมีค่ามากกว่า 1.5 MoM ในแฝดผู้ให้ และมีค่าน้อยกว่า 1 MoM ในแฝดผู้รับ จะวินิจฉัยว่ามีภาวะ TAPS ส่วนการวินิจฉัยหลังคลอด คือมีค่าฮีโมโกลบินหลังคลอดแตกต่างกันมากกว่า 8 g/dL16, 17
ตารางแสดงการแบ่งระยะของ TAPS ก่อนคลอดและหลังคลอด 16
การแบ่งระยะต่างๆของ TAPS โดยใช้ค่า MCA-PSV เพื่อแบ่งระยะตอนก่อนคลอด และใช้ค่าฮีโมโกลบินเพื่อแบ่งระยะตอนหลังคลอด โดยมีทั้งหมด 5 ระยะ ดังต่อไปนี้
| Stage | Antenatal staging | Postnatal staging
Hb difference (g/dL) |
| 1 | Donor MCA-PSV > 1.5 MoM and recipient MCA-PSV < 1 MoM, without other signs of fetal compromise | >8 |
| 2 | Donor MCA-PSV > 1.7 MoM and recipient MCA-PSV < 0.8 MoM, without other signs of fetal compromise | >11 |
| 3 | Stage 1 or 2 and cardiac compromise in donor (UA-AREDF, UV pulsatile flow, or DV increased or reversed flow) | >14 |
| 4 | Hydrops of donor twin | >17 |
| 5 | Death of one or both fetuses, preceded by TAPS | >20 |
ทางเลือกของการรักษาขึ้นอยู่กับหลายปัจจัย ได้แก่ อายุครรภ์ที่วินิจฉัย, การตัดสินใจของสตรีตั้งครรภ์, ระดับความรุนแรงของตัวโรค, ความพร้อมของบุคลากรและการเข้าถึงอุปกรณ์การรักษา
ทางเลือกการรักษา ได้แก่
1. การรักษาแบบตรวจติดตามต่อเนื่อง
2. การให้คลอด
3. การใช้ laser surgery
4. การเติมเลือดให้ทารกในครรภ์ (intrauterine transfusion)
5. การยุติการตั้งครรภ์ของทารกหนึ่งคน (selective feticide)
6. การยุติการตั้งครรภ์
ส่วนการรักษาหลังคลอดแล้ว ได้แก่ การเติมเลือดให้แก่แฝดผู้ให้ และการทำ Partial exchange transfusion ให้แฝดผู้รับ
Twin reversed-arterial-perfusion sequence หรือ acardiac twin พบได้ไม่บ่อย แต่เป็นภาวะแทรกซ้อนที่รุนแรง อุบัติการณ์อยู่ที่ 1 ต่อ 35000 การคลอด โดยเกิดจากการมี artery to artery shunt ขนาดใหญ่ ทำให้เลือดดำที่ค่าออกซิเจนต่ำไหลเวียนจากแฝดผู้ให้ไปยังแฝดผู้รับ โดยไม่ผ่านรก และไหลเวียนสู่ iliac vessels ผ่านไปยังส่วนล่างของร่างกาย ทำให้ไม่มีการเจริญของอวัยวะส่วนบนของร่างกาย และแฝดผู้ให้จะมีภาวะหัวใจล้มเหลว เกิดภาวะบวมน้ำ และเสียชีวิตได้
แนวทางการรักษา (Management)
การทำ radiofrequency ablation (RFA) พบว่าอัตราการรอดชีวิตของแฝดผู้ให้หลังจากทำ RFA คือร้อยละ 80 18
พบได้ร้อยละ 15 ในการตั้งครรภ์แฝด และหากวินิจฉัยก่อนอายุครรภ์ 20 สัปดาห์ พบว่ามีโอกาสเสียชีวิตได้ร้อยละ 8-15
การวินิจฉัย ได้แก่ ร้อยละของความแตกต่างของน้ำหนักตัวทารก คิดได้จาก
(น้ำหนักทารกที่ตัวโตกว่า – น้ำหนักทารกที่ตัวเล็กกว่า) / น้ำหนักทารกที่ตัวโตกว่า
หากมีความแตกต่างที่มากกว่าร้อยละ 20 ถือว่าทารกมีการเจริญเติบโตที่ไม่เท่ากัน
พบว่าร้อยละของความแตกต่างของน้ำหนักตัวทารกที่มีค่ามากกว่า 25-30 จะเพิ่มโอกาสการเกิดภาวะแทรกซ้อนหลังคลอดได้ เช่น ภาวะหายใจเหนื่อยหลังคลอด ภาวะเลือดออกในสมอง เนื้อเยื่อรอบโพรงสมองได้รับความเสียหาย ชัก ติดเชื้อในกระแสเลือด ลำไส้อักเสบชนิดเนื้อตาย เป็นต้น
การตั้งครรภ์แฝดที่มีทารกหนึ่งคนโตช้าในครรภ์ พบได้มากในช่วงปลายของมาสที่ 2 ถึงช่วงต้นของไตรมาสที่ 3 การวินิจฉัย ได้แก่ ร้อยละของความแตกต่างของน้ำหนักตัวทารกมีค่ามากกว่า 20 หรือตรวจพบว่ามีความแตกต่างของเส้นรอบวงท้องมากกว่า 20 มิลลิเมตร จะถือว่าเป็นการตั้งครรภ์แฝดที่มีทารกหนึ่งคนโตช้าในครรภ์ 3 หรือตรวจพบว่าทารกคนใดคนหนึ่งมีน้ำหนักตัวน้อยกว่าเปอร์เซ็นต์ไทล์ที่ 10 และมีความแตกต่างของน้ำหนักตัวมากกว่าร้อยละ 25 16
สาเหตุของการเกิดภาวะทารกหนึ่งคนโตช้าในครรภ์ได้แก่
1. เกิดจากการแบ่งตัวของรกขนาดไม่เท่ากัน
2. ตำแหน่งที่สายสะดือเกาะกับรกผิดปกติ เช่น velamentous insertion, marginal insertion, vasa previa
3. ตำแหน่งที่รกเกาะตัวไม่เพียงพอสำหรับรกทั้งหมด
4. ระบบไหลเวียนโลหิตระหว่างทารก 2 คนไม่เท่ากัน
5. แฝดคนใดคนหนึ่งมีความผิดปกติของอวัยวะ
6. เกิดจากความแตกต่างของพันธุกรรมในแฝด dizygotic twins เช่น แฝดเป็นคนละเพศกัน
ภาวะ selective fetal growth restriction สามารถจำแนกได้เป็น 3 กลุ่ม จาก doppler ultrasound 19
Type 1 : positive end-diastolic flow พบว่ามีการพยากรณ์โรคที่ดีกว่าแบบอื่น
Type 2 : persistently absent end-diastolic flow ในทารกที่โตช้ากว่า พบว่ามีโอกาสสูงที่จะแย่ลงกว่าเดิม และเสียชีวิตได้
Type 3 : intermittently absent or reversed end-diastolic flow มีความเสี่ยงที่จะแย่ลง น้อยกว่า type 2
แนวทางการรักษา (Management)
หากพบว่ามีภาวะ sFGR จำเป็นจะต้องตรวจติดตามดูสุขภาพทารกในครรภ์ ปริมาณน้ำคร่ำ และ umbilical artery doppler velocimetry ทุก 1 สัปดาห์ และตรวจติดตามการเจริญเติบโตของทารกทุก 3 สัปดาห์
สาเหตุของทารกแฝดหนึ่งคนเสียชีวิตในครรภ์ พบว่ามักเกิดจาก ภาวะแทรกซ้อนของการสร้างอวัยวะที่ผิดปกติ หรือเกิดจากภาวะแทรกซ้อนของครรภ์แฝด หากเกิดขึ้นในช่วงไตรมาสแรกของการตั้งครรภ์ ทารกคนหนึ่งที่เสียชีวิตจะหายไป หรือเรียกว่า vanishing twin และเมื่อเกิดขึ้นในไตรมาสหลัง ทารกที่เสียชีวิตอาจจะถูกกดทับ เรียกว่า fetus compressus และเมื่อถูกกดทับจนแบนติดไปกับเยื่อหุ้มทารก จะเรียกว่า fetus papyraceus
ในอายุครรภ์ที่มากขึ้น เมื่อทารกคนหนึ่งเสียชีวิต ทารกอีกคนหนึ่งที่ยังมีชีวิตอยู่ พบว่ามีความเสี่ยงในการเกิด การเสียชีวิต โดยครรภ์แฝดชนิด monochorionic diamniotic จะมีความเสี่ยงเพิ่มขึ้น 16 เท่ามากกว่าครรภ์แฝดชนิด dichorionic diamniotic การคลอดก่อนกำหนด และเกิดความเสียหายต่อระบบประสาท เนื่องจากเกิดความแตกต่างของความดันในหลอดเลือดอย่างรวดเร็ว ทำให้เลือดจากแฝดที่มีชีวิตไหลผ่านรกไปหาแฝดที่เสียชีวิต ทำให้เกิดความเสียหายต่อระบบประสาทในแฝดที่ยังมีชีวิตอยู่ เกิดเป็นความพิการทางสมองที่ไม่สามารถป้องกันได้
ตารางแสดงความเสี่ยงในการเกิดภาวะแทรกซ้อนหลังจากทารกคนหนึ่งเสียชีวิตในแฝด monochorionic และ dichorionic 20
| ภาวะแทรกซ้อน | Monochorionic twins | Dichorionic twins |
| ทารกอีกคนเสียชีวิต | 15% | 3% |
| การคลอดก่อนกำหนด | 68% | 54% |
| พบความผิดปกติจากการตรวจวินิจฉัยทางรังสีบริเวณสมองหลังคลอด | 34% | 16% |
| ความผิดปกติของพัฒนาการทางสมองของทารกที่รอดชีวิต | 26% | 2% |
แนวทางการรักษาทารกอีกคนที่มีชีวิตหลังจากทารกคนหนึ่งเสียชีวิต
1. ส่งตัวผู้ป่วยเข้ารับการรักษาที่โรงพยาบาลที่มีความพร้อมด้านแพทย์ผู้เชี่ยวชาญ
2. ultrasound doppler ดู MCA-PSV
เพื่อดูลักษณะของภาวะซีดทุก 2-4 สัปดาห์
3. การรักษาแบบประคับประคองในรายที่ยังตั้งครรภ์ไม่ครบกำหนด
อายุครรภ์ที่เหมาะสมสำหรับการคลอดคือ 34-36 สัปดาห์ ร่วมกับการให้เสตอรอยด์เพื่อช่วยกระตุ้นการเจริญเติบโตของปอด
ตรวจรังสีวินิจฉัยบริเวณสมอง 4-6 สัปดาห์หลังจากทารกคนหนึ่งเสียชีวิต
4. สำหรับรายที่ตั้งครรภ์ครบกำหนดแล้วแนะนำให้คลอด
5. พูดคุยกับคนไข้เกี่ยวกับการพยากรณ์โรคของทารกในครรภ์
6. ตรวจติดตามพัฒนาการทางสมองหลังทารกคลอดครบ 2 ปี
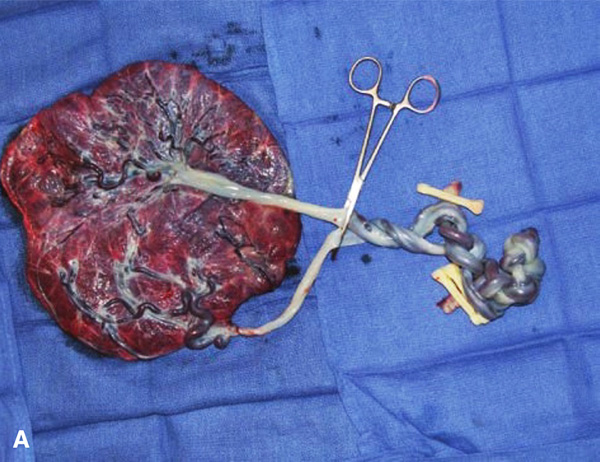
รูปที่ 5 รกของ monochorionic monoamniotic twin แสดงลักษณะของสายสะดือพันกัน
(ที่มา: Cunningham FG, Leveno KJ, Dashe JS, Hoffman BL, Spong CY, Casey BM. Editors. Williams Obstetrics, 26e. New York, NY: McGraw Hill; 2022.)
พบได้บ่อยในแฝดชนิด monochorionic monoamniotic และสามารถทำให้ทารกในครรภ์เสียชีวิตได้ สามารถใช้การทำอัลตราซาวน์ color-flow doppler ช่วยในการวินิจฉัยได้ สายสะดือมีโอกาสที่จะพันกันแบบหลวมตั้งแต่การตั้งครรภ์ไตรมาสแรก และสามารถพันกันแน่นขึ้นได้ตลอด โดยที่ไม่สามารถคาดเดาได้ก่อน
แนะนำให้นอนโรงพยาบาลตั้งแต่อายุครรภ์ 24 ถึง 28 สัปดาห์ และตรวจติดตามสุขภาพทารกในครรภ์ทุกวัน วันละ 1 ชั่วโมง และทำการผ่าตัดคลอดตอนอายุครรภ์ 32 – 24 สัปดาห์ พิจารณาให้สเตอรอยด์เพื่อกระตุ้นการทำงานของปอดทารกก่อน
พบได้ 1:100,000 การตั้งครรภ์ และพบใน monochorionic monoamniotic twin เท่านั้น วินิจฉัยได้จากอัลตราซาวน์ บริเวณที่ติดกันมากที่สุด ได้แก่ ส่วนหน้าอกติดกัน (thoracopagus) สำหรับการวางแผนการคลอด ควรเป็นการนัดผ่าตัดคลอด เนื่องจากการคลอดผ่านทางช่องคลอดมีโอกาสที่จะเกิดการคลอดติด การฉีกขาดของช่องทางคลอด มดลูกแตกได้
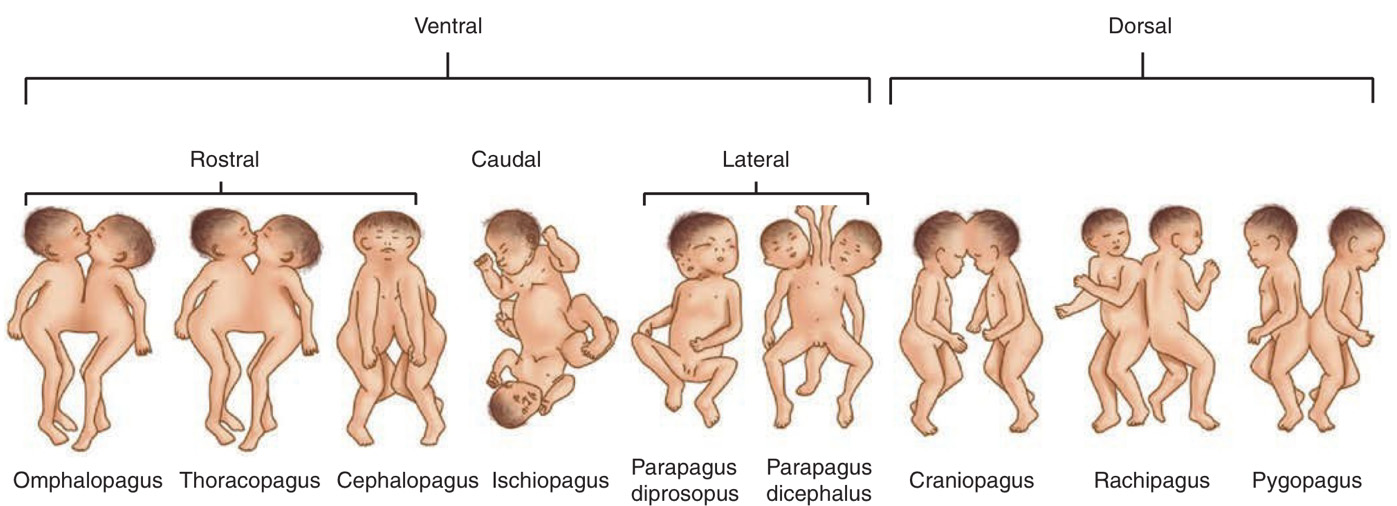
รูปที่ 6 แสดงลักษณะของแฝดที่เชื่อมต่อกันด้วยอวัยวะต่างๆ เกิดเป็น Conjoined twins (ที่มา: Cunningham FG, Leveno KJ, Dashe JS, Hoffman BL, Spong CY, Casey BM. Editors. Williams Obstetrics, 26e. New York, NY: McGraw Hill; 2022.)
ภาวะโภชนาการในหญิงตั้งครรภ์ (Nutrition in pregnancy) 21
สัดส่วนขององค์ประกอบทางโภชนาการที่เหมาะสมคือ โปรตีน : ไขมัน : คาร์โบไฮเดรต ในสัดส่วน 2 : 4 : 4 ในสตรีตั้งครรภ์แฝดปกติ ควรแบ่งมื้ออาหารออกเป็น อาหารหลัก 3 มื้อ และ อาหารมื้อย่อยอีก 3 มื้อ ในสตรีตั้งครรภ์แฝดที่มีค่าดัชนีมวลกายอยู่ต่ำกว่าเกณฑ์ปกติ BMI < 19.8 kg/m2 ควรแบ่งเป็น อาหาร 5 มื้อ ในสัดส่วนเท่ากัน น้ำหนักที่ควรเพิ่มขึ้นตลอดการตั้งครรภ์ จาก 2009 IOM guidelines แนะนำว่าน้ำหนักที่ควรเพิ่มขึ้นในแต่ละ ค่าดัชนีมวลกาย (body mass index, BMI) ค่าดัชนีมวลกายปกติ (BMI 18.5-25 kg/m2) ควรขึ้น 17-25 กิโลกรัม น้ำหนักเกิน (BMI 25-30 kg/m2) ควรขึ้น 14-23 กิโลกรัม โรคอ้วน (BMI > 30 kg/m2) ควรขึ้น 11-19 กิโลกรัม
การตรวจติดตามสุขภาพทารกในครรภ์ (Fetal surveillance) 22
1. Uncomplicated dichorionic
เริ่มตรวจติดตามที่อายุครรภ์ 36 สัปดาห์ สัปดาห์ละ 1 ครั้ง
2. Complicated dichorionic
เริ่มตรวจติดตามตั้งแต่การวินิจฉัย ความถี่ของการติดตามให้พิจารณาเป็นรายบุคคล
3. Uncomplicated monochorionic-diamniotic
เริ่มตรวจติดตามที่อายุครรภ์ 32 สัปดาห์ สัปดาห์ละ 1 ครั้ง
4. Complicated monochorionic-diamniotic
อายุครรภ์ที่เริ่มตรวจติดตามและความถี่ของการติดตามให้พิจารณาเป็นรายบุคคล
5. Monoamniotic
อายุครรภ์ที่เริ่มตรวจติดตามและความถี่ของการติดตามให้พิจารณาเป็นรายบุคคล
Routine monitoring of twin pregnancy with ultrasound 16
1. Uncomplicated dichorionic twin
อัลตราซาวน์ในไตรมาสที่ 1 และไตรมาสที่ 2 หลังจากนั้นควรตรวจติดตามทุก 4 สัปดาห์
2. Uncomplicated monochorionic twin
อัลตราซาวน์ในไตรมาสที่ 1 และตรวจติดตามทุก 2 สัปดาห์ตั้งแต่อายุครรภ์ 16 สัปดาห์ เพื่อเฝ้าระวังภาวะ TTTS และ TAPS
การป้องกันการคลอดก่อนกำหนดในครรภ์แฝด (Preterm prevention)
จากการศึกษาพบว่า การนอนพักตลอดการตั้งครรภ์ การให้ยายับยังการหดตัวของมดลูก การใช้ฮอร์โมนโปรเจสเตอโรน การเย็บผูกปากมดลูก การใช้ห่วงพยุงทางช่องคลอด พบว่าไม่ช่วยลดความเสี่ยงในการคลอดก่อนกำหนดในครรภ์แฝด 23
อายุครรภ์ที่เหมาะสมสำหรับการคลอด (Delivery time) 22
ครรภ์แฝด monochorionic monoamniotic คือ อายุครรภ์ 32-34 สัปดาห์
ครรภ์แฝด monochorionic diamniotic คือ อายุครรภ์ 34-37 สัปดาห์
ครรภ์แฝด dichorionic diamniotic คือ อายุครรภ์ 38-38+6 สัปดาห์
การตั้งครรภ์แฝดจัดอยู่ในกลุ่มที่มีความเสี่ยงสูงกว่าครรภ์เดี่ยว เนื่องจากต้องเฝ้าระวังภาวะแทรกซ้อนต่างๆที่สามารถเกิดขึ้นได้มากกว่าครรภ์เดี่ยว การตรวจติดตามระหว่างการฝากครรภ์จึงเป็นสิ่งสำคัญในครรภ์แฝด รวมไปถึงการเข้ารับการฝากครรภ์ที่เร็ว เพื่อที่จะสามารถแยกชนิดของครรภ์แฝดได้ และสามารถเฝ้าระวังภาวะแทรกซ้อนที่จำเพาะในแต่ละชนิดของการตั้งครรภ์แฝด
การติดเชื้อเอชไอวีจากแม่สู่ลูกเป็นสาเหตุหลักของการติดเชื้อเอชไอวีในเด็ก กรณีไม่ได้รับยาต้านเอชไอวีระหว่างตั้งครรภ์ มีโอกาสถ่ายทอดเชื้อให้ทารกสูงมากถึง 25-40%(1) แม้การติดเชื้อเอชไอวีไม่เพิ่มความพิการแต่กำเนิดของทารกในครรภ์(2) แต่รายงานพบว่าการติดเชื้อเอชไอวีเพิ่มอัตราการแท้งบุตร ทารกโตช้าในครรภ์ การคลอดก่อนกำหนด ทารกน้ำหนักน้อย ทารกตายคลอดและตายปริกำเนิด(3) แต่หากสตรีตั้งครรภ์ได้รับยาต้านไวรัส HAART ในช่วงระหว่างตั้งครรภ์พบว่าภาวะเหล่านี้ลดลงอย่างมีนัยสำคัญเมื่อเทียบกับสตรีที่ไม่ได้รับยา(4)
จากรายงานการติดตามการป้องกันการถ่ายทอดเชื้อเอชต้านไวรัสไอวีจากแม่สู่ลูก กรมอนามัย กระทรวงสาธารณสุข พบอัตราการติดเชื้อเอชไอวีจากแม่สู่ลูก 1.34% ในปีพ.ศ. 2561 (1) โดยประเทศไทยตั้งเป้าหมายที่จะลดอัตราการถ่ายทอดเชื้อเอชไอวีจากแม่สู่ลูกให้ต่ำกว่าร้อยละ 1 ดังนั้นสิ่งสำคัญคือจำเป็นต้องให้ความสำคัญกับการวินิจฉัยการติดเชื้อเอชไอวีในหญิงตั้งครรภ์ตั้งแต่ฝากครรภ์ครั้งแรก ไม่ล่าช้าในการเริ่มยาต้านไวรัส ตรวจติดตามการรักษาอย่างใกล้ชิด( รวมถึงในกลุ่ม discordant couple ) เพื่อวางแผนการให้ยาและวางแผนการคลอดเพื่อลดการถ่ายทอดเชื้อเอชไอวีจากแม่สู่ลูกให้น้อยที่สุด
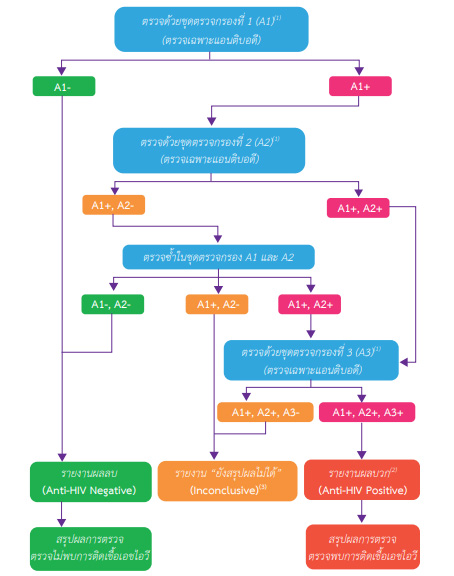
ภาพจาก Thailand National Guidelines onHIV/AIDS Treatment and Prevention 2021/2022 (1)
ใช้การตรวจโดยชุดตรวจอย่างเร็ว ( rapid test ) รุ่นที่ 4 หรือรุ่นที่ 3 ถ้าผล “มีปฏิกิริยา” (reactive) พิจารณารับยาต้านเอชไอวี และต้องนำตัวอย่างเลือดเข้าสู่กระบวนการตรวจปกติอีกครั้งอย่างรวดเร็ว หากผลเป็นลบแต่ความเสี่ยงสูง ให้ทำการตรวจซ้ำ 2 สัปดาห์งดให้นมบุตรไปก่อน
ให้ซักประวัติ ความเสี่ยง การมีเพศสัมพันธ์โดยไม่ได้ป้องกัน อาการ Acute Retroviral Syndrome
ติดตามผล anti-HIV 2 สัปดาห์ ถ้าพบ inconclusive 2 ครั้งให้ถือว่าไม่ติดเชื้อ
ให้พิจารณาจากความเสี่ยงต่อการติดเชื้อจากคู่
| ความเสี่ยงต่อการติดเชื้อจากคู่ | การตรวจเลือดติดตามผลเลือด |
ความเสี่ยงต่ำ
|
|
ความเสี่ยงสูง
|
อายุครรภ์ < 36 สัปดาห์
อายุครรภ์ > 36 สัปดาห์
|
การพิจารณาให้ยา nPEP และ PrEP
|
|
ดัดแปลงจาก Thailand National Guidelines onHIV/AIDS Treatment and Prevention 2021/2022 (1)
หญิงตั้งครรภ์ที่ได้รับการวินิจฉัยว่าติดเชื้อเอชไอวีควรได้รับยาต้านไวรัสโดยเร็วที่สุดในวันเดียวกันกับการวินิจฉัย ( same day ART ) โดยไม่คำนึงถึงจำนวน CD4 โดยการให้ยาในช่วงระหว่างฝากครรภ์ การให้ยาระหว่างคลอด และหลังคลอดสรุปดังตาราง (ดัดแปลงจาก Thailand National Guidelines onHIV/AIDS Treatment and Prevention 2021/2022) (1)
| Antepartum | Intrapartum | Postpartum |
| กรณีที่ 1 หญิงตั้งครรภ์ไม่เคยได้รับยาต้านเอชไอวีก่อนเริ่มตั้งครรภ์ | ||
| แนะนำ TDF + 3TC + DTG
สูตรยาทางเลือก |
ให้ยาสูตรเดิม
และ AZT 600 มก. ครั้งเดียว หากมีความเสี่ยงสูงต่อการติดเชื้อในทารก* |
ให้ยาต่อในสตรีหลังคลอดทุกราย ตามแนวทางการดูแลรักษาผู้ใหญ่ |
ฝากครรภ์ครั้งแรกที่อายุครรภ์มากกว่า 32 สัปดาห์
|
ให้ยาสูตรเดิม (+RAL ถ้าไม่มี DTG)
และ AZT 600 มก. ครั้งเดียว หากมีความเสี่ยงสูงต่อการติดเชื้อในทารก* |
หยุดยา RAL ได้หลังคลอดทันที |
| กรณีที่ 2 หญิงตั้งครรภ์ที่เคยได้รับยาต้านเอชไอวีมาก่อน | ||
|
ให้ยาสูตรเดิม และ AZT 600 มก. ครั้งเดียว หากมีความเสี่ยงสูงต่อการติดเชื้อในทารก* | ให้ยาสูตรเดิม |
| กรณีที่ 3 สตรีตั้งครรภ์ที่มาคลอดโดยไม่ได้รัยการฝากครรภ์ | ||
| ให้ยา TDF + 3TC + DTG กินทันที และ AZT 600 มก. ครั้งเดียว | ให้ยา TDF + 3TC + DTG ต่อเนื่องตามแนวทางการดูแลรักษาผู้ใหญ่ | |
สูตรยาแนะนำ TDF 300 มก + 3TC 300 มก + DTG 50 มก ทุก 24 ชม โดยแนะนำเป็นเม็ดรวม
สูตรยาทางเลือก
สูตรทางเลือกสูตรแรก : TDF + 3TC + EFV
สูตรยาทางเลือกอื่นๆ : TDF + 3TC + LPV/r
TDF + 3TC + ATV/r
AZT + 3TC + LPV/r หรือ ATV/r
ความเสี่ยงสูงต่อการติดเชื้อในทารก ได้แก่ (ประเมินช่วงระหว่างคลอด)
– มาคลอดโดยไม่เคยฝากครรภ์ และไม่เคยกินยาต้านเอชไอวีมาก่อน
– เคยได้รับยามาก่อน แต่ผล HIV VL เมื่อใกล้คลอด (ที่อายุครรภ์ 32-36 สัปดาห์) > 50 copies/mL
– หากไม่มีผล HIV VL เมื่อใกล้คลอด และมีประวัติต่อไปนี้
– กรณีการติดเชื้อเอชไอวีเกิดขึ้นระหว่างตั้งครรภ์ เช่น ผลเลือดเป็นลบเมื่อมาฝากครรภ์ครั้งแรกแต่ผลเลือดเปลี่ยนเป็นบวกในระหว่างตั้งครรภ์ (seroconversion)
3.การตรวจติดตามการรักษา และ เฝ้าระวังผลข้างเคียงของยา
แนวทางการตรวจทางห้องปฏิบัติการที่แนะนำ
| การตรวจทางห้องปฏิบัติการ | ฝากครรภ์ครั้งแรก | ตรวจติดตาม |
| CD4 |
|
|
| HIV VL |
|
|
| CBC |
|
|
| Creatinine |
|
|
| ALT |
|
|
| UA , Urine protein |
|
|
| 50 gm GCT |
|
|
(ดัดแปลงจาก Ruxrungtham K CK, Chetchotisakd P, Chariyalertsak S, Kiertburanakul S PO, et a. Thailand National Guidelines onHIV/AIDS Treatment and Prevention 2021/2022) (1)
การตรวจติดตามการรักษามีประโยชน์เพื่อใช้ในการจำแนกความเสี่ยงต่อการติดเชื้อเอชไอวีของทารก และมีผลต่อการวางแผนการรักษาในช่วงระหว่างคลอด (1)
ตรวจติดตาม HIV Viral loadที่ GA 32-36 สัปดาห์
ถ้ากินยาสูตรที่ไม่มี DTG ให้เพิ่มยา DTG เป็นยาตัวที่ 4 (ถ้าไม่มีใช้ RAL แทน) หรือเปลี่ยนเป็นสูตร TDF + 3TC + DTG แล้วตรวจเลือดซ้ำอีกทีที่ 4 สัปดาห์
4. การวางแผนการรักษาในช่วงระหว่างคลอด
การเลือกช่องทางคลอด
| หญิงตั้งครรภ์ที่ติดเชื้อเอชไอวี | การเลือกช่องทางคลอด |
|
|
|
|
|
|
|
|
|
|
|
การให้ยาช่วงระหว่างคลอด
4. การให้ยาต้านเอชไอวีในทารกแรกเกิดตามความเสี่ยงของการติดเชื้อจากแม่สู่ลูก
พิจารณาการให้ยาในทารกแรกเกิดตามความเสี่ยงของการติดเชื้อเอชไอวีจากแม่สู่ลูก
| ความเสี่ยงของการติดเชื้อเอชไอวีจากแม่สู่ลูก | สูตรยาต้านไวรัส |
Standard risk
|
( เริ่มยาให้เร็วที่สุด ภายใน 1 ชม.หลังคลอดดีที่สุด ) |
High risk
|
3TC syrup 2 มก./กก. ทุก 12 ชม. + NVP syrup 4 มก./กก. ทุก 24 ชม. + นาน 4 สัปดาห์ |
| หากผลตรวจ PCR ที่แรกเกิด หรืออายุ 1 เดือนเป็นบวก ให้เปลี่ยนเป็นยาต้านเอชไอวีขนาดรักษาแทน | |
(ดัดแปลงจาก Ruxrungtham K CK, Chetchotisakd P, Chariyalertsak S, Kiertburanakul S PO, et a. Thailand National Guidelines onHIV/AIDS Treatment and Prevention 2021/2022) (1)
5. แนวทางการดูแลหญิงหลังคลอด
ประเมินความประสงค์ของคู่สามีภรรยาในการมีบุตร ให้คำปรึกษาแนะนำการคุมกำเนิด และการวางแผนมีบุตร
ภาวะหมดระดู คือการที่มีการขาดหายไปของระดูเกิดขึ้นติดต่อกัน 12 เดือน โดยอายุเฉลี่ยของผู้หญิงจะเข้าสู่ภาวะหมดระดูอายุประมาณ 51 ปี(1, 2) วัยหมดระดูนี้เกิดจากการลดลงของจำนวน ovarian follicle จากกระบวนการ apoptosis หรือ programmed cell death ส่งผลให้มีการสร้างฮอร์โมนเอสโตรเจน โปรเจสเตอร์โรน และ antimullerian hormone (AMH) ลดลง รวมถึง inhibin ซึ่งสร้างจาก granulosa cell ลดลง จึงทำให้การสร้าง FSH ที่ pituitary gland เพิ่มขึ้น (โดยปกติแล้ว inhibin จะกดการสร้างและการหลั่ง FSH) อย่างไรก็ตามฮอร์โมนเอสโตรเจนในกระแสเลือดจะยังคงมีอยู่ในระดับต่ำ เนื่องจากการมี peripheral aromatization ที่เนื้อเยื่อไขมัน(1)
The STRAW (The Stage of Reproductive Aging Workshop) ได้อธิบายถึงการเปลี่ยนแปลงช่วงเปลี่ยนผ่านตั้งแต่ reproductive stage ไปจนถึง postmenopause stage โดยการแบ่งระยะของภาวะเจริญพันธุ์ ดังรูป (3)
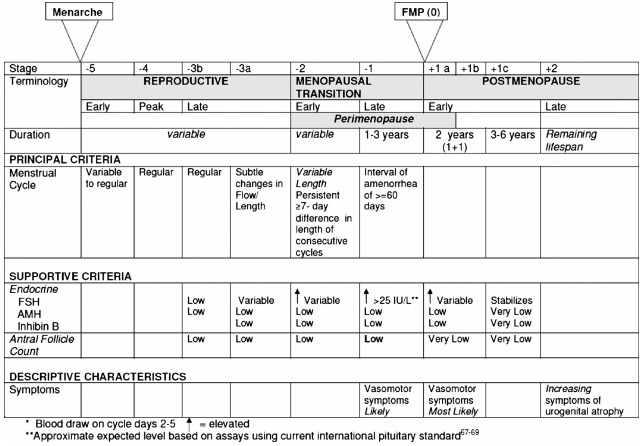
รูปที่ 1: ระยะ (staging) ของภาวะเจริญพันธุ์ (reproductive aging)
ที่มา Harlow SD, Gass M, Hall JE, et al. Executive Summary of the Stages of Reproductive Aging Workshop + 10. J Clin Endocrinol Metab 2012.(3)
ในความหมายคือ การรักษาด้วยฮอร์โมนในวัยหมดระดูเป็นคำที่ใช้แทน hormonal replacement therapy หรือการให้ฮอร์โมนทดแทนที่ใช้เรียกกันในอดีต เป้าหมายในการใช้ฮอร์โมนเพื่อรักษาอาการที่ vasomotor (VMS) หรือ/และ genitourinary syndrome of menopause (GSM) เป็นหลัก ไม่ได้ใช้ในหญิงวัยหมดระดูทุกคนเพื่อป้องกัน cardiovascular disease หรือ dementia อย่างที่เคยใช้ในอดีต(4)
หลักการของการรักษาด้วยฮอร์โมนในวัยหมดระดู คือการให้ในปริมาณฮอร์โมนน้อยที่สุดที่จะสามารถบรรเทาอาการเนื่องมาจากการขาดฮอร์โมนในวัยหมดระดูหรือใกล้หมดระดูได้อย่างมีประสิทธิภาพ โดยการให้ฮอร์โมนทดแทนนั้นควรจะพิจารณาจำเพาะเป็นรายบุคคล อาศัยการพิจารณาจาก
มีอาการร้อนวูบวาบโดยเฉพาะบริเวณหน้า คอ และอก อาจมีอาการเหงื่อออก ลำตัวเย็นชื้น วิตกกังวล หรือรู้สึกใจสั่นได้ อาการรุนแรงจนรบกวนการนอนหลับ รบกวนการใช้ชีวิตประจำวัน
มีอาการทางระบบสืบพันธุ์โดยเฉพาะอาการช่องคลอดแห้ง ระคายเคือง รู้สึกแสบร้อน (จาก vulvovaginal atrophy) เจ็บตอนมีเพศสัมพันธ์ อาการรุนแรงจนรบกวนกิจกรรมทางเพศได้ รวมไปถึงอาการของระบบทางเดินปัสสาวะ เช่น กลั้นปัสสาวะไม่ได้ ปัสสาวะแสบขัด
“ควรเริ่มให้ยาฮอร์โมนทดแทน ในหญิงวัยหมดระดูที่อายุน้อยกว่า 60 ปี และอยู่ในช่วง 10 ปีหลังหมดประจำเดือน (window of opportunity หรือ timing hypothesis )”(5)
การศึกษาขนาดใหญ่ Women’s Health initiative (WHI) ได้เปรียบเทียบกลุ่มอายุที่เริ่มให้ยาและระยะเวลาหลังหมดประจำเดือน พบว่าการให้ยาฮอร์โมน conjugated equine estrogen (CEE) +/- medroxyprogesterone acetate (MPA) ในหญิงวัยหมดระดูที่อายุมากกว่า 60 ปี หรือ เริ่มให้ยาฮอร์โมนหลังหมดประจำเดือนไปแล้วมากกว่า 10 ปี จะยิ่งเพิ่มความเสี่ยง coronary heart disease , stroke , breast cancer , colorectal cancer , endometrial cancer , hip fracture และเพิ่ม mortality (6)
เนื่องจากการรักษาด้วยฮอร์โมนมีความเสี่ยงของการเกิดโรคหัวใจและหลอดเลือด มะเร็งเต้านม และภาวะลิ่มเลือดอุดตันในหลอดเลือดดำ ดังนั้นจึงจำเป็นต้องซักประวัติ ตรวจร่างกาย ประเมินความเสี่ยงก่อนพิจารณาให้ยา รวมไปถึงตรวจเลือดเพื่อประเมินการทำงานของตับ ตรวจระดับไขมันและน้ำตาลในร่างกาย และตรวจเพิ่มเติมทางรังสีวิทยาโดยเฉพาะอย่างยิ่งการตรวจ mammography
จากการศึกษา WHI ที่ศึกษาต่อเนื่องนานถึง 18 ปี พบว่าการเสียชีวิตจากมะเร็งเต้านมในกลุ่มที่ได้รับ MHT เป็น CEE เพียงอย่างเดียวน้อยกว่ากลุ่มที่ได้ยาหลอกอย่างมีนัยสำคัญ(6)
| 10-year ASCVD risk score
( By ACC/AHA guideline)* |
Year since menopause onset | Risk assessment |
| <10 year | ||
| Low (<5%) | MHT |
|
| Moderate (5-10%) | MHT (suggested transdermal) | |
| High (>10%) | Avoid MHT |
*CVD risk calculated by ACC/AHA Cardiovascular Risk Calculator. Methods to calculate risk and risk stratification vary among countries.
ดัดแปลงจาก Stuenkel CA, Davis SR, Gompel A, et al. Treatment of symptoms of the menopause: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab 2015; 100:3975(7)
| Risk category
5-year NCI breast cancer risk assessment* |
Suggestion | Risk assessment |
| Low (<1.67 %) | MHT |
|
| Intermediate (1.67-5%) | Caution (counseling risk-benefit or nonhormonal therapy) | |
| High (>5%) | Avoid MHT |
*Breast Cancer Risk Assessment Tool by national cancer institution
ดัดแปลงจาก Stuenkel CA, Davis SR, Gompel A, et al. Treatment of symptoms of the menopause: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab 2015; 100:3975(7)
Endocrine society’s 2015 treatment of the symptoms of menopause guideline แนะนำให้คำนวณความเสี่ยงต่อ cardiovascular disease และ breast cancer ก่อนเริ่มให้ยาฮอร์โมนในผู้ป่วยทุกราย (7)
เมื่อพิจาณาข้อบ่งชี้ ข้อห้าม ประโยชน์และความเสี่ยงในการได้รับฮอร์โมนในผู้ป่วยแต่ละรายแล้วตัดสินใจให้การรักษา ลำดับถัดไปให้พิจารณาการให้การรักษา ตารางแสดงสรุปการรักษาแบบต่างๆ เมื่อพิจาณาข้อบ่งชี้ ข้อห้าม ประโยชน์และความเสี่ยงในการได้รับฮอร์โมนในผู้ป่วยแต่ละรายแล้วจึงตัดสินใจให้การรักษา ลำดับถัดไปให้พิจารณาการให้การรักษา ตารางแสดงสรุปการรักษาแบบต่างๆ
| Hormone therapy | FDA-approved |
Systemic estrogen Vaginal/local estrogen (for GSM)
|
/
/ / / X / X X |
| Nonhormonal therapy / Alternative treatment | FDA-approved |
|
X
/ X / X X X |
| Lifestyle Change and supplementation / Complementary medicine | FDA-approved |
|
additional |
ดัดแปลงจาก 1. Berek JS, Berek DL. Berek & Novak’s gynecology. Sixteenth ed. Philadelphia: Wolters Kluwer; 2020. 431-444 p.(1)
2. ACOG Practice Bulletin No. 141: management of menopausal symptoms. Obstet Gynecol. 2014;123(1):202-16.(2)
ฮอร์โมนทดแทนที่มีวิธีให้ที่แตกต่างกันอยู่สองชนิดคือ เอสโตรเจนตัวเดียว (unopposed estrogen therapy) และเอสโตรเจนร่วมกับการให้โปรเจสติน (combined estrogen-progestin therapy)
พิจารณาให้ในรายที่ทำการตัดมดลูกไปแล้ว เนื่องจากการได้รับเอสโตรเจนเพียงตัวเดียวจะเพิ่มความเสี่ยงต่อการเป็นมะเร็งเยื่อบุโพรงมดลูกในรายที่ยังมีมดลูก ไม่ว่าจะเป็นการให้แบบต่อเนื่องหรือการให้แบบเป็นรอบคือได้รับฮอร์โมนเอสโตรเจน 3 สัปดาห์ และหยุดฮอร์โมนอีก 1 สัปดาห์ พบว่าต่างเพิ่มความเสี่ยงต่อมะเร็งเยื่อบุโพรงมดลูก(8) และจากการศึกษาพบว่าในหญิงที่ได้รับฮอร์โมนเอสโตรเจนตัวเดียวเพิ่มความเสี่ยงในการเกิด thromboembolic event โดยเฉพาะในหนึ่งปีแรก แต่ไม่เพิ่มความเสี่ยงในการเกิดมะเร็งเต้านม (6, 9)
การให้เอสโตรเจนร่วมกับโปรเจสติน ใช้ในหญิงที่ต้องการฮอร์โมนและยังมีมดลูก จะมีการให้อยู่สองแบบ คือ แบบเป็นรอบๆ (sequential) และแบบการให้ต่อเนื่อง (continuous)
progestin therapy) เป็นการให้ฮอร์โมนเอสโตรเจนทุกวันร่วมกับการให้ฮอร์โมนโปรเจสติน 12-14 วันทุกเดือน เพื่อลดการเกิดมะเร็งเยื่อบุโพรงมดลูกจากการให้ฮอร์โมนเอสโตรเจน โดยการให้ฮอร์โมนวิธีนี้ทำให้มีระดูได้ร้อยละ 90 (10)
therapy) วิธีนี้จะทำให้ส่วนใหญ่ขาดระดู เนื่องจากากรที่ฮอร์โมนโปรเจสตินทำให้เกิดเยื่อบุโพรงมดลูกฝ่อ ยกเว้น 3-6 เดือนแรกหลังเริ่มใช้ฮอร์โมนซึ่งเป็นผลข้างเคียงที่พบบ่อย โดยฮอร์โมนที่ให้อาจจะให้แยกกันหรือเป็นฮอร์โมนรวมในยาเม็ดเดียวกันก็ได้ โดยพบว่ามีผลดีต่อการป้องกันมะเร็งเยื่อบุโพรงมดลูกและเยื่อบุโพรงมดลูกหนาตัวผิดปกติได้(11) ทั้ง 2 วิธีมีข้อดีข้อเสียแตกต่างกันไป จากการศึกษาพบว่าการให้แบบ continuous regimen มีความเสี่ยงในการเกิด breast cancer มากกว่าแบบ sequential regimen แต่เป็นเพียงผลจากการศึกษาแบบ observation
ขนาดยาและรูปแบบการให้ยา
ฮอร์โมนทดแทนที่มีในท้องตลาดมีหลากหลายชนิดและหลากหลายแหล่งผลิต เอสโตรเจนที่ให้มีหลายรูปแบบ ทั้งแบบรับประทาน แบบแผ่นแปะหรือแบบเจลทาผิวหนัง พบว่าทุกวิธีสามารถลดอาการวัยทองได้อย่างมีประสิทธิภาพ (2) สรุปขนาดยาและรูปแบบการให้ยาเอสโตรเจนและโปรเจสตินข้อดีข้อเสีย ดังนี้
| Estrogen | รูปแบบการให้ยา | ||
| Equivalent dose | Oral route | Transdermal route | Vaginal route |
Standard dose:
0.0375–0.05 mg/d
|
|
|
|
| Progestin | รูปแบบการให้ยา | |
| Equivalent dose (sequential regimen) | Oral route | Intrauterine |
*ควรเลือกใช้ชนิดที่ใกล้เคียงกับฮอร์โมนในร่างกายและมีฤทธิ์ androgenic effect ต่ำ (เนื่องจาก androgenic effect จะทำให้ผลดีของ estrogen ต่อ CVS ลดลง) |
continuous |
|
Uptodate guideline Treatment of menopausal symptoms with hormone therapy แนะนำการเลือกใช้ยาในหญิงวัยหมดประจำเดือนที่ยังมีมดลูก ตาม patient’s menopausal stage และกรณีต่างๆ ดังนี้(16)
แนะนำ sequential combined regimen (17β estradiol ทุกวันและให้ sequential oral micronized progesterone 200 mg/day 12 วันต่อเดือน)
2. Women >2 -3 years post-final menstrual period
Continuous combined regimen สามารถให้ได้ทั้งแบบเม็ดรวม หรือให้แบบแยกมีผลในการรักษาพอๆกัน ขนาดที่แนะนำคือ
3. Pre- or perimenopausal women ที่ได้รับการตัดรังไข่ทั้งสองข้าง
4. Use oral contraception during menopausal transition
Low dose estrogen oral contraception (20 mcg of ethinyl estradiol) สามารถใช้เป็นทางเลือกในการรักษาอาการร้อนวูบวาบในช่วงใกล้หมดประจำเดือนได้ในผู้หญิงที่จำเป็นต้องใช้ยาเพื่อหวังผลคุมกำเนิดหรือใช้รักษาโรคทางนรีเวชเพื่อคุมควบอาการเลือดออกผิดปกติ (supraphysiologic dose of estrogen and progestin) (17) แต่ควรหลีกเลี่ยงในผู้ป่วย perimenopause ที่อ้วนหรือสูบบุหรี่เพราะเพิ่มโอกาสเสี่ยงในการเกิดลิ่มเลือดอุดตัน
แม้ว่าในช่วง perimenopause อัตราการตั้งครรภ์ต่ำมาก แต่พบว่าผู้หญิงช่วงอายุ 45-49 หากไม่ได้คุมกำเนิดมีโอกาสตั้งครรภ์ 2-3% และลดลงเหลือ 1 % หากอายุมากกว่า 50 ปี ในทางปฏิบัติจึงแนะนำให้หยุดใช้ยาคุมกำเนิดได้หากอายุมากกว่า 50 ปี โดยค่อยๆลดขนาดยาลงสัปดาห์ละ 1 เม็ด เนื่องจากถ้าหยุดทันทีอาจเกิดอาการร้อนวูบวาบได้ แต่หากมีอาการของภาวะหมดระดูให้ใช้ postmenopausal estrogen regimen เหมือนหญิงวัยหมดระดูทั่วไป(16)
5. Special consideration
แนะนำให้เริ่มฮอร์โมนทดแทนไปอย่างต่อเนื่องจนถึงเมื่อหมดประจำเดือนเลย เพื่อป้องกันภาวะกระดูกพรุน และ cardiovascular disease โดยให้หยุดได้เมื่อเข้าสู่ช่วงอายุเฉลี่ยของ menopause (50-51ปี) หากหยุดยาแล้วมีอาการให้พิจารณาเหมือนการเริ่มยาในหญิงวัยหมดระดูทั่วไป(16)
HABITS trial (Hormonal replacement after breast cancer- Is it safe) ไม่แนะนำให้ใช้ฮอร์โมนเอสโตรเจนในผู้ป่วยที่มีประวัติเป็นโรคมะเร็งเต้านม แม้ว่าจะหมดระดูก่อนวัยอันควร เนื่องจากพบว่าการใช้ฮอร์โมนเพิ่มโอกาสการกลับมาเป็นซ้ำของโรคมะเร็งเต้านมได้ แนะนำให้ใช้ยาทางเลือกแทน
ฮอร์โมนทดแทนสามารถใช้รักษาอาการร้อนวูบวาบและ estrogen-associated migraine ได้ การศึกษาความเสี่ยงการเกิด stroke ในการใช้ยาฮอร์โมนทดแทนของหญิงวัยหมดระดูที่เป็นโรคไมเกรนยังมีไม่มากพอ โรคปวดศีรษะไมเกรนจึงไม่ถือเป็นข้อห้ามที่ชัดเจนในการใช้ยาฮอร์โมนทดแทน แต่ควรใช้อย่างระมัดระวังแนะนำให้ใช้เป็น low dose transdermal regimen (<50 mcg transdermal estradiol )(7, 18)
แนะนำเป็นการให้ยาฮอร์โมนเฉพาะที่ แบบให้ทางช่องคลอด ทั้งในรูปแบบครีมทา วงแหวน หรือยาเม็ดสอดช่องคลอด หากอาการไม่ดีขึ้นให้ให้พิจารณาเพิ่มสารหล่อลื่น (vaginal lubricants) หรือสารเพิ่มความชุ่มชื่น (vaginal moisturizers) อาจจะช่วยทำให้อาการทางช่องคลอดดีขึ้นได้
มีการศึกษา meta-analysis ของ Cochrane ในหญิง 4,162 คนเกี่ยวกับการใช้เอสโตรเจนแบบเฉพาะที่ เทียบกับกลุ่มยาหลอก พบว่าไม่ทำให้มีเยื่อบุโพรงมดลูกหนาตัวผิดปกติเพิ่มขึ้น ฉะนั้นการใช้เอสโตรเจนเฉพาะที่อาจไม่ต้องให้โปรเจสตินร่วมด้วย แต่หากหญิงที่ใช้ฮอร์โมนเอสโตรเจนเฉพาะที่แล้วเกิดมีเลือดออกผิดปกติก็ควรจะต้องค้นหาสาเหตุของการเลือดออกผิดปกติด้วย(14)
ในหญิงที่มีประวัติเรื่องมะเร็งเต้านม ควรหลีกเลี่ยงการให้เอสโตรเจน รวมถึงการให้แบบเฉพาะที่ทางช่องคลอด ควรจะใช้วิธีอื่นที่ไม่เกี่ยวกับฮอร์โมน เช่น estrogen agonists–antagonists เช่น ospemifene 60 mg ต่อวัน ได้รับการรับรองจาก FDA ว่าช่วยในเรื่องช่องคลอดแห้งฝ่อได้ และช่วยรักษาในรายที่มีอาการเจ็บขณะมีเพศสัมพันธ์(moderate-to-severe dyspareunia) โดยยาอาจจะมีผลข้างเคียงเรื่อง ร้อนวูบวาบ สารคัดหลั่งทางช่องคลอด เหงื่อออกมาก หรือมี muscle spasm ได้(19)
จากที่กล่าวข้างต้น หลักการของการให้ฮอร์โมนคือการให้ในปริมาณน้อยที่สุดที่จะสามารถบรรเทาอาการได้ และปรับขนาดยาขึ้นจนสามารถควบคุมอาการผู้ป่วยได้ คงขนาดยาดังกล่าวจนอาการคงที่ 3-5 ปี จึงเริ่มปรับลดขนาดยา(20) (ขึ้นกับอายุผู้ป่วยขณะนั้น ถ้าเริ่มยาตั้งแต่อายุน้อยไม่มีโรคประจำตัวอาจให้ยาติดต่อกันถึง 5 ปีแล้วเริ่มลดระดับยาได้)
Endometrial monitoring
ยังไม่มีความจำเป็นต้องทำ routine transvaginal ultrasound เพื่อเฝ้าระวังเยื่อบุโพรงมดลูกหลังจาการใช้ฮอร์โมน หากมีเลือดออกผิดปกติจำเป็นต้อง ซักประวัติ ตรวจร่างกาย และได้ชิ้นเนื้อเยื่อบุโพรงมดลูกมาตรวจดูแน่ชัดว่าไม่มีภาวะ endometrial hyperplasia หรือ endometrial cancer โดยอาการเลือดออกกระปริบกระปรอยหลังจากใช้ฮอร์โมนแบบ continuous combined regimen (unscheduled bleeding) อาจเกิดขึ้นได้ในช่วง 6 เดือนแรก
Mammography
ในทางปฏิบัติแนะนำให้ตรวจ routine mammography ทุก 1-2 ปีแม้ใช้ฮอร์โมนในระยะสั้น(16) ทั้งในผู้ป่วยที่รักษาด้วยฮอร์โมนแบบ estrogen therapy และ estrogen-progesterone therapy ในการศึกษาของ WHI พบว่า estrogen-progesterone therapy มีความเสี่ยงในการเกิดมะเร็งเต้านมมากกว่าและจะเพิ่มอัตราการเกิดมะเร็งเต้านมเมื่อใช้ฮอร์โมนทดแทนไปมากกว่า 4 ปี(7)
การปรับลดขนาดยาและการหยุดยาฮอร์โมน
จากการศึกษาหลังจากหยุดยาแล้วมีโอกาสกลับมามีอาการซ้ำถึง 50% โดยขึ้นอยู่กับอายุและระยะเวลาที่ใช้(2) ยังไม่มีหลักฐานสนับสนุนมากพอว่าวิธีการลดขนาดยาแบบค่อยเป็นค่อยไปหรือแบบหยุดยาทันทีลดโอกาสการกลับมาเป็นซ้ำได้มากกว่า(20) Uptodate แนะนำให้ลดขนาดยาแบบค่อยเป็นค่อยไปแบบลดสัปดาห์ละ 1 เม็ดติดต่อกัน 1 เดือน (เช่น ลดเหลือสัปดาห์ละ 6 เม็ด เดือนถัดไปเหลือสัปดาห์ละ 5 เม็ด ) เพื่อง่ายต่อการกลับไปเพิ่มขนาดยาที่สามารถคุมอาการได้(16)
The North American Menopause Society and ACOG แนะนำให้สามารถยืดระยะเวลาการให้ฮอร์โมนไปมากกว่า 5 ปีหรือให้หยุดอายุ 65 ปี โดยพิจารณาความรุนแรงของอาการ โรคประจำตัว และความเสี่ยงของผู้ป่วยแต่ละคนเป็นรายๆไป(2, 18) เพราะพบว่า 40%ของผู้ป่วยช่วงอายุ 60-65 ปียังมีอาการร้อนวูบวาบจนรบกวนการนอนหลับและรบกวนชีวิตประจำวัน
โรคอุ้งเชิงกรานอักเสบ (pelvic inflammatory disease or PID) คือ โรคที่เกิดการอักเสบจากการติดเชื้อของอวัยวะสืบพันธ์ส่วนบนของผู้หญิง ซึ่งอาจมีการอักเสบที่เยื่อบุโพรงมดลูก ท่อนำไข่ รังไข่ รวมไปถึงเยื่อบุช่องท้องบริเวณอุ้งเชิงกราน(1) การติดเชื้อในอุ้งเชิงกรานถือว่าเป็นโรคที่ติดต่อทางเพศสัมพันธ์เป็นหลัก โดยจะมีการลุกลามของเชื้อก่อโรคจากอวัยวะสืบพันธ์ส่วนล่างขึ้นไปสู่อวัยวะสืบพันธ์ส่วนบน (2) โรคนี้มีแสดงอาการได้หลากหลาย บางรายอาจมีอาการเพียงเล็กน้อย ส่วนในรายที่มีอาการรุนแรงอาจเกิดภาวะแทรกซ้อน เช่น ก้อนฝีหนองในอุ้งเชิงกราน (Tubo-ovarian abscess or TOA) หรือการอักเสบในช่องท้องรุนแรงซึ่งอาจถึงขั้นเสียชีวิตได้หากได้รับการวินิจฉัย และการรักษาที่ล่าช้า (1, 3, 4)
การติดเชื้อในอุ้งเชิงกราน เกิดขึ้นจากการที่มีการติดเชื้อบริเวณปากมดลูก และมีการลุกลามขึ้นไปที่เยื่อบุโพรงมดลูก ท่อนำไข่ รังไข่ เยื่อบุช่องท้อง และอวัยวะใกล้เคียงในอุ้งเชิงกราน (2) มากกว่า 85% ของเชื้อก่อโรคเกิดจากเชื้อติดต่อทางเพศสัมพันธ์ ส่วนอีกประมาณ 15% เกิดมาจากเชื้อในทางเดินอาหาร หรือเชื้อในระบบทางเดินหายใจที่อาจปนเปื้อนเข้ามาภายในช่องคลอด (5) โดยปกติแล้วปากมดลูกจะทำหน้าที่ป้องกันเชื้อโรคต่าง ๆ ไม่ให้เข้าสู่โพรงมดลูก ทำให้โพรงมดลูกอยู่ในสภาวะปราศจากเชื้อ (Sterile) เมื่อเกิดการติดเชื้อที่บริเวณปากมดลูกขึ้น ส่งผลให้การป้องกันนี้เสียไป ทำให้เชื้อก่อโรคสามารถลุกลามเข้าสู่โพรงมดลูกได้ (2)
ความเสี่ยงหลักของการเกิดอุ้งเชิงกรานอักเสบ คือการมีเพศสัมพันธ์กับคู่นอนหลายคนโดยไม่ได้ป้องกัน แต่ในทางตรงกันข้าม การใช้ถุงยางอนามัยอย่างสม่ำเสมอและถูกต้องจะเป็นปัจจัยที่ช่วยป้องกันการเกิดอุ้งเชิงกรานอักเสบได้ อย่างไรก็ตามจากการศึกษาพบว่าปัจจัยเสี่ยงของการเกิด PID มีดังนี้
ผู้ป่วยที่มีความเสี่ยงต่อการเกิดอุ้งเชิงกรานอักเสบ คือหญิงที่ยังมีเพศสัมพันธ์ โดยเฉพาะผู้ที่มีคู่นอนหลายคนจะยิ่งเพิ่มความเสี่ยงมากขึ้น(4) นอกจากนี้ผู้ที่มีประวัติเป็นโรคอุ้งเชิงกรานอักเสบ หรือมีประวัติคู่นอนเป็นโรคติดต่อทางเพศสัมพันธ์ ก็จะยิ่งมีความเสี่ยงต่อการติดเชื้ออุ้งเชิงกรานมากขึ้น (2)
โรคอุ้งเชิงกรานอักเสบ มีความรุนแรงและการดำเนินโรคที่แตกต่างกันได้หลายรูปแบบ มีทั้งความรุนแรงน้อยไปจนถึงรุนแรงมาก ทำให้การวินิจฉัยในผู้ป่วยบางรายทำได้ยาก (1, 4) จากการที่โรคอุ้งเชิงกรานอักเสบมีความรุนแรงและการดำเนินโรคที่หลากหลาย ทำให้แบ่ง Spectrum ของโรคได้ ดังนี้
Symptoms
Signs:
Perihepatitis (Fitz-Hugh Curtis Syndrome) (4, 10)
เป็นภาวะที่เกิดการอักเสบที่บริเวณ Liver capsule และ peritoneal surface บริเวณ anterior right upper quadrant โดยไม่ได้เกิดการอักเสบเข้าสู่ Liver parenchyma โดยเกิดจากการติดเชื้อผ่านเข้าสู่ช่องท้องและไปสู่บริเวณตับ การอักเสบดังกล่าวทำให้เกิดพังผืดขึ้น สามารถมองเห็นเป็นลักษณะ Violin string-like adhesion จากการทำ Laparoscopy หรือการมองเห็นด้วยตาเปล่า (รูปที่ 1) อาการของผู้ป่วยจะปวดท้องด้านขวาบน อาการปวดอาจแย่ลงหากเคลื่อนไหว หรือเป็นไปตามการหายใจ อาจมีอาการปวดไปที่บริเวณไหล่ขวาร่วมด้วย การตรวจร่างกายจะพบ Right upper quadrant tenderness อาจมี rebound tenderness หรือ guarding ในผู้ป่วยภาวะนี้ liver aminotransferases มักปกติ หรือสูงขึ้นเพียงเล็กน้อย
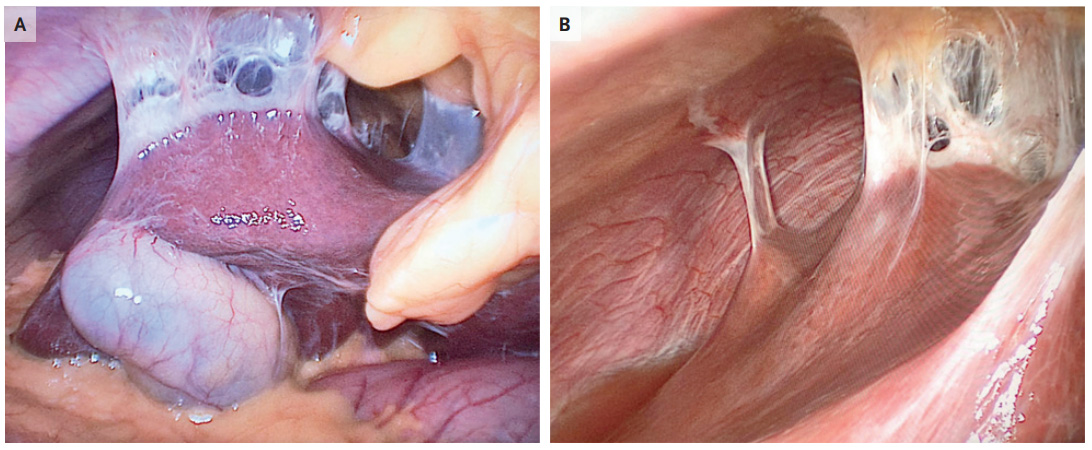
รูปที่ 1 แสดง Violin string–like adhesions ตำแหน่ง anterior surfaces of the liver (A), superior surfaces of the liver (B) (ดัดแปลงจาก (11))
Tubo-ovarian abscess (TOA)
เป็นภาวะแทรกซ้อนจาก PID ที่กลายเป็นก้อนฝีหนองเกิดขึ้นบริเวณท่อนำไข่ และ/หรือรังไข่ TOA เป็นภาวะแทรกซ้อนที่อันตราย อาจถึงแก่ชีวิตได้ หากเกิด TOA ขึ้น และมี systemic sepsis ร่วมด้วย จะมีอัตราการเสียชีวิตของผู้ป่วยสูงถึง 5-10% (3) โดยรายละเอียดเกี่ยวข้องกับ TOA จะได้กล่าวถัดไปในเอกสารฉบับนี้
เนื่องจากการวินิจฉัยอุ้งเชิงกรานอักเสบอาจทำให้ยากเนื่องจากมีอาการและอาการแสดงที่หลากหลาย และโรคนี้มีโอกาสเกิดผลกระทบต่อระบบการสืบพันธุ์ของเพศหญิง CDC จึงได้แนะนำให้แพทย์วินิจฉัยอุ้งเชิงกรานอักเสบในสตรีโดยใช้ขีดระดับความไวที่ต่ำ (Low threshold)
จากข้อมูลการศึกษาที่ผ่านมาพบว่า หากใช้การวินิจฉัยอุ้งเชิงกรานอักเสบโดยอาศัยอาการและอาการแสดงทางคลินิก จะมี Positive predictive value (PPV) อยู่ที่ 65-90% เมื่อเทียบกับ Laparoscopy โดยที่ PPV ของการวินิจฉัยจะเพิ่มสูงขึ้นในกลุ่มผู้ป่วยที่เป็น sexually active young women โดยเฉพาะในวัย Adolescents หรือผู้ที่อาศัยในพื้นที่ที่มีความชุกของเชื้อ Gonorrhea และ Chlamydia สูง ในการวินิจฉัยอุ้งเชิงกรานอักเสบนั้น ไม่ได้มีอาการหรืออาการแสดงอย่างใดอย่างหนึ่งที่มีความไวและความจำเพาะต่อการวินิจฉัย ดังนั้นการใช้หลายลักษณะอาการและอาการแสดงทางคลินิกร่วมกันเพื่อช่วยในการวินิจฉัยนั้นจะส่งผลต่อทั้งความไวและความจำเพาะของการวินิจฉัยในทิศทางตรงกันข้าม
CDC แนะนำว่าควรสงสัย และให้การวินิจฉัยอุ้งเชิงกรานอักเสบ ในหญิง Sexually active young women และหญิงที่มีความเสี่ยงต่อโรคติดต่อทางเพศสัมพันธ์ ที่มาด้วยอาการปวดท้องน้อย โดยไม่มีสาเหตุอื่นนอกเหนือจากอุ้งเชิงกรานอักเสบ หรือ มี Minimum criteria ที่เข้าได้อย่างน้อย 1 ข้อ ดังนี้
โดย Minimum criteria ที่กล่าวมา อาจมีแม่นยำในการวินิจฉัยไม่เพียงพอ ดังนั้น การจะให้การวินิจฉัยและตัดสินใจเริ่มการรักษา จึงควรพิจารณาลักษณะอาการทางคลินิก หรือการส่งตรวจเบื้องต้นเพิ่มเติม เพื่อเพิ่มความจำเพาะในการวินิจฉัย โดยมี Additional criteria ที่ช่วยเพิ่มความจำเพาะจาก Minimum criteria ดังนี้
โดยส่วนใหญ่ของผู้ป่วยอุ้งเชิงกรานอักเสบจะมี cervical mucopurulent discharge หรือมี WBCs on saline microscopy of vaginal fluid หากผู้ป่วยรายใดสงสัยอุ้งเชิงกรานอักเสบ แต่ไม่มีตกขาวผิดปกติ หรือไม่พบเม็ดเลือดขาวจากการตรวจ Vaginal fluid การวินิจฉัยอุ้งเชิงกรานอับเสบจะมีความเป็นไปได้น้อย ควรพิจารณาถึงสาเหตุของอาการปวดท้องอื่น ๆ ก่อน
การนำ vaginal secretion ไปส่องตรวจด้วยกล้องจุลทรรศน์จะพบมีเม็ดเลือดขาวสูงขึ้น โดยการศึกษาพบว่าการตรวจ Microscopy มี Negative predictive value สูงถึง 94.5% (7, 12)
ระดับ ESR และ CRP ที่เพิ่มสูงขึ้นจะช่วยสนับสนุนการวินิจฉัย PID อย่างไรก็ตาม Inflammatory marker ทั้งสองนี้ไม่ได้ specific ต่อ PID และอาจมีระดับที่ปกติได้ในรายที่ความรุนแรงของโรคน้อย ดังนั้น Marker เหล่านี้อาจมีประโยชน์ในการประเมินความรุนแรง และใช้ในการติดตามการรักษา (4, 7)
ในกรณีที่ตรวจ Cervical discharge gram stain พบมี Intracellular diplococci จะช่วยสนับสนุนการวินิจฉัย PID อย่างไรก็ตาม การตรวจไม่พบเชื้อดังกล่าวก็ไม่สามารถใช้ในการแยกโรค PID ออกได้ เนื่องจาก gram stain มีความไวของการตรวจพบเชื้อที่ต่ำ และ PID ก็อาจเกิดจากการติดเชื้ออื่น ๆ นอกจาก Gonorrhea ได้ (4)
ในผู้ป่วย PID อาจพบจำนวนเม็ดเลือดขาวสูงขึ้นได้ แต่ไม่จำเป็นต้องพบเม็ดเลือดขาวสูงในทุกราย พบว่าประมาณ 60% ของผู้ป่วยเท่านั้นที่จะมี WBC สูงขึ้น (13)
ในหญิงวัยเจริญพันธุ์ที่สงสัย PID ควรได้รับการตรวจ UPT เพื่อแยกภาวะฉุกเฉินทางสูติกรรม เช่น Ectopic pregnancy หรือ Abortion (4)
อาจมีส่วนช่วยในการแยกโรคติดเชื้อในทางเดินปัสสาวะ อย่างไรก็ตามการพบเม็ดเลือดขาวในปัสสาวะก็ไม่สามารถแยกโรค PID ออกไปได้ เนื่องจากการติดเชื้อใน female genital tract จะสามารถทำให้เกิด Sterile pyuria ได้ (4, 14)
เพื่อเป็นการตรวจโรคติดต่อทางเพศสัมพันธ์ที่อาจพบร่วมกันกับการเกิด PID ได้(4)
ในบางครั้งการใช้เพียงลักษณะอาการทางคลินิก อาจไม่เพียงพอสำหรับการวินิจฉัย PID หรือ อาจแยกยากจากภาวะอื่น เช่น Ruptured/Hemorrhagic ovarian cyst, acute appendicitis หรือ acute diverticulitis ซึ่งอาจต้องใช้ Imaging เพื่อช่วยสนับสนุนการวินิจฉัย (15) ในกรณีที่จะส่ง Imaging แนะนำให้ทำ Ultrasound เป็นอย่างแรก โดย Transvaginal ultrasound เป็นตัวเลือกแรกที่แนะนำ (13, 15) สำหรับในผู้ป่วยบางรายการส่งตรวจ CT หรือ MRI เพิ่มเติมก็อาจมีประโยชน์ในการช่วยประเมินขอบเขตของก้อน Abscess หรือในกรณีที่สงสัย Ruptured TOA และยังช่วยในการวินิจฉัยแยกโรคทางศัลยกรรมได้อีกด้วย (4, 15) อย่างไรก็ตาม การทำ Ultrasound ถือว่ามี sensitivity ที่ค่อนข้างต่ำ โดยเฉพาะในผู้ป่วย PID ที่มีความรุนแรงน้อย และยังมี Specificity ที่ไม่ดีในหลาย ๆ ราย(15)
Ultrasound findings (15) ที่พบได้ในผู้ป่วย PID ได้แก่
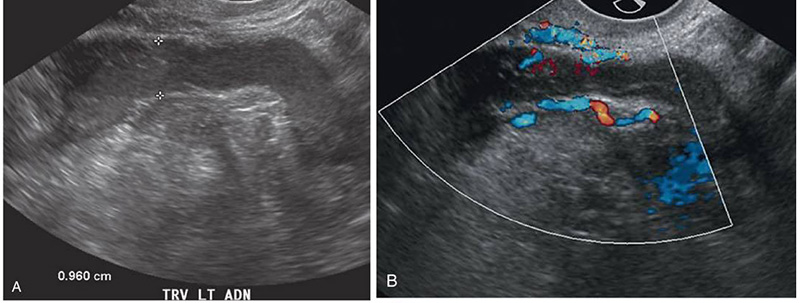
รูปที่ 2 แสดง Thickened left fallopian tube (A) และ Increased vascularity in the wall of the tube and in the surrounding inflamed peritubal fat (B) (ดัดแปลงจาก (15))
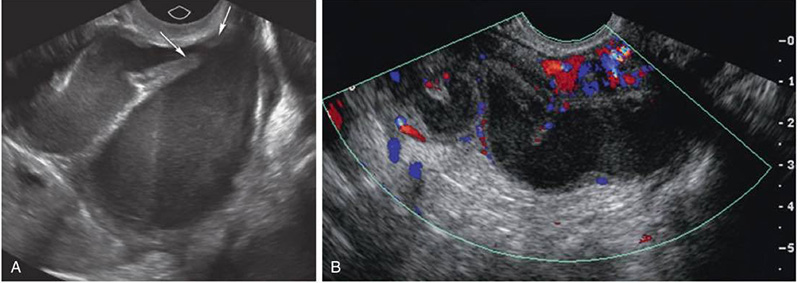
รูปที่ 3 แสดง Pyosalpinx A: The left fallopian tube is markedly dilated and filled with echogenic material, consistent with pus, hemorrhage, or debris. The tube is curled back upon itself demonstrating the incomplete septation sign and is also focally symmetrically indented, the “waist sign” (arrows). B: Color Doppler image of the left adnexa demonstrating a dilated serpiginous tubular structure containing low level intraluminal echoes and increased mural vascularity.
(ดัดแปลงจาก (15))
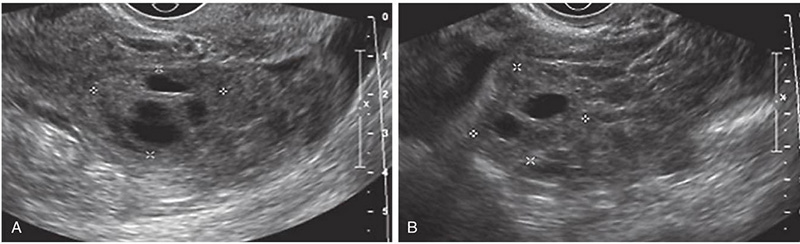
รูปที่ 4 แสดง Tubo-ovarian complex: Transverse (A) and sagittal (B) images demonstrating a complex adnexal mass. The ovary (calipers) is recognizable and is surrounded by complex inflammatory material suggesting tubo-ovarian complex (TOC) rather than tubo-ovarian abscess (TOA).
(ดัดแปลงจาก (15))
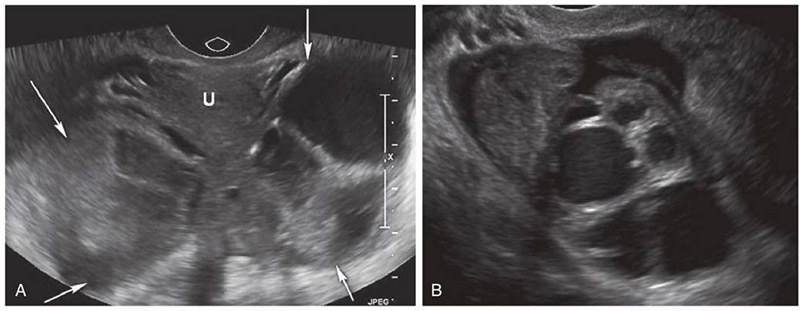
รูปที่ 5 แสดง Tubo-ovarian abscess (TOA): A: The uterus (U) with bilateral TOAs (arrows) demonstrating solid and complex cystic components with ill-defined borders. No normal-appearing ovary could be identified. B: The complex, multilocular adnexal mass with surrounding free fluid. The ovary and tube are not discretely recognizable.
(ดัดแปลงจาก (15))
การทำ Laparoscopy ในการช่วยวินิจฉัย PID ถือเป็น Invasive procedure โดยความไวในการวินิจฉัยของ Laparoscopy อาจไม่ได้สูงมากนัก เนื่องจากการส่องกล้องตรวจสอบภายในช่องท้องอาจไม่พบความผิดปกติในกรณีที่เป็น isolated endometritis หรือเป็น mild intratubal inflammation แต่การทำ Laparoscopy ก็มีความจำเพาะในการวินิจฉัยที่สูง (4)
การทำ Laparoscopy ในการช่วยวินิจฉัยอาจมีประโยชน์ในกรณีที่ Imaging ยังไม่สามารถให้ Definite diagnosis โดยเฉพาะในผู้ป่วยที่ไม่ตอบสนองต่อการรักษาด้วยยาทั้งแบบผู้ป่วยนอกและใน ซึ่งต้องการหาสาเหตุที่เป็นไปได้อย่างอื่นเพิ่มเติม (4)
ลักษณะความผิดปกติของ Acute salpingitis ที่พบได้จากการทำ Laparoscopic examination(13) คือ
การทำ Endometrial biopsy สามารถใช้ในการบอกถึง Endometritis ที่เกิดขึ้นร่วมกับ Salpingitis เพื่อเป็นการยืนยันการเกิด Upper genital tract infection โดยผลทางเซลล์วิทยาจะพบว่ามี Neutrophils and plasma cells in endometrium อย่างไรก็ตาม endometrial biopsy ไม่ได้เป็นที่นิยมทำ เนื่องจากผลมีความล่าช้า ซึ่งทำให้ไม่ได้มีส่วนในการตัดสินใจให้การรักษา และต้องอาศัยการทำหัตถการโดยแพทย์ที่ได้รับการฝึกมา (4, 12)
การรักษา PID ควรให้ยาฆ่าเชื้อที่เป็น Board spectrum เพื่อครอบคลุมเชื้อก่อโรคที่เป็นไปได้ และการให้ยาไม่ว่าสูตรใดก็ตาม ควรมียาที่ครอบคลุมเชื้อ N. gonorrhoeae and C. trachomatis นอกจากนี้เชื้อกลุ่ม anaerobes สามารถพบได้จากอวัยวะสืบพันธ์ส่วนบนของผู้ป่วย PID และมักพบ BV ร่วมด้วยในผู้ป่วยที่เป็น PID ดังนั้นจึงควรพิจารณาให้ยาฆ่าเชื้อที่คลุมกลุ่ม Anaerobes ร่วมด้วย การรักษา PID ควรเริ่มให้โดยเร็วหลังจากที่วินิจฉัย เนื่องจากการได้รับยาฆ่าเชื้อที่รวดเร็วจะช่วยป้องกันการเกิดภาวะแทรกซ้อนระยะยาวได้
การรักษา PID ที่ระดับรุนแรงน้อยถึงปานกลางสามารถให้การรักษาแบบผู้ป่วยนอกได้ CDC ได้มีการแนะนำ Criteria ในการพิจารณาให้การรักษาแบบผู้ป่วยใน ดังนี้
Parenteral treatment (1)
การให้ยาฆ่าเชื้อทางหลอดเลือด สามารถเปลี่ยนเป็นการรักษาโดยยาทานได้ โดยพิจารณาเปลี่ยนหลังจากที่อาการทางคลินิกดีขึ้น 24-48 ชั่วโมง สำหรับผู้ป่วยที่มี TOA แนะนำให้นอนโรงพยาบาลเพื่อสังเกตอาการนานกว่า 24 ชั่วโมง
| Recommended Parenteral Regimens for Pelvic Inflammatory Disease |
| Ceftriaxone 1 g IV every 24 hours PLUS Doxycycline 100 mg orally or IV every 12 hours PLUS Metronidazole 500 mg orally or IV every 12 hours |
| Cefotetan 2 g IV every 12 hours PLUS Doxycycline 100 mg orally or IV every 12 hours |
| Cefoxitin 2 g IV every 6 hours
PLUS Doxycycline 100 mg orally or IV every 12 hours |
สำหรับยา Doxycycline การให้ยาทางหลอดเลือดอาจส่งผลให้เกิดอาการเจ็บปวดบริเวณหลอดเลือดที่ให้ยา ดังนั้นหากเป็นไปได้จึงควรให้ยา Doxycycline แบบรับประทาน
ยา Doxycycline และ Metronidazole ทั้งรูปแบบฉีดและแบบรับประทานมี Bioavailability ที่ใกล้เคียงกัน
ยา Metronidazole รูปแบบรับประทานมีการดูดซึมยาที่ดี และสามารถใช้แทนรูปแบบฉีดได้ หากผู้ป่วยไม่ได้มีอาการที่รุนแรง หรือไม่มี TOA
หลังจากที่อาการผู้ป่วยดีขึ้น สามารถเปลี่ยนจากยาฉีดเข้าหลอดเลือดเป็นยารับประทานได้ โดยแนะนำให้เปลี่ยนเป็นยา Doxycycline 100 mg จำนวน 2 ครั้ง/วัน และ metronidazole 500 mg จำนวน 2 ครั้ง/วัน จนครบ 14 วัน
Alternative Parenteral Regimens (1)
| Alternative Parenteral Regimens |
| Ampicillin-sulbactam 3 g IV every 6 hours PLUS Doxycycline 100 mg orally or IV every 12 hours |
| Clindamycin 900 mg IV every 8 hours
PLUS Gentamicin loading dose IV or IM (2 mg/kg body weight), followed by a maintenance dose (1.5 mg/kg body weight) every 8 hours; single daily dosing (3–5 mg/kg body weight) can be substituted |
ในกรณีที่ใช้ clindamycin และ gentamicin ผู้ป่วยที่อาการดีขึ้นแล้วหลังได้รับยา 24-48 ชั่วโมง สามารถเปลี่ยนเป็นยารับประทานโดยใช้ clindamycin 450 mg รับประทาน 4 ครั้ง/วัน หรือ doxycycline 100 mg รับประทาน 2 ครั้ง/วัน ให้จนครบ 14 วัน
หากกรณีที่มี TOA ร่วมด้วย ควรใช้เป็น clindamycin 450 mg รับประทาน 4 ครั้ง/วัน หรือ metronidazole 500 mg รับประทาน 2 ครั้ง/วัน ร่วมกับ doxycycline รับประทาน จนครบ 14 วัน
Intramuscular or Oral Treatment (1)
การใช้ยาสูตรฉีดเข้ากล้ามเนื้อและยารับประทาน สามารถพิจารณาให้ได้ในผู้ป่วย acute PID ที่มีความรุนแรงน้อยถึงปานกลาง เนื่องจากผลลัพธ์ของการรักษาไม่แตกต่างจากการใช้ยาทางหลอดเลือดในผู้ป่วยกลุ่มนี้ ผู้ป่วยที่ไม่ตอบสนองต่อยาสูตรฉีดเข้ากล้ามเนื้อและยารับประทานภายใน 72 ชั่วโมง ควรได้รับการประเมินเพื่อยืนยันการวินิจฉัยอีกครั้ง และควรได้รับการให้ยาทางหลอดเลือดแทน
| Recommended Intramuscular or Oral Regimens for Pelvic Inflammatory Disease |
| Ceftriaxone 500 mg IM in a single dose* PLUS Doxycycline 100 mg orally 2 times/day for 14 days WITH Metronidazole 500 mg orally 2 times/day for 14 days |
| Cefoxitin 2 g IM in a single dose and Probenecid 1 g orally administered concurrently in a single dose PLUS Doxycycline 100 mg orally 2 times/day for 14 days WITH Metronidazole 500 mg orally 2 times/day for 14 days |
| Other parenteral third-generation cephalosporin (e.g., ceftizoxime or cefotaxime)
PLUS Doxycycline 100 mg orally 2 times/day for 14 days WITH Metronidazole 500 mg orally 2 times/day for 14 days *For persons weighing >150 kg (~300 lbs.) with documented gonococcal infection, 1 g of ceftriaxone should be administered. |
การให้ Metronidazole จะช่วยทำให้การรักษาครอบคลุมเชื้อกลุ่ม Anaerobic organisms มากขึ้น และครอบคลุมการรักษา BV ที่มักพบร่วมกับ PID
Alternative Intramuscular or Oral Regimens (1)
Follow-Up (1)
ผู้ป่วยควรมีอาการดีขึ้นภายใน 3 วันหลังจากเริ่มให้การรักษา เช่น ไข้ลดลง กดเจ็บหน้าท้องลดลง การกดเจ็บบริเวณปากมดลูก มดลูก และปีกมดลูกลดลง หากอาการไม่ดีขึ้นภายใน 72 ชั่วโมงหลังจากการรักษาแบบผู้ป่วยนอก หรือยาแบบรับประทาน ควรได้รับการรักษาในโรงพยาบาล และควรมีการประเมินความถูกต้องของการวินิจฉัยหรือการรักษาอีกครั้ง
สำหรับผู้ป่วยที่ได้รับการวินิจฉัยเป็น Chlamydial หรือ Gonococcal PID ควรได้รับการตรวจหาเชื้ออีกครั้งที่ 3 เดือนหลังการรักษา หากไม่สามารถตรวจซ้ำที่ 3 เดือนได้ ควรได้รับการตรวจซ้ำภายใน 12 เดือนหลังจากการรักษา
Sex partner (1)
ผู้ที่เคยมีเพศสัมพันธ์กับผู้ป่วยที่เป็น PID ในช่วง 60 วันก่อนมีอาการ ควรได้รับการตรวจและได้รับการรักษาที่ครอบคลุมเชื้อ Chlamydia และ Gonorrhea หากมีเพศสัมพันธ์ล่าสุดนานกว่า 6 สัปดาห์ก่อนมีอาการ ผู้ที่มีเพศสัมพันธ์ด้วยคนล่าสุดก็ควรได้รับการรักษา ผู้ป่วยและคู่นอนควรงดจากการมีเพศสัมพันธ์ในขณะรับการรักษาจนกระทั่งทั้งคู่ได้รับการรักษาจนครบและอาการกลับมาเป็นปกติ
Pregnancy (1, 16)
ในระหว่างการตั้งครรภ์มีโอกาสเกิด PID น้อยลงมาก เนื่องจาก mucus plug ที่ปากมดลูก จะช่วยป้องกันเชื้อโรคเข้าสู่โพรงมดลูกได้ อย่างไรก็ตามในช่วงอายุครรภ์ 12 สัปดาห์แรกก่อนที่จะเกิด Mucus plug ก็มีโอกาสเกิด PID ได้เช่นกัน หญิงตั้งครรภ์ที่เป็น PID จะเพิ่มความเสี่ยงต่อ Maternal morbidity และการคลอดก่อนกำหนด ผู้ป่วยที่ตั้งครรภ์ควรได้รับการรักษาโดยนอนโรงพยาบาล และให้ยาฆ่าเชื้อทางหลอดเลือด
HIV infection (1)
การศึกษาพบว่าอาการของโรค PID ในผู้ป่วยที่ติดเชื้อ HIV ไม่ได้แตกต่างจากผู้ป่วยปกติ และการตอบสนองต่อยาฆ่าเชื้อก็ไม่แตกต่างกัน แต่ในผู้ป่วย HIV อาจมีโอกาสพบ TOA ได้สูงขึ้น ดังนั้นการรักษา PID ในผู้ที่ติดเชื้อ HIV ก็สามารถให้การรักษาได้ตามปกติเหมือนผู้ป่วยทั่วไป
Intrauterine devices (1)
ความเสี่ยงของการติดเชื้ออุ้งเชิงกรานจากการใส่ IUD จะอยู่ในช่วง 3 สัปดาห์แรกหลังการใส่ หากเกิดการติดเชื้อในอุ้งเชิงกรานขึ้น ยังไม่จำเป็นต้องถอดห่วงออก ผู้ป่วยสามารถให้การรักษา PID ตามปกติ และควรได้รับการติดตามใกล้ชิด หากอาการไม่ดีขึ้นภายใน 48-72 ชั่วโมงหลังเริ่มการรักษา อาจพิจารณานำห่วง IUD ออก จากการศึกษาแบบ systematic review พบว่าผลการรักษา PID ระหว่างกลุ่มผู้ป่วยที่ใส่ห่วงไว้ และนำห่วงออกไม่ได้มีความแตกต่างกัน แต่อย่างไรก็ตามการศึกษายังไม่ได้มีข้อมูลผู้ป่วยที่ใช้ Levonorgestrel-releasing IUD
Long term sequelae (17)
ผู้ป่วยที่เป็นอุ้งเชิงกรานอักเสบแล้ว มีโอกาสเกิดผลที่ตามมาในระยะยาวได้ เช่น อุ้งเชิงกรานอักเสบกลับมาเป็นซ้ำ การมีบุตรยาก ภาวะตั้งครรภ์นอกมดลูก และปวดท้องน้อยเรื้อรัง
Chronic pelvic pain คืออาการปวดท้องน้อยที่มีระยะนานกว่า 6 เดือน ผู้ป่วยอุ้งเชิงกรานอักเสบประมาณหนึ่งในสาม อาจมีอาการปวดท้องน้อยเรื้อรังตามมาได้ โดยคาดว่าเกิดจากการที่มี adhesion หรือ scar ขึ้นภายหลังจากการที่มีการอักเสบติดเชื้อ อัตราการเกิด chronic pelvic pain จะยิ่งสูงขึ้นตามจำนวนครั้งที่เกิด PID
การเกิดอุ้งเชิงกรานอักเสบทั้งผู้ป่วยที่แสดงอาการและไม่แสดงอาการ สามารถส่งผลต่อทำให้เกิดภาวะมีบุตรยากได้ทั้งหมด โดยเมื่อเกิดการอักเสบขึ้นที่บริเวณท่อนำไข่จะทำให้เกิดการบาดเจ็บของเนื้อเยื่อบริเวณท่อนำไข่ขึ้น ส่งผลทำให้เกิดการเปลี่ยนแปลงตามหลังจากบาดเจ็บ เช่น การเสีย ciliary function ของ fallopian tube การเกิด fibrosis และเกิดการอุดตันของท่อนำไข่ตามมา ซึ่งทั้งหมดนี้ส่งผลต่อภาวะการมีบุตรยากได้ ปัจจัยเสี่ยงต่อการเกิดภาวะมีบุตรยาก ได้แก่
TOA หรือก้อนฝีหนองที่เกิดจากการติดเชื้อของท่อนำไข่และรังไข่ เป็นภาวะแทรกซ้อนอันตรายที่อาจเกิดตามหลัง PID ที่ไม่ได้รับการรักษา หรือรักษาล่าช้าได้ ผู้ป่วยที่เป็น TOA จะมีอัตราการเกิดทุพพลภาพ และการเสียชีวิตที่เพิ่มขึ้น โดยอัตราการเสียชีวิตอยู่ที่ประมาณ 5-10% (3)
ปัจจัยเสี่ยงของ TOA และ PID จะเหมือนกัน เช่น การมีคู่นอนหลายคน อายุช่วง 15-25 ปี หรือเคยมีประวัติเป็น PID มาก่อน เป็นต้น (18)
Clinical presentation
ลักษณะอาการของผู้ป่วยที่เป็น TOA จะมีลักษณะคล้ายกับ PID แต่จากการตรวจร่างกายอาจคลำพบก้อนบริเวณ Adnexa ได้ (9) ในผู้ป่วยที่มี sepsis อาจพบมี Tachycardia, increased respiratory rate หรือ Hypotension (3, 9) ในผู้ป่วย TOA ที่ก้อน intact ดีอาจไม่ได้มาด้วยลักษณะอาการแบบ severe sepsis (18) อาการไข้และถ่ายเหลวอาจพบได้มากขึ้นในผู้ป่วยที่มี TOA (3) ในกรณีที่มี Ruptured TOA ผู้ป่วยจะมีอาการปวดท้องเฉียบพลัน มี peritonitis และอาจมี signs ของ sepsis ร่วมด้วย (9, 18)
Diagnosis
การส่งตรวจทางห้องปฏิบัติการในรายที่มี TOA พบว่า WBC ในเลือดมักจะสูงขึ้น แต่บางรายอาจมี WBC ในระดับปกติได้ ผู้ป่วยที่มี TOA จะพบว่ามีระดับ Inflammatory marker ทั้ง ESR และ CRP ที่สูงขึ้นกว่าในผู้ป่วย PID โดย CRP เป็น marker ที่พบว่าเป็น predictor ที่ดีที่สุดของการเกิด TOA (18, 19)
ในผู้ป่วยที่มาด้วยลักษณะอาการของ PID ควรส่งตรวจ Imaging เพิ่มเติมในรายที่สงสัยว่าอาจมี TOA เช่นในผู้ป่วยที่มีลักษณะอาการดังต่อไปนี้ (18)
โดยควรส่งตรวจ Transvaginal ultrasound เป็นอย่างแรก เนื่องจากสามารถประเมิน Upper genital tract ได้ดี
Approach to treatment of TOA
ผู้ป่วยที่เป็น TOA ส่วนใหญ่สามารถรักษาโดยการให้ยาฆ่าเชื้อได้ โดยที่ไม่ต้องผ่าตัด การให้ยาฆ่าเชื้ออย่างเดียวจะให้ผลการรักษาที่ดีในผู้ป่วยที่มี Hemodynamically stable และไม่มี Signs of ruptured TOA, ก้อน Abscess ขนาดเส้นผ่านศูนย์กลาง < 7 cm และมีอาการทางคลินิกตอบสนองต่อการให้ยาฆ่าเชื้อ (20, 21)
TOA ในกลุ่มผู้ป่วยที่อยู่ในกลุ่ม Postmenopause จะมีอัตราการพบ Malignancy ร่วมด้วยสูงขึ้น โดยมีรายงานดังนี้
ดังนั้นในกลุ่ม Post menopause ควรมีการพิจารณาถึงการรักษาด้วยการผ่าตัดร่วมด้วย เนื่องจากมีโอกาสเป็น Malignancy ได้ ในกลุ่มผู้ป่วยที่สงสัย Malignancy ไม่มาก ควรต้องมีการติดตาม Imaging เป็นระยะหลังการรักษาเพื่อประเมินว่าตัวก้อนมี Complete resolution หรือไม่ หากยังพบ Mass อยู่ควรได้รับการผ่าตัด (20)
หลังจากได้รับยาฆ่าเชื้อทางหลอดเลือด 48-72 ชั่วโมง ในผู้ป่วยที่ไม่ตอบสนองต่อการรักษาด้วยยา หรือมีอาการแย่ลง ควรได้รับการรักษาด้วยการ Drainage หรือการผ่าตัด ผู้ป่วยที่ไม่ตอบสนองต่อการรักษาอาจมีลักษณะที่ช่วยสนับสนุน ดังต่อไปนี้ (20)
Drainage and surgical management
การรักษาโดยการระบายฝีหนอง (Drainage) หรือการผ่าตัด มีบทบาทในการรักษาในผู้ป่วยที่ไม่ตอบสนองต่อยาฆ่าเชื้อ หรือมีภาวะ Ruptured abscess และในกรณีที่สงสัย Malignancy ร่วมด้วย โดยเฉพาะในผู้ป่วย Postmenopause (8, 20)
Drainage
ในผู้ป่วยที่มี sepsis หรือมีขนาดของก้อน Abscess ที่ใหญ่มาก มักจำเป็นต้องได้รับการรักษาโดยการผ่าตัดแบบ Urgent surgery และควรได้รับยาฆ่าเชื้อ 48-72 ชั่วโมงก่อนที่จะทำการรักษาโดยการ Drainage หรือการผ่าตัด (8) การทำ Imaging-guided drainage อาจพิจารณาทำได้ในผู้ป่วยบางราย โดยพบว่ามีอัตราการทำสำเร็จประมาณ 70-100% ในผู้ป่วยที่สามารถระบายฝีหนองได้อย่างเหมาะสม (8)การทำ drainage อาจไม่เหมาะสม และไม่ประสบความสำเร็จในผู้ป่วยบางราย เช่น ผู้ป่วยที่มี Multiloculated collection หรือมีหลายก้อน หรือในกรณีที่มีปัญหาการเข้าถึงก้อนฝีหนอง เช่น การมีลำไส้ หรืออวัยวะในช่องท้องอื่นมาขวางกั้น เป็นต้น (8, 20) และการทำ Drainage จะใช้เวลาในการกำจัดการติดเชื้อที่นานกว่าการผ่าตัด (8)
ทางเลือกของการ Drainage คือการทำ Laparoscopic drainage ซึ่งสามารถเป็นทางเลือกเมื่อคิดว่าไม่สามารถทำ Percutaneous drainage ได้ ในอีกกรณีหนึ่งที่สามารถพิจารณาทำ Laparoscopic drainage คือการพบก้อนฝีหนองโดยบังเอิญในระหว่างการส่องกล้องเพื่อช่วยในการวินิจฉัย (20)
Surgical treatment
ในกรณีที่การรักษาด้วยการใช้ยาล้มเหลว และไม่สามารถทำ Percutaneous drainage ได้ อาจจำเป็นต้องใช้การผ่าตัด
เยื่อบุโพรงมดลูกเจริญผิดที่ คือ การมีเยื่อบุโพรงมดลูกอยู่ภายนอกมดลูก ซึ่งอาจแทรกตัวอยู่ในชั้นกล้ามเนื้อมดลูก หรือตำแหน่งอื่นๆ โดยอวัยวะในอุ้งเชิงกรานและเยื่อบุช่องท้องเป็นตำแหน่งที่พบได้บ่อย หรืออาจพบได้ในบริเวณอื่น เช่น เยื่อหุ้มหัวใจ เยื่อหุ้มปอด ปอด หรือสมอง
พบมากในหญิงวัยเจริญพันธุ์โดยความชุกอยู่ที่ประมาณร้อยละ 10 อย่างไรก็ตามสามารถพบได้ในหญิงอายุน้อยและวัยหมดประจำเดือนได้เช่นกัน โดยภาวะเยื่อบุโพรงมดลูกเจริญผิดที่มักสัมพันธ์กับอาการปวดตามตำแหน่งต่างๆที่มีโรค และสัมพันธ์กับภาวะมีบุตรยาก(1)
ภาวะเยื่อบุโพรงมดลูกเจริญผิดที่ส่งผลอย่างมากต่อผู้ป่วย ทั้งด้านอาการที่อาจกระทบต่อการทำงาน คุณภาพชีวิต เศรษฐานะ ครอบครัว จิตใจ และอารมณ์ของผู้ป่วย(2)
| ปัจจัยเสี่ยง | ปัจจัยป้องกัน |
|
|
ภาวะเยื่อบุโพรงมดลูกเจริญผิดที่สัมพันธ์กับฮอร์โมนเอสโตรเจน โดยมีทฤษฎีที่เชื่อว่าเป็นกลไกในการเกิดโรคอยู่ 3 ทฤษฎี คือ
ในปัจจุบันไม่สามารถอธิบายการเกิดโรคได้ในทฤษฎีเดียว
มีการศึกษาแบบ systematic review และ meta-analysis ของ Kvaskoff และคณะ ในปี ค.ศ.2020 พบว่าภาวะเยื่อบุโพรงมดลูกเจริญผิดที่มีโอกาสพัฒนาเป็นมะเร็งน้อย โดยค่าความเสี่ยงสัมพัทธ์อยู่ที่ 1.02 ซึ่งอาจสัมพันธ์กับมะเร็งรังไข่ชนิด clear-cell และ endometrioid cell มะเร็งเต้านม มะเร็งต่อมไทรอยด์(6)
การวินิจฉัยตาม 2022 ESHRE Endometriosis guideline(2) กล่าวว่า การส่องกล้องทางหน้าท้องไม่ถือว่าเป็น Gold standard อีกต่อไป แนะนำให้วินิจฉัยตามลักษณะทางคลินิกเป็นหลัก
โดยผู้ป่วยภาวะเยื่อบุโพรงมดลูกเจริญผิดที่ มักจะมีอาการปวดท้องประจำเดือน มีบุตรยาก ปวดขณะมีเพศสัมพันธ์แบบลึก ปัสสาวะแสบขัด ปวดทวารหนัก ปัสสาวะเป็นเลือด อุจจาระเป็นเลือด ปวดหัวไหล่ ซึ่งอาจสัมพันธ์หรือไม่สัมพันธ์กับรอบเดือนก็ได้
นอกจากนั้น ขณะมีประจำเดือนอาจพบภาวะลมรั่วในเยื่อหุ้มปอด ไอเป็นเลือด เจ็บหน้าอก รอบแผลเป็นมีอาการปวดและบวม อ่อนเพลีย อาการที่พบขึ้นอยู่กับตำแหน่งของรอยโรค(1, 2)
การตรวจร่างกาย
ตรวจร่างกายบริเวณอุ้งเชิงกราน และช่องท้อง แนะนำให้ใช้ speculum เพื่อดูบริเวณช่องคลอด ตรวจอุ้งเชิงกรานและช่องท้องโดยการดูและคลำ ตรวจทางทวารหนัก และตรวจร่างกายบริเวณอื่นที่สงสัยว่ามีรอยโรคตามความเหมาะสม(7, 8)
โดยอาจตรวจพบรอยขรุขระหรือรอยนูนบริเวณ uterosacral ligament หรือบริเวณ cul-de-sac อาจพบว่าตำแหน่งปากมดลูกเอียงไปด้านหนึ่ง สามารถตรวจพบถุงน้ำรังไข่ได้ หรืออาจมี rectovaginal septum บวมและเจ็บ(1, 9)
การสืบค้นเพิ่มเติม
แนะนำให้สืบค้นทางรังสีเพิ่มเติมในผู้ป่วยที่สงสัยภาวะเยื่อบุโพรงมดลูกเจริญผิดที่ทุกรายแม้ว่าการตรวจร่างกายพบว่าปกติ(2, 10)
พึงระวังว่าการสืบค้นด้วยภาพพบว่าผลปกติ ก็ยังคงสามารถนึกถึงภาวะเยื่อบุโพรงมดลูกเจริญผิดที่ได้
พึงระวังว่า แม้ไม่พบรอยโรคจากการผ่าตัดส่องกล้องหรือจากผลพยาธิวิทยา ก็ยังสามารถนึกถึงภาวะเยื่อบุโพรงมดลูกเจริญผิดที่ได้(2)
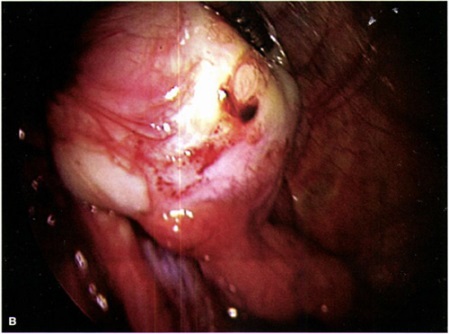
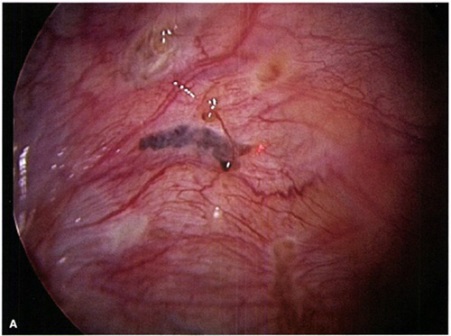
รูปที่ 1 ภาพแสดงตัวอย่างรอยโรคเยื่อบุโพรงมดลูกเจริญผิดที่จากการผ่าตัดส่องกล้อง
ที่มา: คัดลอกจาก Barek&Novak’s Gynecology: Endometriosis. 16th edition
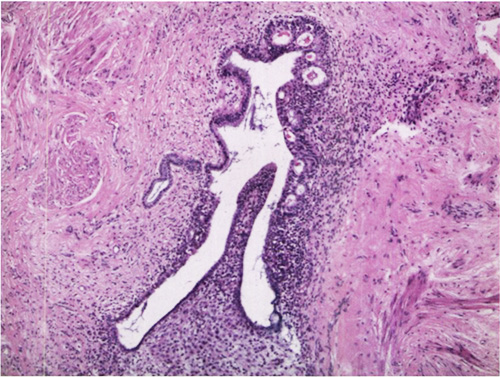
รูปที่ 2 ภาพแสดงลักษณะทางพยาธิวิทยาของโรคเยื่อบุโพรงมดลูกเจริญผิดที่
ที่มา: คัดลอกจาก Barek&Novak’s Gynecology: Endometriosis. 16th edition
มีหลายระบบที่ใช้สำหรับการแบ่งระยะ โดยแต่ระบบมีความเหมาะสมในการใช้ที่แตกต่างกัน เช่น
ควรพิจารณาแนวทางการรักษาแบบเฉพาะบุคคล โดยคำนึงถึงปัญหาหลัก คุณภาพชีวิตของผู้ป่วยแต่ละรายรวมถึงผลข้างเคียงของการรักษาและทรัพยากรที่มีอยู่(1)
การรักษามีทั้งแบบการรักษาด้วยยา และการผ่าตัด โดยในที่นี้จะกล่าวถึงการรักษาด้วยยา
สามารถใช้ยาแก้ปวดในกลุ่ม non-steroidal anti-inflammatory drugs (NSAIDs), paracetamol,
neuromodulators เช่น anti-depressants, selective serotonin uptake inhibitors, anticonvulsants โดยสามารถใช้ยาแก้ปวดอย่างเดียวหรือใช้ร่วมกับการรักษาประเภทอื่นก็ได้ โดยยาแต่ละชนิดยังไม่มีหลักฐานที่ชัดเจนในการรักษาอาการปวด(18, 19)
โดยฮอร์โมนกดการทำงานของรังไข่ กดการสร้างและทำงานของเอสโตรเจน ทำให้เยื่อบุโพรงมดลูกฝ่อ(1, 2)
ทำให้เยื่อบุโพรงมดลูกฝ่อลง สามารถลดอาการปวดจากเยื่อบุโพรงมดลูกเจริญผิดที่ได้(25)
Medroxyprogesterone acetate (MPA) ช่วยลดอาการปวดและระยะของเยื่อบุโพรง
มดลูกเจริญผิดที่ โดยสามารถลดอาการปวดได้ดีเท่ากับ GnRH agonist แต่มีผลต่อมวลกระดูกและเกิดภาวะเอสโตรเจนต่ำได้น้อยกว่า(26) แบบรับประทานขนาด MPA 10-30 มก. ต่อวัน ส่วนแบบฉีดขนาด DMPA 150 มก. ฉีดทุก 1 หรือ 3 เดือน(11) ไม่ควรใช้ในผู้ป่วยมีบุตรยากเนื่องจากสามารถทำให้เกิดภาวะไม่ตกไข่และขาดประจำเดือนที่พยากรณ์ระยะเวลาการกลับมาปกติได้ยากหลังจากหยุดยา
Dienogest สามารถลดอาการปวดได้เทียบเท่ากับ GnRH agonist แต่ผลต่อมวลกระดูก และอาการจากเอสโตรเจนต่ำน้อยกว่า(27) ขนาดที่แนะนำคือ รับประทาน 2 มก. ต่อวัน(11)
Megestrol acetate 40 มก. ต่อวัน, Dydrogesterone 20-30 มก. ต่อวัน, Lynestrenol
10มก. ต่อวัน สามารถลดอาการปวดได้เช่นกัน(28, 29)
ห่วงคุมกำเนิดในโพรงมดลูกโปรเจสเตอโรน (LNG-IUS) สามารถลดอาการปวดและเพิ่มคุณภาพชีวิตได้เทียบเท่ากับ GnRH agonist(29) ส่วนยาคุมกำเนิดแบบฝังโปรเจสเตอโรน (subdermal implantation) สามารถลดอาการปวด(30)
Danazol ทำให้เกิดภาวะแอนโดรเจนสูง และเอสโตรเจนต่ำ จึงมีผลข้างเคียงค่อนข้างมาก
ดังนั้นในปัจจุบันจึงไม่แนะนำให้ใช้ในการรักษาภาวะเยื่อบุโพรงมดลูกเจริญผิดที่ (2)
ใช้เป็น 2nd line ในการรักษาอาการปวดจากภาวะเยื่อบุโพรงมดลูกเจริญผิดที่ ขนาดและระยะเวลาในการรักษายังไม่แน่ชัด วิธีการใช้แบบฉีดใต้ผิวหนัง ฉีดเข้ากล้ามเนื้อ และการพ่นทางจมูกมีประสิทธิภาพไม่ต่างกัน (31)
มีการศึกษาพบว่าหลังจากใช้ GnRH agonist นานหกเดือน พบว่าร้อยละ 6-8 มีมวลกระดูกลดลง(32) ดังนั้นควรมี add-back therapy ควบคู่กัน โดยสามารถใช้ tibolone เอสโตรเจน หรือโปรเจสโตเจนก็ได้
ไม่แนะนำให้ยาฮอร์โมนก่อนการผ่าตัด แต่หลังการผ่าตัดสามารถพิจารณาให้ยาฮอร์โมนเพื่อเพิ่มประสิทธิภาพในการลดอาการปวดในผู้ป่วยที่ยังไม่ต้องการตั้งครรภ์
ยังไม่มีคำแนะนำสำหรับการใช้วิธีฝังเข็ม กายภาพบำบัด การนวด แพทย์แผนจีน การออกกำลังกาย การใช้ไฟฟ้าในการรักษา จิตบำบัด การควบคุมรับประทานอาหารบางชนิด ในการลดปวดเนื่องจากยังมีข้อมูลไม่เพียงพอ
ไม่แนะนำให้ยาฮอร์โมนหลังการผ่าตัดในผู้ป่วยที่ต้องการมีบุตรเพื่อเพิ่มโอกาสการตั้งครรภ์ แต่อาจ
พิจารณาให้ยาฮอร์โมนหลังการผ่าตัดในผู้ป่วยที่ยังไม่ต้องการตั้งครรภ์ในช่วงเวลาอันใกล้
ยังไม่มีคำแนะนำเนื่องจากยังมีข้อมูลไม่เพียงพอ
และระดับ AMH ต่ำ รวมถึงการผ่าตัดรักษาอาจทำให้ ovarian reserve ลดลงได้ อย่างไรก็ตามมีการศึกษาว่าการทำ fertility preservation ไม่ได้มีประโยชน์มากนัก(36) ดังนั้นจึงควรพิจารณาการทำร่วมกับผู้ป่วย(2)
คือ การพบรอยโรคเยื่อบุโพรงมดลูกเจริญผิดที่จากการสืบค้นด้วยภาพหรือการผ่าตัดซ้ำหลังจากที่เคยรักษา
ด้วยการผ่าตัดออกหมด(2) หรืออาจหมายถึงผู้ป่วยที่กลับมามีอาการซ้ำหลังจากหยุดยาเนื่องจากไม่มีอาการนาน 6-24 เดือน(1) โดยโอกาสการกลับมาเป็นซ้ำอยู่ที่ร้อยละ 2-20
ควรซักประวัติอย่างละเอียดเพื่อช่วยในการรักษา โดยวัยรุ่นที่มีภาวะเยื่อบุโพรงมดลูกเจริญผิดที่มักมาด้วย
อาการปวดท้องประจำเดือน ปวดท้องน้อยเรื้อรัง(37) หรืออาการอื่นที่เกี่ยวข้องลักษณะเดียวกับผู้ใหญ่ อาจมีประวัติปัจจัยเสี่ยง หรืออาการไม่ตรงไปตรงมา เช่น ขาดเรียนช่วงมีรอบเดือนจากอาการปวด(38)
การตรวจร่างกาย ควรพิจารณาร่วมกับผู้ป่วยและผู้ปกครองในการตรวจภายในและการตรวจทางทวารหนัก
การสืบค้นเพิ่มเติม ยังคงแนะนำการสืบค้นด้วยภาพจากคลื่นเสียงความถี่สูง(ultrasonography) โดยแนะนำเป็นการตรวจทางช่องคลอดเช่นเดียวกับผู้ใหญ่ แต่หากพิจารณาแล้วไม่เหมาะสมอาจทำเป็นการตรวจทางหน้าท้อง ทางทวารหนัก หรือการตรวจด้วยคลื่นแม่เหล็กไฟฟ้าความถี่สูง(MRI)
การผ่าตัดส่องกล้องเพื่อวินิจฉัย(Diagnostic laparoscopy) มีแนวทางการปฏิบัติเช่นเดียวกับผู้ใหญ่
ตามปกติภาวะเยื่อบุโพรงมดลูกเจริญผิดที่มักหายหลังจากวัยหมดประจำเดือน อย่างไรก็ตามสามารถพบได้ประมาณร้อยละ 2-5(42) โดยอาจสัมพันธ์กับการใช้ฮอร์โมนทดแทนหลังวัยหมดประจำเดือนหรือไม่ก็ได้
ไม่แนะนำให้รักษาทั้งยาและการผ่าตัด เนื่องจากโอกาสการดำเนินโรคจนเกิดอาการมีน้อย(45) โดยแนะนำให้ติดตามโดยการตรวจภาพจากคลื่นเสียงความถี่สูง(ultrasonography) เป็นระยะ(2)
ไม่มีคำแนะนำสำหรับการป้องกันภาวะเยื่อบุโพรงมดลูกเจริญผิดที่ ระดับปฐมภูมิที่มีหลักฐานเพียงพอในปัจจุบัน(2)
พญ.คันธารัตน์ หลวงฟอง
ที่ปรึกษา ผศ.นพ.มนัสวี มะโนปัญญา
การตั้งครรภ์นอกมดลูก หมายถึง การตั้งครรภ์ที่เกิดขึ้นภายนอกโพรงมดลูก(1) มีอุบัติการณ์ประมาณร้อยละ 1-2 ของการตั้งครรภ์(2, 3) โดยภาวะ ruptured ectopic pregnancy นำไปสู่การเสียชีวิตได้มากถึงร้อยละ 2.7(4) ดังนั้นการตั้งครรภ์นอกมดลูกจึงเป็นภาวะสำคัญและฉุกเฉินทางสูตินรีเวชกรรม(1)
ประเภทของการตั้งครรภ์นอกมดลูกแบ่งตามตำแหน่งการฝังตัว ดังนี้ คือ ตั้งครรภ์ที่ท่อนำไข่บริเวณ ampullar (มากกว่าร้อยละ 70) บริเวณ isthmus (ร้อยละ 12) และบริเวณ fimbria (ร้อยละ 11) รังไข่ (ร้อยละ 3) Cornue (ร้อยละ 2-3) ในช่องท้อง (ร้อยละ 1) ปากมดลูก (น้อยกว่าร้อยละ 1) Cesarean scar (น้อยกว่าร้อยละ 1)(5) ดังแสดงในรูปที่ 1
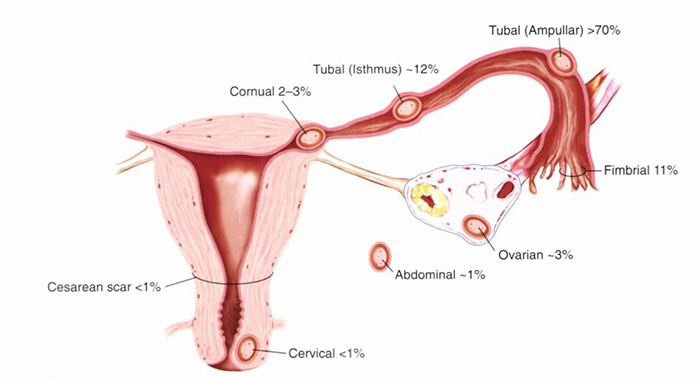
รูปที่ 1 แสดงตำแหน่งที่พบบ่อยของครรภ์นอกมดลูก
ที่มา: คัดลอกจาก Jonathan S. Berek, Deborah L. Berek. Berek & Novak’s Gynecology: Ectopic pregnancy. 16th ed: Wolters Kluwer; 2020.
โดยการตั้งครรภ์อาจจะดำเนินไปได้หลายรูปแบบ คือ ท่อนำไข่แตก ฝ่อไปเอง หรือแท้งออกไปทาง fimbria (tubal abortion) แต่มีบางรายที่แท้งแล้วแต่รกยังทำงานอยู่และไปฝังตัวต่อที่อื่น(6)
ปัจจัยส่งเสริมการตั้งครรภ์นอกมดลูก
การตั้งครรภ์นอกมดลูกไม่มีอาการจำเพาะ แต่มีอาการหลายๆ อย่างร่วมกัน กลุ่มอาการทางคลินิกที่พบร่วมได้บ่อย (Classic triad) คือ การขาดระดู มีอาการปวดท้องน้อย และมีเลือดออกผิดปกติทางช่องคลอด ซึ่งสามารถพบได้ประมาณร้อยละ 50 ของผู้ป่วย(12) ดังนั้นสตรีวัยเจริญพันธุ์ที่มีอาการปวดท้องหรือเลือดออกผิดปกติทางช่องคลอดควรได้รับการทดสอบการตั้งครรภ์ทุกรายแม้ว่าจะคุมกำเนิดอยู่(13, 14) นอกจากนี้อาจมีอาการอื่นที่ไม่เฉพาะเจาะจง เช่น อาการหน้ามืดเป็นลม ปวดหลัง ปวดไหล่ อาการทางระบบทางเดินอาหาร โดยมีอาการแสดง ได้แก่ สัญญาณชีพผิดปกติ หากมีเลือดออกมากจะพบชีพจรเต้นเบาเร็วและความดันโลหิตต่ำ อาการกดเจ็บบริเวณหน้าท้องและในรายที่ครรภ์นอกมดลูกแตกแล้วหรือแท้งออกมาอาจมีอาการแสดงของ peritoneal irritation เสียงการเคลื่อนไหวของลำไส้ลดลงหรือหายไป เมื่อตรวจภายในจะพบว่า โดยส่วนใหญ่มดลูกจะมีขนาดปกติแต่บางรายอาจโตเล็กน้อย เจ็บเมื่อโยกปากมดลูก คลำได้ก้อนบริเวณปีกมดลูกและกดเจ็บ (12, 15)
การตรวจด้วยคลื่นเสียงความถี่สูงทางช่องคลอด (transvaginal ultrasonography: TVS)
ถือเป็นทางเลือกแรกในการตรวจเพื่อช่วยวินิจฉัย(16, 17) โดยสามารถให้การวินิจฉัยได้ทันทีเมื่อเห็นถุงการตั้งครรภ์ร่วมกับ yolk sac หรือเห็นตัวอ่อน (embryonic pole) บริเวณปีกมดลูก แต่โดยส่วนมากแล้วมักเห็นเพียงก้อนที่ปีกมดลูก (complex adnexal mass) แต่อย่างไรก็ตามควรวินิจฉัยแยกกับโรคอื่น เช่น paratubal cyst, corpus luteal cyst, hydrosalpinx, endometrioma, ovarian neoplasm หรือ pedunculated fibroid(18, 19) และการเห็นถุงการตั้งครรภ์ในโพรงมดลูกร่วมด้วยอาจจะไม่สามารถสรุปได้ว่าเป็นการตั้งครรภ์ในมดลูกได้ เนื่องจากอาจจะเป็น pseudogestational sac ซึ่งไม่ใช่ถุงการตั้งครรภ์จริง(20)
การตรวจด้วยคลื่นเสียงความถี่สูงทางหน้าท้อง (transabdominal ultrasonography)
ใช้ในการช่วยประเมินปริมาณเลือดที่ออกในช่องท้อง (hemoperitoneum) ได้(12)
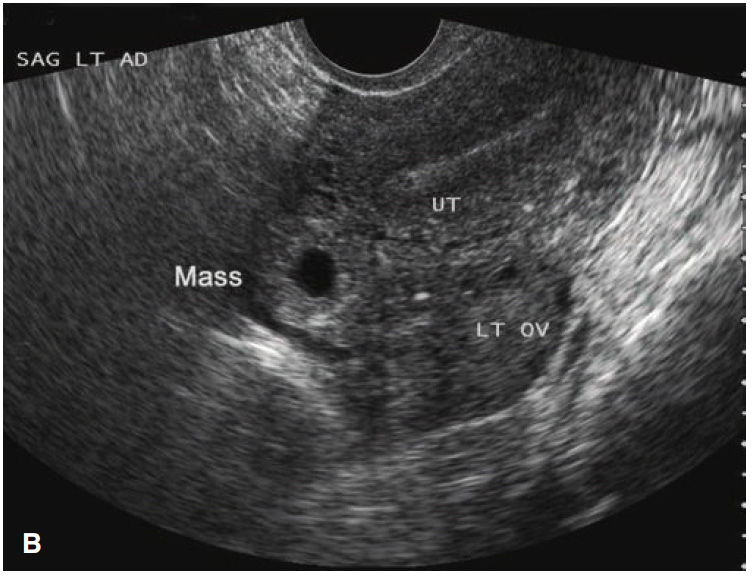
รูปที่ 2 ภาพการตรวจด้วยคลื่นเสียงความถี่สูงแสดงก้อนที่ปีกมดลูกที่เกิดจากการตั้งครรภ์นอกมดลูกบริเวณท่อนำไข่
ที่มา: คัดลอกจาก William Obstetrics: Ectopic pregnancy. 26th edition
หากไม่พบหลักฐานการตั้งครรภ์ทั้งในและนอกโพรงมดลูกจากการตรวจด้วยคลื่นเสียงความถี่สูงจะเรียกภาวะนี้ว่า “Pregnancy of Unknown Location”(6) ซึ่งอาจจะเกิดจากภาวะใดภาวะหนึ่งดังต่อไปนี้ การตั้งครรภ์ในโพรงมดลูกแต่ตัวอ่อนไม่สามารถเจริญต่อได้ (failed IUP) แท้งครบ การตั้งครรภ์ในโพรงมดลูกแต่อายุครรภ์ยังน้อย หรือการตั้งครรภ์นอกมดลูก
ช่วยในการวินิจฉัยการตั้งครรภ์นอกมดลูกร่วมกับประวัติ อาการ และการตรวจด้วยคลื่นเสียงความถี่สูง(21) มักใช้เมื่อไม่สามารถวินิจฉัยการตั้งครรภ์นอกมดลูกได้จากการตรวจด้วยคลื่นเสียงความถี่สูง(12)
อย่างไรก็ตามเกณฑ์การตรวจวัดระดับ serum hCG ดังกล่าวยังมีความแตกต่างกันขึ้นอยู่กับข้อมูลจากการศึกษาที่แนวเวชปฏิบัตินั้นๆ อ้างอิง ดังแสดงในตารางที่ 1
ตารางที่1 แสดงเกณฑ์การวัดระดับ serum hCG เพื่อประกอบการวินิจฉัยการตั้งครรภ์นอกมดลูก
| เกณฑ์ระดับ serum hCG | Novak 16thedition (12, 23) |
William 26thedition (6, 21, 24, 25) |
ACOG 2018 (1, 23, 25) |
NICE 2019(15) |
| Discriminatory zone | ≥3,510 | Vary
> 3510 ≥ 1500 ≥ 2000 |
≥3,500 | ≥1,500 |
| B-hCG rising value
ใน 48 ชั่วโมง |
ขึ้นอยู่กับระดับตั้งต้น
49% (< 1,500) 40% (1,500-3,000) 33% หรือ 35-53% (>3,000) |
35-53% | ขึ้นอยู่กับระดับตั้งต้น
49% (<1,500) 40% (1,500-3,000) 33% (>3,000) |
63% |
| B-hCG decreasing value | 35-50% ใน 48 ชั่วโมง
87% ใน 7 วัน |
ระดับตั้งต้น 250-5,000
35-50% ใน 48 ชั่วโมง 66-87% ใน 7 วัน |
21–35%
ใน 48 ชั่วโมง |
> 50%
ใน 48 ชั่วโมง |
มักจะเจาะตรวจในกรณีที่ระดับ serum hCG และผลการตรวจด้วยคลื่นเสียงความถี่สูงไม่สามารถสรุปการวินิจฉัยได้(27) ในการตั้งครรภ์ปกติ (viable intrauterine pregnancy) ระดับ serum progesterone จะสูงกว่า 25 ng/mL (26) แต่ถ้าระดับต่ำกว่า 5 ng/mL จะเป็นการตั้งครรภ์ที่ผิดปกติ อย่างไรก็ตามการตั้งครรภ์นอกมดลูกส่วนใหญ่จะมีระดับ serum progesterone อยู่ระหว่าง 5-25 ng/mL ทำให้ มีคุณค่าทางคลินิกน้อย
เลือกทำในรายที่ยืนยันแล้วว่าเป็นการตั้งครรภ์ที่ผิดปกติ แต่ไม่ทราบว่าเป็นการตั้งครรภ์ในหรือนอกมดลูกจากการตรวจด้วยคลื่นเสียงความถี่สูงทางช่องคลอด โดยการนำชิ้นเนื้อที่ได้จากการเก็บตัวอย่างจากโพรงมดลูกมาตรวจดูว่ามี chorionic villi หรือไม่ด้วยการส่งตรวจทางพยาธิวิทยาหรือการนำมาลอยในน้ำเกลือแล้วเห็นลักษณะเป็น frond-like appearance (27) หากยังไม่สามารถยืนยันได้แนะนำให้ตรวจติดดูระดับ serum hCG ถ้าเป็นการตั้งครรภ์ในมดลูกหลังจากการขูดมดลูกแล้วค่าจะลดลงมากกว่าร้อยละ 50 ภายใน 24 ชั่วโมง(28)
เป็นการเจาะบริเวณ cul-de-sac ผ่านทางช่องคลอด ใช้วินิจฉัยภาวะเลือดออกในช่องท้อง แต่ไม่สามารถบอกได้ว่าเลือดมาจากไหน ทำให้ปัจจุบันการทำ culdocentesis มีบทบาทน้อย(29)
ช่วยในการวินิจฉัยครรภ์นอกมดลูกได้แต่เป็นหัตถการที่ค่อนข้างลุกล้ำ และอาจวินิจฉัยผิดพลาดได้ร้อยละ 3-4 ในผู้ป่วยที่มีถุงการตั้งครรภ์มีขนาดเล็กมาก มีพังผืดในอุ้งเชิงกรานมาก หรือมีท่อนำไข่ผิดปกติอยู่เดิม
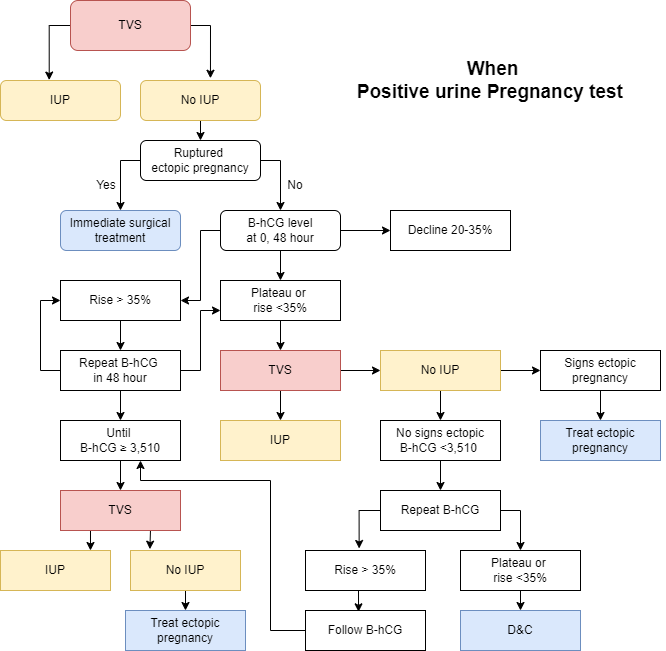
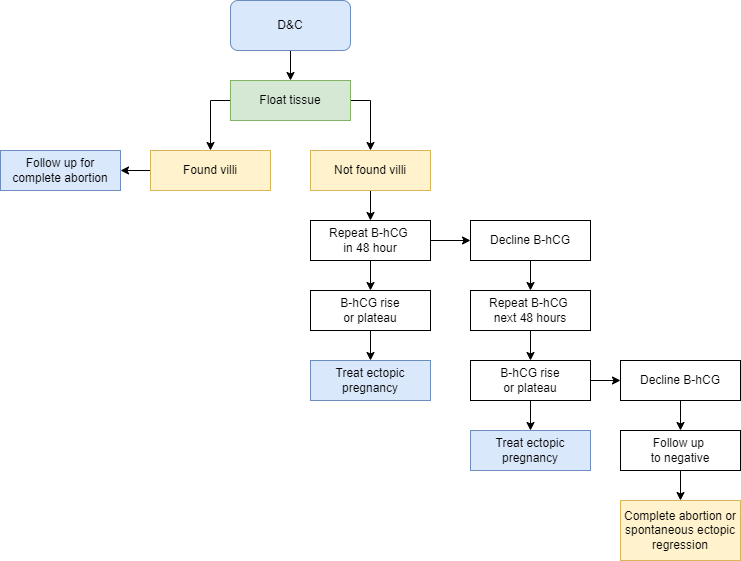
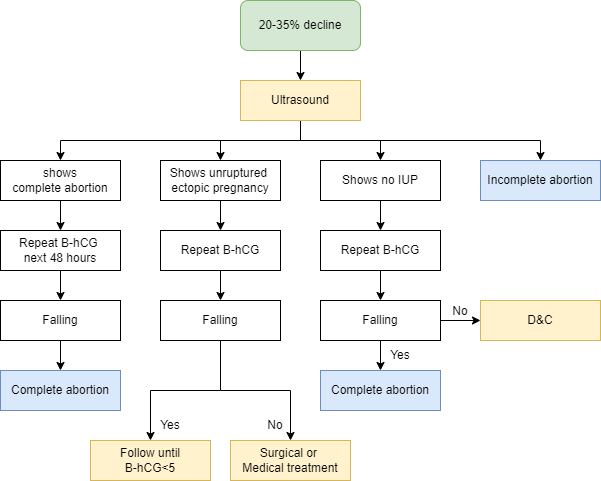
รูปที่ 3 แนวทางการวินิจฉัยการตั้งครรภ์นอกมดลูกในกรณีที่ไม่ใช้การส่องกล้องตรวจในอุ้งเชิงกราน(12)
ที่มา: ดัดแปลงจาก Jonathan S. Berek, Deborah L. Berek. Berek & Novak’s Gynecology: Ectopic pregnancy. 16th ed: Wolters Kluwer; 2020
วิธีการรักษามีอยู่ 3 แนวทางหลัก ได้แก่ การรักษาด้วยยา การรักษาด้วยการผ่าตัด หรือการเฝ้าสังเกต โดยการเลือกวิธีการรักษาให้พิจารณาจากลักษณะทางคลินิก ตำแหน่งของครรภ์นอกมดลูก และทรัพยากรที่มีอยู่เพื่อให้เหมาะสมกับผู้ป่วยแต่ละราย (1, 6, 12)
(1, 6, 12)
ยาที่ใช้ในการรักษาครรภ์นอกมดลูก คือ methotrexate เป็นยากลุ่ม folic acid antagonist ออกฤทธิ์โดยการขัดขวางการสร้าง DNA และ RNA โดยการยับยั้งเอนไซม์ dihydrofolate reductase (6) โอกาสประสบความสำเร็จในการรักษาสูงถึงร้อยละ 78-96(30) ทั้งนี้ยาอาจทำให้เกิดผลข้างเคียงดังนี้ การอักเสบของเยื่อบุทางเดินอาหาร เลือดออกกะปริบกะปรอยทางช่องคลอด(1, 12) ภาวะตับอักเสบ(30), ผมร่วง หรือเยื่อหุ้มปอดอักเสบ(31) ทั้งนี้ความรุนแรงของผลข้างเคียงขึ้นอยู่กับขนาดยาและระยะเวลาที่ให้ยา ก่อนที่จะเริ่มให้ยาควรพิจารณาถึงข้อห้ามและข้อควรระวังดังนี้
โดยการบริหารยามีทั้งหมด 3 วิธี คือ
ตารางที่ 2 การบริหารยา methotrexate แบบ single dose regimen
|
– หากลดลงมากกว่าร้อยละ 15, ตรวจติดตามระดับ hCG ทุกสัปดาห์จนกว่าจะอยู่ในระดับปกติ |
| – หากลดลงน้อยกว่าร้อยละ 15 ให้ methotrexate 50 มก./ตารางเมตรพื้นที่ผิวของร่างกายซ้ำ ทางกล้ามเนื้อ และตรวจติดตามระดับ hCG |
| – หากให้ methotrexate สองครั้งแล้วระดับ hCG ไม่ลดลง พิจารณารักษาโดยการผ่าตัด |
|
ตารางที่ 3 การบริหารยา methotrexate แบบ multidose regimen
|
|
| – หยุดให้ methotrexate หากลดลงมากกว่าร้อยละ 15 แล้วตรวจติดตามระดับ hCG ทุกสัปดาห์จนกว่าจะอยู่ในระดับปกติ |
| – หากให้ methotrexate สี่ครั้งแล้วระดับ hCG ไม่ลดลง พิจารณารักษาโดยการผ่าตัด |
|
ตารางที่ 4 การบริหารยา methotrexate แบบ two-dose regimen
|
|
|
| – หากลดลงมากกว่าร้อยละ 15, ตรวจติดตามระดับ hCG ทุกสัปดาห์จนกว่าจะอยู่ในระดับปกติ |
| – หากลดลงน้อยกว่า 15 ให้ methotrexate 50 มก./ตารางเมตรพื้นที่ผิวของร่างกายซ้ำ ทางกล้ามเนื้อ ในวันที่ 7 แล้วตรวจติดตามระดับ hCG ในวันที่ 11 |
| – หากระดับ hCG ระหว่างวันที่ 7 และ 11 ลดลงมากกว่าร้อยละ 15 ให้ตรวจติดตามระดับ hCG ทุกสัปดาห์จนกว่าจะอยู่ในระดับปกติ
– หากระดับ hCG ระหว่างวันที่ 7 และ 11 ลดลงน้อยกว่าร้อยละ 15 ให้ methotrexate 50 มก./ตารางเมตรพื้นที่ผิวของร่างกายซ้ำ ทางกล้ามเนื้อ ในวันที่ 11 แล้วตรวจติดตามระดับ hCG ในวันที่ 14 |
| – หากให้ methotrexate สี่ครั้งแล้วระดับ hCG ไม่ลดลง พิจารณารักษาโดยการผ่าตัด |
|
ข้อบ่งชี้ในการผ่าตัดในการรักษา คือ สัญญาณชีพผิดปกติ มีข้อบ่งห้ามต่อการรักษาด้วยยา หรือมีโอกาสที่ไม่ประสบความสำเร็จจากการรักษาด้วยยาสูง (1, 6, 12) โดยแนวทางการรักษาขึ้นอยู่กับลักษณะทางคลินิก อุปกรณ์ทางการแพทย์ที่มีและประสบการณ์ของแพทย์ผู้ผ่าตัด
การผ่าตัดผ่านกล้องมีข้อดีคือ แผลขนาดเล็ก ฟื้นตัวเร็ว และมีต้นทุนประสิทธิผลที่ดีกว่าเมื่อเทียบกับการผ่าตัดเปิดหน้าท้อง(34) อย่างไรก็ตามแนะนำให้ทำการผ่าตัดแบบเปิดหน้าท้องในกรณีต่อไปนี้ ผู้ป่วยมีภาวะช็อกจากการสูญเสียเลือดและต้องการผ่าตัดอย่างรวดเร็ว เป็นครรภ์นอกมดลูกชนิด abdominal pregnancy มีพังผืดในช่องท้องมาก หรือคาดว่าจะทำการผ่าตัดผ่านกล้องได้ยาก(12)
การผ่าตัดเชิงอนุรักษ์ (salpingostomy) พิจารณาทำในกรณีที่ท่อนำไข่ข้างที่มีการตั้งครรภ์นอกมดลูกยังไม่แตกหรือมีลักษณะปกติ หรือท่อนำไข่ด้านตรงข้ามผิดปกติหรือถูกเคยถูกตัดแต่ผู้ป่วยยังต้องการธำรงค์ภาวะการเจริญพันธุ์(12) การรักษาด้วยการผ่าตัดเชิงอนุรักษ์มีโอกาสเกิด persistent ectopic pregnancy ได้ประมาณร้อยละ 8 พบได้บ่อยถ้าระดับ serum hCG ตั้งต้นสูง อายุครรภ์น้อย และขนาดก้อนการตั้งครรภ์นอกมดลูกน้อยกว่า 2 เซนติเมตร ดังนั้นจึงควรตรวจติดตามระดับ serum hCG ทุกสัปดาห์จนวัดไม่ได้(35) การตัดท่อนำไข่ออก (salpingectomy) ควรพิจารณาทำในกรณีที่ท่อนำไข่แตกหรือถูกทำลายรุนแรง ควบคุมการเสียเลือดไม่ได้ หรือมีบุตรเพียงพอแล้ว (12)
มักพิจารณาเป็นทางเลือกในการรักษากรณีที่ผู้ป่วยไม่มีอาการ ระดับ serum hCG ตั้งต้นต่ำและเมื่อตรวจติดตามพบว่ามีค่าคงที่หรือลดลง ทั้งนี้ควรเลือกรักษาในผู้ป่วยที่สามารถมาตรวจติดตามได้และยอมรับโอกาสในการเกิด ruptured ectopic pregnancy ซึ่งจำเป็นต้องได้รับการผ่าตัดในทันที(1, 6, 12)
เป็นการตั้งครรภ์นอกมดลูกที่วินิจฉัยได้ค่อนข้างยาก มีเกณฑ์ในการวินิจฉัยจากการตรวจด้วยคลื่นเสียงความถี่สูง(6) ดังนี้
ในกรณีที่ต้องการเก็บมดลูกไว้สามารถรักษาด้วยการผ่าตัดทำ cornual resection หรือ cornuostomy (36) หรือให้การรักษาด้วยยา Methotrexate แต่ยังมีข้อมูลสนับสนุนค่อนข้างน้อย(37) แต่ถ้าไม่ต้องการมีบุตรอีกให้ทำการตัดมดลูกออก
พบอุบัติการณ์ร้อยละ 3 ของครรภ์นอกมดลูก(5) มี Spiegelberg’s criteria(12, 38) เป็นเกณฑ์ช่วยในการวินิจฉัย ดังนี้
1. ท่อนำไข่ข้างเดียวกันกับที่ก้อนการตั้งครรภ์อยู่ต้องมีลักษณะปกติ แยกจากก้อนการตั้งครรภ์ได้ชัดเจน
2. มีถุงการตั้งครรภ์บริเวณรังไข่
3. ก้อนการตั้งครรภ์มีการติดต่อกับตัวมดลูกด้วย ovarian ligament
4. พบเนื้อเยื่อของรังไข่อยู่บริเวณผนังของก้อน
การตั้งครรภ์ที่รังไข่สามารถให้การรักษาโดยการทำการตัดเอาเฉพาะส่วนของถุงการตั้งครรภ์และเนื้อเยื่อรังไข่ที่ติดอยู่ออก (wedge resection) (12) หรือตัดรังข้างนั้นออก (oophorectomy) หรืออาจจะรักษาด้วยยา methotrexate(39-41)
พบได้น้อยมีรายงานอุบัติการณ์เพียงร้อยละ 1-1.4 ของครรภ์นอกมดลูก (5, 42) แบ่งเป็นออกเป็น primary abdominal pregnancy เกิดเมื่อไข่ที่ถูกผสมแล้วมีการฝังตัวในช่องท้องโดยตรงและ secondary abdominal pregnancy ซึ่งมักเกิดจากการตั้งครรภ์ที่ท่อนำไข่แล้วเกิด tubal abortion/rupture หรือตั้งครรภ์ในโพรงมดลูกแล้วเกิด uterine rupture และไปเจริญเติบโตในช่องท้อง
เกณฑ์ในการช่วยวินิจฉัยช่วย primary abdominal pregnancy (Studdiford’s Criteria)(12) มีดังนี้
1. ท่อนำไข่และรังไข่ปกติ โดยไม่พบร่องรอยของการตั้งครรภ์ทั้งเก่าและใหม่
2. ไม่มีรูเชื่อมของรกและมดลูก
3. การตั้งครรภ์ทั้งหมดอยู่ที่ผิวเยื่อบุช่องท้อง และดูใหม่ไม่เหมือนหลุดออกมาฝังต่อจากท่อนำไข่
โดยทั่วไปแนะนำให้ยุติการตั้งครรภ์เมื่อทราบว่าเป็นการตั้งครรภ์ในช่องท้องเพราะการตั้งครรภ์ต่อเพิ่มความเสี่ยงให้มารดา ส่วนมากสามารถทำการผ่าตัดเปิดหน้าท้องเพื่อเอาทารกออกและสามารถเอารกออกได้ แต่บางรายจำเป็นต้องทิ้งรกเอาไว้ในช่องท้องและรอให้สลายไปเอง (42)
พบน้อยมากมีรายงานอุบัติการณ์น้อยกว่าร้อยละ 1 ของครรภ์นอกมดลูก(5) มักแยกจากภาวะ Ongoing spontaneous abortion(43) ได้ยาก มีเกณฑ์การวินิจฉัยด้วยการตรวจด้วยคลื่นเสียงความถี่สูง ดังนี้ (6, 12)
1. เห็นถุงการตั้งครรภ์และรกบริเวณปากมดลูก
2. หัวใจของทารกเต้นอยู่ใต้ต่อระดับ internal os
3. ไม่เห็นการตั้งครรภ์ในโพรงมดลูก
4. มดลูกมีรูปร่างคล้ายนาฬิกาทรายและปากมดลูกมีบวมโตออกwith
5. ถุงการตั้งครรภ์ไม่ขยับเมื่อใช้ transvaginal probe กดหรือไม่มี sliding sign
6. ปากมดลูกส่วน internal os ปิด
สามารถให้การรักษาด้วยการให้ยา methotrexate โดยมักจะต้องให้ยาหลายครั้ง ในกรณีที่มีการเต้นของหัวใจของทารกทำการฉีด intraamniotic หรือ intrafetal KCl ก่อน และสามารถทำการขูดมดลูกหรือ suction evacuation โดยอาจจะพิจารณาทำ uterine arterial embolization ร่วมด้วย แต่ถ้าไม่สามารถควบคุมเลือดที่ออกได้ให้พิจารณาตัดมดลูก(44)
พบได้ประมาณ 1 ต่อ 500-2,000 ของการตั้งครรภ์(41, 45) มีเกณฑ์ในการวินิจฉัยจากการตรวจด้วยคลื่นเสียงความถี่สูง ดังนี้(46)
การรักษาทำได้ด้วยการผ่าตัดเอาส่วนของมดลูกที่มีการตั้งครรภ์ออก (uterine isthmic resection) โดยสามารถทำการผ่าตัดผ่านกล้อง ผ่าตัดเปิดหน้าท้อง หรือผ่าตัดทางช่องคลอดโดยเปิดเข้าสู่ช่องท้องทางผนังช่องคลอดด้านหน้า (anterior colpotomy) สำหรับทางเลือกในการรักษาวิธีอื่น ได้แก่ การทำ uterine arterial embolization ตามด้วยการขูดมดลูก การตัดเอาถุงการตั้งครรภ์และรกออกผ่านการส่องกล้องทางโพรงมดลูก (47, 48) การให้ยา methotrexate หรือการฉีด intragestational sac KCl (49, 50)
พบอุบัติการณ์ประมาณ 1:30,000 ของการตั้งครรภ์(31) และจะเพิ่มขึ้นหากเป็นการตั้งครรภ์จากเทคโนโลยีช่วยการเจริญพันธุ์(51) การรักษาขึ้นอยู่กับลักษณะทางคลินิกของผู้ป่วย หากมีการแตกของท่อนำไข่ควรรักษาด้วยการผ่าตัด แต่หากไม่มีสามารถเลือกการรักษาด้วยวิธีผ่าตัดหรือการฉีดยาเข้าไปทำลายถุงการตั้งครรภ์โดยเลือกใช้เป็น KCl หรือ hyperosmolar glucose(6, 52)
การตั้งครรภ์นอกมดลูกเป็นภาวะที่สามารถพบได้บ่อยทางสูตินรีเวชกรรม มีอันตรายสูงต่อผู้ป่วย แพทย์ควรให้วินิจฉัยและรักษาอย่างรวดเร็วและเหมาะสม สตรีวัยเจริญพันธุ์ทุกคนที่มีอาการปวดท้องร่วมกับมีเลือดออกผิดปกติทางช่องคลอดควรได้รับการคัดกรองการตั้งครรภ์โดยไม่คำนึงถึงการคุมกำเนิด และผู้ป่วยที่เคยมีประวัติเป็นเคยตั้งครรภ์นอกมดลูกมาก่อนควรได้รับคำแนะนำให้รีบมาฝากครรภ์เนื่องจากมีโอกาสเป็นซ้ำสูง
พญ.พรปวีณ์ นิรันดร์รุ่งเรือง
อาจารย์ที่ปรึกษา ศาสตราจารย์แพทย์หญิง สายพิณ พงษธา
วัยหมดระดู (Menopause) คือวัยที่ประจำเดือนหยุดอย่างถาวรจาก นาน 12 เดือนขึ้นไป ซึ่งไม่ได้เกิดจากความผิดปกติอื่นๆ โดยอายุของวัยหมดระดูอยู่ในช่วง 45-55 ปี และมีอายุเฉลี่ยอยู่ที่ 51.4 ปี1
Menopause มีสัมพันธ์กับการเปลี่ยนแปลงฮอร์โมนจาก hypothalamus และ pituitary gland โดยเกิดจากรังไข่มี ovarian follicles ลดลง ทำให้รังไข่ไม่สามารถตอบสนองต่อการกระตุ้นของ Follicle-stimulating hormone (FSH) และ Luteinizing hormone (LH) จาก pituitary gland ได้ การสร้าง estrogen และ progesterone จึงลดลง แต่ FSH สูงขึ้นเนื่องจาก ovarian failure และไม่มี negative feedback มาจากรังไข่ Antimullerian hormone (AMH) ลดลงตาม ovarian follicles ที่ลดลง
รังไข่ยังคงสร้าง androgen ต่อ เนื่องจากชั้น stroma และ theca cells ของรังไข่ยังคงปกติ แต่ก็สร้างได้ในปริมาณที่ต่ำกว่าวัยเจริญพันธุ์ เนื่องจากอายุที่มากขึ้นและการทำงานของรังไข่และต่อมหมวกไต(adrenal gland) ลดลง ต่อมไขมัน (adipose tissue) จะเป็นแหล่งหลักในการเกิด aromatization เปลี่ยน androgen จากรังไข่และต่อมหมวกไตเป็น estrogen ทำให้ในวัยหมดระดูก็ยังคงมีปริมาณ estrogen ในระดับต่ำๆอยู่ ส่วนต่อมไขมันเมื่อกลายเป็นแหล่งหลักในการสร้างฮอร์โมนทำให้มีผลเรื่องโรคอ้วน (obesity) ตามมาในวัยหมดระดูได้ และโรคอ้วนยังเป็นปัจจัยเสี่ยงในการเกิดมะเร็งเต้านมและโรคหัวใจและหลอดเลือด แต่เป็นปัจจัยในการป้องกันโรคกระดูกพรุนได้2
Stages of Reproductive Aging Workshop (STRAW) criteria2
ระยะของภาวะเจริญพันธุ์ถูกแบ่งออกตาม STRAW (stages of reproductive aging workshop) criteria (รูปที่ 1) ซึ่งเป็น gold standard ในการบ่งบอกลักษณะของการเปลี่ยนผ่านวัยเจริญพันธุ์เข้าสู่วัยหมดระดู
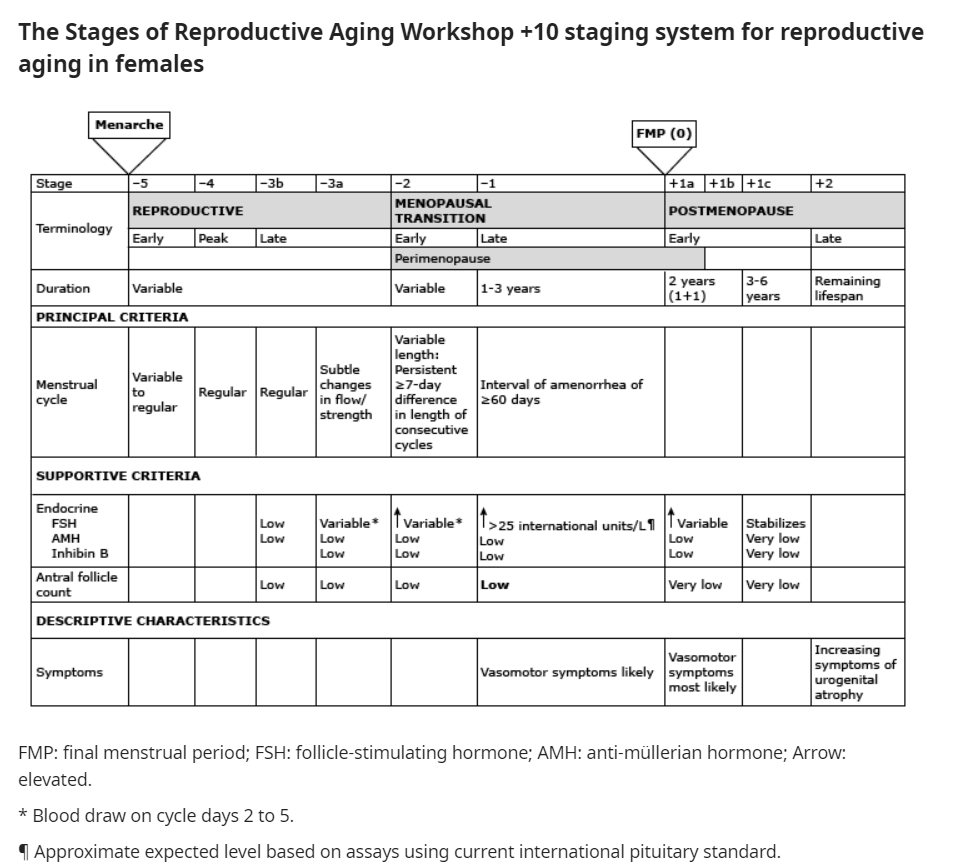
รูปที่1: ระยะของภาวะเจริญพันธุ์ (STRAW criteria) ที่มา Harlow SD, Gass M, Hall JE, et al.
Executive Summary of the Stages of Reproductive Aging Workshop + 10. J Clin Endocrinol Metab 2012
เป็นอาการที่เกิดจาก estrogen withdrawal พบได้ร้อยละ 75 ในสตรีวัยใกล้หมดประจำเดือน (perimenopause) จะมีอาการอยู่นาน 1-2 ปีหลังหมดประจำเดือน ในบางรายอาจมีอาการได้นานกว่า 10 ปี ผู้ป่วยจะมีอาการร้อนวูบวาบตามตัวทันที เริ่มเป็นที่หน้าอกส่วนบนและใบหน้า และกระจายไปทั่วตัว ทำให้ส่งผลต่อการใช้ชีวิตประจำวัน การนอนหลับ และการทำงาน ซึ่งเป็นอาการนำที่พาผู้ป่วยมาพบแพทย์บ่อยที่สุด การรักษา VMS จะทำให้ผู้ป่วยมีคุณภาพชีวิตที่ดีขึ้น2
การขาด estrogen มีผลทำให้อวัยวะสืบพันธุ์ภายนอก ช่องคลอด ท่อปัสสาวะ และกระเพาะปัสสาวะเกิดความเปลี่ยนแปลง เกิด vulvovaginal atrophy (VVA) ทำให้อาการระคายเคืองบริเวณอวัยวะสืบพันธุ์ แห้ง รู้สึกแสบร้อน และเจ็บเวลามีเพศสัมพันธ์ ซึ่งพบร้อยละ 50 % และค่อนข้างส่งผลต่อคุณภาพชีวิต นอกจากนี้ยังมีอาการทางระบบทางเดินปัสสาวะร่วมด้วย ได้แก่ ปัสสาวะเร่งรีบ (urinary urgency) ปัสสาวะแสบขัด มีการติดเชื้อทางเดินปัสสาวะซ้ำๆ2
พบร้อยละ 40 สาเหตุเกิดจากหลายปัจจัย เช่น ภาวะซึมเศร้าหรือวิตกกังวล ปัญหาความสัมพันธ์ ความเครียด ความอ่อนเพลีย การถูกทำร้ายในอดีต ยาต่างๆ และปัญหาสุขภาพที่ส่งผลต่อกิจกรรมทางเพศ ได้แก่ GSM ซึ่งทำให้ช่องคลอดแห้งและรู้สึกเจ็บเวลามีเพศสัมพันธ์2, 3
การมีมวลกระดูกต่ำและภาะกระดูกพรุนเป็นปัจจัยเสี่ยงหลักที่นำไปสู่การเกิดกระดูกหัก ซึ่งสามารถป้องกันการเกิดภาวะกระดูกพรุนและกระดูกหักได้ด้วยการปรับเปลี่ยนปัจจัยเสี่ยง ได้แก่ การให้วิตามินดีและแคลเซียมเสริมในรายที่ได้ไม่เพียงพอ งดบุหรี่ ลดปริมาณการดื่มสุรา ออกกำลังกาย ปรับเปลี่ยนบ้านให้มีความปลอดภัย รักษาเรื่องการมองเห็นในรายที่มีการมองเห็นผิดปกติ2
เป็นสาเหตุหลักของการเสียชีวิตในหญิงวัยหมดระดู ซึ่งอัตราการเสียชีวิตจาก cardiovascular disease ในหญิงวัยหมดระดูมากกว่าอัตราการเสียชีวิตจากมะเร็งเต้านม ปัจจัยเสี่ยงในการเกิดโรคหัวใจและหลอดเลือด ได้แก่ อายุ ประวัติครอบครัว การใช้ชีวิตประจำวัน โรคอ้วน การสูบบุหรี่ และโรคประจำตัว เช่น เบาหวาน ความดันโลหิตสูง และไขมันในเลือดสูง การลดปัจจัยเสี่ยงและรักษาโรคประจำตัวเป็นสิ่งสำคัญในการลดการเกิดโรคหัวใจและหลอดเลือด2, 4
มะเร็งเต้านมเป็นปัญหาสำคัญในหญิงวัยหมดระดู การได้รับเอสโตรเจนเป็นเวลานานเพิ่มความเสี่ยงในการเกิดมะเร็งเต้านมที่มากขึ้น การได้ menopausal hormone therapy (MHT) เพิ่มความเสี่ยงในการเกิดมะเร็งเต้านมเช่นกัน2
ในหญิงวัยหมดระดูจะมีกระบวนการคิดและการจดจำที่ลดลง การได้ MHT ไม่ช่วยการรักษาภาวะสมองเสื่อม การปรับเปลี่ยนพฤติกรรม เช่น ออกกำลังกาย รักษาโรคความดันโลหิตสูง เบาหวาน การเรียนรู้สิ่งต่างๆ สามารถลดความเสี่ยงในการเกิดภาวะสมองเสื่อมได้2
Menopause เป็นปัจจัยเสี่ยงในการเกิดโรคหัวใจและหลอดเลือด เพราะ estrogen withdrawal ส่งผลต่อการทำงานและ metabolism ของระบบหัวใจและหลอดเลือดเอง และมีผลต่อการเพิ่มความเสี่ยงในการเกิดโรค ได้แก่
Cardiovascular effects of estrogen5
Cardiovascular effect of progestins5
Synthetic progestins เช่น medroxyprogesterone acetate (MPA) อาจต้านผลของ estrogen ต่อไขมันและ endothelial function ได้ (WHI trial and HERS) ส่วน natural progesterone ยังมีการศึกษาน้อยอยู่
Women’s Health Initiative (WHI) trial แนะนำว่า MHT ไม่มีประสิทธิภาพ ในการป้องกัน coronary heart disease (CHD) แบบปฐมภูมิ หนึ่งในการศึกษา มีการเปรียบเทียบ continuous combined estrogen-progestin regimen (CEE 0.625 mg และ MPA 2.5 mg/day) เทียบกับ placebo ในหญิงวัยหมดระดูจำนวน 16,608 คน อายุ 50-79 ปี ที่ยังมีมดลูกอยู่ ผลการศึกษาพบว่าการได้ MHT มีผลเพิ่มความเสี่ยงในการเกิด breast cancer, stroke, CHD และ VTE เมื่อติดตามไป 5.2 ปี ทำให้ต้องถูกระงับไประหว่างการทดลอง แม้ว่าจะลดความเสี่ยงในการเกิด hip fracture และ colon cancer อย่างมีนัยสำคัญก็ตาม5, 6
WHI trial ในสูตรของ unopposed estrogen ได้ศึกษาเปรียบเทียบ conjugated equine estrogen (CEE 0.625 mg/day) กับ placebo ในหญิงวัยหมดระดูจำนวน 10,739 คน อายุ 50-79 ปี ที่ตัดมดลูกแล้ว ซึ่งถูกยุติการวิจัยก่อนกำหนด เนื่องจากผลการศึกษาพบว่าการได้ unopposed estrogen เพิ่มความเสี่ยงในการเกิด stroke และลดความเสี่ยงในการเกิด hip fracture แต่ไม่มีผลต่อการเกิด CHD5, 7
Continuous combined estrogen-progestin
จาก WHI trial เริ่มแรก พบว่าการใช้ MHT มีความเสี่ยงในการเกิด CHD8 แต่การศึกษาต่อๆมาพบว่าความเสี่ยงที่เพิ่มน่าจะเป็นจากอายุที่มากขึ้นด้วย นอกจากนี้ปัจจัยร่วมอื่นๆ ได้แก่ BMI, VMS, coronary risk factor อื่นๆ เช่น โรคเบาหวาน ความดันโลหิตสูง ประวัติครอบครัว และการสูบบุหรี่ โดยที่การรับประทานยา aspirin หรือ statin พบว่าไม่มีผลต่อ CHD risk ในคนที่ได้ MHT5
Women’s international study of long-duration oestrogen after menopause (WISDOM) ได้ทำการศึกษาคล้ายกับ โดยเปรียบเทียบกลุ่มที่ได้ continuous combined estrogen-progestin regimen (CEE 0.625 mg และ MPA 2.5 mg/day) เทียบกับ placebo ในหญิงวัยหมดระดู อายุ 50-69 ปี ซึ่งถูกระงับไปหลังจากติดตามได้ 12 เดือน เนื่องจากเพิ่มความเสี่ยงในการเกิด CHD และ VTE5, 9
Unopposed estrogen
จาก unopposed estrogen trial ของ WHI ได้ทำการศึกษาในหญิงวัยหมดระดูที่ตัดมดลูกไปแล้ว อายุระหว่าง 50-79 ปี เปรียบเทียบระหว่างกลุ่มที่ได้ CEE 0.625 mg/d และ placebo พบว่าความเสี่ยงในการเกิด CHD ลดลงในกลุ่มที่อายุระหว่าง 50-59 ปี5, 10 แสดงให้เห็นว่า progestin มีบทบาทสำคัญในการเพิ่มความเสี่ยงในการเกิด CHD แต่การใช้ unopposed estrogen ก็เพิ่มความเสี่ยงในการเกิด stroke และ VTE5
Predictors of CHD risk
Timing of exposure
จากหลายการศึกษาพบว่าการได้ MHT ในช่วงที่หมดประจำเดือนระยะแรกๆ ไม่เพิ่ม CVD risk เมื่อเทียบกับการให้ MHT ในช่วงหมดประจำเดือนระยะหลังๆ (Timing hypothesis) เพราะ ยังไม่เกิดการสร้าง atherosclerotic plaque ในกลุ่มที่อายุน้อยกว่า5
จากหลายการศึกษาไม่สามารถยืนยันได้ว่าการได้ MHT จะมีประสิทธิภาพในด้าน secondary prevention ได้5
จากการศึกษไม่แนะนำให้ใช้ MHT เพื่อป้องกันการเกิด CHD event
จากการศีกษาพบว่า ไม่ควรให้ MHT เพื่อลดความเสี่ยงในการเกิด CHD event ในหญิงวัยหมดระดู
Unopposed estrogen
จากการศึกษาต่างๆสรุปได้ว่าการได้ unopposed estrogen ไม่มีประสิทธิภาพใน secondary prevention5
มะเร็งปากมดลูก (Cervical cancer) เป็นมะเร็งในสตรีที่พบบ่อยเป็นอันดับที่ 4 ของโลก มีการตรวจพบมะเร็งปากมดลูกรายใหม่ประมาณ 604,000 ราย และมีผู้เสียชีวิตจากมะเร็งปากมดลูก 342,000 รายในปี ค.ศ. 2020 ซึ่งร้อยละ 90 ของผู้ป่วยและผู้เสียชีวิตพบในประเทศที่มีรายได้ต่ำและปานกลาง (low and middle income countries) และมะเร็งปากมดลูกมากกว่าร้อยละ 95 สัมพันธ์กับการติดเชื้อ Human papilloma virus (HPV) (1)
การตรวจคัดกรองมะเร็งปากมดลูก (Cervical cancer screening) มีจุดประสงค์หลักเพื่อป้องกันการเกิดมะเร็งปากมดลูก โดยการตรวจหารอยโรคก่อนมะเร็ง (Preinvasive cervical lesion) เพื่อให้การรักษาที่ก่อนที่จะกลายเป็นมะเร็งปากมดลูก และตรวจติดตามหลังการรักษาได้อย่างเหมาะสม (2) ซึ่งการตรวจคัดกรองมะเร็งปากมดลูก ได้แก่ การตรวจทางเซลล์วิทยา (Pap smear or liquid-based cytology) และการตรวจ HPV (HPV testing) ในรายที่ผลตรวจคัดกรองพบความผิดปกติจะมีแนวทางในการตรวจติดตามและรักษาต่อไป
| Normal cytology result: | |
| Negative intraepithelial
lesions or malignancy (NILM) |
สิ่งส่งตรวจ satisfactory for evaluation และไม่พบเซลล์ผิดปกติ |
| Squamous lesions: | |
| Atypical squamous cell (ASC) | |
Cells of undetermined significance (ASC-US) |
เซลล์มีความผิดปกติมากกว่า simple reactive change แต่ไม่เข้า criteria ของ squamous intraepithelial lesion ในบางรายสัมพันธ์กับ cervical intraepithelial lesion (CIN) |
|
เซลล์มีลักษณะบางส่วนเข้าได้กับ HSIL หรืออาจมี LSIL ร่วมด้วย |
| Low-grade squamous
intraepithelial lesion (LSIL) |
รอยโรคที่สัมพันธ์กับการติดเชื้อ HPV ซึ่งมีแนวโนมเป็นการเปลี่ยนแปลงแบบชั่วคราว สามารถหายไปตามเวลาได้ |
| High-grade squamous
intraepithelial lesion (HSIL) |
รอยโรคที่สัมพันธ์กับการติดเชื้อ high-risk type HPV ซึ่งมีความเสี่ยงสูงที่จะเป็น CIN2,3 และสามรถกลายเป็นมะเร็งได้ |
| Glandular lesions: | |
| Atypical glandular cell (AGC) | Subcategory: Endocervical, endometrial, or not otherwise specified (NOS) |
| Atypical glandular cell, favor neoplasia | Subcategory: Endocervical เท่านั้น
สิ่งส่งตรวจมีลักษณะบ่งบอก Adenocarcinoma แต่ยังไม่เพียงพอในการแปลผลว่าเป็น adenocarcinoma |
| Endocervical adenocarcinoma in situ (AIS) | Endocervical glands ที่เป็น atypical columnar epithelial cells ซึ่งมีลักษณะคล้ายกับ invasive cervical adenocarcinoma without stromal invasion |
|
ตรวจหาเชื้อ high-risk HPV ในภาพรวม ไม่ได้ระบุสายพันธุ์จำเพาะ
|
genotyping |
ตรวจหาเชื้อและระบุสายพันธุ์จำเพาะของเชื้อ HPV โดยรายงานแยกชนิดของเชื้อ HPV 16 และ 18 ซึ่งมีศักยภาพสูงในการก่อมะเร็งออกจาก high-risk HPV อื่นๆ |
ในอดีต premalignant squamous change ของปากมดลูกถูกแบ่งเป็น mild, moderate และ severe dysplasia แต่ในปัจจุบันได้ใช้คำนิยามตาม Bethesda system แบ่ง cytologic findings เป็น Squamous intraepithelial lesion (SIL) และแบ่ง histologic findings เป็น Cervical intraepithelial Neoplasia (CIN) โดย CIN แบ่งตามความรุนแรงเป็น 3 ระดับ ได้แก่ (5)
| CIN 1 | Low-grade lesion บ่งบอกถึง mildly atypical cellular change บริเวณ lower third of epithelium มักมี HPV cytopathic effect ร่วมด้วย |
| CIN 2 | ถูกพิจารณาเป็น high-grade lesion บ่งบอกถึง moderate atypical cellular change บริเวณ basal two third of epithelium |
| CIN 3 | High-grade lesion บ่งบอกถึง severe atypical cellular change บริเวณมากกว่า two third of epithelium จนถึง full-thickness lesion |
ในปี ค.ศ. 2012 The Lower Anogenital Squamous Terminology (LAST) project ซึ่งเกิดจากความร่วมมือของ The Collage of American Pathologists (CAP) และ The American Society for Colposcopy and Cervical Pathology (ASCCP) ได้แบ่งและจัดการให้นิยามความผิดปกติของรอยโรคก่อนมะเร็ง (preinvasive lesions) ของอวัยวะสืบพันธุ์สตรีส่วนล่างและทวารหนักที่มีความเกี่ยวข้องกับเชื้อ HPV โดยแบ่งลักษณะทาง histology เป็น Low-grade squamous intraepithelial lesion (LSIL) และ High-grade squamous intraepithelial lesion (HSIL) ซึ่งในระบบ LAST นั้น HSIL จะหมายรวมถึง Cervical Intraepithelial Neoplasia (CIN) 2 และ 3 ในระบบ CIN (รูปที่ 1) (6) อย่างไรก็ตามในที่นี้จะกล่าวถึง CIN terminology เนื่องจาก CIN เป็น terminology ที่ใช้เป็นหลักใน ASCCP 2019 risk-based management consensus guidelines for cervical cancer screening tests and cancer precursors ที่จะกล่าวถึงต่อไป
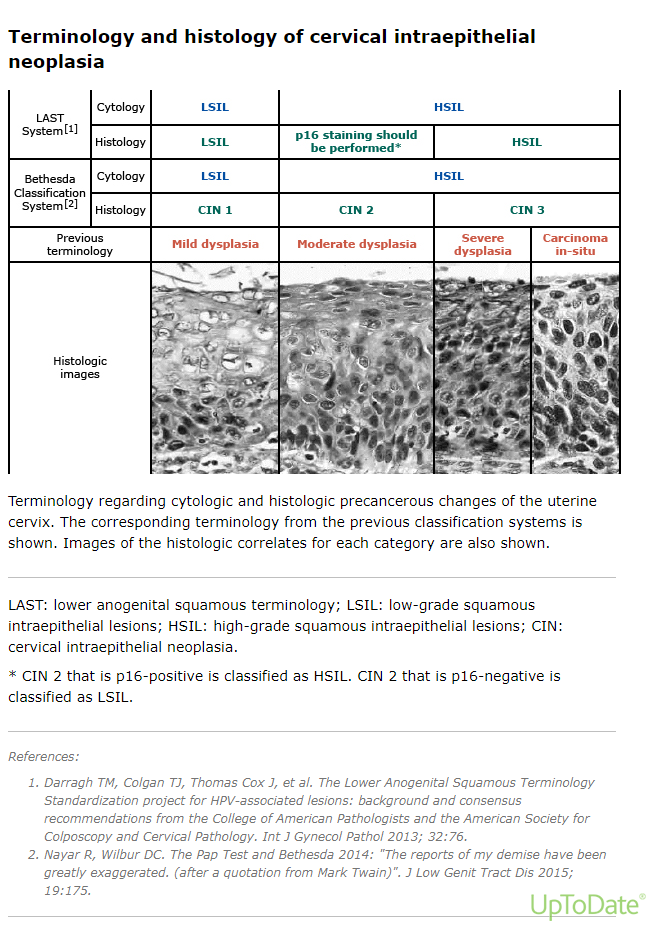
รูปที่ 1 ลักษณะทางพยาธิวิทยาตามระบบ LAST และ Bethesda (5)
2019 ASCCP Risk-based management consensus guidelines for abnormal cervical cancer screening tests and cancer precursors
ความแตกต่างหลักๆ ของ 2019 guidelines กับ guidelines ก่อนหน้า คือ การใช้ risk-based guidelines แทนการใช้ test results-based algorithms โดยการใช้ตารางเพื่อประเมินความเสี่ยง (Risk estimation) ในการเกิด immediate risk of CIN3+ และ 5-Years risk of CIN3+ (CIN3, Adenocarcinoma in situ and cancer) โดยใช้ผลการตรวจคัดกรองในปัจจุบันและอดีต ซึ่งตารางที่ใช้ประเมินความเสี่ยงนี้ถูกคิดค้นจากการศึกษาแบบ prospective longitudinal cohort ในผู้ป่วยกว่า 1.5 ล้านราย และมีการติดตามนานกว่า 10 ปีที่ Kaiser Permanente Northern California (KPNC) (ตารางที่ 2, 3) นอกจากตารางที่ใช้ประเมินความเสี่ยงแล้ว ยังสามารถใช้ข้อมูลแบบเดียวกันได้ผ่านทาง smartphone app (รูปที่ 2) หรือผ่านทาง website http://www.asccp.org ได้ด้วย ซึ่งข้อมูลขั้นต่ำที่ต้องมี คือ อายุ และผลการตรวจปัจจุบัน แต่ความแม่นยำของ management guide จะเพิ่มขึ้นถ้ามีผลการตรวจในช่วง 5 ปีที่ผ่านมาด้วย (7)
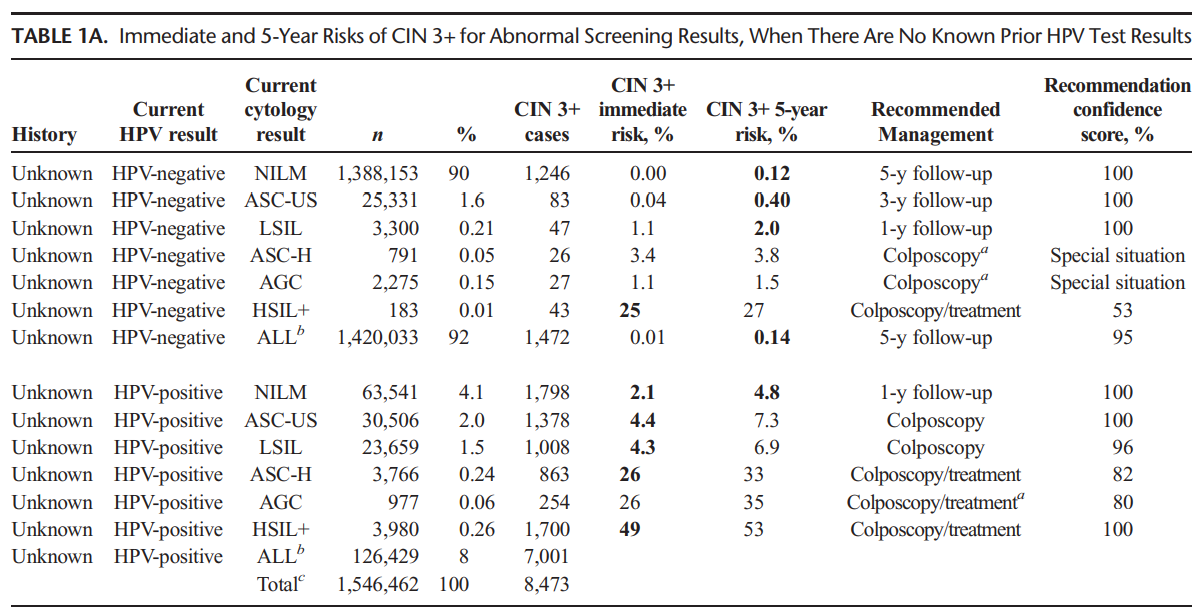
ตารางที่ 1 Immediate and 5-year risks of CIN3+ สำหรับผลการตรวจคัดกรองที่ผิดปกติ กรณีที่ไม่มีผลการตรวจ HPV test ก่อนหน้า (8)
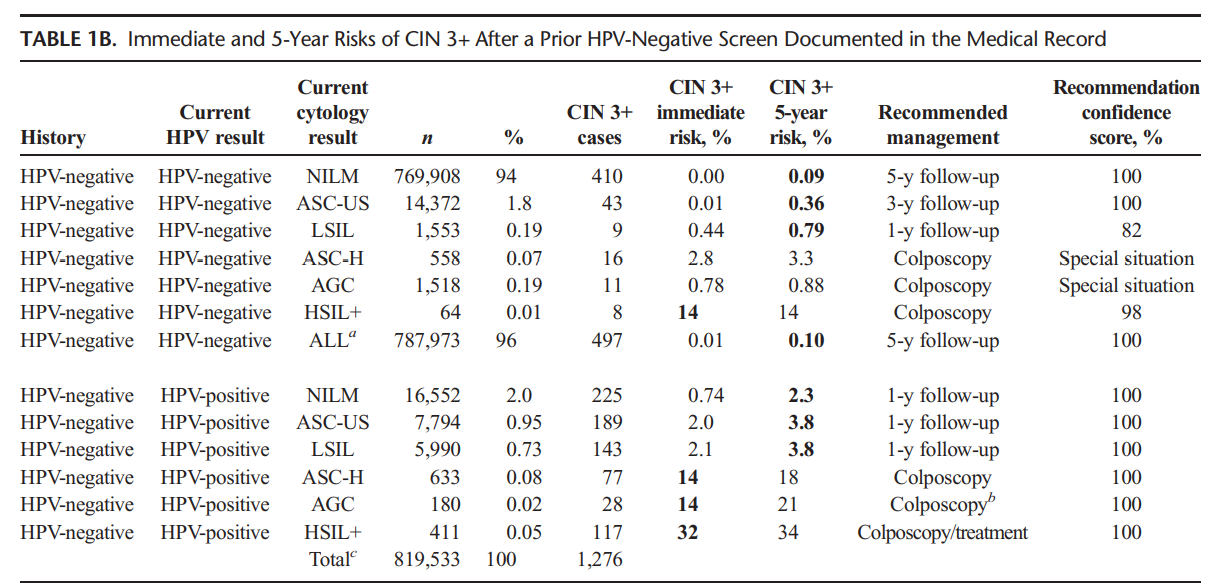
ตารางที่ 2 Immediate and 5-year risks of CIN3+ สำหรับผลการตรวจคัดกรองที่ผิดปกติ กรณีที่มีผลการตรวจ HPV test ก่อนหน้าเป็น negative (8)
รูปที่ 2 Smartphone application: ASCCP Management Guidelines
HPV-based testing ถูกใช้เป็นพื้นฐานใน risk estimation ซึ่งลักษณะของการติดเชื้อ HPV รวมถึง HPV type และระยะเวลาในการติดเชื้อจะเป็นตัวประเมิน risk CIN3+ เพื่อนำไปสู่คำแนะนำในการส่ง colposcopy และระยะเวลาในการตรวจติดตามต่อไป ในที่นี้ HPV-based testing จะหมายถึง primary HPV testing อย่างเดียว หรือ co-testing
Risk CIN3+ ขึ้นกับผลการตรวจปัจจุบันและก่อนหน้า ร่วมถึง precancer treatment ก่อนหน้าด้วย ซึ่ง Risk CIN3+ จะนำไปสู่ Clinical Action Threshold เพื่อแนะนำ management ต่อไป เช่น routine screening, 1-year or 3-year surveillance, colposcopy หรือ treatment
ในอนาคตถ้ามีการตรวจแบบใหม่เกิดขึ้น clinical action threshold ก็จะเปลี่ยนไป รวมถึงในอนาคตจะมีการฉีดวัคซีน HPV ที่มากขึ้น risk of CIN3+ ก็ถูกคาดการณ์ว่าจะลดลงเช่นกัน
ตาม ASCCP Colposcopy Standards การทำ Colposcopy ร่วมกับ targeted biopsy ถือเป็นวิธีหลักในการตรวจพบ precancers ที่ต้องได้รับการรักษา โดย biopsy บริเวณ acetowhite areas ทุกที่ที่แยกกัน 2-4 ที่ ไม่แนะนำให้ทำ untargeted biopsy และในรายที่การตรวจ colposcopy ปกติสามารถตรวจติดตามต่อโดยไม่ต้อง biopsy ได้
จุดประสงค์หลัก (primary goal) ของการตรวจคัดกรองและการดูแลรักษา คือ การป้องกันมะเร็งปากมดลูกโดยการค้นหาและรักษารอยโรคก่อนมะเร็งปากมดลูก (cervical precancer) ซึ่งจากหลายการศึกษาพบว่าการค้นหาและรักษา high-grade histologic cervical abnormality (CIN2+) ที่เพิ่มมากขึ้น สามารถลดอุบัติการณ์และอัตราการเสียชีวิตจากมะเร็งปากมดลูกได้ ทำให้ใน 2019 ASCCP guideline ยังคงใช้เป็นจุดประสงค์หลักอยู่
จุดประสงค์รอง (secondary goal) คือ การวินิจฉัยมะเร็งปากมดลูกได้ตั้งแต่ระยะต้นๆ ซึ่งจะสามารถลดอัตราการเจ็บป่วยและอัตราการเสียชีวิตได้
แนวทางการดูแลนี้ใช้ได้กับผู้หญิงและ transgender men ที่มีปากมดลูก รวมถึงรายที่ได้รับการผ่าตัด supracervical hysterectomy และรายที่ได้รับการผ่าตัด hysterectomy with removal of cervix ที่เคยมีประวัติก่อนหน้าเป็น histologic HSIL, CIN2, CIN2/3, CIN3 หรือ AIS
ประวัติการรักษาก่อนหน้าและผลการตรวจปัจจุบันจะถูกนำมาคำนวณความเสี่ยง CIN3+ ในอนาคต ดังนั้นรายที่มีความเสี่ยงคล้ายกันก็จะมีการดูแลคล้ายกัน
แนวทางการดูแลรักษามุ่งเน้นไปที่ความสมดุลระหว่างการป้องกันมะเร็งและการตรวจหาหรือรักษาที่มากเกิน โดยจะป้องกันมะเร็งให้มากที่สุดโดยที่คนไข้จะได้รับอันตรายจากการตรวจหาและรักษาที่มากเกินไปน้อยที่สุด
แนวทางการรักษานี้ไม่สามารถครอบคลุมผู้ป่วยที่มีอาการนำมาก่อน เช่น abnormal uterine bleeding หรือ vaginal bleeding หรือ ปากมดลูกมีความผิดปกติชัดเจนที่สงสัยมะเร็ง เป็นต้น
CIN3+ as Main clinical end point for risk estimates (7)
Clinical Action Thresholds (7)
เมื่อผู้ป่วยได้รับการคำนวณ Immediate CIN3+ risk และ 5-year CIN3+ risk แล้วก็จะถูกจัดเข้า Clinical Action Thresholds ซึ่งมี 6 ระดับด้วยกัน ซึ่งจะนำไปสู่แนวทางการดูแลต่อไป
Clinical Action Threshold 6 ระดับ ได้แก่
Clinical Action Thresholds leading to recommendation of surveillance (7)
กรณี Immediate CIN3+ risk < 4% จะต้องคำนวณ 5-year CIN3+ risk ต่อเพื่อหา surveillance interval (รูปที่ 3)

รูปที่ 3 แสดงการประเมินความเสี่ยงของผู้ป่วยโดยใช้ Immediate CIN3+ risk และ 5-year CIN3+ risk
กรณี Immediate CIN3+ risk ≥ 4% (รูปที่ 3)
Primary goal of treatment: การป้องกันมะเร็งโดยการทำลายหรือ excision precancerous lesion ก่อนที่จะพัฒนาเป็น invasive cancer มีการศึกษาพบว่า CIN3 ที่ไม่ได้รับการรักษามีโอกาสพัฒนาเป็น invasive cancer ได้สูงถึง 30% ใน 30 ปี
การพิจารณาให้การรักษาขึ้นกับ Immediate CIN3+ risk (รูปที่ 3)
ผู้ป่วยที่มีผลการตรวจคัดกรองมะเร็งปากมดลูกที่ผิดปกติจะเข้าสู่กระบวนการดูแลผ่าน 5 สถานการณ์ที่พบได้บ่อย ได้แก่
Recommendation จะขึ้นกับ immediate and 5-year CIN3+ risk นำไปสู่การดูแลต่อตาม Clinical Action Threshold
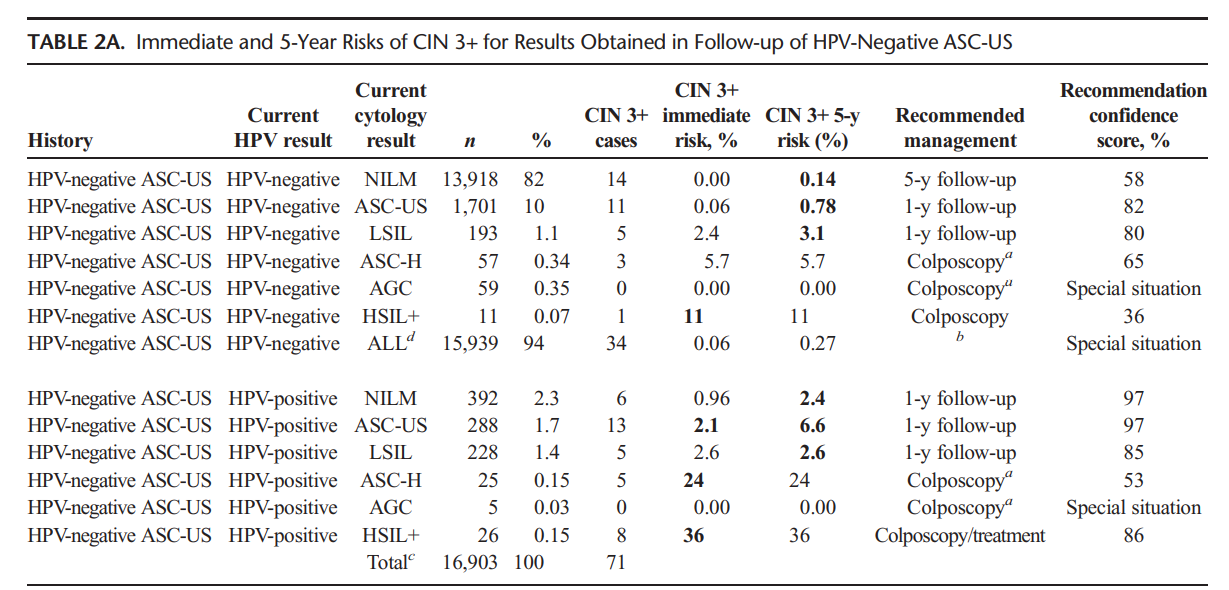
ตารางที่ 3 Immediate and 5-year risks of CIN3+ สำหรับ follow-up HPV-negative ASC-US (8)
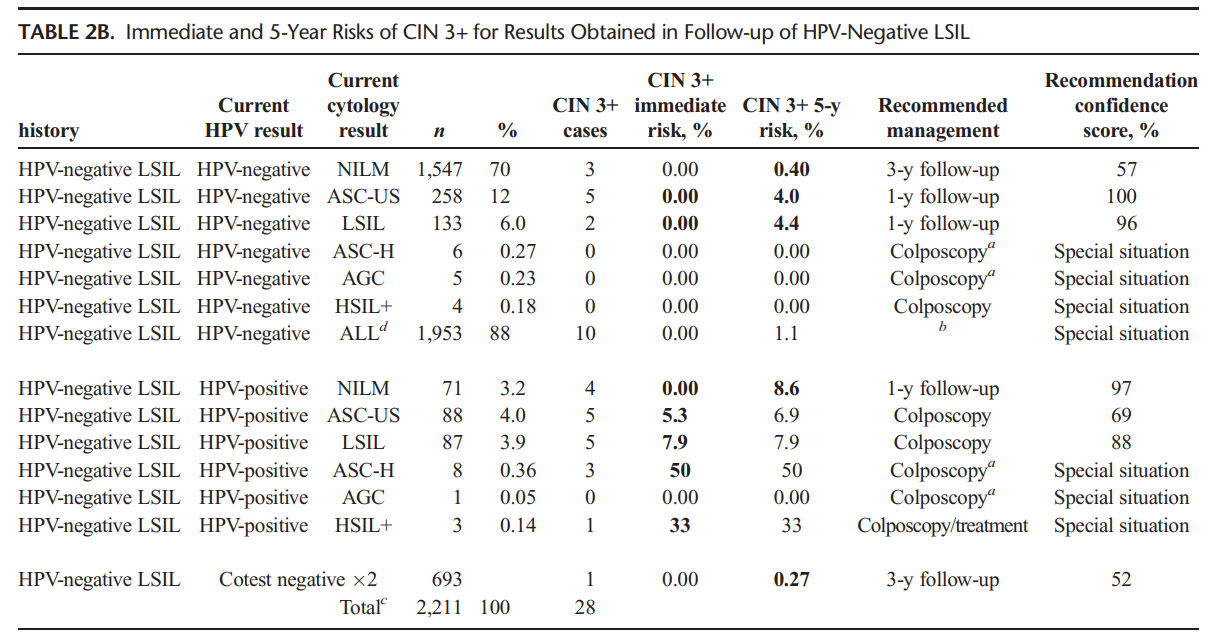
ตารางที่ 4 Immediate and 5-year risks of CIN3+ สำหรับ follow-up HPV-negative LSIL (8)
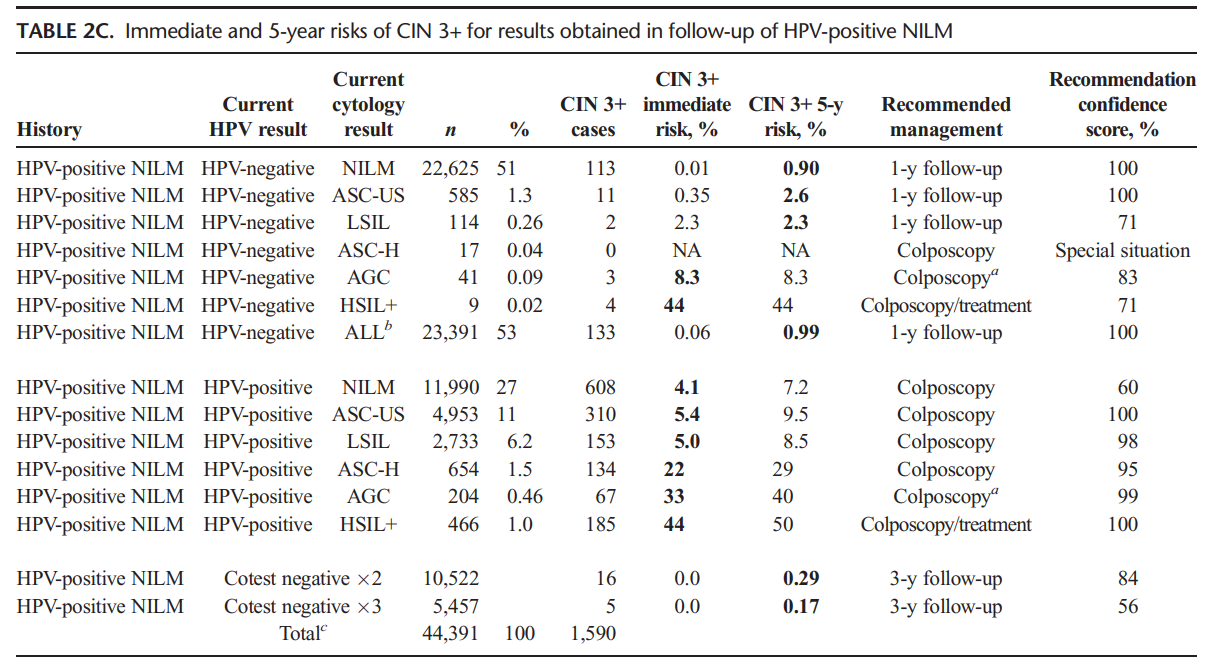
ตารางที่ 5 Immediate and 5-year risks of CIN3+ สำหรับ follow-up HPV-positive NILM (8)
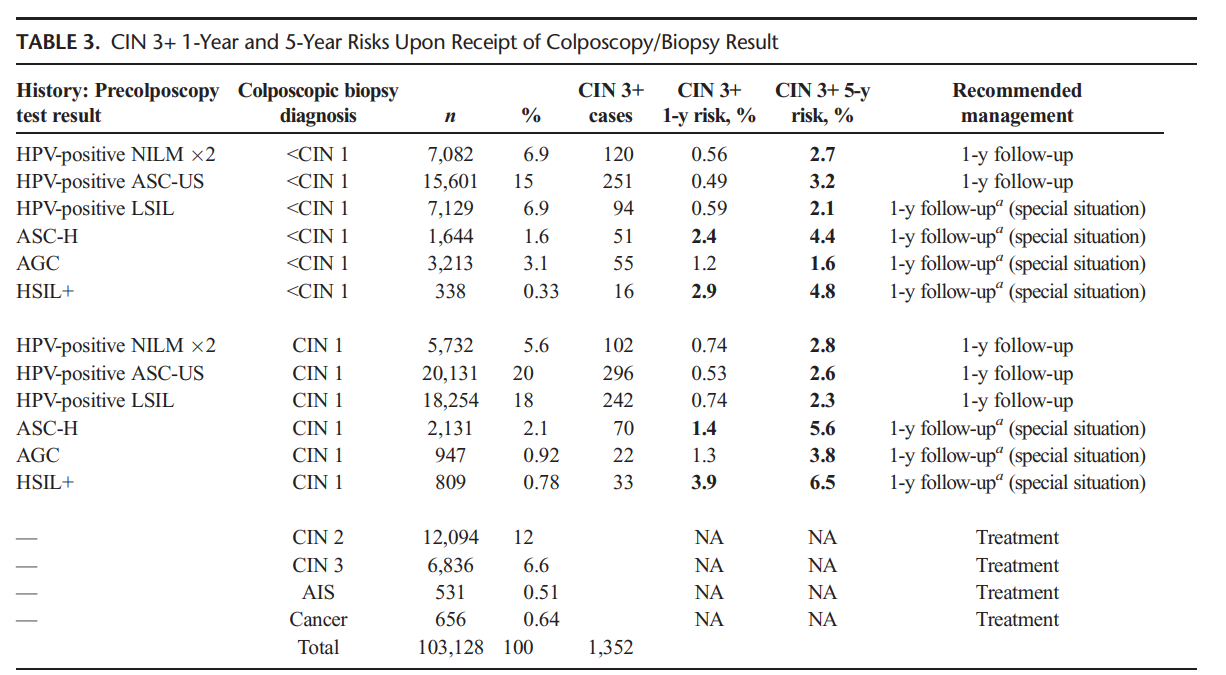
ตารางที่ 6 1-year and 5-year risks of CIN3+ หลังได้ผล colposcopy/biopsy (8)
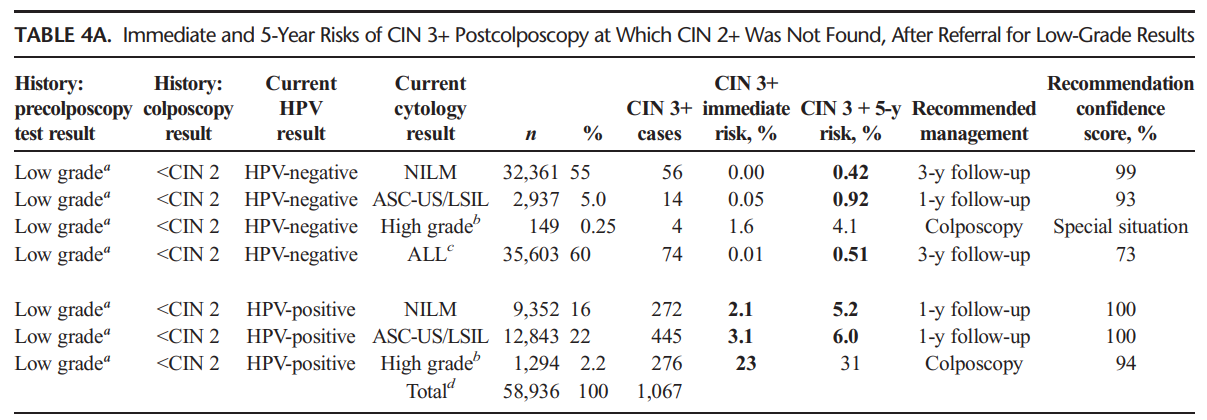
ตารางที่ 7 Immediate and 5-year risks of CIN3+ postcolposcopy after low-grade result (8)
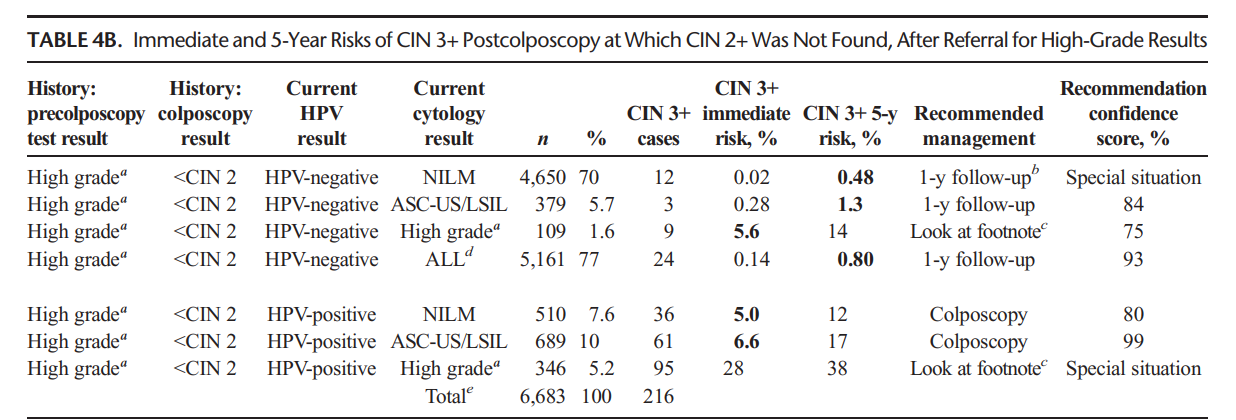
ตารางที่ 8 Immediate and 5-year risks of CIN3+ postcolposcopy after high-grade result (8)
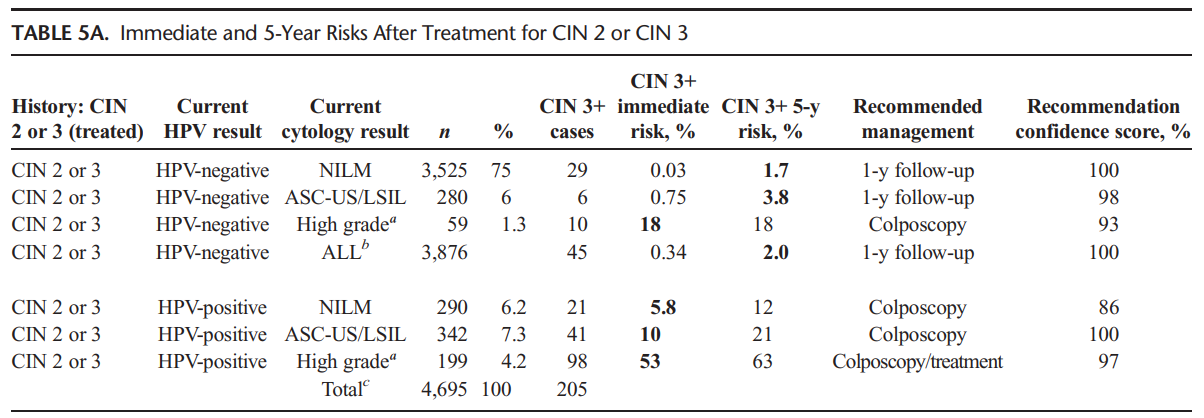
ตารางที่ 9 Immediate and 5-year risks of CIN3+ after treatment for CIN2 or CIN3 (8)
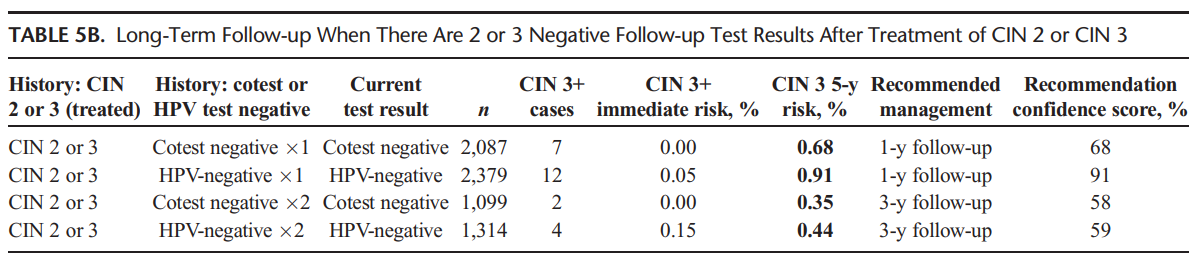
ตารางที่ 10 Long-term follow-up เมื่อผล follow-up test negative 2-3 ครั้งหลังการรักษา CIN2 หรือ CIN3 (8)
ตามแนวทางเวชปฏิบัติของราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย พ.ศ. 2564ได้จำแนกแนวทางการดูแลตามความผิดปกติทาง cytology ที่ตรวจพบดังนี้ (6)
แนวทางการดูแลพิจารณาตามอายุ ศักยภาพของโรงพยาบาล ความวิตกกังวลเรื่องมะเร็ง และเศรษฐานะ
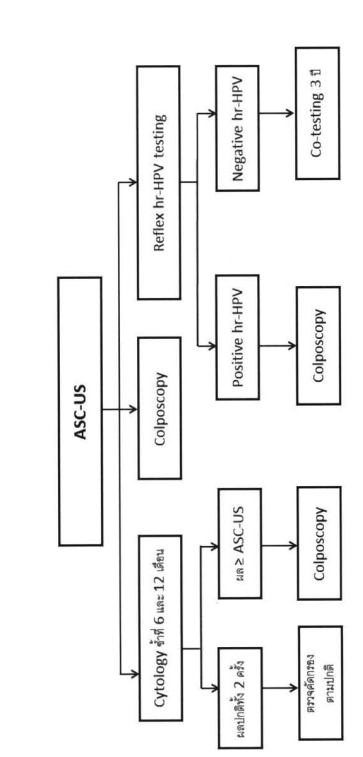
รูปที่ 4 แนวทางการดูแลผู้ป่วยที่ผลการคัดกรองเป็น ASC-US (6)
LSIL มีโอกาสพบ histologic HSIL or AIS ประมาณ 10-30% และพบ invasive cancer 1-2%
ASC-H มีโอกาสพบ histologic HSIL หรือ AIS ประมาณ 11-61% และพบ invasive cancer 1.3-8% ดังนั้นแนะนำให้ส่งตรวจ colposcopy และทำ ECS (รูปที่ 5)
ถ้าผลปกติตลอด 2 ปี 🡪 routine screening
ถ้าผลปกติตลอด 2 ปี 🡪 High-risk HPV testing หรือ co-testing ทุก 3 ปี
ถ้า High-risk HPV testing หรือ co-testing ผิดปกติ 🡪 colposcopy
ถ้า cervical cytology ≥ ASC-H 🡪 LEEP/LLETZ/CKC
ถ้า cervical cytology: ASC-US or LSIL 🡪 Colposcopy
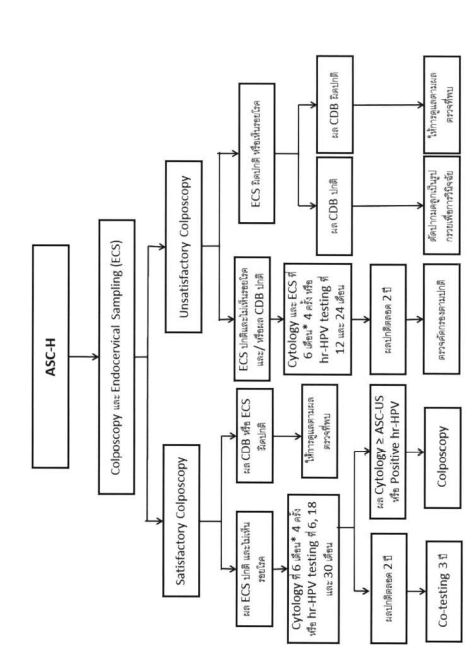
รูปที่ 5 แนวทางการดูแลผู้ป่วยที่ผลคัดกรองมะเร็งปากมดลูกเป็น ASC-H (6)
HSIL มีโอกาสพบ histologic HSIL หรือ AIS ประมาณ 26-75% และพบ invasive cancer 4.5-20% จึงควรได้รับการตรวจวินิจฉัยทันที โดยมี 2 แนวทาง ดังนี้ (รูปที่ 6)
ถ้าผลปกติทั้งหมด 🡪 co-testing ทุก 3 ปี (หรือ cytology ทุก 1 ปี)
ถ้า cytology ≥ ASC-H 🡪 LEEP/LLETZ/CKC
ถ้า cytology เป็น ASC-US หรือ LSIL 🡪 Colposcopy
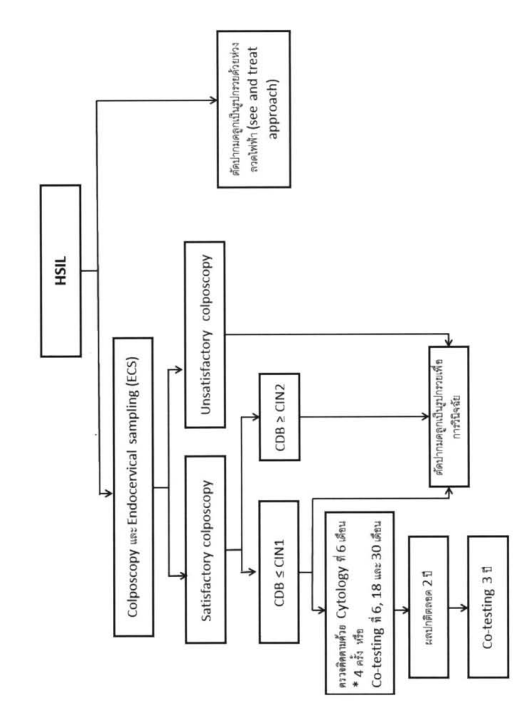
รูปที่ 6 แนวทางการดูแลผู้ป่วยที่ผลคัดกรองมะเร็งปากมดลูกเป็น HSIL (6)
Primary HPV screening
การตรวจ primary HPV screening มีแนวโน้มที่จะใช้เพิ่มมากขึ้นในอนาคต เนื่องจากเป็นการตรวจคัดกรองที่มีประสิทธิภาพมากกว่าการตรวจทาง cytology เพียงอย่างเดียว และมีค่าใช้จ่ายต่ำกว่าการคัดกรองด้วย co-testing ในรายที่ HPV-16 positive และ HPV-18 positive มีความเสี่ยงต่อ CIN3 และ occult cancer สูงมาก ดังนั้นจึงมี diagnostic procedure เพิ่มเติมกรณี HPV positive
ตาม 2019 ASCCP guidelines แนะนำดังนี้ (7)
(ถ้าไม่สามารถทำ reflex cytology ได้ สามารถส่งต่อผู้ป่วยเพื่อทำ colposcopy และเก็บ cytology ก่อนทำ colposcopy ได้)
ตามแนวทางเวชปฏิบัติของราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย เรื่อง การตรวจคัดกรองมะเร็งปากมดลูก พ.ศ. 2564 ได้มีคำแนะนำกรณี HPV testing positive ดังนี้ (4) (รูปที่ 7)
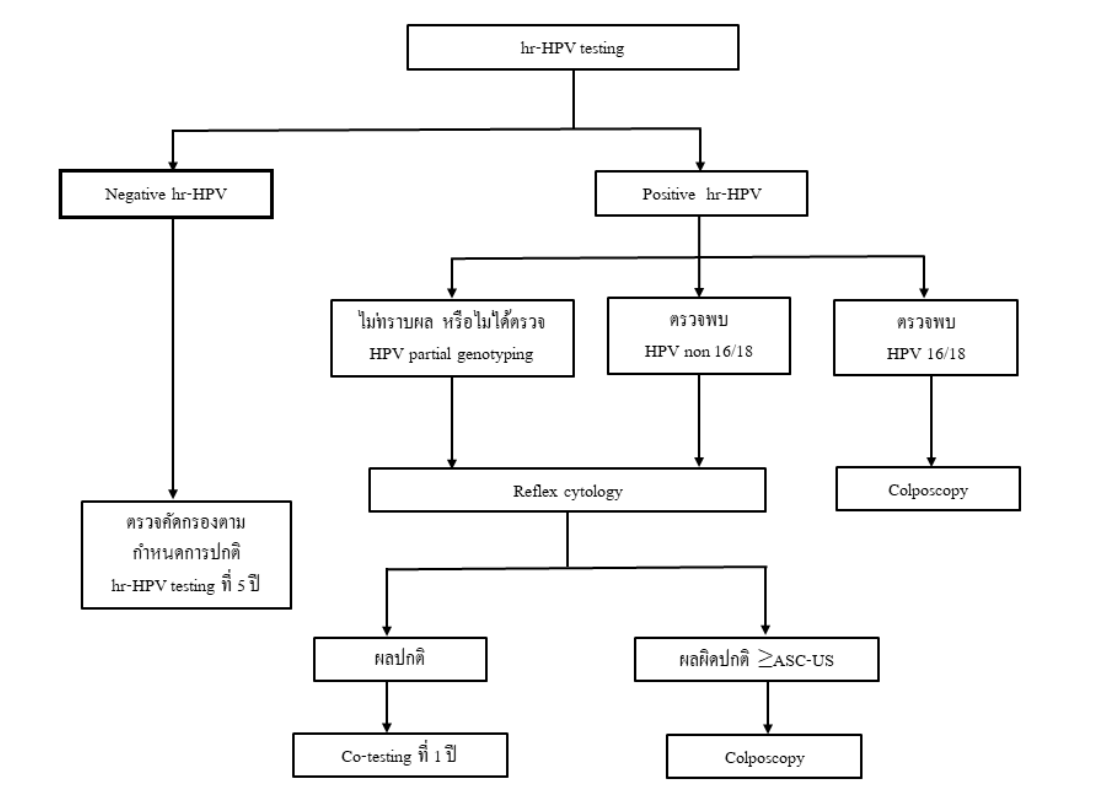
รูปที่ 7 แนวทางการดูแลผู้ป่วยที่คัดกรองมะเร็งปากมดลูกด้วย primary HPV screening (4)
AGC มีต้นกำเนิดได้จาก polyp, metaplasia หรือ neoplasia และอาจพบความผิดปกติได้จากทั้งบริเวณ endocervix, endometrium, ovary, fallopian tube หรืออวัยวะอื่นๆ เช่น ลำไส้ใหญ่ (6) 2019 ASCCP guideline จึงแนะนำแนวทางสำหรับสตรีที่ไม่ตั้งครรภ์ในทุกช่วงอายุ และผลคัดกรองเป็น AGC และ AIS ทุกประเภท ยกเว้น atypical endometrial cells ดังนี้ (รูปที่ 7) (7)
(ไม่แนะนำให้ทำ reflex HPV testing หรือตรวจ cytology ซ้ำ)
Atypical endometrial cells มีแนวทางการดูแลดังนี้ (รูปที่ 8) (7)
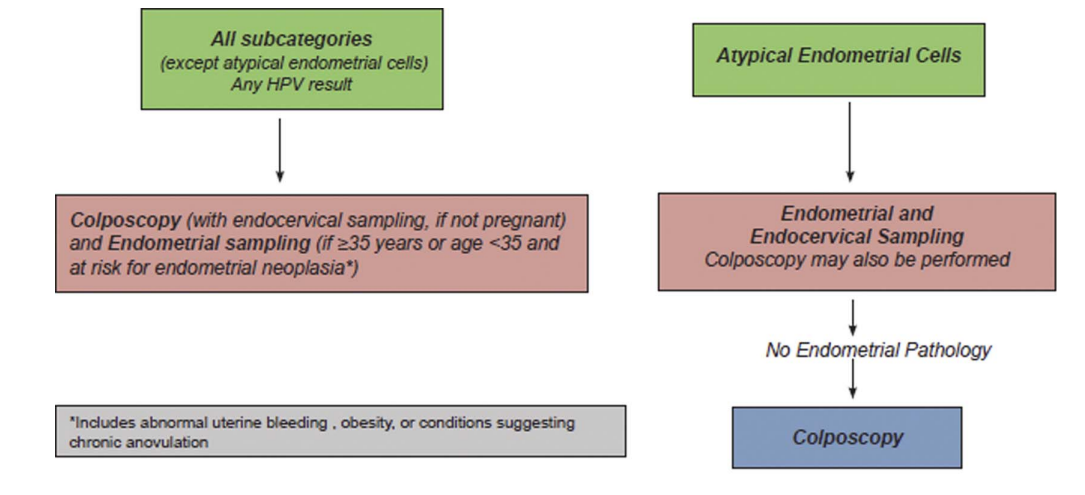
รูปที่ 8 แนวทางการดูแลผู้ป่วยที่ผลคัดกรองมะเร็งปากมดลูกเป็น AGC, AIS หรือ atypical endometrial cells (7)
Subsequent Management
สำหรับรายที่ cytology เป็น AGC not otherwise specified (AGC-NOS) หรือ atypical endocervical cells not otherwise specified (AEC-NOS) และตรวจทาง histology แล้วมีแนวทางการตรวจติดตามดังนี้ (7) (รูปที่ 8)
สำหรับรายที่ cytology เป็น AGC (favor neoplasia) หรือ AIS แล้วผลตรวจทาง histology ไม่พบ AIS หรือ cancer แนะนำทำ diagnostic excisional procedure และ endocervical sampling เหนือ excisional bed ต่อ (7) (รูปที่ 9)
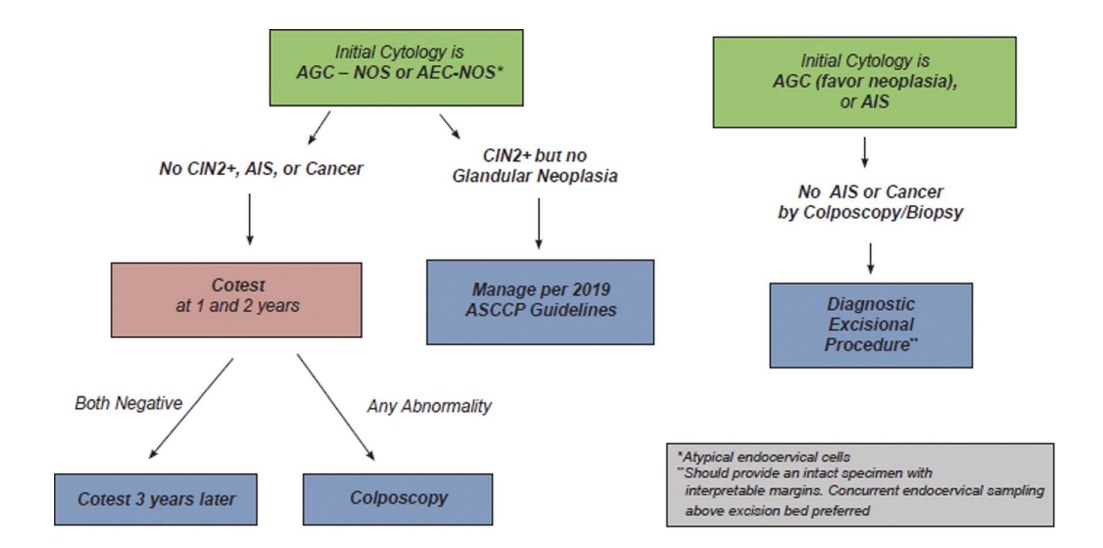
รูปที่ 9 แนวทางการติดตามผู้ป่วยที่ผลคัดกรองมะเร็งปากมดลูกเป็น AGC หรือ AIS (7)
สำหรับรายที่ผลการตรวจคัดกรองทาง cytology เป็น unsatisfactory cytology มีแนวทางการดูแลตาม 2019 ASCCP guideline ดังนี้ (7) (รูปที่ 10)
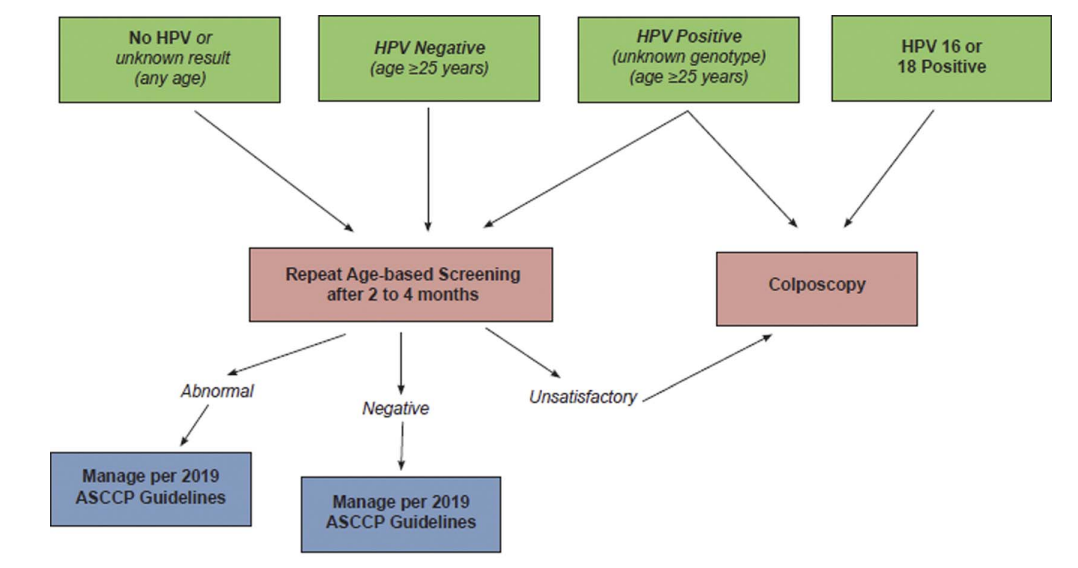
รูปที่ 10 แนวทางการดูแลผู้ป่วยที่ผลคัดกรองมะเร็งปากมดลูกเป็น unsatisfactory cytology (7)
แนวทางการดูแลตาม 2019 ASCCP guideline จะแบ่งตามช่วงอายุ ดังนี้ (7) (รูปที่ 11)
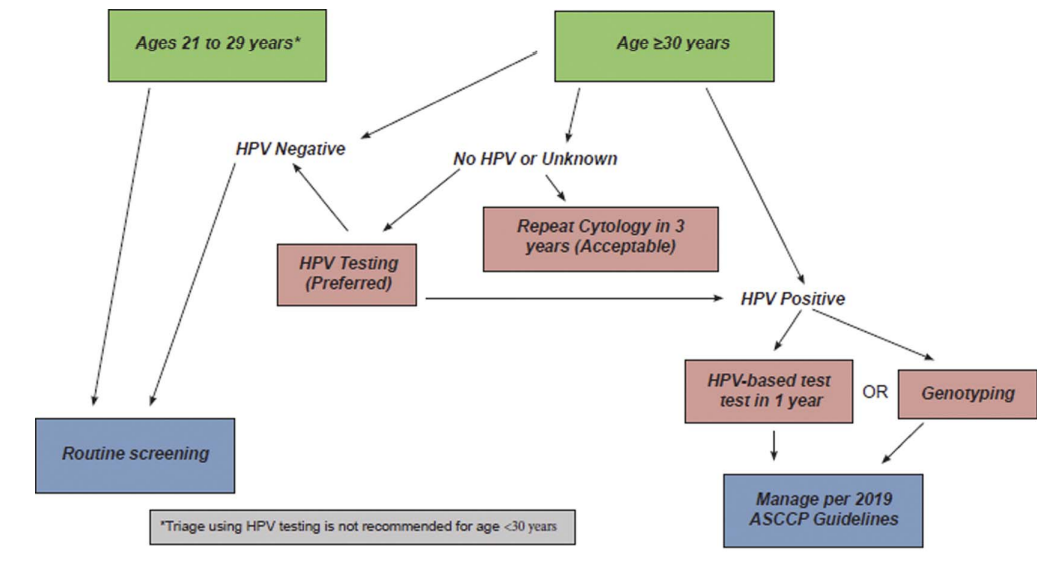
รูปที่ 11 แนวทางการดูแลผู้ป่วยที่ผลคัดกรองมะเร็งปากมดลูกเป็น absent transformation zone ร่วมกับ NILM (7)
แนวทางการดูแลตาม 2019 ASCCP guideline มีดังนี้ (7)
Managing Histologic Results
เนื่องจากไม่สามารถระบุได้ว่ามี CIN3 หรือไม่ ดังนั้นควรดูแลเหมือนเป็น CIN3 เพื่อความปลอดภัยของผู้ป่วย
เนื่องจาก CIN3 เป็น immediate cancer precursor ดังนั้นควรรักษา ไม่ควร observe ยกเว้น กรณีตั้งครรภ์
(CIN2 หายได้เอง 50% persist 32% และเป็น CIN3+ 18%)
Observation สมามรถทำได้โดยการทำ colposcopy ร่วมกับ HPV-based testing ทุก 6 เดือน จนครบ 2 ปี (รูปที่ 12)
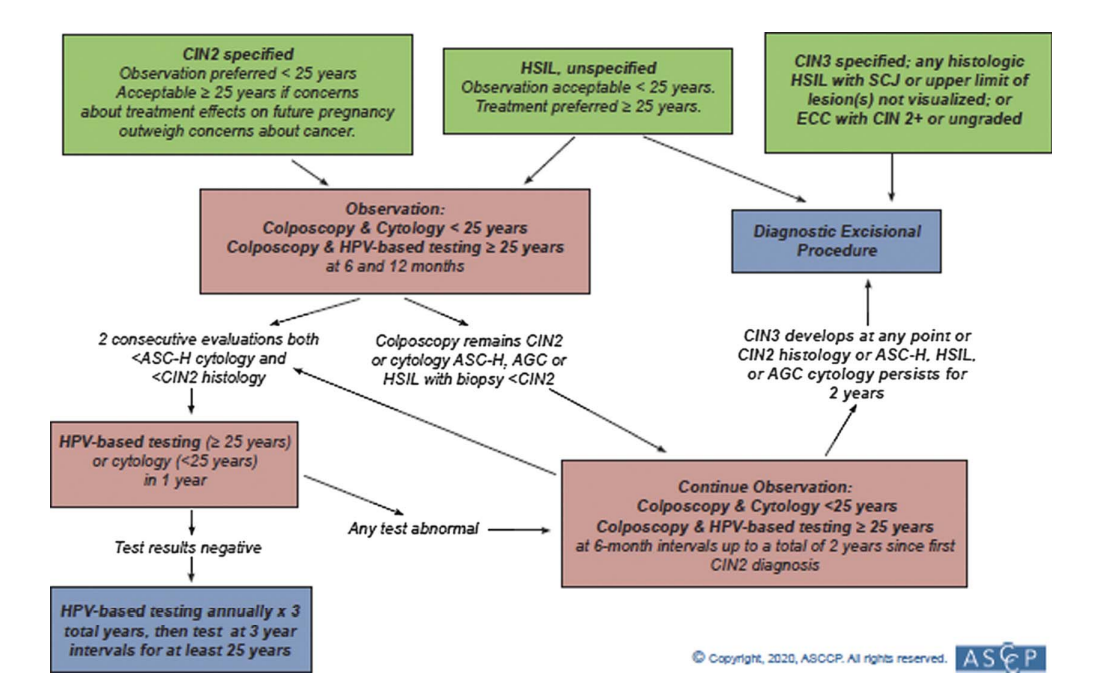
รูปที่ 12 แนวทางการดูแลผู้ป่วยที่มีผล histologic HSIL (CIN2) ที่ต้องการ observation (7)
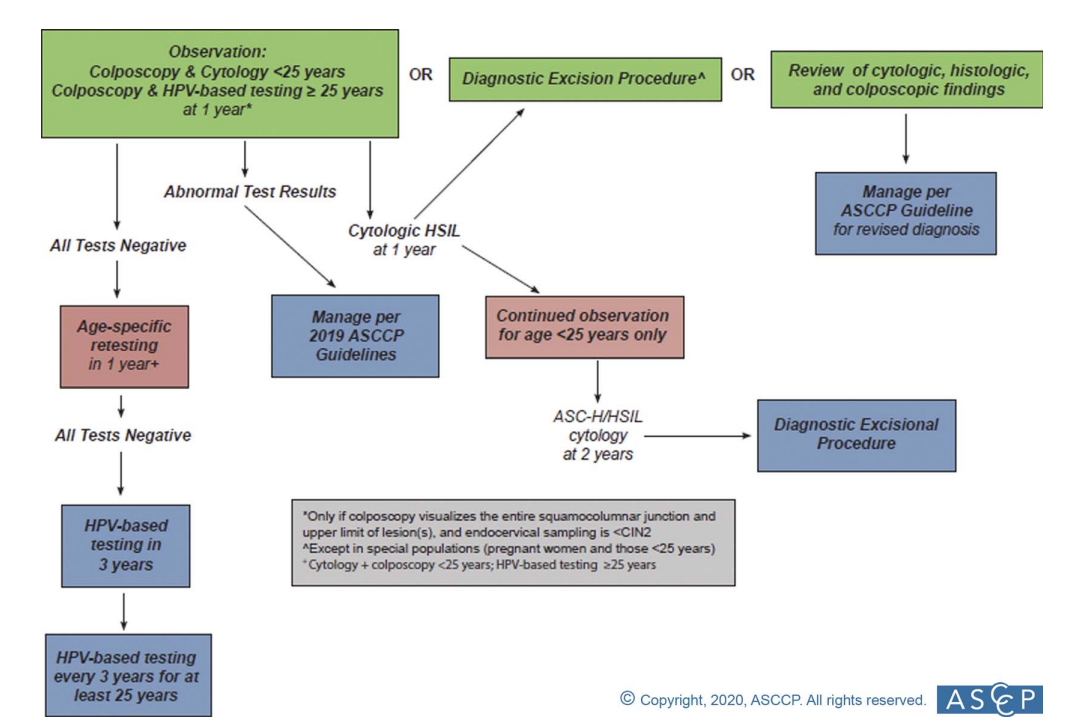
รูปที่ 13 แนวทางการดูแลผู้ป่วยที่มีผล histologic LSIL (CIN) ตามหลัง HSIL cytology (7)
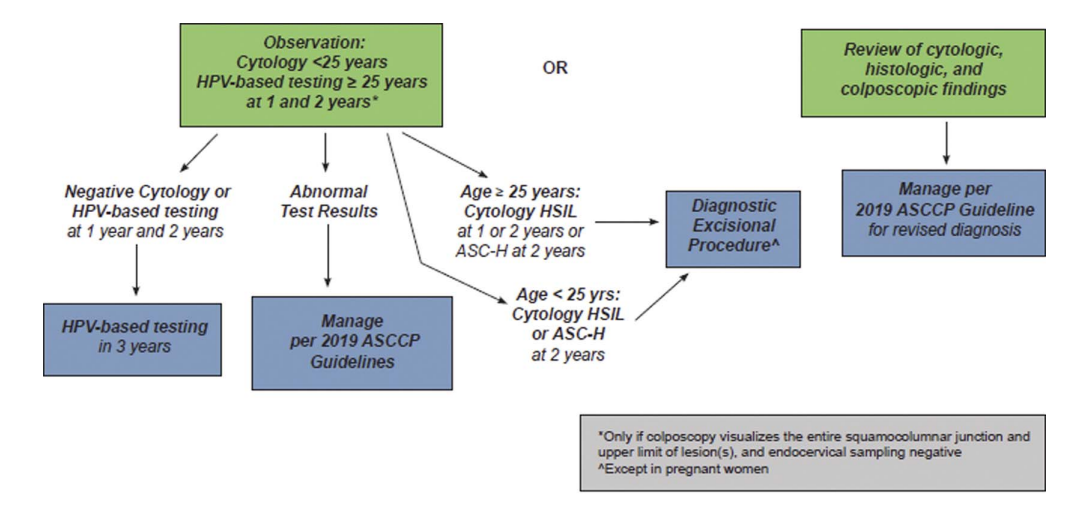
รูปที่ 14 แนวทางการดูแลผู้ป่วยที่มีผล histologic LSIL (CIN) ตามหลัง ASC-H cytology (7)
เนื่องจากกรณีนี้มี immediate estimated CIN3+ risk น้อยกว่า 25% ตาม 2019 ASCCP guideline แนะนำให้ observation แต่ถ้าผู้ป่วยต้องการการรักษาก็สามารถทำได้ ซึ่งสามารถทำได้ทั้ง excision และ ablation
เนื่องจากต้องหา invasive adenocarcinoma ถึงแม้จะวางแผน hysterectomy ก็ควรทำ excisional procedure ก่อนเพื่อดู margin status
ถ้า negative ตลอด 5 ปี 🡪 surveillance ทุก 3 ปีจน hysterectomy หรืออย่างน้อย 25 ปี
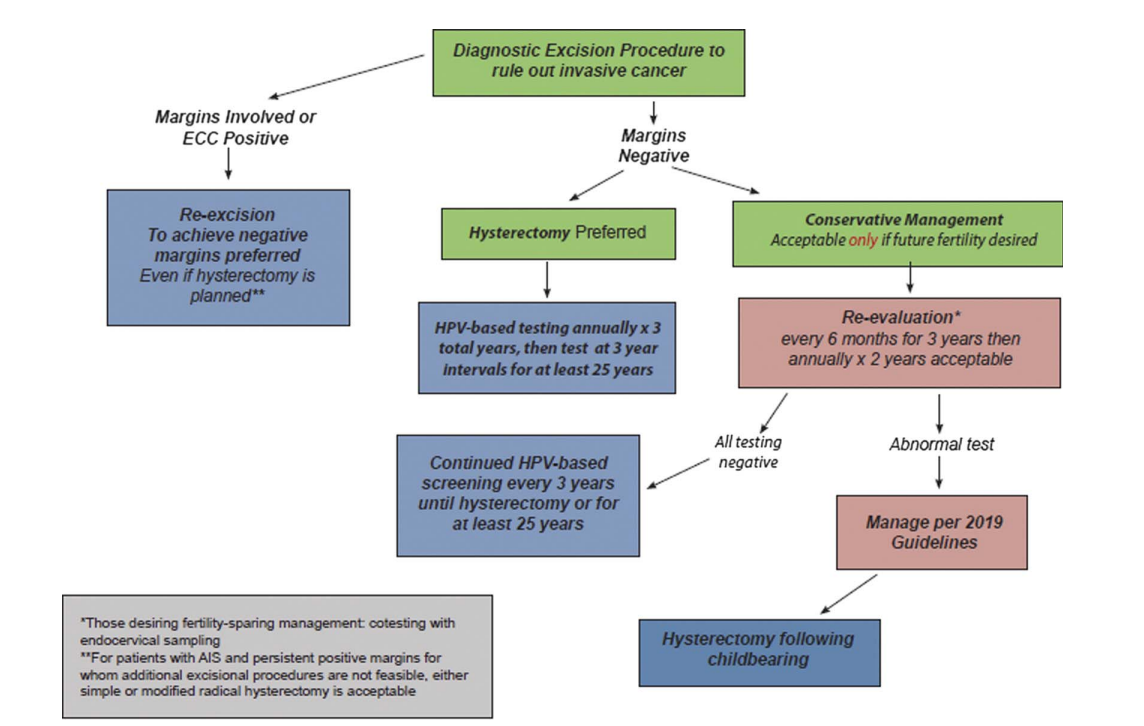
รูปที่ 15 แนวทางการดูแลผู้ป่วยที่มีผล AIS (7)
Surveillance after abnormalities
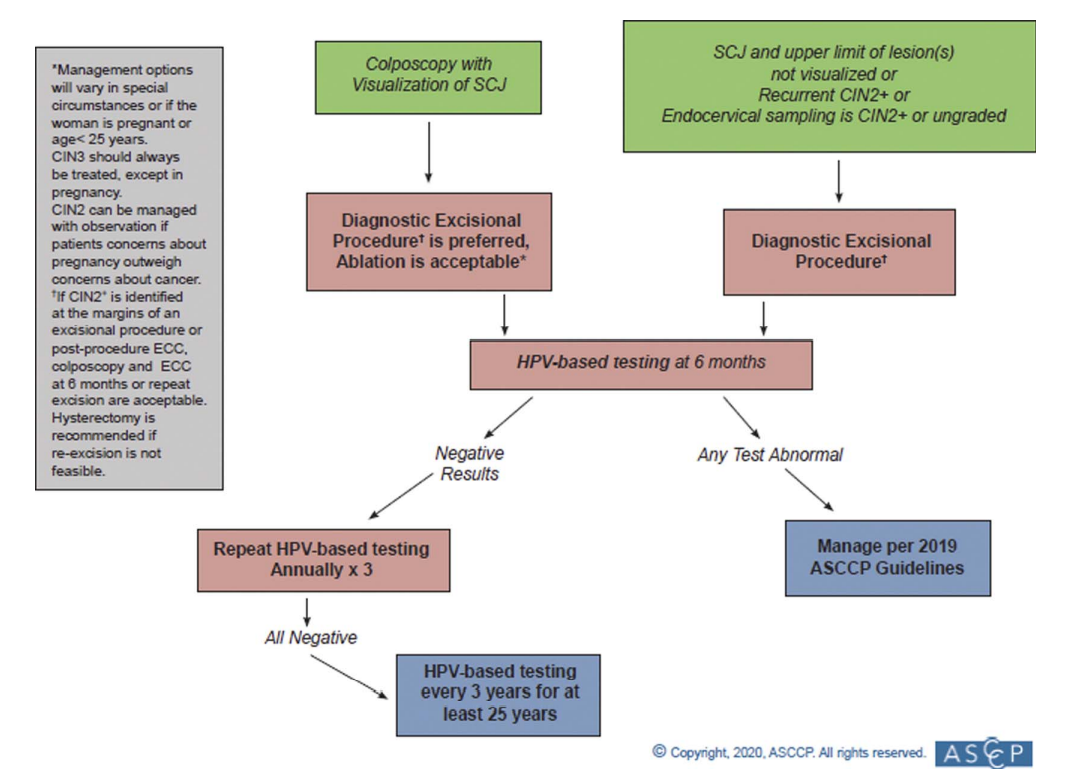
รูปที่ 16 แนวทางการดูแลผู้ป่วยที่มีผล histologic HSIL
แนะนำ surveillance ตาม risk estimation data
Special populations
แนวทางการดูแลข้างต้นที่กล่าวมาสามารถใช้ได้กับผู้ป่วยที่มีปากมดลูกและมีอายุ 25-65 ปี แต่ก็ยังมีผู้ป่วยบางกลุ่มที่จะมีแนวทางการดูแลที่แตกต่างออกไป ดังนี้
🡪 ตรวจ cytology ซ้ำอย่างเดียวที่ 1 ปี
(ไม่แนะนำให้ทำการรักษาทันทีโดยที่ไม่มี histology ยืนยันการวินิจฉัย เนื่องจากมีอัตราการหายจาก CIN2+ สูง และมีอันตรายจากการรักษาร่วมด้วย)
ถ้ายังคง ASC-H หรือ HSIL cytology อยู่เมื่อตรวจซ้ำ 2 ปี
🡪 Diagnostic excision procedure
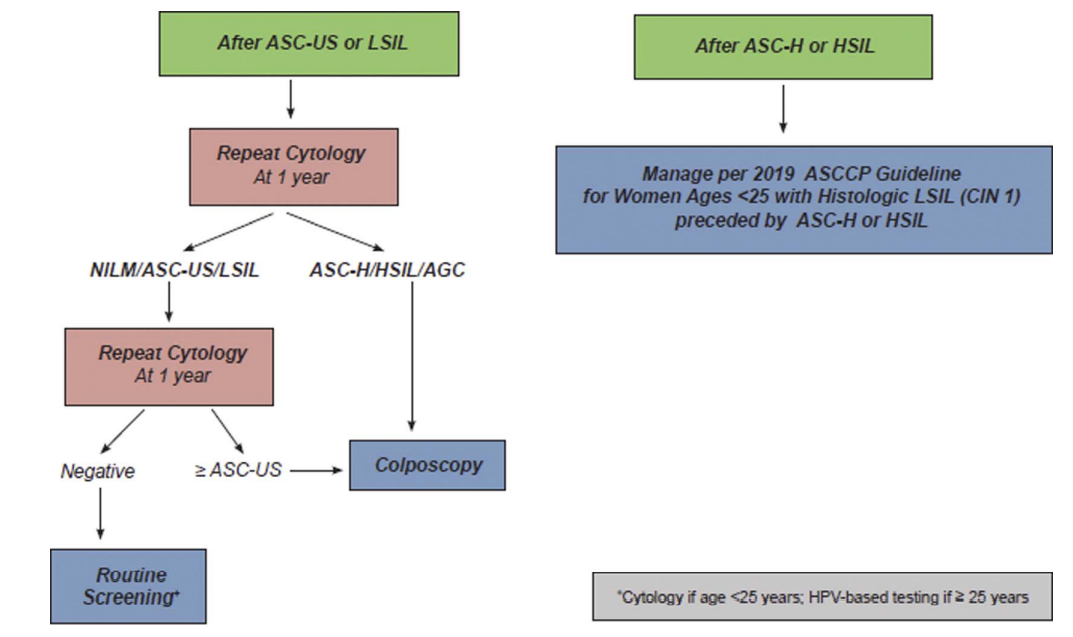
รูปที่ 17 แนวทางการดูแลผู้ป่วยที่อายุน้อยกว่า 25 ปี (7)
สตรีตั้งครรภ์ถือเป็นกลุ่มที่มีการดูแลแตกต่างออกไป เนื่องจากต้องพิจารณาแนวทางการดูแลโดยคำนึงถึงความเสี่ยงต่อมารดาและทารก และความเสี่ยงในการพลาดการวินิจฉัยมะเร็ง นอกจากนี้สตรีตั้งครรภ์ยังมีการเปลี่ยนแปลงทางสรีรวิทยาที่ทำให้ค้นหามะเร็งและรอยโรคก่อนมะเร็งที่คลาดเคลื่อนไป
แนวทางการดูแลผุ้ป่วยที่ตั้งครรภ์และมีผลการคัดกรองมะเร็งปากมดลูกผิดปกตินั้น ให้การดูแลตาม Clinical Action Thresholds สำหรับ surveillance และ colposcopy เหมือนในผู้ป่วยที่ไม่ตั้งครรภ์ แต่อาจมีข้อแตกต่างบางประการ ดังนี้ (7)
ผู้ป่วยในกลุ่ม immunocompromised ได้แก่ HIV infection, solid organ transplant, SLE, inflammatory bowel disease, rheumatologic disease ที่ต้องได้ยากดภูมิคุ้มกัน มีการศึกษาพบว่าผู้ป่วย HIV ที่อายุน้อยกว่า 21 ปี และมีเพศสัมพันธ์ มีความเสี่ยงในการเป็นรอยโรคก่อนมะเร็งมากกว่าในกลุ่มประชากรปกติ จึงมีคำแนะนำตาม 2019 ASCCP guideline ดังนี้ (7)
ผู้ป่วยที่ผ่าตัดมดลูกมีแนวทางการดูแลตาม 2019 ASCCP guideline ดังนี้ (7)
🡪 ไม่แนะนำการตรวจคัดกรองต่อ
เนื่องจากพบ cervical cancer ประมาณ 20% ในผู้ป่วยอายุมากกว่า 65 ปี ดังนั้นในรายที่ตรวจพบความผิดปกติจึงมีแนวทางการดูแลต่อเหมือนในรายที่อายุ 25-65 ปี และไม่แนะนำให้หยุด surveillance ในผู้ป่วยที่ยังสุขภาพแข็งแรง แต่สามมารถหยุด surveillance ต่อในรายที่มี life expectancy จำกัด
โรคปอดเป็นสิ่งที่พบได้บ่อยขณะตั้งครรภ์ มีการศึกษาพบว่าโรคหอบหืดและโรคปอดอักเสบเป็นสาเหตุของการรักษาตัวในโรงพยาบาลระหว่างตั้งครรภ์ที่ไม่ได้เกิดจากภาวะทางสูติศาสตร์ถึงร้อยละ 10 และการตั้งครรภ์ส่งผลให้โรคปอดรุนแรงมากขึ้นได้เนื่องจากมีการเปลี่ยนแปลงทางสรีรวิทยาของระบบทางเดินหายใจ โดยเฉพาะช่วงไตรมาสสุดท้ายของการตั้งครรภ์ (1)
ขณะตั้งครรภ์ กระบังลม (diaphragm) จะยกสูงขึ้นประมาณ 4 ซม. Subcostal angle กว้างมากขึ้น เส้นรอบวงทรวงอก (thoracic circumference) มากขึ้นประมาณ 6 ซม. AP diameter ของทรวงอกเพิ่มขึ้นประมาณ 2 ซม. แต่ไม่สามารถป้องกันการลดของ residual lung volumes ที่เกิดจากการยกขึ้นของกระบังลมได้ ทำให้เกิดอาการเหนื่อยขณะตั้งครรภ์ได้ (1)
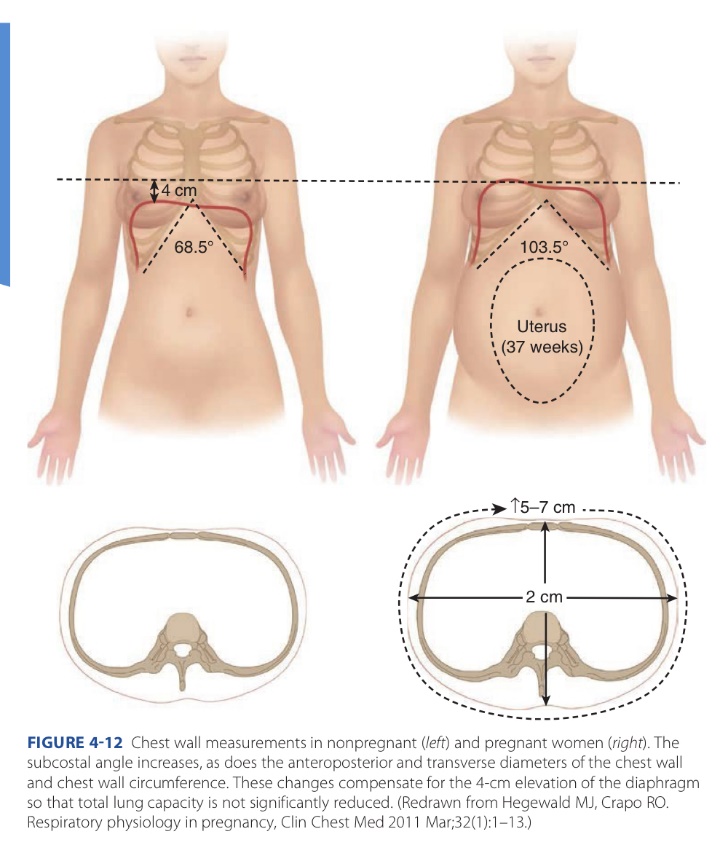
รูปที่ 1 ขนาดผนังทรวงอกในสตรีที่ไม่ได้ตั้งครรภ์ (ซ้าย) ในสตรีตั้งครรภ์ (ขวา) จาก Williams Obstetrics, 26th ed, 2022 (1)
การเปลี่ยนแปลงที่เกิดขึ้นระหว่างตั้งครรภ์ทำให้เกิด hyperventilation เนื่องจากต้องหายใจลึกขึ้นแต่ไม่ได้เพิ่มอัตราการหายใจ ซึ่งเกิดจากมี oxygen consumption ที่เพิ่มมากขึ้นระหว่างตั้งครรภ์จาก 20 เป็น 40 mL/min ในช่วงไตรมาสที่ 2 ของการตั้งครรภ์ (1)
โรคหอบหืดเป็นโรคที่เกิดจากการอักเสบเรื้อรังของท่อหายใจ (Chronic airway inflammation) ทำให้มีอาการและอาการแสดงทางระบบทางเดินหายใจ เช่น หายใจเสียงวี๊ด หายใจเหนื่อย แน่นหน้าอก และไอ ซึ่งอาการจะแตกต่างกันออกไปตามระยะเวลาและความรุนแรง ร่วมกับมี expiratory airflow limitation ที่แตกต่างกัน (2)
โรคหอบหืดเป็นโรคที่มีสาเหตุมาจากหลายปัจจัย (Heterogeneous disease) ร่วมกับมีปัจจัยกระตุ้นจากสิ่งแวดล้อม เช่น ไข้หวัดใหญ่ (Influenza) และควันบุหรี่ ซึ่งสิ่งกระตุ้นจะทำให้มี eosinophil, mast cell, T-lymphocyte เพิ่มมากขึ้น เพิ่มการหลั่ง inflammatory mediators ต่างๆ ได้แก่ histamine, leukotrienes, prostaglandins, cytokines, immunoglobulin E (IgE) และอื่นๆ ทำให้เกิดการหดรัดตัวของกล้ามเนื้อเรียบที่หลอดลม มีการคั่งของหลอดเลือด มีการหลั่งมูกมากขึ้น และเยื่อบุหลอดลมบวมซึ่งทำให้เกิดการอุดกันของหลอดลมแบบไม่ถาวร (reversible airway obstruction) (1)
โรคหอบหืดมีอาการแสดงที่รุนแรงแตกต่างกันไปตั้งแต่หายใจเสียงวี๊ดเล็กน้อยไปจนถึงมีหลอดลมตีบอย่างรุนแรง ทำให้เกิดการอุดกั้นของหลอดลมและอากาศผ่านหลอดลมได้ลดลง ต้องใช้แรงในการหายใจที่มาก เกิดอาการเหนื่อย หายใจเสียงวี๊ด แน่นหน้าอกและหายใจไม่ออก
การแบ่งความรุนแรงของโรคหอบหืดในที่นี่จะกล่าวถึงการแบ่งความรุนแรงตาม National Asthma Education and Prevention Program (NAEPP) 2020 และ Global Initiative for Asthma (GINA) 2022
| Component | Severity | |||
| Intermittent | Persistent | |||
| Mild | Moderate | Severe | ||
| Symptoms | ≤ 2 d/wk | >2 d/wk, not daily | Daily | Throughout day |
| Nocturnal awakenings | ≤2x/mo | 3-4x/mo | >1x/wk, not nightly | Often 7x/wk |
| Short-acting β-agonist for symptoms | ≤2d/wk | ≥2d/wk, but not >1x/d | Daily | Several times daily |
| Interference with normal activity | None | Minor limitation | Some limitation | Extremely limited |
| Lung function | Normal between exacerbations | |||
| FEV1 | >80% predicted | ≥80% predicted | 60-80% predicted | <60% predicted |
| FEV1/FVC | Normal | Normal | Reduced 5% | Reduced >5% |
ตารางที่ 1 การแบ่งระดับความรุนแรงของโรคหอบหืด จาก Williams Obstetrics, 26th ed, 2022 (1)
| Severity | Definition |
| Mild | Well controlled with
|
| Moderate | Well controlled with step 3 or step 4 treatment |
| Severe |
|
ตารางที่ 2 การแบ่งระดับความรุนแรงของโรคหอบหืด ตาม GINA 2022 (2)
ในรายที่มีการอุดกั้นหลอดลมถาวรหรือรุนแรงจะมีอาการที่มากขึ้นเป็นลำดับ (ภาพที่ 2) เริ่มจากมี respiratory alkalosis จากภาวะ hypoxia ทำให้เกิด hyperventilation เพื่อทำให้ระดับ PaO2 อยู่ในระดับปกติ แต่ทำให้ PaCO2 ต่ำลง เมื่อหลอดลมตีบมากขึ้น ventilation-perfusion defect มากขึ้น ก็จะเกิด hypoxemia มากขึ้น เมื่อเกิดหลอดลมอุดกั้นอย่างรุนแรง จะทำให้เกิดการคั่งของ CO2 และ ventilation ที่แย่ลง เกิดภาวะการหายใจล้มเหลวตามมา (1)
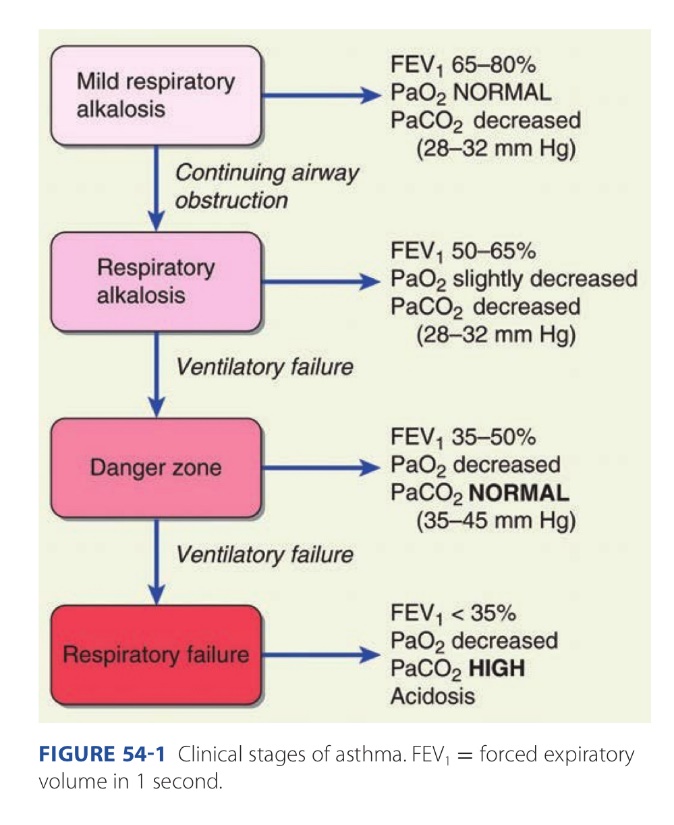
รูปที่ 2 การเปลี่ยนแปลงอาการเมื่อเกิดการอุดกั้นหลอดลมอย่างถาวรหรือรุนแรง จาก Williams Obstetrics, 26th ed, 2022 (1)
การเปลี่ยนแปลงเหล่านี้เป็นแค่ชั่วคราวสามารถกลับคืนภาวะปกติได้ ซึ่งมักไม่รุนแรงในสตรีที่ไม่ได้ตั้งครรภ์และมีสุขภาพแข็งแรง แต่ในสตรีตั้งครรภ์จะมี residual capacity ที่ลดลงจากมดลูกที่ขยายขนาดขึ้นทำให้เกิดภาวะ hypoxemia ได้ง่ายกว่า ดังนั้นในสตรีตั้งครรภ์แม้จะมีอาการของโรคหอบหืดในระยะต้น ก็สามารถทำให้เกิดอัตรายต่อมารดาและทารกในครรภ์ได้ (1)
การดำเนินโรคระหว่างการตั้งครรภ์มักไม่อาจทำนายได้ ประมาณ 1/3 อาการดีขึ้น 1/3 อาการไม่เปลี่ยนแปลง และ1/3 อาการแย่ลง การกำเริบเกิดได้บ่อยระหว่างการตั้งครรภ์ และมีแนวโน้มบ่อยขึ้นในไตรมาสที่ 2 ของการตั้งครรภ์ ในรายที่เป็นโรคหอบหืดรุนแรงจะมีโอกาสเกิดการกำเริบได้มากกว่าและมีอัตราการนอนโรงพยาบาลมากกว่า รายที่มีอาการเล็กน้อยมักไม่มีปัญหาในระหว่างการตั้งครรภ์ อัตราการกำเริบอาจเกิดได้ร้อยละ 10-20 ในระยะคลอด และอาจเพิ่มมากขึ้นหลังผ่าตัดคลอด ซึ่งมากกว่าการคลอดทางช่องคลอด (1,2,3)
โรคหอบหืดยังคงเป็นปัจจัยเสี่ยงที่ทำให้ผลการตั้งครรภ์แย่ลง แต่โรคหอบหืดไม่ถือเป็นข้อห้ามของการตั้งครรภ์ ซึ่งการรักษาและควบคุมอาการของโรคได้ดีสามารภลดภาวะแทรกซ้อนที่อาจเกิดขึ้นได้ ในกรณีที่โรคไม่รุนแรง ผลลัพธ์การตั้งครรภ์ไม่แตกต่างกับครรภ์ทั่วไป ผลต่อการตั้งครรภ์ที่พบ ได้แก่ เพิ่มอุบัติการณ์ small-for-gestational-age, perinatal mortality, ปอดอักเสบ, preeclampsia และเพิ่มอัตราการผ่าตัดคลอด ซึ่งโรคหอบหืดที่รุนแรงหรือควบคุมตัวโรคได้ไม่ดี สัมพันธ์กับ maternal and perinatal mortality rate ที่สูงมากขึ้น ซึ่งเพิ่มขึ้นชัดเจนในกรณีเกิด status asthmaticus หรือ life-threatening complications อื่นๆ เช่น ภาวะหายใจล้มเหลว ลมรั่วในปอด เป็นต้น (1,4)
สาเหตุที่เป็นไปได้ที่ทำให้ผลลัพธ์การตั้งครรภ์แย่ลง ได้แก่ ภาวะ hypoxia ของมารดาขณะที่โรคกำเริบ เกิดภาวะ respiratory alkalosis ซึ่งทำให้ fetal oxygenation และ uteroplacental blood flow ลดลง เกิด fetal hypoxia ตามมา ซึ่งโรคหอบหืดที่รุนแรงมากจะมีอัตราการเกิด fetal growth restriction ที่มากขึ้น (1)
อีกสาเหตุที่เป็นไปได้ คือ ยาโรคหอบหืดขณะตั้งครรภ์ที่มีโอกาสเป็น teratogen หรือส่งผลต่อทารกในครรภ์ได้ มีบางการศึกษาพบว่า inhaled β2-agonist อาจเพิ่มความเสี่ยงในการเกิด cleft lip and palate และ autism spectrum ได้เล็กน้อย แต่เนื่องจากโรคหอบหืดที่ควบคุมไม่ได้ส่งผลต่อทั้งมารดาและทารกในทางที่แย่ลง ดังนั้นควรพิจารณาถึงโทษและประโยชน์จากการใช้ยารักษาโรคหอบหืดอย่างระมัดระวัง (1,5,6)
การรักษาโรคหอบหืดเรื้อรังมีเป้าหมายเพื่อควบคุมอาการและป้องกันการกำเริบ ซึ่งแนวทางการรักษาด้วยยาแบ่งตามระดับความรุนแรงของอาการเหมือนในสตรีที่ไม่ตั้งครรภ์ แนวทางปฏิบัติที่เป็นมาตรฐานมีหลายแนวทาง ซึ่งในที่นี้จะกล่าวถึงแนวทางปฏิบัติของ National Asthma Education and Prevention Program (NAEPP) 2020 และ แนวทางปฏิบัติของ Global Initiative for Asthma (GINA) 2022
แนวทางการรักษาตาม NAEPP 2020 (9) เป็นแบบ stepwise approach คือ การรักษาจะเพิ่มทีละขั้นจนกว่าจะควบคุมอาการได้ และลดการรักษาที่ละขั้นหลังสามารถควบคุมอาการได้อย่างน้อย 3 consecutive month แบ่ง step การรักษาเป็น 6 step ได้แก่ (รูปที่ 3)
รูปที่ 3 Stepwise approach for management of asthma ในคนอายุ 12 ปีขึ้นไป จาก Managing asthma in adolescents and adults 2020 Asthma guideline update from the national asthma education and prevention program, JAMA 2020 (9)
อีกแนวทางการรักษาหนึ่ง คือ แนวทางการรักษาตาม GINA 2022 (2) จะแบ่งการรักษาเป็น 2 track
การรักษาจะแบ่งการรักษาเป็น 5 step ซึ่งสามารถ step up การรักษาถ้าควบคุมโรคไม่ได้ และ step down การรักษาได้เมื่อควบคุมโรคได้ดี (รูปที่ 4)
แม้ว่ายาที่ใช้รักษาโรคหอบหืด ยังไม่ทราบ adverse effect ต่อการตั้งครรภ์ที่แน่ชัด แต่การรักษาโรคหอบหืดระหว่างตั้งครรภ์ถือว่ามีประโยชน์มากกว่าความเสี่ยงที่จะเกิดขึ้นถ้ามีอาการกำเริบระหว่างตั้งครรภ์ (2) ซึ่งชนิดของยาและขนาดยารักษาโรคหอบหืดเรื้อรัง เป็นดังรูปที่ 4 (1)
การตรวจติดตามโรคหอบหืดขณะตั้งครรภ์ แนะนำให้ติดตามทุกเดือน แม้ว่าในรายที่ควบคุมอาการได้ดีโดยไม่ต้องใช้ controller หรือไม่มีอาการกำเริบมาก่อนจะมีความเสี่ยงต่ำที่จะเกิดการกำเริบระหว่างตั้งครรภ์ แต่ก็ควรได้รับการตรวจติดตามอย่างใกล้ชิด (2)
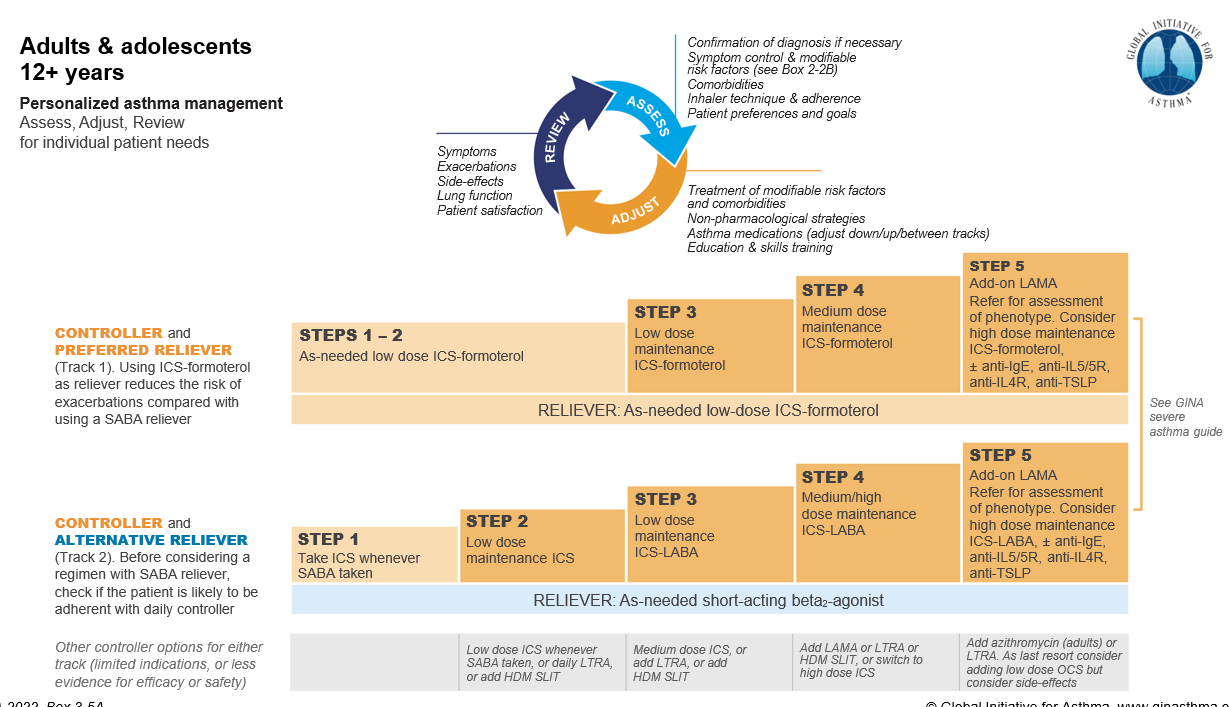
รูปที่ 3 Management of asthma ในคนอายุ 12 ปีขึ้นไป จาก GINA 2022 (2)
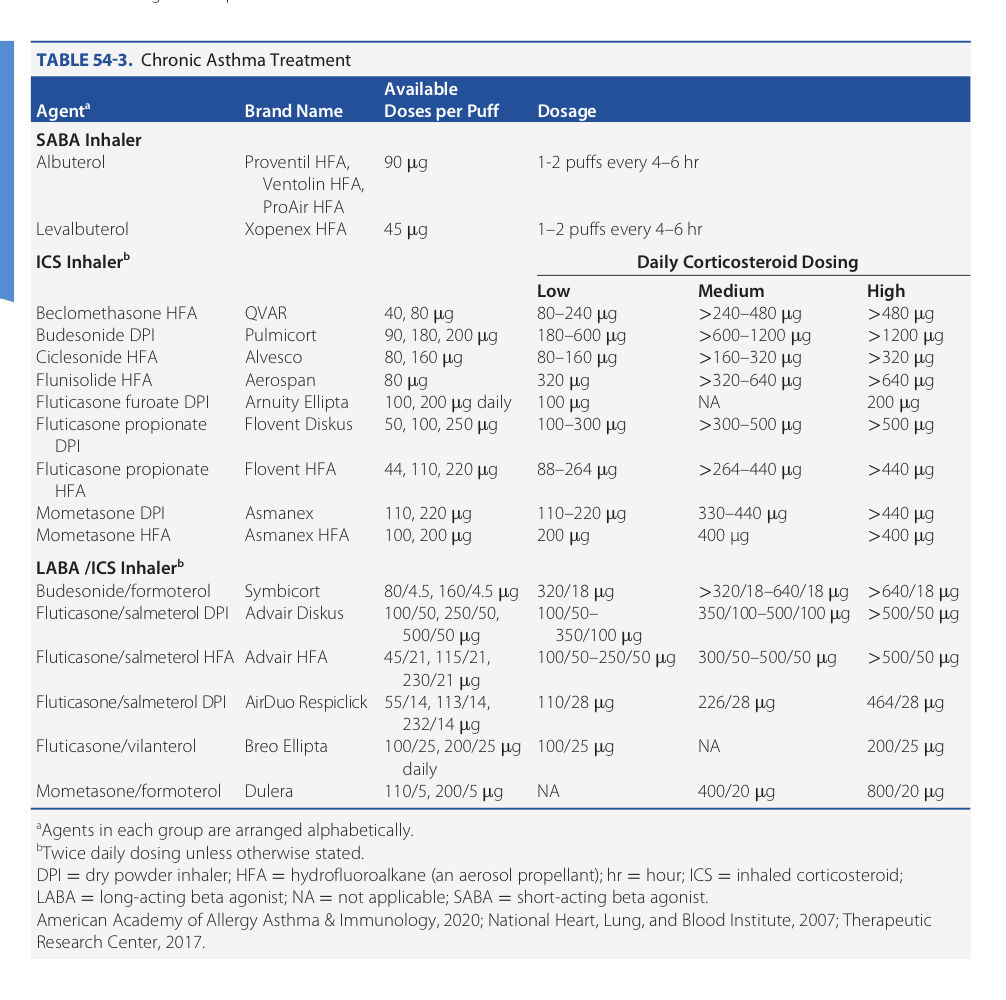
รูปที่ 4 ชนิดและขนาดยาที่ใช้ในการรักษาโรคหอบหืดเรื้อรัง จาก Williams Obstetrics, 26th ed, 2022 (1)
การรักษาโรคหอบหืดกำเริบเฉียบพลันในสตรีตั้งครรภ์คล้ายกับสตรีไม่ตั้งครรภ์ แต่เกณฑ์การนอนโรงพยาบาลสำหรับสตรีตั้งครรภ์ควรต่ำกว่าสตรีไม่ตั้งครรภ์อย่างชัดเจน เมื่อคนไข้มาโรงพยาบาลด้วยอาการกำเริบควรประเมินสัญญาณชีพและตรวจร่างกายเพื่อประเมินความรุนแรงของการกำเริบ และให้การรักษาตามระดับความรุนแรงนั้นๆ (แผนผังที่ 1) (2)
ให้ low flow oxygen ผ่าน nasal canulae หรือ mask เพื่อให้ oxygen saturation อยู่ระหว่าง 93-95%
ควรอยู่ท่านั่งหรือนอนตะแคง มากกว่านอนหงาย โดยเฉพาะไตรมาสที่ 3 ของการตั้งครรภ์ เพื่อหลีกเลี่ยง aortocaval compression จากมดลูกที่โตขึ้นขณะตั้งครรภ์
Continuous electronic fetal monitoring แต่ก็ขึ้นกับอายุครรภ์ด้วย
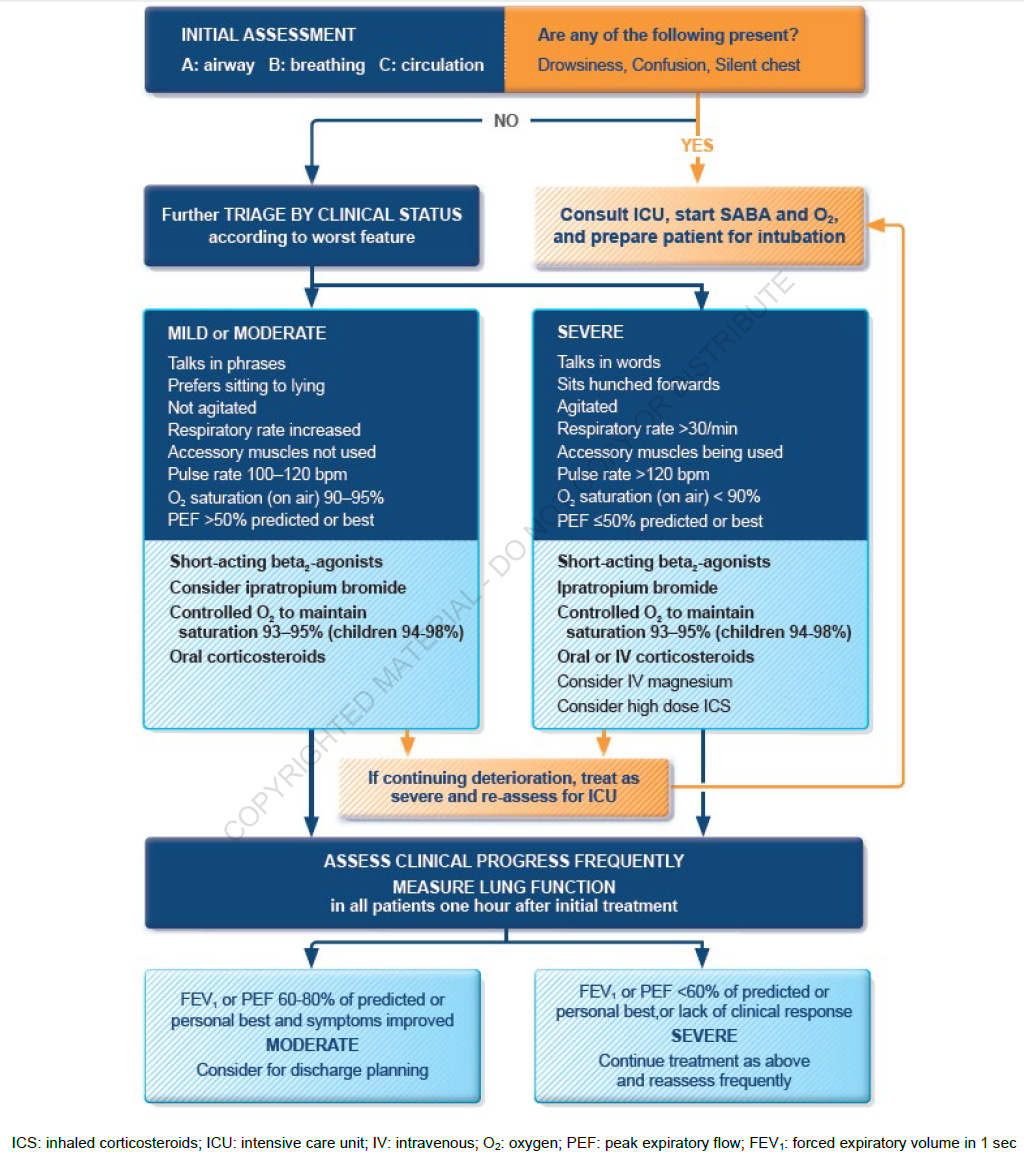
แผนผังที่ 1 แนวทางการรักษาโรคหอบหืดกำเริบเฉียบพลัน จาก GINA 2022 (2)
ขนาดยาและวิธีใช้ตามตารางที่ 2 (10)
ในสตรีตั้งครรภ์ การรักษาอาการกำเริบควรเป็นการรักษาแบบ aggressive ด้วย SABA, oxygen และ early corticosteroid เพื่อป้องกัน fetal hypoxemia หลังการรักษาเบื้องต้น ควรประเมินการตอบสนองต่อการรักษาเป็นระยะ และตรวจ pulmonary function test หลังการรักษา 1 ชั่วโมง เช่น หลังได้ bronchodilator 3 doses เป็นต้น ในรายที่มีอาการรุนแรงไม่ตอบสนองต่อการรักษาหลังได้ intensive bronchodilator และ corticosteroid หรือ status asthmaticus ควรประเมินผู้ป่วยซ้ำอีกครั้ง พิจารณารักษาใน intensive care ในสตรีตั้งครรภ์ควรพิจารณา early intubation กว่าคนทั่วไป (1)

ตารางที่ 2 ขนาดยาและวิธีใช้ จาก Management of asthma during pregnancy www.UpToDate.com (10)
การดูแลระยะคลอด (Intrapartum management) (1,7,10)
ยาที่ใช้รักษาโรคหอบหืดผ่านทางน้ำนมเพียงเล็กน้อย การใช้ prednisolone, theophylline, antihistamines, inhaled corticosteroid และ β2-agonist ไม่ได้เป็นข้อห้ามของการให้นมบุตร (7)