Ectopic Pregnancy: การตั้งครรภ์นอกมดลูก
พญ.คันธารัตน์ หลวงฟอง
ที่ปรึกษา ผศ.นพ.มนัสวี มะโนปัญญา
การตั้งครรภ์นอกมดลูก หมายถึง การตั้งครรภ์ที่เกิดขึ้นภายนอกโพรงมดลูก(1) มีอุบัติการณ์ประมาณร้อยละ 1-2 ของการตั้งครรภ์(2, 3) โดยภาวะ ruptured ectopic pregnancy นำไปสู่การเสียชีวิตได้มากถึงร้อยละ 2.7(4) ดังนั้นการตั้งครรภ์นอกมดลูกจึงเป็นภาวะสำคัญและฉุกเฉินทางสูตินรีเวชกรรม(1)
ประเภทของการตั้งครรภ์นอกมดลูกแบ่งตามตำแหน่งการฝังตัว ดังนี้ คือ ตั้งครรภ์ที่ท่อนำไข่บริเวณ ampullar (มากกว่าร้อยละ 70) บริเวณ isthmus (ร้อยละ 12) และบริเวณ fimbria (ร้อยละ 11) รังไข่ (ร้อยละ 3) Cornue (ร้อยละ 2-3) ในช่องท้อง (ร้อยละ 1) ปากมดลูก (น้อยกว่าร้อยละ 1) Cesarean scar (น้อยกว่าร้อยละ 1)(5) ดังแสดงในรูปที่ 1
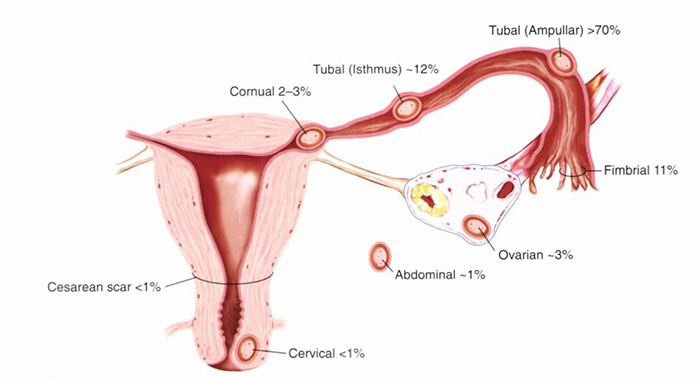
รูปที่ 1 แสดงตำแหน่งที่พบบ่อยของครรภ์นอกมดลูก
ที่มา: คัดลอกจาก Jonathan S. Berek, Deborah L. Berek. Berek & Novak’s Gynecology: Ectopic pregnancy. 16th ed: Wolters Kluwer; 2020.
โดยการตั้งครรภ์อาจจะดำเนินไปได้หลายรูปแบบ คือ ท่อนำไข่แตก ฝ่อไปเอง หรือแท้งออกไปทาง fimbria (tubal abortion) แต่มีบางรายที่แท้งแล้วแต่รกยังทำงานอยู่และไปฝังตัวต่อที่อื่น(6)
ปัจจัยส่งเสริมการตั้งครรภ์นอกมดลูก
- เคยตั้งครรภ์นอกมดลูกมาก่อน เพิ่มความเสี่ยงของการเกิดซ้ำร้อยละ 10-15 แต่ถ้าหากเคยตั้งครรภ์นอกมดลูกมาแล้ว 2 ครั้งความเสี่ยงจะสูงถึงร้อยละ 30 (7)
- มีประวัติท่อนำไข่บาดเจ็บมาก่อน เช่น เคยผ่าตัดบริเวณท่อนำไข่ มีพังผืดบริเวณอุ้งเชิงกราน หรือเคยติดเชื้อในอุ้งเชิงกราน(8)
- ภาวะมีบุตรยากมีโอกาสตั้งครรภ์นอกมดลูกเพิ่มขึ้น โดยเฉพาะการตั้งครรภ์จากเทคโนโลยีช่วยเจริญพันธุ์(8, 9)
- การสูบบุหรี่(5, 10)
- การคุมกำเนิดบางชนิด โอกาสตั้งครรภ์นอกมดลูกจะสูงขึ้นเมื่อตั้งครรภ์หลังจากใช้ห่วงคุมกำเนิดและการทำหมัน(6, 11)
การวินิจฉัยการตั้งครรภ์นอกมดลูก
การตั้งครรภ์นอกมดลูกไม่มีอาการจำเพาะ แต่มีอาการหลายๆ อย่างร่วมกัน กลุ่มอาการทางคลินิกที่พบร่วมได้บ่อย (Classic triad) คือ การขาดระดู มีอาการปวดท้องน้อย และมีเลือดออกผิดปกติทางช่องคลอด ซึ่งสามารถพบได้ประมาณร้อยละ 50 ของผู้ป่วย(12) ดังนั้นสตรีวัยเจริญพันธุ์ที่มีอาการปวดท้องหรือเลือดออกผิดปกติทางช่องคลอดควรได้รับการทดสอบการตั้งครรภ์ทุกรายแม้ว่าจะคุมกำเนิดอยู่(13, 14) นอกจากนี้อาจมีอาการอื่นที่ไม่เฉพาะเจาะจง เช่น อาการหน้ามืดเป็นลม ปวดหลัง ปวดไหล่ อาการทางระบบทางเดินอาหาร โดยมีอาการแสดง ได้แก่ สัญญาณชีพผิดปกติ หากมีเลือดออกมากจะพบชีพจรเต้นเบาเร็วและความดันโลหิตต่ำ อาการกดเจ็บบริเวณหน้าท้องและในรายที่ครรภ์นอกมดลูกแตกแล้วหรือแท้งออกมาอาจมีอาการแสดงของ peritoneal irritation เสียงการเคลื่อนไหวของลำไส้ลดลงหรือหายไป เมื่อตรวจภายในจะพบว่า โดยส่วนใหญ่มดลูกจะมีขนาดปกติแต่บางรายอาจโตเล็กน้อย เจ็บเมื่อโยกปากมดลูก คลำได้ก้อนบริเวณปีกมดลูกและกดเจ็บ (12, 15)
-
การตรวจด้วยคลื่นเสียงความถี่สูง (Ultrasonography)
การตรวจด้วยคลื่นเสียงความถี่สูงทางช่องคลอด (transvaginal ultrasonography: TVS)
ถือเป็นทางเลือกแรกในการตรวจเพื่อช่วยวินิจฉัย(16, 17) โดยสามารถให้การวินิจฉัยได้ทันทีเมื่อเห็นถุงการตั้งครรภ์ร่วมกับ yolk sac หรือเห็นตัวอ่อน (embryonic pole) บริเวณปีกมดลูก แต่โดยส่วนมากแล้วมักเห็นเพียงก้อนที่ปีกมดลูก (complex adnexal mass) แต่อย่างไรก็ตามควรวินิจฉัยแยกกับโรคอื่น เช่น paratubal cyst, corpus luteal cyst, hydrosalpinx, endometrioma, ovarian neoplasm หรือ pedunculated fibroid(18, 19) และการเห็นถุงการตั้งครรภ์ในโพรงมดลูกร่วมด้วยอาจจะไม่สามารถสรุปได้ว่าเป็นการตั้งครรภ์ในมดลูกได้ เนื่องจากอาจจะเป็น pseudogestational sac ซึ่งไม่ใช่ถุงการตั้งครรภ์จริง(20)
การตรวจด้วยคลื่นเสียงความถี่สูงทางหน้าท้อง (transabdominal ultrasonography)
ใช้ในการช่วยประเมินปริมาณเลือดที่ออกในช่องท้อง (hemoperitoneum) ได้(12)
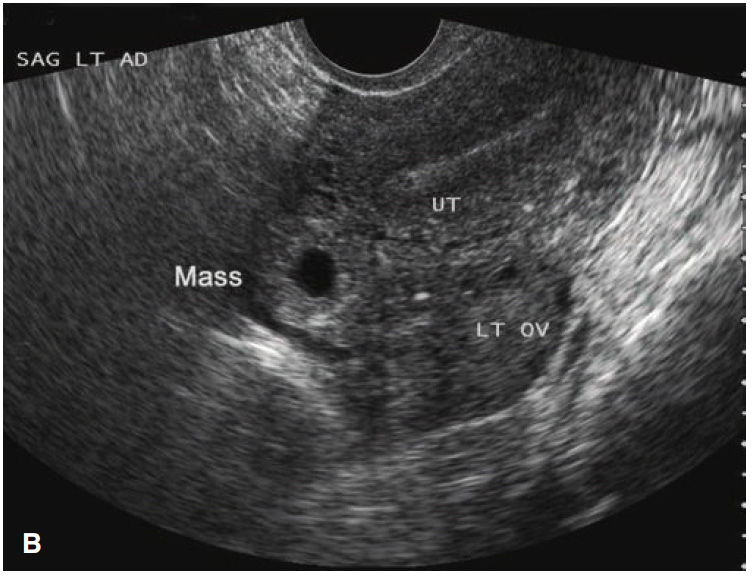
รูปที่ 2 ภาพการตรวจด้วยคลื่นเสียงความถี่สูงแสดงก้อนที่ปีกมดลูกที่เกิดจากการตั้งครรภ์นอกมดลูกบริเวณท่อนำไข่
ที่มา: คัดลอกจาก William Obstetrics: Ectopic pregnancy. 26th edition
หากไม่พบหลักฐานการตั้งครรภ์ทั้งในและนอกโพรงมดลูกจากการตรวจด้วยคลื่นเสียงความถี่สูงจะเรียกภาวะนี้ว่า “Pregnancy of Unknown Location”(6) ซึ่งอาจจะเกิดจากภาวะใดภาวะหนึ่งดังต่อไปนี้ การตั้งครรภ์ในโพรงมดลูกแต่ตัวอ่อนไม่สามารถเจริญต่อได้ (failed IUP) แท้งครบ การตั้งครรภ์ในโพรงมดลูกแต่อายุครรภ์ยังน้อย หรือการตั้งครรภ์นอกมดลูก
-
การตรวจวัดระดับ Serum Human Chorionic Gonadotropin (hCG)
ช่วยในการวินิจฉัยการตั้งครรภ์นอกมดลูกร่วมกับประวัติ อาการ และการตรวจด้วยคลื่นเสียงความถี่สูง(21) มักใช้เมื่อไม่สามารถวินิจฉัยการตั้งครรภ์นอกมดลูกได้จากการตรวจด้วยคลื่นเสียงความถี่สูง(12)
- Single hCG level(22) ใช้ร่วมกับการตรวจด้วยคลื่นเสียงความถี่สูง โดยการตรวจวัดระดับ serum hCG ของผู้ป่วยว่าอยู่ในระดับที่ควรเห็นถุงการตั้งครรภ์ในโพรงมดลูก (intrauterine gestational sac) จากการตรวจด้วยคลื่นเสียงความถี่สูงทางช่องคลอด (TVS) แล้วหรือไม่ ซึ่งระดับ serum hCG ตามเกณฑ์ที่กำหนดไว้นี้เรียกว่า discriminatory zone ถ้าระดับ hCG สูงถึงเกณฑ์แต่ยังตรวจไม่พบถุงการตั้งครรภ์ในโพรงมดลูกแสดงว่าเป็นการตั้งครรภ์ที่ผิดปกติ(12)
- Serial hCG level(12) ช่วยในการประเมินว่าเป็นการตั้งครรภ์ปกติหรือไม่ โดยการตรวจวัดระดับการเปลี่ยนแปลงของ serum hCG ใน 48 ชั่วโมงหรือ 1 สัปดาห์ ถ้าเป็นการตั้งครรภ์ปกติจะมีการเพิ่มขึ้นตามเกณฑ์ที่กำหนด แต่ถ้าเป็นการตั้งครรภ์ที่ผิดปกติจะมีการเพิ่มขึ้นไม่ถึงเกณฑ์หรือลดลงขึ้นอยู่กับภาวะการตั้งครรภ์ว่าเป็นการตั้งครรภ์ผิดปกติแบบใด
อย่างไรก็ตามเกณฑ์การตรวจวัดระดับ serum hCG ดังกล่าวยังมีความแตกต่างกันขึ้นอยู่กับข้อมูลจากการศึกษาที่แนวเวชปฏิบัตินั้นๆ อ้างอิง ดังแสดงในตารางที่ 1
ตารางที่1 แสดงเกณฑ์การวัดระดับ serum hCG เพื่อประกอบการวินิจฉัยการตั้งครรภ์นอกมดลูก
| เกณฑ์ระดับ serum hCG | Novak 16thedition (12, 23) |
William 26thedition (6, 21, 24, 25) |
ACOG 2018 (1, 23, 25) |
NICE 2019(15) |
| Discriminatory zone | ≥3,510 | Vary
> 3510 ≥ 1500 ≥ 2000 |
≥3,500 | ≥1,500 |
| B-hCG rising value
ใน 48 ชั่วโมง |
ขึ้นอยู่กับระดับตั้งต้น
49% (< 1,500) 40% (1,500-3,000) 33% หรือ 35-53% (>3,000) |
35-53% | ขึ้นอยู่กับระดับตั้งต้น
49% (<1,500) 40% (1,500-3,000) 33% (>3,000) |
63% |
| B-hCG decreasing value | 35-50% ใน 48 ชั่วโมง
87% ใน 7 วัน |
ระดับตั้งต้น 250-5,000
35-50% ใน 48 ชั่วโมง 66-87% ใน 7 วัน |
21–35%
ใน 48 ชั่วโมง |
> 50%
ใน 48 ชั่วโมง |
-
การตรวจอื่น ๆ
- การตรวจวัดระดับ serum progesterone(6, 12)
มักจะเจาะตรวจในกรณีที่ระดับ serum hCG และผลการตรวจด้วยคลื่นเสียงความถี่สูงไม่สามารถสรุปการวินิจฉัยได้(27) ในการตั้งครรภ์ปกติ (viable intrauterine pregnancy) ระดับ serum progesterone จะสูงกว่า 25 ng/mL (26) แต่ถ้าระดับต่ำกว่า 5 ng/mL จะเป็นการตั้งครรภ์ที่ผิดปกติ อย่างไรก็ตามการตั้งครรภ์นอกมดลูกส่วนใหญ่จะมีระดับ serum progesterone อยู่ระหว่าง 5-25 ng/mL ทำให้ มีคุณค่าทางคลินิกน้อย
- การเก็บตัวอย่างชิ้นเนื้อจากโพรงมดลูก (Endometrial sampling)(12)
เลือกทำในรายที่ยืนยันแล้วว่าเป็นการตั้งครรภ์ที่ผิดปกติ แต่ไม่ทราบว่าเป็นการตั้งครรภ์ในหรือนอกมดลูกจากการตรวจด้วยคลื่นเสียงความถี่สูงทางช่องคลอด โดยการนำชิ้นเนื้อที่ได้จากการเก็บตัวอย่างจากโพรงมดลูกมาตรวจดูว่ามี chorionic villi หรือไม่ด้วยการส่งตรวจทางพยาธิวิทยาหรือการนำมาลอยในน้ำเกลือแล้วเห็นลักษณะเป็น frond-like appearance (27) หากยังไม่สามารถยืนยันได้แนะนำให้ตรวจติดดูระดับ serum hCG ถ้าเป็นการตั้งครรภ์ในมดลูกหลังจากการขูดมดลูกแล้วค่าจะลดลงมากกว่าร้อยละ 50 ภายใน 24 ชั่วโมง(28)
- การเจาะเพื่อตรวจดูเลือดที่ออกในช่องท้อง (Culdocentesis)
เป็นการเจาะบริเวณ cul-de-sac ผ่านทางช่องคลอด ใช้วินิจฉัยภาวะเลือดออกในช่องท้อง แต่ไม่สามารถบอกได้ว่าเลือดมาจากไหน ทำให้ปัจจุบันการทำ culdocentesis มีบทบาทน้อย(29)
- การส่องกล้องตรวจในอุ้งเชิงกราน (Laparoscopy)(12)
ช่วยในการวินิจฉัยครรภ์นอกมดลูกได้แต่เป็นหัตถการที่ค่อนข้างลุกล้ำ และอาจวินิจฉัยผิดพลาดได้ร้อยละ 3-4 ในผู้ป่วยที่มีถุงการตั้งครรภ์มีขนาดเล็กมาก มีพังผืดในอุ้งเชิงกรานมาก หรือมีท่อนำไข่ผิดปกติอยู่เดิม
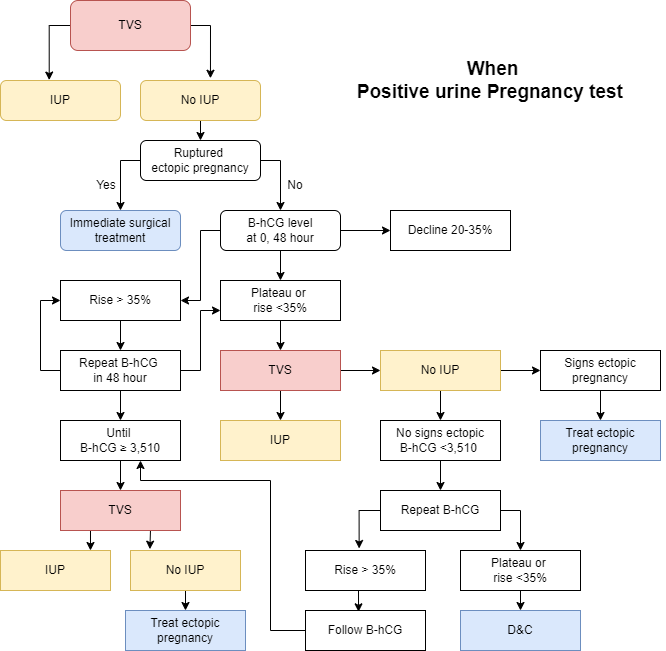
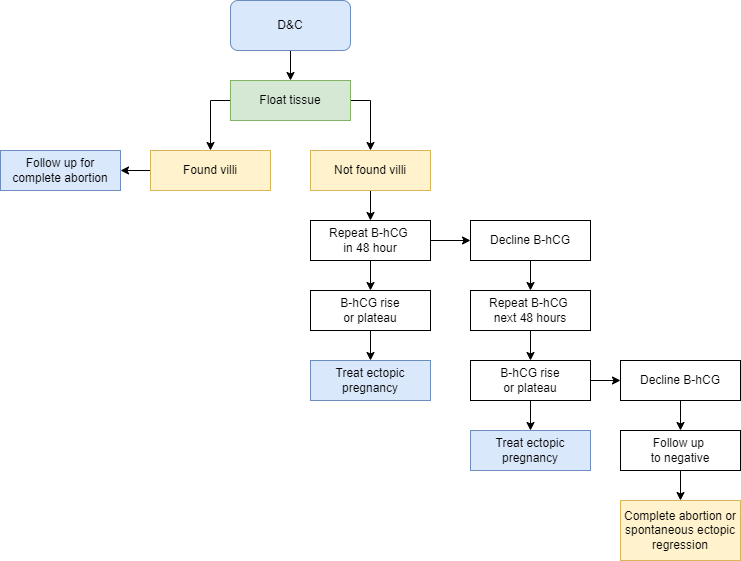
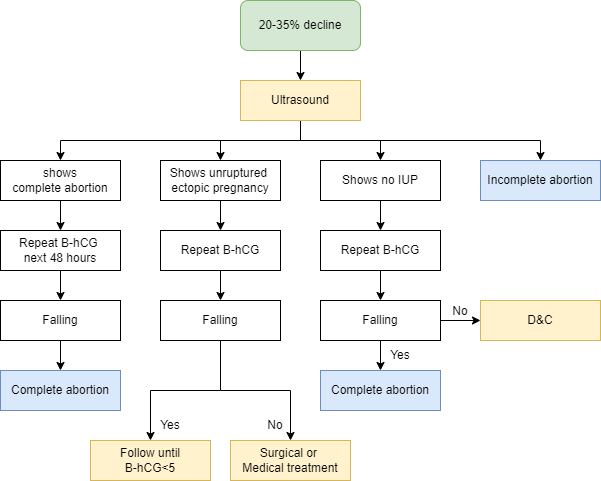
รูปที่ 3 แนวทางการวินิจฉัยการตั้งครรภ์นอกมดลูกในกรณีที่ไม่ใช้การส่องกล้องตรวจในอุ้งเชิงกราน(12)
ที่มา: ดัดแปลงจาก Jonathan S. Berek, Deborah L. Berek. Berek & Novak’s Gynecology: Ectopic pregnancy. 16th ed: Wolters Kluwer; 2020
การรักษา
วิธีการรักษามีอยู่ 3 แนวทางหลัก ได้แก่ การรักษาด้วยยา การรักษาด้วยการผ่าตัด หรือการเฝ้าสังเกต โดยการเลือกวิธีการรักษาให้พิจารณาจากลักษณะทางคลินิก ตำแหน่งของครรภ์นอกมดลูก และทรัพยากรที่มีอยู่เพื่อให้เหมาะสมกับผู้ป่วยแต่ละราย (1, 6, 12)
-
การรักษาด้วยยา
(1, 6, 12)
ยาที่ใช้ในการรักษาครรภ์นอกมดลูก คือ methotrexate เป็นยากลุ่ม folic acid antagonist ออกฤทธิ์โดยการขัดขวางการสร้าง DNA และ RNA โดยการยับยั้งเอนไซม์ dihydrofolate reductase (6) โอกาสประสบความสำเร็จในการรักษาสูงถึงร้อยละ 78-96(30) ทั้งนี้ยาอาจทำให้เกิดผลข้างเคียงดังนี้ การอักเสบของเยื่อบุทางเดินอาหาร เลือดออกกะปริบกะปรอยทางช่องคลอด(1, 12) ภาวะตับอักเสบ(30), ผมร่วง หรือเยื่อหุ้มปอดอักเสบ(31) ทั้งนี้ความรุนแรงของผลข้างเคียงขึ้นอยู่กับขนาดยาและระยะเวลาที่ให้ยา ก่อนที่จะเริ่มให้ยาควรพิจารณาถึงข้อห้ามและข้อควรระวังดังนี้
- ข้อบ่งห้ามโดยสมบูรณ์ (Absolute contraindications)(1)
- มีการตั้งครรภ์ในโพรงมดลูกร่วมด้วย – มีแผลในกระเพาะอาหาร
- ภูมิคุ้มกันบกพร่อง – การทำงานของตับผิดปกติ
- มีภาวะซีด เม็ดเลือดขาวหรือเกร็ดเลือดต่ำ – การทำงานของไตผิดปกติ
- ให้นมบุตร
- มีประวัติแพ้ methotrexate – มีการแตกของท่อนำไข่
- เป็นโรคปอดที่อาการยังไม่สงบ – สัญญาณชีพไม่ปกติ
- ไม่สามารถมารับการตรวติดตามได้
- ข้อบ่งห้ามโดยอนุโลม (Relative contraindications)(1)
- ตรวจพบการเต้นของหัวใจของตัวอ่อน
- ระดับ serum hCG ตั้งต้นสูงเกิน 5,000 mIU/mL (พบว่ามีโอกาสที่การรักษาจะไม่ประสบความสำเร็จสูงถึงร้อยละ14.3) หรือเมื่อทำการตรวจติดตามที่ 48 ชั่วโมงแล้วพบว่าเพิ่มขึ้นเกินร้อยละ 50
- ขนาดก้อนที่ท่อนำไข่มีขนาดเส้นผ่านศูนย์กลางเกิน 4 เซนติเมตร
- ปฏิเสธการเติมเลือดหรือองค์ประกอบของเลือด
โดยการบริหารยามีทั้งหมด 3 วิธี คือ
- Single dose regimen มีข้อดีคือบริหารยาง่าย มีค่าใช้จ่ายไม่สูงมาก และไม่ต้องติดตามบ่อยครั้งมากเท่าวิธีการอื่น เหมาะสำหรับครรภ์นอกมดลูกที่ระดับ serum hCG ค่อนข้างต่ำ แต่อาจจะต้องให้ยาเพิ่มเติม(1, 12, 32) ดังแสดงในตารางที่ 2
ตารางที่ 2 การบริหารยา methotrexate แบบ single dose regimen
|
– หากลดลงมากกว่าร้อยละ 15, ตรวจติดตามระดับ hCG ทุกสัปดาห์จนกว่าจะอยู่ในระดับปกติ |
| – หากลดลงน้อยกว่าร้อยละ 15 ให้ methotrexate 50 มก./ตารางเมตรพื้นที่ผิวของร่างกายซ้ำ ทางกล้ามเนื้อ และตรวจติดตามระดับ hCG |
| – หากให้ methotrexate สองครั้งแล้วระดับ hCG ไม่ลดลง พิจารณารักษาโดยการผ่าตัด |
|
- Multidose regimen มีประสิทธิภาพในการรักษาสูงแต่การบริหารจัดการยากกว่า เหมาะสำหรับการตั้งครรภ์นอกมดลูกที่มีระดับ serum hCG ค่อนข้างสูง (1, 33) ดังแสดงในตารางที่ 3
ตารางที่ 3 การบริหารยา methotrexate แบบ multidose regimen
|
|
| – หยุดให้ methotrexate หากลดลงมากกว่าร้อยละ 15 แล้วตรวจติดตามระดับ hCG ทุกสัปดาห์จนกว่าจะอยู่ในระดับปกติ |
| – หากให้ methotrexate สี่ครั้งแล้วระดับ hCG ไม่ลดลง พิจารณารักษาโดยการผ่าตัด |
|
- Two-dose regimen ประสิทธิภาพสูงกว่า single dose regimen และมีผลข้างเคียงน้อยกว่าเมื่อเทียบกับการบริหารยาแบบ multidose regimen(1, 12)
ตารางที่ 4 การบริหารยา methotrexate แบบ two-dose regimen
|
|
|
| – หากลดลงมากกว่าร้อยละ 15, ตรวจติดตามระดับ hCG ทุกสัปดาห์จนกว่าจะอยู่ในระดับปกติ |
| – หากลดลงน้อยกว่า 15 ให้ methotrexate 50 มก./ตารางเมตรพื้นที่ผิวของร่างกายซ้ำ ทางกล้ามเนื้อ ในวันที่ 7 แล้วตรวจติดตามระดับ hCG ในวันที่ 11 |
| – หากระดับ hCG ระหว่างวันที่ 7 และ 11 ลดลงมากกว่าร้อยละ 15 ให้ตรวจติดตามระดับ hCG ทุกสัปดาห์จนกว่าจะอยู่ในระดับปกติ
– หากระดับ hCG ระหว่างวันที่ 7 และ 11 ลดลงน้อยกว่าร้อยละ 15 ให้ methotrexate 50 มก./ตารางเมตรพื้นที่ผิวของร่างกายซ้ำ ทางกล้ามเนื้อ ในวันที่ 11 แล้วตรวจติดตามระดับ hCG ในวันที่ 14 |
| – หากให้ methotrexate สี่ครั้งแล้วระดับ hCG ไม่ลดลง พิจารณารักษาโดยการผ่าตัด |
|
-
การรักษาด้วยการผ่าตัด (Surgical treatment)
ข้อบ่งชี้ในการผ่าตัดในการรักษา คือ สัญญาณชีพผิดปกติ มีข้อบ่งห้ามต่อการรักษาด้วยยา หรือมีโอกาสที่ไม่ประสบความสำเร็จจากการรักษาด้วยยาสูง (1, 6, 12) โดยแนวทางการรักษาขึ้นอยู่กับลักษณะทางคลินิก อุปกรณ์ทางการแพทย์ที่มีและประสบการณ์ของแพทย์ผู้ผ่าตัด
- การผ่าตัดผ่านกล้อง (Laparoscopy) เทียบกับการผ่าตัดเปิดหน้าท้อง (Laparotomy)
การผ่าตัดผ่านกล้องมีข้อดีคือ แผลขนาดเล็ก ฟื้นตัวเร็ว และมีต้นทุนประสิทธิผลที่ดีกว่าเมื่อเทียบกับการผ่าตัดเปิดหน้าท้อง(34) อย่างไรก็ตามแนะนำให้ทำการผ่าตัดแบบเปิดหน้าท้องในกรณีต่อไปนี้ ผู้ป่วยมีภาวะช็อกจากการสูญเสียเลือดและต้องการผ่าตัดอย่างรวดเร็ว เป็นครรภ์นอกมดลูกชนิด abdominal pregnancy มีพังผืดในช่องท้องมาก หรือคาดว่าจะทำการผ่าตัดผ่านกล้องได้ยาก(12)
การผ่าตัดเชิงอนุรักษ์ (salpingostomy) พิจารณาทำในกรณีที่ท่อนำไข่ข้างที่มีการตั้งครรภ์นอกมดลูกยังไม่แตกหรือมีลักษณะปกติ หรือท่อนำไข่ด้านตรงข้ามผิดปกติหรือถูกเคยถูกตัดแต่ผู้ป่วยยังต้องการธำรงค์ภาวะการเจริญพันธุ์(12) การรักษาด้วยการผ่าตัดเชิงอนุรักษ์มีโอกาสเกิด persistent ectopic pregnancy ได้ประมาณร้อยละ 8 พบได้บ่อยถ้าระดับ serum hCG ตั้งต้นสูง อายุครรภ์น้อย และขนาดก้อนการตั้งครรภ์นอกมดลูกน้อยกว่า 2 เซนติเมตร ดังนั้นจึงควรตรวจติดตามระดับ serum hCG ทุกสัปดาห์จนวัดไม่ได้(35) การตัดท่อนำไข่ออก (salpingectomy) ควรพิจารณาทำในกรณีที่ท่อนำไข่แตกหรือถูกทำลายรุนแรง ควบคุมการเสียเลือดไม่ได้ หรือมีบุตรเพียงพอแล้ว (12)
-
การเฝ้าสังเกต (Expectant management)
มักพิจารณาเป็นทางเลือกในการรักษากรณีที่ผู้ป่วยไม่มีอาการ ระดับ serum hCG ตั้งต้นต่ำและเมื่อตรวจติดตามพบว่ามีค่าคงที่หรือลดลง ทั้งนี้ควรเลือกรักษาในผู้ป่วยที่สามารถมาตรวจติดตามได้และยอมรับโอกาสในการเกิด ruptured ectopic pregnancy ซึ่งจำเป็นต้องได้รับการผ่าตัดในทันที(1, 6, 12)
การตั้งครรภ์นอกมดลูกในตำแหน่งอื่น
- การตั้งครรภ์ที่ท่อนำไข่ที่ฝังตัวในกล้ามเนื้อมดลูก (Interstitial/Cornual pregnancy)(6, 12)
เป็นการตั้งครรภ์นอกมดลูกที่วินิจฉัยได้ค่อนข้างยาก มีเกณฑ์ในการวินิจฉัยจากการตรวจด้วยคลื่นเสียงความถี่สูง(6) ดังนี้
- มดลูกว่างเปล่า
- ถุงการตั้งครรภ์แยกออกจากเยื่อบุโพรงมดลูก
- ถุงการตั้งครรภ์เอียงออกจากขอบด้านข้างของโพรงมดลูกมากกว่า 1 เซนติเมตร
- ถุงการตั้งครรภ์มีกล้ามเนื้อมดลูกบาง ๆ (น้อยกว่า 5 มิลลิเมตร) หุ้มอยู่
- เห็น Interstitial line (เส้นเข้มเชื่อมจากโพรงมดลูกไปยังถุงการตั้งครรภ์ที่อยู่ขอบ)
ในกรณีที่ต้องการเก็บมดลูกไว้สามารถรักษาด้วยการผ่าตัดทำ cornual resection หรือ cornuostomy (36) หรือให้การรักษาด้วยยา Methotrexate แต่ยังมีข้อมูลสนับสนุนค่อนข้างน้อย(37) แต่ถ้าไม่ต้องการมีบุตรอีกให้ทำการตัดมดลูกออก
-
การตั้งครรภ์ที่รังไข่ (Ovarian pregnancy)
พบอุบัติการณ์ร้อยละ 3 ของครรภ์นอกมดลูก(5) มี Spiegelberg’s criteria(12, 38) เป็นเกณฑ์ช่วยในการวินิจฉัย ดังนี้
1. ท่อนำไข่ข้างเดียวกันกับที่ก้อนการตั้งครรภ์อยู่ต้องมีลักษณะปกติ แยกจากก้อนการตั้งครรภ์ได้ชัดเจน
2. มีถุงการตั้งครรภ์บริเวณรังไข่
3. ก้อนการตั้งครรภ์มีการติดต่อกับตัวมดลูกด้วย ovarian ligament
4. พบเนื้อเยื่อของรังไข่อยู่บริเวณผนังของก้อน
การตั้งครรภ์ที่รังไข่สามารถให้การรักษาโดยการทำการตัดเอาเฉพาะส่วนของถุงการตั้งครรภ์และเนื้อเยื่อรังไข่ที่ติดอยู่ออก (wedge resection) (12) หรือตัดรังข้างนั้นออก (oophorectomy) หรืออาจจะรักษาด้วยยา methotrexate(39-41)
-
การตั้งครรภ์ในช่องท้อง (Abdominal pregnancy)
พบได้น้อยมีรายงานอุบัติการณ์เพียงร้อยละ 1-1.4 ของครรภ์นอกมดลูก (5, 42) แบ่งเป็นออกเป็น primary abdominal pregnancy เกิดเมื่อไข่ที่ถูกผสมแล้วมีการฝังตัวในช่องท้องโดยตรงและ secondary abdominal pregnancy ซึ่งมักเกิดจากการตั้งครรภ์ที่ท่อนำไข่แล้วเกิด tubal abortion/rupture หรือตั้งครรภ์ในโพรงมดลูกแล้วเกิด uterine rupture และไปเจริญเติบโตในช่องท้อง
เกณฑ์ในการช่วยวินิจฉัยช่วย primary abdominal pregnancy (Studdiford’s Criteria)(12) มีดังนี้
1. ท่อนำไข่และรังไข่ปกติ โดยไม่พบร่องรอยของการตั้งครรภ์ทั้งเก่าและใหม่
2. ไม่มีรูเชื่อมของรกและมดลูก
3. การตั้งครรภ์ทั้งหมดอยู่ที่ผิวเยื่อบุช่องท้อง และดูใหม่ไม่เหมือนหลุดออกมาฝังต่อจากท่อนำไข่
โดยทั่วไปแนะนำให้ยุติการตั้งครรภ์เมื่อทราบว่าเป็นการตั้งครรภ์ในช่องท้องเพราะการตั้งครรภ์ต่อเพิ่มความเสี่ยงให้มารดา ส่วนมากสามารถทำการผ่าตัดเปิดหน้าท้องเพื่อเอาทารกออกและสามารถเอารกออกได้ แต่บางรายจำเป็นต้องทิ้งรกเอาไว้ในช่องท้องและรอให้สลายไปเอง (42)
-
การตั้งครรภ์ที่ปากมดลูก (Cervical pregnancy)
พบน้อยมากมีรายงานอุบัติการณ์น้อยกว่าร้อยละ 1 ของครรภ์นอกมดลูก(5) มักแยกจากภาวะ Ongoing spontaneous abortion(43) ได้ยาก มีเกณฑ์การวินิจฉัยด้วยการตรวจด้วยคลื่นเสียงความถี่สูง ดังนี้ (6, 12)
1. เห็นถุงการตั้งครรภ์และรกบริเวณปากมดลูก
2. หัวใจของทารกเต้นอยู่ใต้ต่อระดับ internal os
3. ไม่เห็นการตั้งครรภ์ในโพรงมดลูก
4. มดลูกมีรูปร่างคล้ายนาฬิกาทรายและปากมดลูกมีบวมโตออกwith
5. ถุงการตั้งครรภ์ไม่ขยับเมื่อใช้ transvaginal probe กดหรือไม่มี sliding sign
6. ปากมดลูกส่วน internal os ปิด
สามารถให้การรักษาด้วยการให้ยา methotrexate โดยมักจะต้องให้ยาหลายครั้ง ในกรณีที่มีการเต้นของหัวใจของทารกทำการฉีด intraamniotic หรือ intrafetal KCl ก่อน และสามารถทำการขูดมดลูกหรือ suction evacuation โดยอาจจะพิจารณาทำ uterine arterial embolization ร่วมด้วย แต่ถ้าไม่สามารถควบคุมเลือดที่ออกได้ให้พิจารณาตัดมดลูก(44)
-
การตั้งครรภ์ที่แผลผ่าตัดคลอด (Cesarean scar pregnancy: CSP)
พบได้ประมาณ 1 ต่อ 500-2,000 ของการตั้งครรภ์(41, 45) มีเกณฑ์ในการวินิจฉัยจากการตรวจด้วยคลื่นเสียงความถี่สูง ดังนี้(46)
- ไม่เห็นการตั้งครรภ์ในโพรงมดลูกและคอมดลูก
- เห็นรกหรือถุงการตั้งครรภ์ฝังตัวที่แผลผ่าตัดคลอด
- เห็นชั้นกล้ามเนื้อมดลูกบางๆ คั่นระหว่างถุงการตั้งครรภ์และกระเพาะปัสสาวะ
- เห็นหลอดเลือดมาเลี้ยงบริเวณแผลผ่าตัดคลอดโป่งขยาย (prominent vascular pattern)
การรักษาทำได้ด้วยการผ่าตัดเอาส่วนของมดลูกที่มีการตั้งครรภ์ออก (uterine isthmic resection) โดยสามารถทำการผ่าตัดผ่านกล้อง ผ่าตัดเปิดหน้าท้อง หรือผ่าตัดทางช่องคลอดโดยเปิดเข้าสู่ช่องท้องทางผนังช่องคลอดด้านหน้า (anterior colpotomy) สำหรับทางเลือกในการรักษาวิธีอื่น ได้แก่ การทำ uterine arterial embolization ตามด้วยการขูดมดลูก การตัดเอาถุงการตั้งครรภ์และรกออกผ่านการส่องกล้องทางโพรงมดลูก (47, 48) การให้ยา methotrexate หรือการฉีด intragestational sac KCl (49, 50)
-
การตั้งครรภ์ทั้งในและนอกมดลูกพร้อมกัน (Heterotopic Pregnancy)
พบอุบัติการณ์ประมาณ 1:30,000 ของการตั้งครรภ์(31) และจะเพิ่มขึ้นหากเป็นการตั้งครรภ์จากเทคโนโลยีช่วยการเจริญพันธุ์(51) การรักษาขึ้นอยู่กับลักษณะทางคลินิกของผู้ป่วย หากมีการแตกของท่อนำไข่ควรรักษาด้วยการผ่าตัด แต่หากไม่มีสามารถเลือกการรักษาด้วยวิธีผ่าตัดหรือการฉีดยาเข้าไปทำลายถุงการตั้งครรภ์โดยเลือกใช้เป็น KCl หรือ hyperosmolar glucose(6, 52)
สรุป
การตั้งครรภ์นอกมดลูกเป็นภาวะที่สามารถพบได้บ่อยทางสูตินรีเวชกรรม มีอันตรายสูงต่อผู้ป่วย แพทย์ควรให้วินิจฉัยและรักษาอย่างรวดเร็วและเหมาะสม สตรีวัยเจริญพันธุ์ทุกคนที่มีอาการปวดท้องร่วมกับมีเลือดออกผิดปกติทางช่องคลอดควรได้รับการคัดกรองการตั้งครรภ์โดยไม่คำนึงถึงการคุมกำเนิด และผู้ป่วยที่เคยมีประวัติเป็นเคยตั้งครรภ์นอกมดลูกมาก่อนควรได้รับคำแนะนำให้รีบมาฝากครรภ์เนื่องจากมีโอกาสเป็นซ้ำสูง
เอกสารอ้างอิง
- ACOG Practice Bulletin No.191: Tubal Ectopic Pregnancy. OBSTETRICS & GYNECOLOGY. 2018;Vol.131, No.2,.
- Hoover KW, Tao G, Kent CK. Trends in the diagnosis and treatment of ectopic pregnancy in the United States. Obstet Gynecol. 2010;115:495-502.
- (CDC) CfDCaP. Ectopic pregnancy–United States, 1990-1992. MMWR Morb Mortal Wkly Rep. 1995;44:46-8.
- Creanga AA, Syverson C, Seed K, Callaghan WM. Pregnancy-Related Mortality in the United States, 2011-2013. Obstet Gynecol. 2017;130:366-73.
- Bouyer J, Coste J, Fernandez H, Pouly JL, Job-Spira N. Sites of ectopic pregnancy: a 10 year population-based study of 1800 cases. Human Reproduction. 2002;17:3224-30.
- F. Gary Cunningham, Kenneth J. Leveno, Jodi S. Dashe, Babara L. Hoffman, Catherine Y. Spong, Brian M. Casey. Williams Obstetrics: Ectopic pregnancy. 26th ed. United states: McGraw Hill; 2022.
- Bouyer J, Coste J, Shojaei T, et al. Risk factors for ectopic pregnancy: a comprehensive analysis based on a large case-control, population-based study in France. Am J Epidemiol. 2003;157:185-94.
- Juneau C, Bates GW. Reproductive outcomes after medical and surgical management of ectopic pregnancy. Clin Obstet Gynecol. 2012;55:455-60.
- Farquhar CM. Ectopic pregnancy. The Lancet. 2005;366:583-91.
- Saraiya M, Berg CJ, Kendrick JS, Strauss LT, Atrash HK, Ahn YW. Cigarette smoking as a risk factor for ectopic pregnancy. Am J Obstet Gynecol. 1998;178:493-8.
- Backman T, Rauramo I, Huhtala S, Koskenvuo M. Pregnancy during the use of levonorgestrel intrauterine system. Am J Obstet Gynecol. 2004;190:50-4.
- Jonathan S. Berek, Deborah L. Berek. Berek & Novak’s Gynecology: Ectopic pregnancy. 16th ed: Wolters Kluwer; 2020.
- Kirk E, Papageorghiou AT, Condous G, Tan L, Bora S, Bourne T. The diagnostic effectiveness of an initial transvaginal scan in detecting ectopic pregnancy. Hum Reprod. 2007;22:2824-8.
- van Mello NM, Mol F, Opmeer BC, et al. Diagnostic value of serum hCG on the outcome of pregnancy of unknown location: a systematic review and meta-analysis. Hum Reprod Update. 2012;18:603-17.
- NICE Guideline 2019: Ectopic pregnancy and miscarriage diagnosis and initial management. The National Institute for Health and Care Excellence. 2019.
- Kirk E. Ultrasound in the diagnosis of ectopic pregnancy. Clin Obstet Gynecol. 2012;55:395-401.
- Condous G, Okaro E, Khalid A, et al. The accuracy of transvaginal ultrasonography for the diagnosis of ectopic pregnancy prior to surgery. Hum Reprod. 2005;20:1404-9.
- Brown DL, Doubilet PM. Transvaginal sonography for diagnosing ectopic pregnancy: positivity criteria and performance characteristics. J Ultrasound Med. 1994;13:259-66.
- Hill LM, Guzick D, Fries J, Hixson J. Fetal loss rate after ultrasonically documented cardiac activity between 6 and 14 weeks, menstrual age. J Clin Ultrasound. 1991;19:221-3.
- Nyberg DA, Mack LA, Harvey D, Wang K. Value of the yolk sac in evaluating early pregnancies. J Ultrasound Med. 1988;7:129-35.
- Seeber BE, Sammel MD, Guo W, Zhou L, Hummel A, Barnhart KT. Application of redefined human chorionic gonadotropin curves for the diagnosis of women at risk for ectopic pregnancy. Fertil Steril. 2006;86:454-9.
- Cartwright PS, Moore RA, Dao AH, Wong SW, Anderson JR. Serum beta-human chorionic gonadotropin levels relate poorly with the size of a tubal pregnancy. Fertil Steril. 1987;48:679-80.
- Barnhart KT, Guo W, Cary MS, et al. Differences in Serum Human Chorionic Gonadotropin Rise in Early Pregnancy by Race and Value at Presentation. Obstet Gynecol. 2016;128:504-11.
- Connolly A, Ryan DH, Stuebe AM, Wolfe HM. Reevaluation of discriminatory and threshold levels for serum β-hCG in early pregnancy. Obstet Gynecol. 2013;121:65-70.
- Barnhart KT, Sammel MD, Rinaudo PF, Zhou L, Hummel AC, Guo W. Symptomatic patients with an early viable intrauterine pregnancy: HCG curves redefined. Obstet Gynecol. 2004;104:50-5.
- Stovall TG, Ling FW, Andersen RN, Buster JE. Improved sensitivity and specificity of a single measurement of serum progesterone over serial quantitative beta-human chorionic gonadotrophin in screening for ectopic pregnancy. Hum Reprod. 1992;7:723-5.
- Barnhart KT, Gracia CR, Reindl B, Wheeler JE. Usefulness of pipelle endometrial biopsy in the diagnosis of women at risk for ectopic pregnancy. Am J Obstet Gynecol. 2003;188:906-9.
- Rivera V, Nguyen PH, Sit A. Change in quantitative human chorionic gonadotropin after manual vacuum aspiration in women with pregnancy of unknown location. Am J Obstet Gynecol. 2009;200:e56-9.
- Glezerman M, Press F, Carpman M. Culdocentesis is an obsolete diagnostic tool in suspected ectopic pregnancy. Arch Gynecol Obstet. 1992;252:5-9.
- Pisarska MD, Carson SA, Buster JE. Ectopic pregnancy. Lancet. 1998;351:1115-20.
- Dasari P, Sagili H. Life-threatening complications following multidose methotrexate for medical management of ectopic pregnancy. BMJ Case Rep. 2012;2012.
- Menon S, Colins J, Barnhart KT. Establishing a human chorionic gonadotropin cutoff to guide methotrexate treatment of ectopic pregnancy: a systematic review. Fertil Steril. 2007;87:481-4.
- Barnhart KT, Gosman G, Ashby R, Sammel M. The medical management of ectopic pregnancy: a meta-analysis comparing “single dose” and “multidose” regimens. Obstet Gynecol. 2003;101:778-84.
- Lundorff P, Thorburn J, Lindblom B. Fertility outcome after conservative surgical treatment of ectopic pregnancy evaluated in a randomized trial. Fertil Steril. 1992;57:998-1002.
- Gracia CR, Brown HA, Barnhart KT. Prophylactic methotrexate after linear salpingostomy: a decision analysis. Fertil Steril. 2001;76:1191-5.
- Lau S, Tulandi T. Conservative medical and surgical management of interstitial ectopic pregnancy. Fertil Steril. 1999;72:207-15.
- Jermy K, Thomas J, Doo A, Bourne T. The conservative management of interstitial pregnancy. Bjog. 2004;111:1283-8.
- Spiegelberg O. Zur Casuistik der Ovarialschwangerschaft. Archiv für Gynäkologie. 1878;13:73-9.
- Habbu J, Read MD. Ovarian pregnancy successfully treated with methotrexate. J Obstet Gynaecol. 2006;26:587-8.
- Papillon-Smith J, Krishnamurthy S, Mansour FW. Ovarian Pregnancy. J Obstet Gynaecol Can. 2016;38:1-2.
- Alalade AO, Smith FJE, Kendall CE, Odejinmi F. Evidence-based management of non-tubal ectopic pregnancies. J Obstet Gynaecol. 2017;37:982-91.
- Shaw SW, Hsu JJ, Chueh HY, et al. Management of primary abdominal pregnancy: twelve years of experience in a medical centre. Acta Obstet Gynecol Scand. 2007;86:1058-62.
- Kung FT, Lin H, Hsu TY, et al. Differential diagnosis of suspected cervical pregnancy and conservative treatment with the combination of laparoscopy-assisted uterine artery ligation and hysteroscopic endocervical resection. Fertil Steril. 2004;81:1642-9.
- Fowler ML, Wang D, Chia V, et al. Management of Cervical Ectopic Pregnancies: A Scoping Review. Obstet Gynecol. 2021;138:33-41.
- Rotas MA, Haberman S, Levgur M. Cesarean scar ectopic pregnancies: etiology, diagnosis, and management. Obstet Gynecol. 2006;107:1373-81.
- Timor-Tritsch IE, Monteagudo A, Santos R, Tsymbal T, Pineda G, Arslan AA. The diagnosis, treatment, and follow-up of cesarean scar pregnancy. Am J Obstet Gynecol. 2012;207:44.e1-13.
- Birch Petersen K, Hoffmann E, Rifbjerg Larsen C, Svarre Nielsen H. Cesarean scar pregnancy: a systematic review of treatment studies. Fertil Steril. 2016;105:958-67.
- Wang G, Liu X, Bi F, et al. Evaluation of the efficacy of laparoscopic resection for the management of exogenous cesarean scar pregnancy. Fertil Steril. 2014;101:1501-7.
- Maheux-Lacroix S, Li F, Bujold E, Nesbitt-Hawes E, Deans R, Abbott J. Cesarean Scar Pregnancies: A Systematic Review of Treatment Options. J Minim Invasive Gynecol. 2017;24:915-25.
- Miller R, Timor-Tritsch IE, Gyamfi-Bannerman C. Society for Maternal-Fetal Medicine (SMFM) Consult Series #49: Cesarean scar pregnancy. Am J Obstet Gynecol. 2020;222:B2-b14.
- Perkins KM, Boulet SL, Kissin DM, Jamieson DJ. Risk of ectopic pregnancy associated with assisted reproductive technology in the United States, 2001-2011. Obstet Gynecol. 2015;125:70-8.
- Wu Z, Zhang X, Xu P, Huang X. Clinical analysis of 50 patients with heterotopic pregnancy after ovulation induction or embryo transfer. European Journal of Medical Research. 2018;23:17.
- Barnhart KT, Sammel MD, Gracia CR, Chittams J, Hummel AC, Shaunik A. Risk factors for ectopic pregnancy in women with symptomatic first-trimester pregnancies. Fertil Steril. 2006;86:36-43.
- Ankum WM, Mol BW, Van der Veen F, Bossuyt PM. Risk factors for ectopic pregnancy: a meta-analysis. Fertil Steril. 1996;65:1093-9.
- Cleland K, Raymond E, Trussell J, Cheng L, Zhu H. Ectopic pregnancy and emergency contraceptive pills: a systematic review. Obstet Gynecol. 2010;115:1263-6.
- Practice Bulletin No. 152: Emergency Contraception. Obstet Gynecol. 2015;126:e1-e11.
- Rajah K, Goodhart V, Zamora KP, Amin T, Jauniaux E, Jurkovic D. How to measure size of tubal ectopic pregnancy on ultrasound. Ultrasound Obstet Gynecol. 2018;52:103-9.

