การเตรียมลำไส้ในผู้ป่วยที่เข้ารับการผ่าตัดทางนรีเวชวิทยา
การเตรียมลำไส้ในผู้ป่วยที่เข้ารับการผ่าตัดทางนรีเวชวิทยา
พ.ญ.แพรทิพย์ พรายแก้ว
ที่ปรึกษา รศ.นพ.กิตติภัต เจริญขวัญ
การเตรียมลำไส้ก่อนการผ่าตัดทางนรีเวชวิทยาจัดเป็นกระบวนการที่สําคัญก่อนการผ่าตัดโดยเฉพาะผู้ป่วยที่มีความเสี่ยงต่อการได้รับบาดเจ็บต่อลำไส้ขณะผ่าตัดจุดมุ่งหมายเพื่อ ทําให้ลําไส้ปราศจากอุจจาระและเพิ่มทัศนวิสัยในการทำหัตถการ หลักการของการเตรียมลําไส้ ที่ดีคือง่าย สะดวก และเกิดผลข้างเคียงน้อยที่สุด
วิวัฒนาการของการเตรียมลำไส้
ปี ค.ศ. 1877 William Sir เริ่มนำ Mechanical bowel preparation มาใช้ในผู้ป่วยที่เข้า รับการผ่าตัดลำไส้ใหญ่ พบว่าสามารถช่วยลดภาวะแทรกซ้อนจากการติดเชื้อที่แผลผ่าตัดและ
ลดการรั่วซึมของแผลผ่าตัดได้โดยลดปริมาณอุจจาระและเชื้อแบคทีเรียในลำไส้ที่จะผ่านบริเวณ ตำแหน่งที่ผ่าตัดและเพิ่มทัศนวิสัยในการผ่าตัดดีขึ้น ต่อมาได้มีการนำหลักการนี้ไปใช้กันอย่าง
แพร่หลายมากขึ้น และได้นำมาใช้ในผู้ป่วยที่เข้ารับการผ่าตัดทางนรีเวชวิทยาในปี ค.ศ. 1930 โดยมีข้อบ่งชี้ในกลุ่มเสี่ยงที่อาจได้รับบาดเจ็บต่อลำไส้จากการทำหัตถการรวมไปถึงการประยุกต์ใช้ร่วมกับการให้ยาปฏิชีวนะก่อนการผ่าตัดด้วย
หลักการเตรียมลำไส้
- สามารถขจัดอุจจาระได้หมด
- ใช้ระยะเวลาสั้น ง่ายและสะดวก
- ไม่มีผลข้างเคียงต่อผู้ป่วยหรือมีน้อย
- ไม่ทำให้เกิด Fluid/Electrolyte imbalance
วิธีการเตรียมลำไส้
ปัจจุบันมีการศึกษาเกี่ยวกับยาที่ใชัเตรียมลําไส้ใหญ่ออกมาเป็นจํานวนมากโดยเฉพาะ
ชนิดรับประทาน ผลิตภัณฑ์สําเร็จรูปเหล่านี้มีข้อบ่งชี้และข้อห้าม ดังนั้นควรมีความรู้ความเข้าใจ
หลักการในการเลือกใช้ยาแต่ละชนิดให้เหมาะสมกับผู้ป่วยแต่ละราย
การเตรียมลําไส้ใหญ่แบ่งได้เป็น 2 วิธี ได้แก่
1. Whole Gut lavage
ไม่แนะนำในผู้ป่วยที่สงสัยภาวะลำไส้อุดตัน อาจพิจารณาใช้ในผู้ป่วยนรีเวชวิทยา กรณีมะเร็งรังไข่ที่มีภาวะลำไส้อุดตันไม่สมบูรณ์ได้
ข้อดี
- ภาวะสมดุลของเกลือแร่และน้ำในร่างกายเปลี่ยนแปลงน้อย
- น้ำหนักคงตัว
- โภชนาการมีการปรับเปลี่ยนน้อย
- วิธีการง่ายและสะดวก
- การเตรียมลำไส้ใช้เวลาไม่นาน
ข้อเสีย
ผู้ป่วยอาจทนต่อการรับยาไม่ได้และอาจพิจารณาให้ทางสายให้ทางกระเพาะอาหารแทน (Nasogastric intubation)
2. Traditional multiple day cathartics and enemas
โดยทั่วไปใช้เวลาเตรียมลำไส้ประมาณ 3 วัน ร่วมกับการควบคุมอาหารสำหรับผู้ป่วยได้เฉพาะของเหลว (Clear liquid fluid)
การควบคุมอาหาร หรือ Diet control ร่วมด้วยนั้นมีจุดมุงหมายเพื่อลดปริมาณอุจจาระในลําไสใหญ่โดยให้ผู้ป่วยดื่ม Clear liquid ได้แก่ น้ํา น้ําซุปใส กาแฟหรือชาที่ปราศจากนม น้ําแข็งและน้ําผลไม้ ควรหลีกเลี่ยงน้ําที่มีสีแดงเพราะอาจสับสนกับเลือด หรืออาหารที่มีกากน้อย (Low-residue diet or low-fiber diet) โดยหลีกเลี่ยงอาหารประเภทธัญพืช (whole grains) ผลไม้และผัก ก่อนหน้าจะทําการผ่าตัดอย่างน้อย 1 วัน มักใช้ร่วมกับยาระบายและงดดื่มน้ําหรืออาหารก่อนทําการตรวจ 4 ถึง 8 ชั่วโมง ผู้ป่วยจะได้รับยาระบาย ยกตัวอย่าง เช่น Magnesium citrate, Sodium sulfate เป็นต้น ซึ่งวิธีนี้มีผลต่อสมดุลของเกลือแร่ในร่างกาย จึงควรมีการ ติดตามระดับเกลือแร่ในเลือดก่อนการผ่าตัด
ยาที่ใช้
การรับประทานยาเตรียมลําไส้ หรือ Oral preparation เป็นวิธีที่ใช้กันอย่างแพร่หลาย แบ่งได้เป็น 3 กลุ่ม(1) ได้แก่
Emollient ทำให้อุจจาระนิ่ม ได้แก่ Ducosate
ออกฤทธิ์โดยการเพิ่มปริมาณน้ําในลําไสใหญโดยดึงน้ําจาก extracellular fluid ผ่านผนังลําไส้ และคงปริมาณน้ําดื่ม เข้าไปให้อยูในช่องว่างในลําไส้ (lumen)
Osmolar Agent ได้แก่ sodium or magnesium preparations, polyethylene glycol (PEG), lactulose, sorbitol, glycerine
PEG เป็น high-molecular-weight non-absorbable macrogol polymer ในสารละลาย เจือจางของเกลือแร่(dilute electrolyte solution) มีผลให้เกิด osmotic effect ดึงน้ําจากผนัง ลําไส้เข้าสู่ช่องว่างของลําไส้ และ ตัว polymer จะทําหน้าที่คงน้ําไว้ในช่องว่างของลําไส้ โดย จํากัดการแลกเปลี่ยน โดยมีการใช้อย่างแพร่หลาย มีสองแบบ
- Sulfate free solution
- Electrolyte solution ประกอบไปด้วยเกลือแร่ชนิดต่างๆ (Sodium 125 mmol/L, sulfate 40 mmol/L, Chloride 35 mmol/L , bicarbonate 20 mmol/L , potassium 10 mmol/L) เหมาะสมกับผู้ป่วยกลุ่ม Chronic kidney disaese, congestive heart failure, liver disease with ascites ที่ทนต่อการเปลี่ยนแปลงสารน้ำในร่างกายและภาวะเกลือแร่ไม่สมดุลได้น้อย
ก่อนการผ่าตัดนิยมใช้สารที่มีชื่อว่า Polyethylene glycol โดยมีอัตราการสวนล้างอยู่ที่ 1-4 ลิตรต่อชั่วโมง ต่อเนื่องเป็นระยะเวลา 3-4 ชั่วโมในกรณีผู้ป่วยบางรายที่ไม่สามารถกลืนทาง ปากได้ สามารถให้ยาผ่านสายให้อาหารทางกระเพาะได้
Stimulant กระตุ้นการบีบตัวของลำไส้ ได้แก่ casanthranol, senokot, bisacodyl, and castor oil
วิธีการใช้ยา

อาการไม่พึงประสงค์จากการเตรียมลำไส้ (Adverse effects) (2)
- Dehydration
- Delayed return to normal bowel movement
- Metabolic disturbances ได้แก่ hypernatremia, hypokalemia,hypocalcemia, hyperphosphatemia, metabolic acidosis
- Decrease in exercise capacity and weight
- Increase plasma osmolarity and urea concentration
- Abdominal pain/Distention
- Cramps
- Insomnia
- Fatigue
- Nausea
- Patient distress
จนกระทั่งปี ค.ศ.2007 การศึกษาในผู้ป่วยและการใช้ Mechanical Bowel Preparation ที่เข้ารับการผ่าตัดลำไส้(3) สรุปผลไม่แตกต่างกันเมื่อเปรียบเทียบกับกลุ่มที่ไม่ได้ใช้ ในเรื่องการช่วยลดภาวะแทรกซ้อนจากการติดเชื้อ เช่น Surgical site infection และ anastomosis leakage รวมไปถึงทำให้รู้สึกคลื่นไส้และทำให้การทำงานของลำไส้กลับมาช้าลง (Delayed gastric emptying time) โดยการศึกษาส่วนใหญ่อ้างอิงจากการศึกษาในผู้ป่วยที่เข้ารับการผ่าตัด ลำไส้ (4, 5)ต่อมาจึงได้มีการศึกษาอีกมากมายเกี่ยวกับบทบาทของ Mechanical bowel preparation ในผู้ป่วยที่เข้าการผ่าตัดทางนรีเวชวิทยามากขึ้น(6-9) จนกระทั่งมีผลการศึกษาของ Jing Zhang cochrane review (2)เปรียบเทียบการเตรียมลำไส้ในผู้ป่วยที่เข้ารับการผ่าตัดทาง นรีเวชวิทยา พบว่า Mechanical bowel preparation มีประโยชน์ไม่แตกต่างกับการไม่เตรียมลำไส้ เช่น Surgical visualization quality, small an large bowel preparation, bowel handling, length of stay, surgical time รวมไปถึงภาวะแทรกซ้อนหลังการผ่าตัด แต่พบว่าใน กลุ่มผู้ป่วยที่ได้รับการเตรียมลำไส้มีอาการทางระบบทางเดินอาหาร เช่น ปวดท้อง ท้องอืด คลื่นไส้มากกว่า (10)
การศึกษาเปรียบเทียบการเตรียมลำไส้ก่อนการผ่าตัดทางนรีเวชวิทยา333 คน ที่โรงพยาบาลมหาราชนครเชียงใหม่พบว่าผู้ป่วยที่ไม่ได้เตรียมลำไส้ก่อนการผ่าตัด ไม่แตกต่างกันในด้าน surgeon perspective, ease of surgery, efficacy of bowel packinล, surgery visualization และ quality อย่างมีนัยยะสำคัญ แต่มีความแตกต่างกันในด้านคุณภาพ ชีวิตของผู้ป่วย ซึ่งผู้ป่วยที่ไม่ได้รับการเตรียมลำไส้มีความพึงพอใจมากกว่า(11)
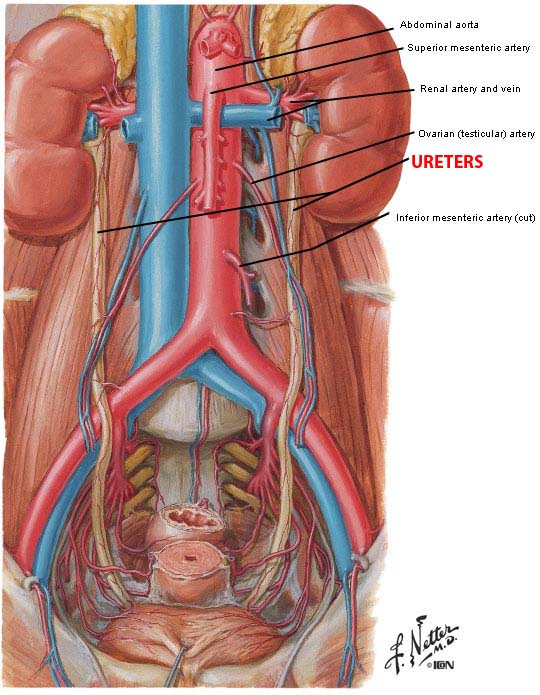
ในการผ่าตัดทางนรีเวชทั่วไปไม่มีความจำเป็นต้องเตรียมลำไส้ แต่ในบางกรณี การผ่าตัดอาจเกิดการบาดเจ็บต่อลำไส้ได้จึงมีการแนะนำให้เตรียมลำไส้ในผู้ป่วยที่มีความเสี่ยงดังกล่าว(6, 12) เช่น
- Advanced ovarian cancer cytoreductive surgery
- Severe PID
- Endometriosis
- Complex surgery
อย่างไรก็ตาม หลักฐานถึงประโยชน์ทางการเตรียมลำไส้ในผู้ป่วยนรีเวชยังมีค่อนข้างน้อย ดังนั้นจึงใช้หลักการเตรียมลำไส้จากกการศึกษาใน colorectal surgery เป็นส่วนใหญ่ ซึ่งแต่ก่อน เคยเชื่อว่าการเตรียมลำไส้สามารถลดภาวะแทรกซ้อนเรื่องไข้หลังผ่าตัดได้ อย่างไรก็ตาม ในปัจจุบันมี meta-analysis พบว่า mechanical bowel preparation ไม่มีประโยชน์ อีกทั้งยังอาจเกิดผลเสียคือทำให้เกิด Spillage of bowel contents ซึ่งเพิ่มการติดเชื้อตามมา ดังนั้นการเตรียมลำไส้ก่อนผ่าตัดอาจไม่จำเป็นในการผ่าตัดทางนรีเวช รวมไปถึงผู้ป่วยมะเร็งด้วย
บทบาทของการเตรียมลำไส้และการให้ยาปฏิชีวนะ
สำหรับยาปฏิชีวนะแบบรับประทานได้มีเริ่มมีการนำมาใช้ในการเตรียมลำไส้ก่อนการ
ผ่าตัดลำไส้ในปี ค.ศ.1940(13-16) ต่อมาได้มีการใช้อย่างแพร่หลายมากขึ้นในปี ค.ศ. 1970 ด้วย Nichol preparation* โดยมีหลักฐานแนะนำว่าช่วยอัตราการติดเชื้อที่แผลและการรั่วซึมของ แผลได้ การศึกษาเปรียบที่ผ่านมาในผู้ป่วยที่เข้ารับการผ่าตัดทางนรีเวชวิทยาด้วยเทคนิคผ่าเปิด หน้าท้อง การผ่าตัดผ่านทางช่องคลอดและการผ่าตัดส่องกล้องจำนวน 1,792 คน พบว่ามีภาวะ แทรกซ้อนจากการแผลผ่าตัดติดเชื้อและการบาดเจ็บของลำไส้ร้อยละ 0.79 และ 0.3 ตามลำดับ(17)
*Nichol preparation with Condon prep
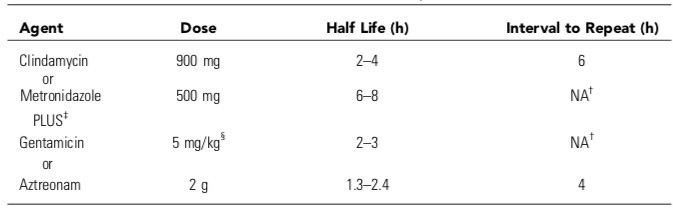
1g oral neomycin at 2pm ,3 pm and 10 pm and 1g erythromycin base at 2pm, 3 pm and 10 pm (or Metronidazole 500 mg แทน erythromycin for better tolerate cover anaerobic activity, enterohepatic circulation, clinical effective)
ตำรับยาปฏิชีวนะที่แนะนำ

การศึกษาเปรียบเทียบระหว่างการไม่เตรียมลำไส้กับการเตรียมลำไส้โดยใช้ยาปฏิชีวนะ แบบรับประทานร่วมกับ Mechanical bowel preparation (Combined preparation) ในผู้ป่วย มะเร็งนรีเวชที่เข้ารับการผ่าตัดพบว่าการเตรียมลำไส้ลดการติดเชื้อที่แผลผ่าตัดอย่างมีนัยยะสำคัญและได้มีการศึกษาเกี่ยวกับความสัมพันธ์ของการใช้ยาปฏิชีวนะและการติดเชื้อ Clostridium Difficile พบว่าการศึกษาส่วนใหญ่ยาปฏิชีวนะมีประสิทธิภาพในการลดการติดเชื้อนี้ได้(4, 18, 19) บางการศึกษาพบว่าช่วยเพิ่มภูมิต้านทานต่อเชื้อ Clostridium Difficile อีกด้วย(20) อย่างไรก็ตามยังไม่มีการศึกษาเกี่ยวกับผลลัพธ์ของการใช้เฉพาะยาปฏิชีวนะเปรียบเทียบกับการ ไม่เตรียมลำไส้ ซึ่งตั้งแต่ปีค.ศ. 1990 การเตรียมลำไส้ก่อนการผ่าตัดด้วยวิธี Combinded preparation มีการใช้อย่างแพร่หลาย จนกระทั่งในปี ค.ศ. 2000 การใช้ยาฏิชีวนะโดยการฉีดเข้า ทางหลอดเลือดเป็นที่นิยมมากกว่า ยาปฏิชีวนะแบบรับประทานจึงถูกพักการใช้งานไป(21)
สรุปข้อแนะนำเกี่ยวกับการเตรียมลำไส้ก่อนการผ่าตัด
- ไม่แนะนำให้เตรียมลำไส้ด้วยวิธี Mechanical bowel preparation ในผู้ป่วยที่เข้ารับการ ผ่าตัดนรีเวชแบบ ERAS (Enhanced Recovery After Surgery), minimally invasive surgery (MIS) รวมถึงการผ่าตัดมดลูดทางหน้าท้องที่มีความเสี่ยงต่ำต่อการบาดเจ็บของ ลำไส้
- การใช้ยาปฏิชีวนะแบบรับประทานร่วมกับ Mechanical bowel preparation พิจารณา ใช้เฉพาะกรณีผู้ป่วยที่มีความเสี่ยงสูงต่อการบาดเจ็บของลำไส้ในการผ่าตัด เพื่อลดภาวะ แทรกซ้อนจากการติดเชื้อ
- การพิจารณาใช้เฉพาะยาปฏิชีวนะแบบรับประทานในการเตรียมลำไส้สามารถใช้ได้แต่ยังไม่พบประโยชน์ชัดเจน เนื่องจากการศึกษาน้อย
- องค์กรที่แนะนำการเตรียมลำไส้ด้วยวิธี Combinded preparation ได้แก่ WHO (World Health Organization) Surgical Site Infection (SSI) Prevention Guidelines, American Society colon and rectal surgeon (ASCRS), Society of American Gastrointestinal and Endoscopic Surgeons (SAGES) และ American College of Surgeons (ASC) and Surgical Infection Society’s (SIS)
- องค์กรที่ไม่แนะนำให้เตรียมลำไส้ด้วย Mechanical bowel preparation ได้แก่ NICE, RCOG guideline, the Canadian Society of Colon and Rectal Sur- geons (CSCRS), American College of Obstetricians and Gynecologists(ACOG) Number 750(22, 23)
เอกสารอ้างอิง
- Cohen SL, Einarsson JI. The role of mechanical bowel preparation in gynecologic laparoscopy. Rev Obstet Gynecol. 2011;4(1):28-31.
- Zhang J, Xu L, Shi G. Is Mechanical Bowel Preparation Necessary for Gynecologic Surgery? A Systematic Review and Meta-Analysis. Gynecol Obstet Invest. 2015.
- Jung B, Lannerstad O, Pahlman L, Arodell M, Unosson M, Nilsson E. Preoperative mechanical preparation of the colon: the patient’s experience. BMC Surg. 2007;7:5.
- Toh JWT, Phan K, Ctercteko G, Pathma-Nathan N, El-Khoury T, Richardson A, et al. The role of mechanical bowel preparation and oral antibiotics for left-sided laparoscopic and open elective restorative colorectal surgery with and without faecal diversion. Int J Colorectal Dis. 2018;33(12):1781-91.
- Scarborough JE, Mantyh CR, Sun Z, Migaly J. Combined Mechanical and Oral Antibiotic Bowel Preparation Reduces Incisional Surgical Site Infection and Anastomotic Leak Rates After Elective Colorectal Resection: An Analysis of Colectomy-Targeted ACS NSQIP. Ann Surg. 2015;262(2):331-7.
- Diakosavvas M, Thomakos N, Psarris A, Fasoulakis Z, Theodora M, Haidopoulos D, et al. Preoperative Bowel Preparation in Minimally Invasive and Vaginal Gynecologic Surgery. ScientificWorldJournal. 2020;2020:8546037.
- Bakay K, Aytekin F. Mechanical bowel preparation for laparoscopic hysterectomy, is it really necessary? J Obstet Gynaecol. 2017;37(8):1032-5.
- Lijoi D, Ferrero S, Mistrangelo E, Casa ID, Crosa M, Remorgida V, et al. Bowel preparation before laparoscopic gynaecological surgery in benign conditions using a 1-week low fibre diet: a surgeon blind, randomized and controlled trial. Arch Gynecol Obstet. 2009;280(5):713-8.
- Kushnir CL, Diaz-Montes TP. Perioperative care in gynecologic oncology. Curr Opin Obstet Gynecol. 2013;25(1):23-8.
- Guenaga KF, Matos D, Wille-Jorgensen P. Mechanical bowel preparation for elective colorectal surgery. Cochrane Database Syst Rev. 2011(9):CD001544.
- Suadee W, Suprasert P. Appropriate Bowel Preparation for Laparotomy Gynecologic Surgery: A Prospective, Surgeon-Blinded Randomized Study. Gynecol Obstet Invest. 2017;82(3):287-93.
- Iyer R, Gentry-Maharaj A, Nordin A, Burnell M, Liston R, Manchanda R, et al. Predictors of complications in gynaecological oncological surgery: a prospective multicentre study (UKGOSOC-UK gynaecological oncology surgical outcomes and complications). Br J Cancer. 2015;112(3):475-84.
- Garfinkle R, Abou-Khalil J, Morin N, Ghitulescu G, Vasilevsky CA, Gordon P, et al. Is There a Role for Oral Antibiotic Preparation Alone Before Colorectal Surgery? ACS-NSQIP Analysis by Coarsened Exact Matching. Dis Colon Rectum. 2017;60(7):729-37.
- Cannon JA, Altom LK, Deierhoi RJ, Morris M, Richman JS, Vick CC, et al. Preoperative oral antibiotics reduce surgical site infection following elective colorectal resections. Dis Colon Rectum. 2012;55(11):1160-6.
- Hayashi MS, Wilson SE. Is there a current role for preoperative non-absorbable oral antimicrobial agents for prophylaxis of infection after colorectal surgery? Surg Infect (Larchmt). 2009;10(3):285-8.
- McSorley ST, Steele CW, McMahon AJ. Meta-analysis of oral antibiotics, in combination with preoperative intravenous antibiotics and mechanical bowel preparation the day before surgery, compared with intravenous antibiotics and mechanical bowel preparation alone to reduce surgical-site infections in elective colorectal surgery. BJS Open. 2018;2(4):185-94.
- Kafy S, Huang JY, Al-Sunaidi M, Wiener D, Tulandi T. Audit of morbidity and mortality rates of 1792 hysterectomies. J Minim Invasive Gynecol. 2006;13(1):55-9.
- Wren SM, Ahmed N, Jamal A, Safadi BY. Preoperative oral antibiotics in colorectal surgery increase the rate of Clostridium difficile colitis. Arch Surg. 2005;140(8):752-6.
- Krapohl GL, Phillips LR, Campbell DA, Jr., Hendren S, Banerjee M, Metzger B, et al. Bowel preparation for colectomy and risk of Clostridium difficile infection. Dis Colon Rectum. 2011;54(7):810-7.
- Kim EK, Sheetz KH, Bonn J, DeRoo S, Lee C, Stein I, et al. A statewide colectomy experience: the role of full bowel preparation in preventing surgical site infection. Ann Surg. 2014;259(2):310-4.
- Zelhart MD, Hauch AT, Slakey DP, Nichols RL. Preoperative antibiotic colon preparation: have we had the answer all along? J Am Coll Surg. 2014;219(5):1070-7.
- Committee on Gynecologic P. ACOG Committee Opinion No. 750: Perioperative Pathways: Enhanced Recovery After Surgery. Obstet Gynecol. 2018;132(3):e120-e30.
- Fanning J, Valea FA. Perioperative bowel management for gynecologic surgery. Am J Obstet Gynecol. 2011;205(4):309-14.