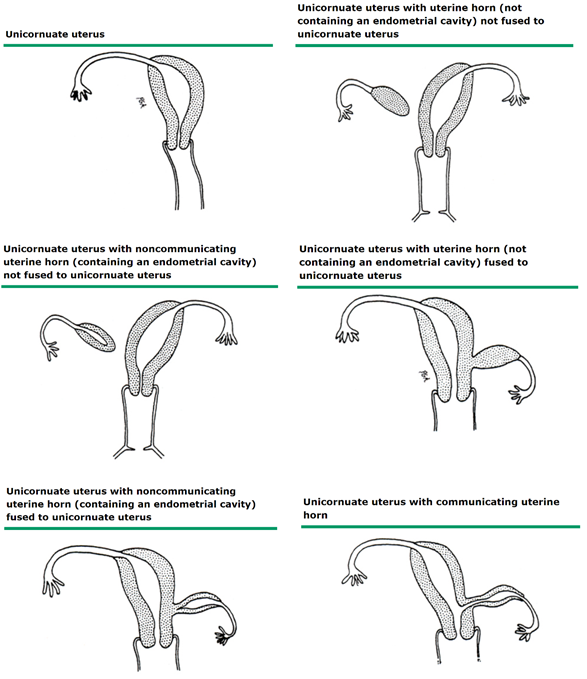
โรคผิวหนังในสตรีตั้งครรภ์ (Skin diseases in pregnancy)
โรคผิวหนังในสตรีตั้งครรภ์ (Skin diseases in pregnancy)
นพ.พุทธิภณ ไชยพรหม
อาจารย์ที่ปรึกษา อ.พญ.อุบล แสงอนันต์
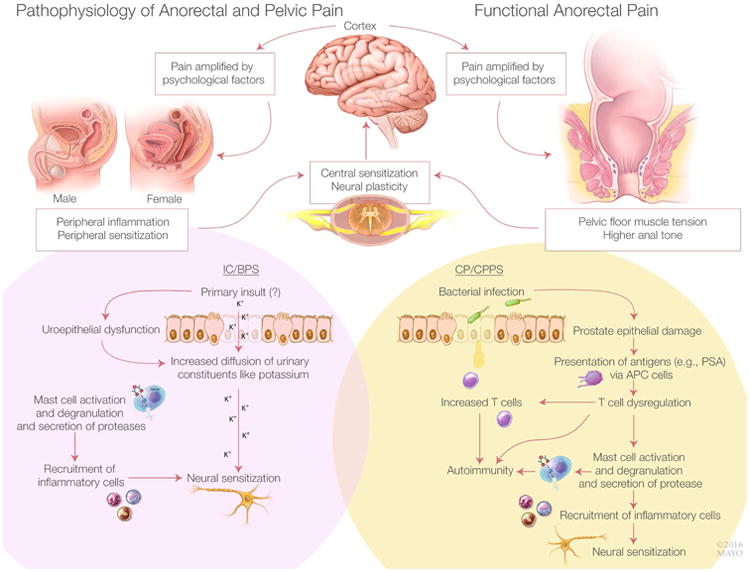
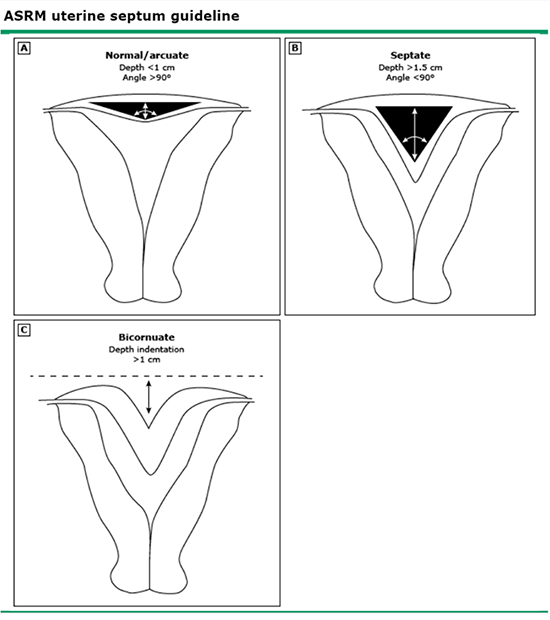
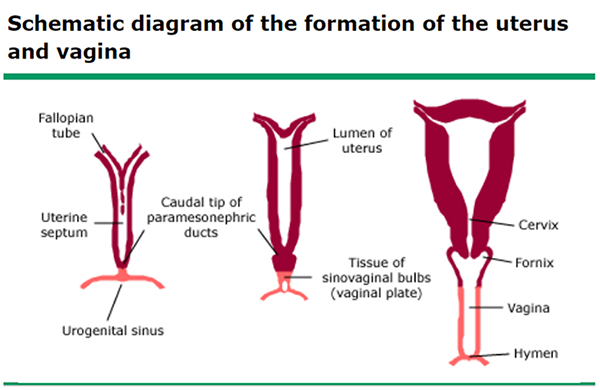
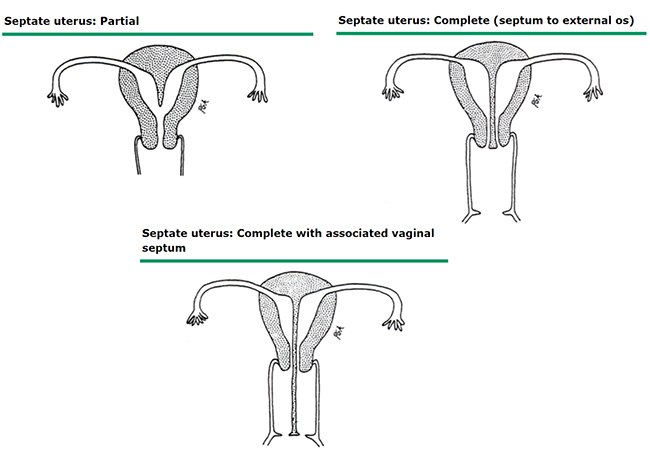
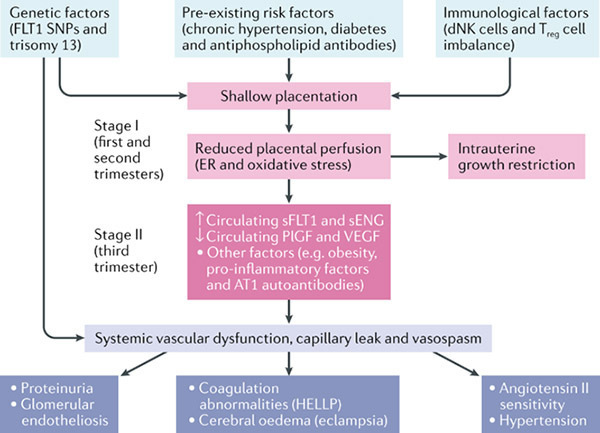
ลักษณะรอยโรคที่ปรากฏบนผิวหนังในระหว่างตั้งครรภ์ หรือหลังคลอด สามารถจัดแบ่งเป็น 2 กลุ่มใหญ่ คือกลุ่มที่เป็นรอยโรคผิวหนังที่พบได้ทั่วไปทั้งในสตรีตั้งครรภ์ หรือไม่ตั้งครรภ์ก็ตาม (dermatological conditions not specific to pregnancy) และกลุ่มที่เป็นรอยโรคผิวหนังชนิดจำเพาะที่เกิดในสตรีตั้งครรภ์ (pregnancy-specific dermatoses)1 จากการเก็บรวบรวมข้อมูลส่วนใหญ่ของสตรีตั้งครรภ์ที่มีปัญหาเรื่องผิวหนัง พบว่า โรคในกลุ่ม pregnancy-specific dermatoses โรคที่พบมากที่สุด คือ atopic eruption of pregnancy รองลงมาคือโรค polymorphic eruption of pregnancy ส่วนอีกกลุ่มหนึ่ง โรคที่พบมากที่สุด คือ urticaria และ Angioedema รองลงมาเป็นกลุ่มโรคผิวหนังที่มีสาเหตุมาจากเชื้อไวรัสต่างๆ2-5 ในบทความนี้จะกล่าวถึงกลุ่มโรคดังกล่าว เพื่อให้สูติแพทย์นำความรู้ไปประยุกต์ใช้ในการดูแลรักษาสตรีตั้งครรภ์ได้อย่างเหมาะสม
Dermatological conditions not specific to pregnancy
โรคเริม สาเหตุเกิดจากการติดเชื้อ herpes simplex virus (HSV) ซึ่งได้แก่ HSV-1 และ HSV-2 การได้รับเชื้อไวรัสครั้งแรกจัดเป็น primary herpes simplex infection ซึ่งภายหลังจากการติดเชื้อครั้งแรก เชื้อไวรัสจะไปซ่อนตัวอยู่ในระยะ latent stage ที่ dorsal root ซึ่งจะไม่ก่อให้เกิดอาการของโรค แต่หากมีปัจจัยกระตุ้น ให้เกิด reactivation ของเชื้อขึ้นมาจะ จัดเป็น recurrent herpes simplex infection ในหญิงตั้งครรภ์ที่เป็นโรค primary herpes simplex infection มีโอกาสติดต่อไปยังทารกได้มากกว่า recurrent herpes simplex infection โดยเฉพาะในระหว่างคลอด เนื่องจากทารกมีการสัมผัสรอยโรคโดยตรง หรืออาจติดเชื้อขณะอยู่ในครรภ์ หรือหลังคลอดได้เช่นกัน แต่โอกาสเกิดการติดเชื้อในทารกน้อยกว่าระหว่างคลอด6-8
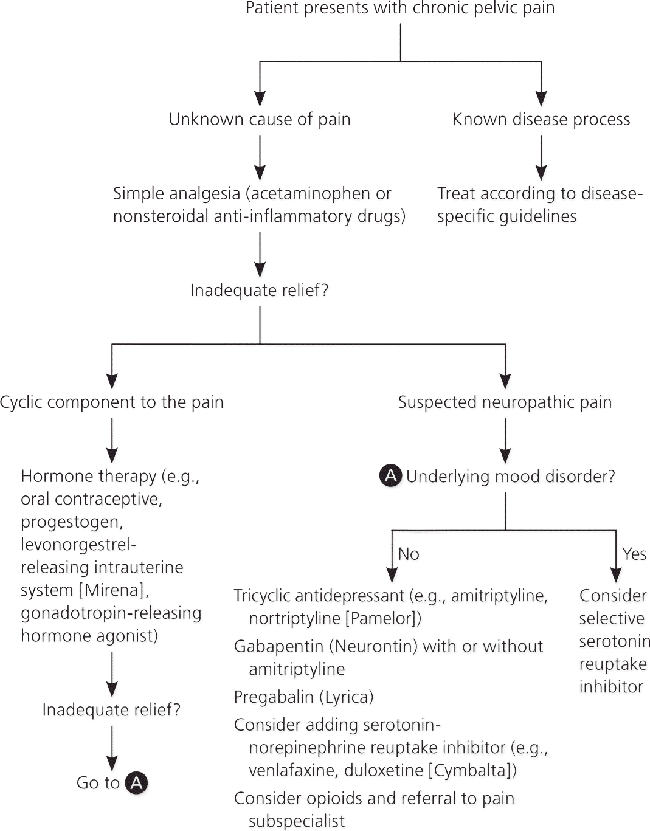
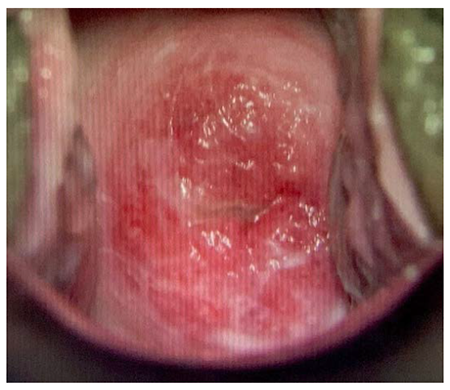
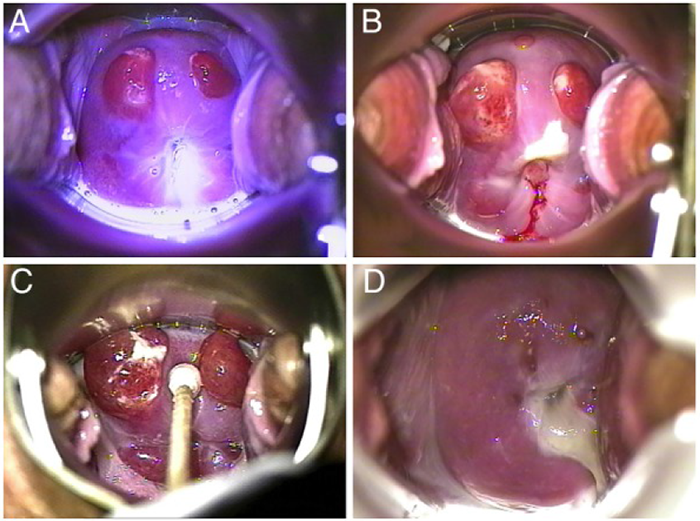
บริเวณติดเชื้อที่พบได้บ่อย ได้แก่บริเวณริมฝีปาก (herpes labialis, gingivostomatitis) ซึ่งจะสัมพันธ์กับเชื้อ HSV-1 เป็นส่วนใหญ่ แต่ก็พบจาก HSV-2 ได้บ้าง และบริเวณอวัยวะเพศ (herpes genitalis) ที่สัมพันธ์กับการติดเชื้อ HSV-2 ซึ่งมีความสำคัญมากหากมีการติดเชื้อนี้ขณะตั้งครรภ์ รอยโรคเริมที่อวัยวะเพศ ทั้ง primary และ recurrent genital herpes simplex infection บนผิวหนังจะพบลักษณะเป็นกลุ่มของตุ่มน้ำใส โดยขนาดของตุ่มน้ำมีขนาดใกล้เคียงกัน บนพื้นสีแดงของผิวหนัง (รูปที่1) อาการร่วมที่พบได้บ่อย คือ อาการแสบ คัน ร้อน ภายหลังจะมีการแตกของตุ่มน้ำเกิดเป็นแผลตื้นๆ หลายแผลติดกัน เมื่อแผลแห้งจะตกสะเก็ดและ หายไปในที่สุด
โรคเริมสามารถวินิจฉัยได้จากอาการทางคลินิกเป็นสำคัญ อย่างไรก็ตามควรได้รับการส่งตรวจทางห้องปฏิบัติการเพื่อยืนยันการวินิจฉัยในกรณีที่วินิจฉัยได้ยากในบางกรณี การวินิจฉัยจากรอยโรคบริเวณอวัยวะเพศ อย่างเดียว พบว่ามีความไว (sensitiveity) ร้อยละ 40% และมี ความจำเพาะ (specificity) ถึงร้อยละ 99%6 สำหรับการส่งตรวจทางห้องปฏิบัติการที่ทำได้ง่าย คือการทำ Tzanck test วิธีการคือขูดเนื้อเยื่อบริเวณก้นแผล แล้วป้ายบนสไลด์ ทิ้งไว้ให้แห้ง แล้วย้อมด้วยสี wright หรือ Giemsa stain แล้วดูลักษณะเซลล์ในกล้องจุลทรรศน์ จะพบ multinucleated giant cell
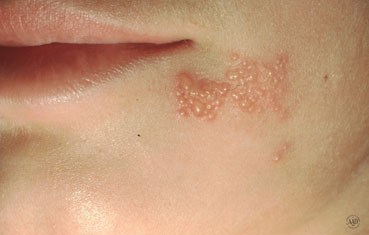
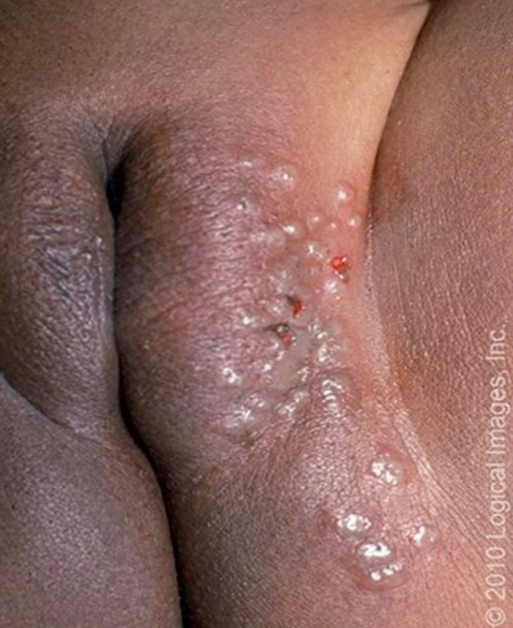
รูปที่ 1 รูปบน herpes labialis รูปล่าง herpes genitalisบริเวณอวัยวะเพศ (ที่มา https://pariserderm.com/services/ common-concerns/herpes-simplex/)
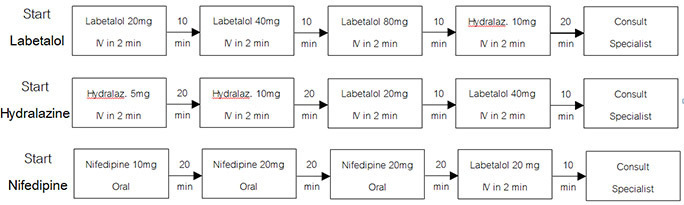
สำหรับการรักษาสตรีตั้งครรภ์ที่ได้รับการวินิจฉัยแล้วว่าเป็นโรคเริม จะต้องแยกว่าเป็น primary herpes simplex infection หรือ symptomatic recurrent herpes simplex infection ก่อนพิจารณาให้การรักษาด้วยยา acyclovir หรือ valacyclovir ตามคำแนะนำของ American college of obstetricians and gynecologists (ACOG) ในปี 2007 (ตารางที่ 1) ซึ่งยาทั้งสองตัว จัดอยู่ใน pregnancy category B6
|
Indication |
Acyclovir |
Valacyclovir |
|
Primary or first-episode infection |
400 mg orally, three times daily, for 7-10 days |
1 g orally, twice daily, for 7-10 days |
|
Symptomatic recurrent episode infection |
400 mg orally, three times daily, for 5 days or 800 mg orally, twice daily, for 5 days |
500 mg orally, twice daily, for 3 days or 1 g orally, daily, for 5 days |
|
Daily suppression |
400 mg orally, three times daily, from 36 weeks estimated gestational age until delivery |
|
|
Severe or disseminated disease |
5-10 mg/kg, intravenously, every 8 hours for 2-7 days, then oral therapy for primary infection to complete 10 days |
|
ตารางที่ 1 ดัดแปลงมาจาก ACOG : Management of herpes in pregnancy 2007
โรคอีสุกอีใส และโรคงูสวัด สาเหตุเกิดจากการติดเชื้อ vericella zoster virus (VZV) เหมือนกัน ถ้าเป็นการติดเชื้อนี้ครั้งแรกจะก่อโรคอีสุกอีใส เชื้อนี้จะมีการเคลื่อนตัวไปตามแนวเส้นประสาทที่อยู่ใกล้ๆ และ ไปหลบซ่อนตัวอยู่ในระยะแฝงที่ระบบประสาทเช่นเดียวกับ HSV ซึ่งจะไม่ก่อให้เกิดอาการของโรค แต่หากมีปัจจัยกระตุ้น ให้เกิด reactivation ของเชื้อขึ้นมา ก็จะแสดงอาการของโรคงูสวัด อย่างไรก็ตามการติดเชื้อ VZV ในสตรีตั้งครรภ์มีอัตราการเกิดที่ค่อนข้างต่ำ เนื่องมาจากปัจจุบันมีการรณรงค์ให้มีการฉีดวัคซีนป้องกันโรค สตรีตั้งครรภ์ ที่ติดเชื้อ VZV จะสามารถถ่ายทอดเชื้อนี้ผ่านทางรก (transplacental transmission) ไปสู่ทารกในครรภ์ได้ นอกการนี้ติดเชื้อในช่วงใกล้คลอดหรือหลังคลอด ก็สามารถติดต่อสู่ทารกได้ผ่านทาง respiratory droplets หรือ direct contact ส่งผลให้ทารกติดเชื้อได้ ซึ่งเป็นสาเหตุหนึ่งที่ทำให้เด็กเสียชีวิตได้9, 10
ทั้งโรคอีสุกอีใส และงูสวัด ก่อนที่จะมีรอยโรคที่ผิวหนังปรากฏ จะมีอาการปวด แสบ บริเวณผิวหนังนำมาก่อน ประมาณ 1-3 วัน หรืออาจมีไข้ อ่อนเพลียได้ แล้วจึงเริ่มมีผื่นแดง จากนั้นจะเริ่มมีกลุ่มของตุ่มน้ำ ขนาดใหญ่เล็กสลับกันไป โดยในโรคอีสุกอีใส อาจพบรอยโรคหลายระยะปนกัน การกระจายของตุ่มน้ำจะพบตามลำตัว มากกว่าแขนและขา (รูปที่ 2) สำหรับโรคงูสวัดนั้น การกระจายของผื่นและกลุ่มตุ่มน้ำเป็นไปตาม dermatome (รูปที่ 2) แล้วค่อยๆแห้งลงจนตกสะเก็ดไปในเวลาประมาณ 3 สัปดาห์ ในสตรีตั้งครรภ์ต้องเฝ้าระวังการเกิดภาวะแทรกซ้อนที่อาจจะเกิดตามมา ได้แก่การเกิดปอดอักเสบ (pneumonia) ตับอักเสบ (hepatitis) และภาวะสมองอักเสบ (encephalitis)
การวินิจฉัยโรคอีสุกอีใสและงูสวัดอาศัยอาการทางคลินิกเป็นสำคัญ แต่ในรายที่วินิจฉัยยากอาจพิจารณาส่งตรวจทางห้องปฏิบัติการ โดยเก็บ fluid จาก vesicles ส่งตรวจ PCR หรือ culture เพื่อช่วยในการวินิจฉัย หรืออาจทำ Tzanck test ซึ่งจะให้ผลเช่นเดียวกับโรคเริม สำหรับการรักษาหญิงตั้งครรภ์ที่เป็นโรคอีสุกอีใสและงูสวัด จากคำแนะนำของ ACOG ในปี 2015 พิจารณาให้ acyclovir รับประทานภายใน 24 ชั่วโมงที่เกิดผื่นขึ้น โดยทานยา acyclovir 800 mg 5 ครั้งต่อวัน เป็นเวลา 7 วัน10, 11
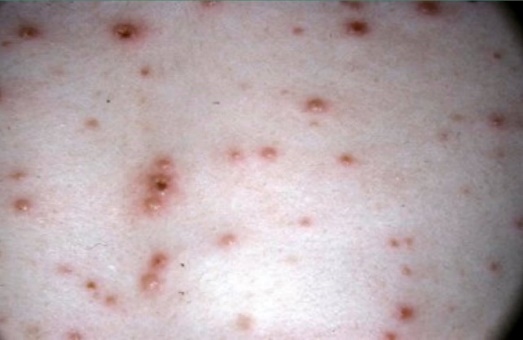
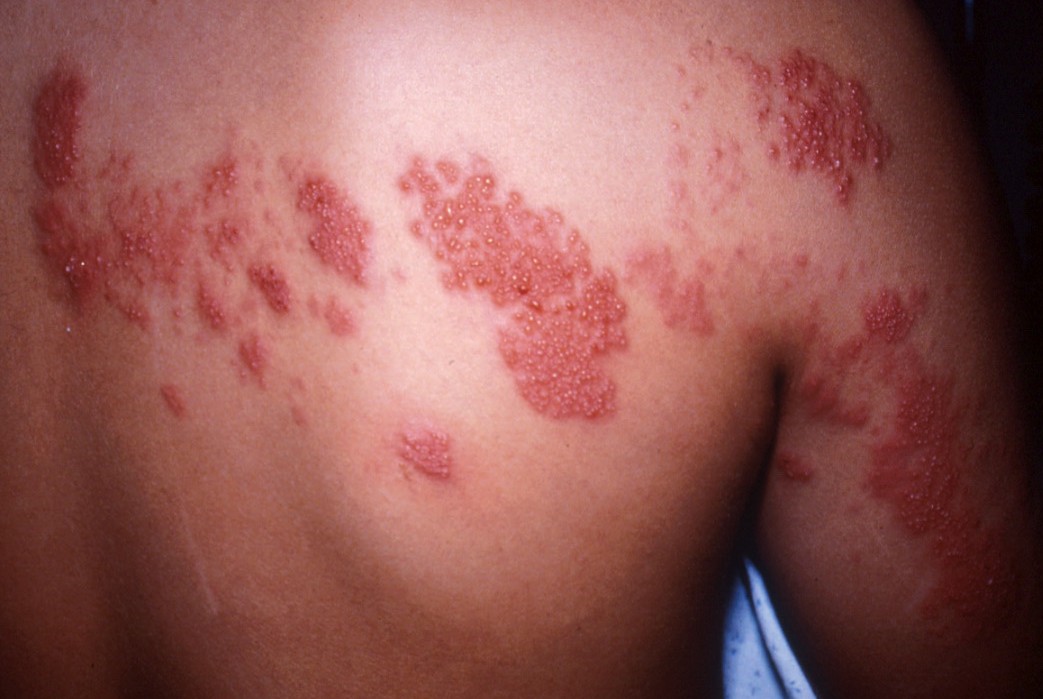
รูปที่ 2 รูปบน chickenpox รูปล่าง herpes zoster (ที่มา uptodate 2019 : varicella-zoster virus infection in pregnancy)
โรคซิฟิลิส เกิดจากการติดเชื้อแบคทีเรีย Treponema pallidum หลังจากได้รับเชื้อครั้งแรก จะแสดงลักษณะรอยโรคที่อวัยวะเพศ ซึ่งเป็นการดำเนินโรคในระยะแรก สำหรับการติดเชื้อที่เป็นระยะที่สอง หรือระยะที่สามนั้น การดำเนินของโรคสามารถทำให้เกิดโรคในระบบต่างๆ ในร่างกายได้หลายระบบ ในบทความนี้จะกล่าวถึง การติดเชื้อในระยะแรก (primary syphilis) ในระหว่างตั้งครรภ์ และสามารถติดต่อไปสู่ทารกในครรภ์ได้ โดยผ่าน transplacenta transmission ซึ่งทำให้เกิด การติดเชื้อในทารกที่คลอดออกมาได้ รอยโรคในระยะ primary syphilis จะพบเป็นตุ่มน้ำขนาดเล็กๆบริเวณอวัยวะเพศ ต่อมาตุ่มน้ำเหล่านี้จะแตกรวมกันเป็นแผลเดียว (รูปที่ 3) ซึ่งมีขนาดใหญ่ขึ้น มีขนาดเส้นผ่าศูนย์กลาง 1-2 เซนติเมตร มีขอบนูนแข็ง ไม่เจ็บ มีก้นแผลที่สะอาด มีน้ำเหลืองเยิ้มคลุมแผล ส่วนใหญ่แผลจะหายเองได้ในระยะเวลา 3-6 สัปดาห์ และอาจพบต่อมน้ำเหลืองขาหนีบโตได้
การวินิจฉัยโรคซิฟิลิสจากลักษณะของแผลที่อวัยวะเพศมีความไวร้อยละ 30 แต่มีความจำเพาะสูงถึงร้อยละ 90 12 การส่งตรวจทางห้องปฏิบัติการที่ช่วยยืนยันการวินิจฉัยคือการตรวจหนองจากก้นแผลด้วย Dark-field microscopy เพื่อตรวจหาตัวเชื้อ Treponema pallidum ในขณะที่การส่งตรวจ serology เช่น Venereal Disease Research Laboratory (VDRL) และ Rapid Plasma Reagin (RPR) ในระยะแรกอาจจะให้ผลลบได้ ถ้าสงสัยจำเป็นต้องส่งตรวจซ้ำ ในปัจจุบันสตรีตั้งครรภ์ทุกคนที่มาฝากครรภ์ในครั้งแรกจะได้รับการคัดกรองโรคซิฟิลิสด้วย VDRL หรือ RPR ซึ่งเป็นการค้นหาโรคซิฟิลิสในระยะ secondary or latent syphilis ที่อาจจะไม่พบอาการแสดงทางคลินิก
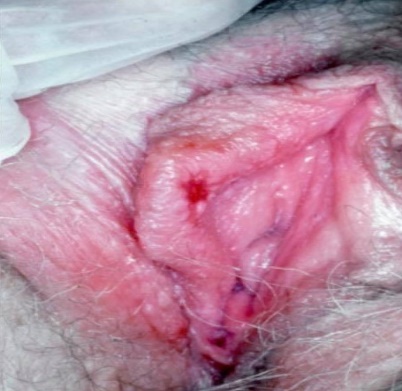
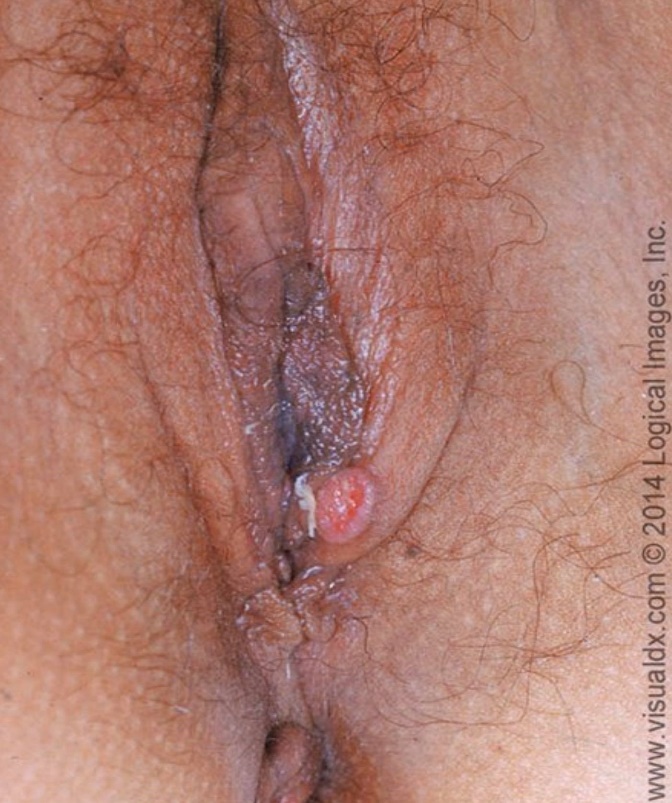
รูปที่ 3 แสดงลักษณะ primary syphilis (ที่มา uptodate 2020 : syphilis in pregnancy )
การรักษาโรคซิฟิลิสระยะแรก ในสตรีตั้งครรภ์ ตามคำแนะนำของ WHO ในปี 2017 ให้รักษาด้วยยา benzathine penicillin G 2.4 ล้านยูนิต ฉีดเข้ากล้ามครั้งเดียว สำหรับผู้ที่มีประวัติแพ้ยากลุ่ม penicillin ควรต้องทำการ desensitization ก่อนเสมอ หาก desensitization ไม่ผ่าน อาจพิจารณาให้ยา erythromycin 500 มิลลิกรัม รับประทาน วันละ 4 ครั้ง เป็นเวลานาน 14 วัน หรือใช้ยา ceftriaxone 1 กรัม ฉีดเข้ากล้าม วันละครั้ง เป็นเวลานาน 10-14 วัน 13 นอกจากนี้ต้องให้การรักษาคู่นอนหรือสามีที่มีเพศสัมพันธ์กับผู้ติดเชื้อภายใน 90 วันด้วย ส่วนทารกในครรภ์ควรได้รับการติดตามสุขภาพในครรภ์ด้วยอัลตราซาวด์อย่างใกล้ชิด
โรคผิวหนังที่เกี่ยวข้องกับระบบภูมิคุ้มกัน ที่พบบ่อยในระหว่างตั้งครรภ์ โรคผื่นภูมิแพ้ผิวหนัง (atopic dermatitis) โรคผื่นลมพิษ (urticaria) และโรคสะเก็ดเงิน (psoriasis)ในขณะตั้งครรภ์ สตรีตั้งครรภ์อาจมีอาการของโรคเดิมที่เปลี่ยนแปลงในทางแย่ลงได้
โรคผื่นภูมิแพ้ผิวหนัง (atopic dermatitis) เป็นโรคผิวหนังอักเสบเรื้อรัง เป็นๆ หายๆ โดยอาจเกิดร่วมกับกลุ่มอาการภูมิแพ้อื่นๆ เช่น โรคหืด โรคแพ้ละอองเกสรดอกไม้ เป็นต้น ยังไม่ทราบสาเหตุของโรคที่ชัดเจน แต่ในปัจจุบันยอมรับว่าพันธุกรรมเป็นสาเหตุหนึ่ง ที่มีส่วนสำคัญในการก่อโรคเหล่านี้ ลักษณะอาการของรอยโรคจะมี 3 ระยะ ดังนี้
- ผื่นระยะเฉียบพลัน ซึ่งจะเป็นผื่นบวมแดง คัน และมีตุ่มน้ำ เมื่อตุ่มน้ำแตกจะมีน้ำเหลืองไหลออกมา (รูปที่ 4)
- ผื่นระยะกึ่งเฉียบพลัน ผื่นจะมีลักษณะเป็นขุย คัน อาจมีตุ่มน้ำบ้าง แต่ไม่พบน้ำเหลืองไหลซึม (รูปที่ 4)
- ผื่นระยะเรื้อรัง ลักษณะเป็นผื่นหนา แห้ง มีสะเก็ด ผิวแตกเป็นร่อง12 (รูปที่ 4)
โรคผื่นภูมิแพ้ผิวหนังนี้พบได้บ่อยในสตรีตั้งครรภ์ และภาวะตั้งครรภ์ก็ส่งผลทำให้โรค แย่ลง ดีขึ้น หรือคงเดิม ก็ได้ แต่จากการศึกษาส่วนใหญ่พบว่าผู้ป่วยจะมีอาการของโรคที่แย่ลงในช่วงการตั้งครรภ์ ทั้งนี้อาจเนื่องมาจากการเปลี่ยนแปลงของระบบภูมิคุ้มกันในช่วงการตั้งครรภ์
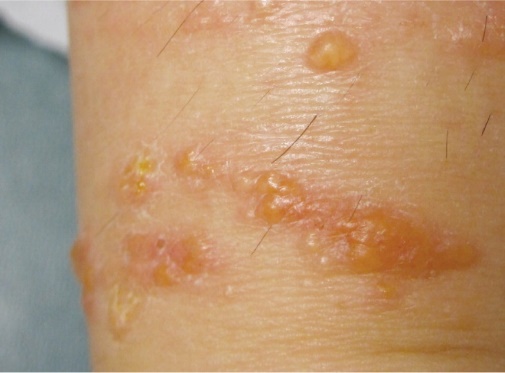
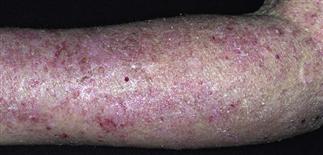
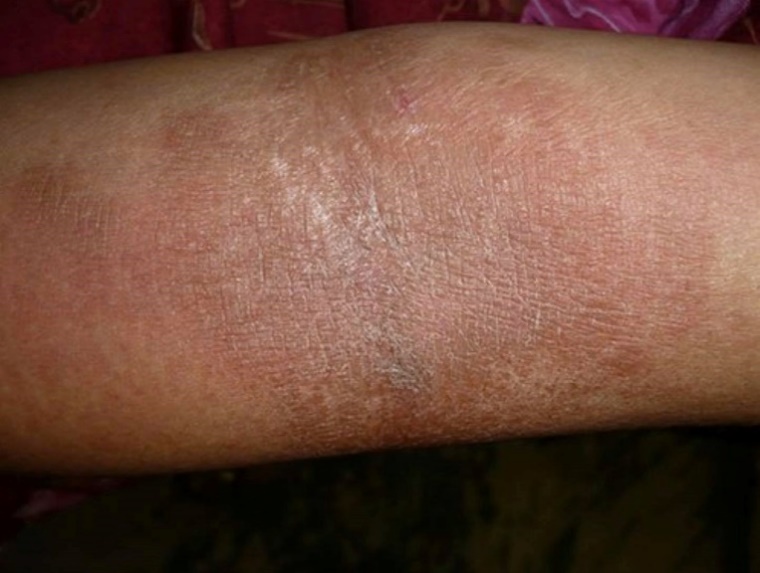
รูปที่ 4 รูปบน Acute atopic dermatitis รูปกลาง Subacute atopic dermatitis รูปล่าง Chronic atopic dermatitis
(ที่มา https://www.aafp.org/afp/2012/0701/p35.html, https://plasticsurgerykey.com/subacute-eczematous-inflammation/)
จากการศึกษาที่ผ่านมาในส่วนของ การแสดงลักษณะอาการของโรคนี้ในสตรีตั้งครรภ์ พบว่ารอยโรคที่ผิวหนังจะปรากฏที่ตำแหน่งบริเวณข้อพับ ซอกแขนขา (flexural surface of extremities) รองลงมาจะเป็น ใบหน้า มือและเท้า ในขณะที่บริเวณลำตัวพบได้น้อย13 การวินิจฉัยอาศัยอาการทางคลินิกเป็นสำคัญ โดยอาการที่สำคัญได้แก่ อาการคัน (pruritus) อาการเรื้อรังหรือกลับมาเป็นซ้ำ (chronic or recurring course) ลักษณะรูปแบบผื่นและการกระจายของผื่น (typical appearing rash and distribution) ประวัติภูมิแพ้อื่นๆ หากผู้ป่วยให้ข้อมูลเดิมจากประวัติก่อนหน้านี้ว่าเคยได้รับการวินิจฉัยมาก่อนก็จะง่ายขึ้น แต่หากไม่เคยเป็นมาก่อน ก็อาจจะปรากฏรอยโรคครั้งแรกในขณะตั้งครรภ์ ก็เป็นไปได้
การรักษาโรคผื่นภูมิแพ้ ในขณะตั้งครรภ์ จะเหมือนกับการรักษาขณะที่ไม่ตั้งครรภ์ ซึ่งประกอบด้วย13, 14 การให้คำแนะนำแก่ผู้ป่วยให้เข้าใจถึงโรคที่เป็น รวมถึงการควบคุมปัจจัยที่กระตุ้นให้เกิดโรค เช่นงดอาบน้ำอุ่น ซึ่งจะทำให้ผิวแห้งง่าย กับการรักษาความชุ่มชื่นของผิวหนัง ได้แก่ lotion, oil, Vaseline และ urea cream โดยแนะนำให้ทาสารเพิ่มความชุ่มชื่นที่ผิวหนังได้บ่อยๆ การใช้ยาเพื่อลดอาการคัน ซึ่งเป็นอาการหนึ่งที่เด่นชัดในโรคนี้ ยาที่ใช้ได้แก่ ยากลุ่ม antihistamine ซึ่งสามารถใช้ได้ทั้ง first generation และ second generation (ตารางที่2) สำหรับ ACOG, American College of Allergy Asthma and Immunology ได้ให้คำแนะนำว่า ยา chlopheniramine และ tripelennamine จัดเป็น drug of choice ที่ใช้ในสตรีตั้งครรภ์ นอกจากนี้ สามารถพิจารณาใช้ cetirizine และ loratadine เมื่อพ้นระยะสามเดือนแรกของการตั้งครรภ์ไปแล้ว15 ส่วนการใช้ยา corticosteroid ชนิดทา เพื่อลดการอักเสบ ซึ่งยากลุ่มนี้จัดอยู่ใน pregnancy category C โดยแนะนำให้ผู้ป่วยทายาสเตอรอยด์ที่มีฤทธิ์อ่อน หรือปานกลาง วันละ 2 ครั้ง เมื่อควบคุมอาการของโรคได้ ควรลดการใช้ยาทาลง หรือหยุดยา หรืออาจพิจารณาทายาเป็นช่วงๆ ส่วนยาสเตอรอยด์ที่มีฤทธิ์สูง ให้ใช้เป็น second-line หากต้องใช้ควรทาเป็นเวลาสั้นๆ13, 14 ผลข้างเคียงของยาเหล่านี้ ทำให้ผิวหนังบริเวณที่ทายาบางลง หลอดเลือดใต้ผิวหนังเปราะแตกง่าย เป็นต้น
โรคผื่นลมพิษ (Urticaria) เป็นภาวะที่มีการบวมน้ำ (Wheal) ของผิวหนังแท้ส่วนบน (Superficial dermis) มีขอบเขตชัดเจน และล้อมรอบด้วยสีแดง (Flare) มีอาการคันหรือแสบ ร่วมด้วยอาการเป็นอยู่ชั่วคราว 24-48 ชั่วโมง ซึ่งสาเหตุส่วนใหญ่เกิดจาก การแพ้ เช่นการแพ้ยาแพ้อาหาร การติดเชื้อ เป็นต้น โดยกลไกการเกิดผื่นลมพิษ มาจากการกระตุ้น mast cell และ basophil ให้หลั่งสารต่างๆ (mediators) ก่อให้เกิดการขยายตัวของหลอดเลือดบริเวณผิวหนัง ทำให้สารน้ำไหลออกนอกหลอดเลือด เกิดการบวมของผิวหนัง การวินิจฉัยอาศัยการซักประวัติถึงปัจจัยกระตุ้นให้เกิดอาการ ร่วมกับการดูรอยโรคที่ผิวหนังที่จะมีลักษณะเป็น Wheal and flare 16, 17 (รูปที่ 5)
|
Drug name |
Pregnancy category |
|
Chlorpheniramine |
B |
|
Cyproheptadine |
B |
|
Dexchlorpheniramine |
B |
|
Hydroxyzine |
C |
|
Tripelennamine |
B |
|
Drug name |
Pregnancy category |
|
Cetirizine |
B |
|
Fexofenadine |
C |
|
Loratidine |
B |
|
Levocetrizine |
B |
|
Desloratidine |
C |
ตารางที่ 2 First และ Second generation antihistamines
สำหรับผื่นลมพิษที่เกิดขึ้นในขณะตั้งครรภ์ ยังไม่ทราบสาเหตุที่แน่ชัด ส่วนหนึ่งเชื่อว่าเป็นผลมาจากการเปลี่ยนแปลงของฮอร์โมนในร่างกายในช่วงตั้งครรภ์ โดยเฉพาะ ฮอร์โมน estrogen และ progesterone อย่างไรก็ตามหากสงสัยภาวะนี้ในขณะตั้งครรภ์ ต้องวินิจฉัยแยกโรคจาก pruritic urticarial papules and plaques of pregnancy (PUPPP) และ Pemphigoid gestationis แนวทางการรักษาโรคผื่นลมพิษ ในขณะตั้งครรภ์ ไม่แตกต่างจากภาวะไม่ตั้งครรภ์ คือการหลีกเลี่ยงสิ่งกระตุ้นที่ทำให้เกิดผื่น ร่วมกับการใช้ยาในกลุ่ม antihistamines ส่วนใหญ่จะถูกรักษาด้วย second generation antihistamines เช่น cetirizine, levocetirizine หรือ loratadine ซึ่งจัดเป็น Pregnancy category B การบริหารยานั้นทำได้ง่าย โดยให้รับประทานทานเพียงวันละครั้ง16, 17
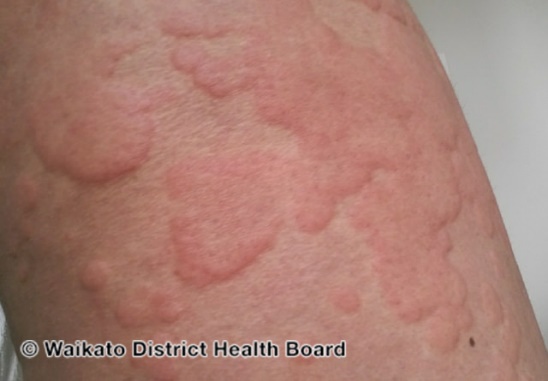
รูปที่ 5 Urticaria (ที่มา https://dermnetnz.org/topics/heat-urticaria/)
โรคสะเก็ดเงิน (Psoriasis) เป็นโรคผิวหนังอักเสบเรื้อรัง ซึ่งเกิดจากปัจจัยทางพันธุกรรมและสิ่งแวดล้อม โดยมีรอยโรคที่สำคัญคือ มีผื่นที่ผิวหนัง เป็นผื่นนูนแดง ปกคลุมด้วยสะเก็ดสีเงิน (Erythematous, thickening with silvery scale) (รูปที่ 6)
อาจเห็นผิวหนังรอบๆมีสีซีดกว่าผิวหนังปกติ (Pale blanch ring) สะเก็ดสีเงินติดแน่น ถ้าขูดสะเก็ดออกจะพบจุดเลือดออก (pinpoint bleeding) เรียกว่า Auspitz sign นอกจากผิวหนังแล้ว ยังพบความผิดปกติของเล็บและข้อ โดยลักษณะของเล็บจะเป็น เล็บบุ๋ม (Pitting nail) เล็บมีสีขาวแทรกในตัวเล็บ (Leukonychia) เล็บมีสีเหลืองเป็นวง (Oil spot) มีการหนาตัวขึ้นของผิวหนังใต้เล็บ (Subungual hyperkeratosis) เป็นต้น และมีการอักเสบของข้อร่วมด้วย การวินิจฉัยโรคอาศัยการซักประวัติ การตรวจร่างกาย และการตัดชิ้นเนื้อส่งตรวจทางพยาธิวิทยา12 ในขณะตั้งครรภ์ พบว่าการดำเนินโรคสะเก็ดเงินดีขึ้นถึง 40-60 % ทั้งนี้อาจเนื่องมาจากอิทธิพลของฮอร์โมน estrogen แต่ก็ยังมีอีกส่วนหนึ่งที่อาการของโรคแย่ลงในขณะตั้งครรภ์ ซึ่งจำเป็นต้องได้รับการดูแลรักษาเบื้องต้น
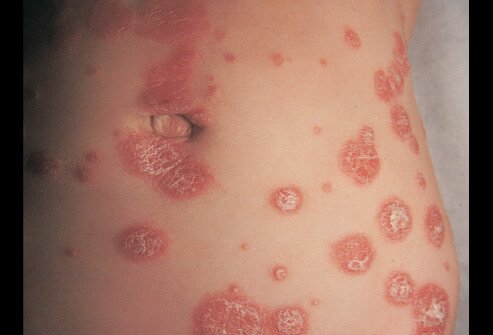
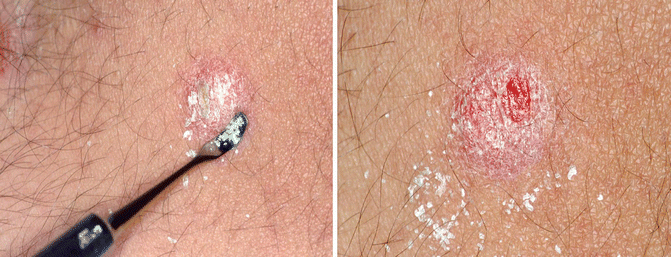
รูปที่ 6 Psoriasis (ที่มา https://www.medicinenet.com/image-collection/psoriasis_2_picture/picture.htm, https://link.springer.com/chapter/10.1007/978-3-319-19530-8_14)
การรักษาความชุ่มชื่นของผิวหนังด้วย moisturizer ด้วย Emollients เพื่อเพิ่มความชุ่มชื่นให้ผิวหนัง ถ้าขุยมีมาก ให้ยาละลาย เช่น urea cream ในขณะที่ยา salicytic acid ไม่แนะนำให้ใช้ ส่วนยาทาสเตอรอยด์ แนะนำให้ใช้ได้ในขณะตั้งครรภ์ ใช้เป็นยาทาที่มีฤทธิ์อ่อน หรือปานกลาง แต่ถ้าต้องใช้ยาที่มีฤทธิ์สูง ควรใช้ในช่วง second and third trimester สำหรับยาทาในกลุ่ม Calcineurin inhibitors เช่นยา Tacrolimus เพื่อยับยั้ง calcineurin ใน T lymphocyte, Langerhans cell, mast cell และ keratinocyte จัดอยู่ใน Pregnancy category C สามารถใช้ได้แต่ควรระมัดระวัง
Pregnancy-specific dermatoses
กลุ่มโรคผิวหนังจำเพาะที่เกิดในระหว่างตั้งครรภ์ มี 4 โรค โดยแบ่งเป็นโรคที่ไม่มีผลกระทบต่อทารกในครรภ์ ได้แก่1, 2, 18, 19 pruitic urticarial papules and plaques of pregnancy (PUPPP) หรือเรียกว่า Polymorphic eruption of pregnancy (PEP) และ atopic eruption of pregnancy (AEP) ส่วนโรคผิวหนังที่มีผลกระทบต่อทารกในครรภ์ ได้แก่ pemphigoid gestationis (PG) และIntrahepatic cholestasis of pregnancy (ICP)
Polymorphic eruption of pregnancy (PEP) เป็นโรคที่พบบ่อยในการตั้งครรภ์โดยเฉพาะเป็นการตั้งครรภ์แรก มักพบในช่วงหลังของไตรมาสสุดท้าย เวลาโดยเฉลี่ยของการเกิดโรคคือ เมื่ออายุครรภ์ 36 สัปดาห์ ยังไม่ทราบสาเหตุที่แท้จริง แต่มีสมมติฐานว่า เกิดจากการขยายของผนังหน้าท้องระหว่างการตั้งครรภ์ ทำให้เกิดการทำลายเนื้อเยื่อของผิวหนัง แอนติเจนในเส้นใยคอลลาเจลไปกระตุ้นระบบภูมิคุ้มกันของร่างกาย จนนำไปสู่ภาวะ allergic reaction ทำให้เกิดผื่นบริเวณรอยแตกลายที่ผิวหนังหนาท้อง นอกจากนี้ยังมีสมมติฐานอื่น ที่เชื่อว่าการเกิดโรคนี้สัมพันธ์กับฮอร์โมน19, 20
ลักษณะผื่นเป็นผื่นนูนแดง คล้ายผื่นลมพิษ เกิดที่บริเวณรอยแตกลายที่หน้าท้อง (striae) และบริเวณใกล้เคียง โดยจะเว้นบริเวณรอบๆสะดือ (periumbilical sparing) ขนาดผื่นมีหลายขนาด บางครั้งผื่นจะรวมกันเป็นแผ่นหรือปื้นขนาดใหญ่ (รูปที่ 7) บางครั้งอาจพบตุ่มน้ำใส (papulovesicles or microvesicle) ต่อมาผื่นก็จะลามลงมาที่ต้นขา หรือก้นกบ หรือไปที่แผ่นหลัง และแขนได้ นอกจากนี้จะมีอาการคันร่วมด้วย ทำให้ผู้ป่วยนอนไม่หลับ
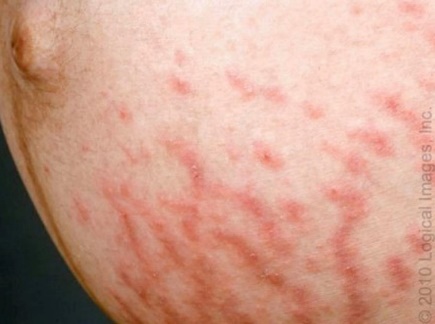
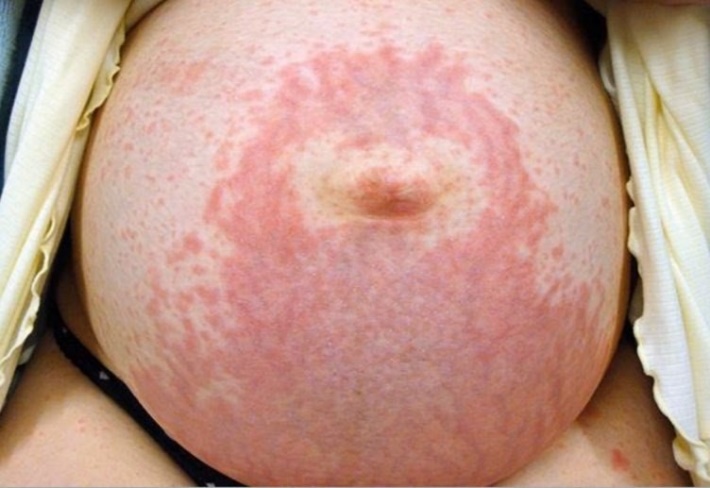
รูปที่ 7 Polymorphic eruption of pregnancy (ที่มา uptodate 2018: dermatoses of pregnancy)
การวินิจฉัยโรคอาศัยลักษณะรอยโรคที่ปรากฏเป็นสำคัญ ไม่จำเป็นต้องส่งตรวจทางห้องปฏิบัติการ สำหรับการรักษาโรค PEP ไม่มีการรักษาที่จำเพาะ เนื่องจากโรคนี้สามารถหายได้เองหลังคลอด แต่ถ้าผู้ป่วยมีปัญหาเรื่องอาการคัน หรือไม่ต้องการให้ผื่นลามมากขึ้น สามารถพิจารณาใช้ยากลุ่ม antihistamine ในการลดอาการคันได้ และสามารถใช้ยา topical corticosteroids ทาบางๆที่รอยผื่นได้ โดยผื่นจะหายไปใน 2-3 วัน
Atopic eruption of pregnancy (AEP) ประกอบไปด้วย กลุ่มอาการ 3 แบบด้วยกัน2, 21 ได้แก่ prurigo of pregnancy (PP) pruritic folliculitis in pregnancy (PFP) และ Atopic eczema (AE) โดยที่ PP จะมีลักษณะผื่นเป็นตุ่มแดง ร่วมกับอาการคัน พบได้บริเวณแขนขาด้านนอก (extensor surface) และอาจเกิด บริเวณหน้าท้องได้ การแกะเกาจะทำให้มีสะเก็ด (รูปที่ 8) ส่วน PEP เป็นผื่นที่เกิดตุ่มแดงหรือตุ่มหนอง บริเวณลำตัว ร่วมกับมีอาการคันมาก ส่วน AE เป็นผื่นตุ่มแดง หรือผื่น eczema สัมพันธ์กับประวัติ atopy ของตนเองหรือคนในครอบครัว ซึ่งจะพบบริเวณข้อพับ เกิดได้ทุกไตรมาสของการตั้งครรภ์ มีอาการคันเด่น จะเห็นได้ว่าทั้ง 3 กลุ่มอาการจะมีลักษณะร่วมกันอยู่
การวินิจฉัยโรคนี้อาศัยลักษณะรอยโรคที่แสดง อาจจะไม่มีความจำเป็นในการส่งตรวจทางห้องปฏิบัติการ สำหรับการรักษาจะเน้นเรื่องความชุ่มชื่นของผิวหนัง โดยใช้ 3-10% urea cream ร่วมกับการทายา low potency corticosteroid ในช่วงเวลาสั้นๆ ร่วมกับการให้ยาในกลุ่ม antihistamine เพื่อลดอาการคัน แต่หากอาการยังไม่ดีขึ้น อาจจะพิจารณาให้ high topical steroid หรือส่งพบแพทย์โรคผิวหนังต่อไป
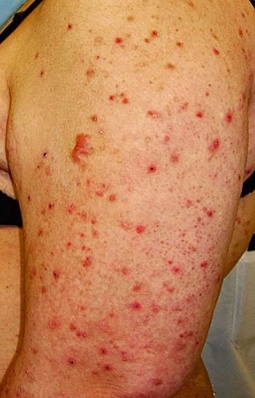
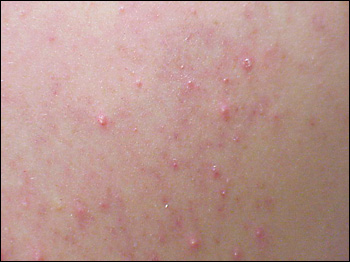
รูปที่ 8 ด้านซ้าย prurigo of pregnancy ด้านขวา pruritic folliculitis in pregnancy (ที่มา uptodate 2018 : dermatoses of pregnancy)
Pemphigoid gestationis (PG) หรือเรียกอีกชื่อว่า herpes gestationis (HG) เป็นโรคในกลุ่ม autoimmune vesiculobullous disorder ที่พบได้ไม่บ่อย สาเหตุเกิดจากการตอบสนองของระบบภูมิต้านทานของตนเองที่เกิดขึ้นบริเวณรก ตรงตำแหน่ง placental basement membrane (BMZ) ซึ่งต่อมาเกิดการ cross reaction ระหว่างเนื้อเยื่อของรกและผิวหนังทำให้เกิดผื่นขึ้นมา และแอนติบอดีต่อ BMZ ที่เกิดขึ้นสามารถส่งผ่านรกไปยังทารกในครรภ์ได้ จึงทำให้ทารกที่เกิดมามีอาการของผื่นลมพิษ หรือผื่นตุ่มน้ำได้ ประมาณร้อยละ 10 ผื่นในทารกจะหายไปเองหลังจากแอนติบอดีในทารกสลายไป นอกจากนี้ทารกยังเสี่ยงต่อภาวะน้ำหนักตัวน้อย และการคลอดก่อนกำหนด19, 22 ลักษณะของผื่นเป็นตุ่มน้ำหนาใส (intense vesicles) ร่วมกับรอยปื้นแดงนูนคล้ายผื่นลมพิษ มีอาการคันมาก ผู้ป่วยร้อยละ 50-90 จะมีรอยโรคเริ่มที่สะดือ ต่อมาจึงลามไปที่อก หลัง ก้น แขนและขา (รูปที่9) มีรอยเกาและสะเก็ดได้ อาการมักดีขึ้นในช่วงหลังของการตั้งครรภ์ แต่จะกำเริบขึ้นเมื่อเวลาคลอด รอยโรคจะหายไปเองภายใน 3 เดือนหลังคลอด
การวินิจฉัยอาศัยการแสดงลักษณะของรอยโรคที่ผิวหนัง ร่วมกับการตรวจทางพยาธิวิทยา และการตรวจทางอิมมูโน โดยการตรวจ direct immunofluorescence (DIF) จากชิ้นเนื้อ และการตรวจ Indirect immunofluorescence (IIF) จากเลือด ซึ่งจะให้ผลออกมาเป็นบวกทั้งคู่ และการตรวจเลือดพบแอนติบอดีต่อ BP 180 NC 16a antigen ด้วยวิธี ELISA สำหรับการรักษาโรคนี้ จะใช้ potent topical corticosteroid และ emollients ทาบริเวณรอยโรค ร่วมกับการใช้ยายา antihistamine เพื่อบรรเทาอาการคันผิวหนัง ส่วนรายที่เป็นมากอาจพิจารณาทานยา prednisolone 0.5-1 มิลลิกรัมต่อน้ำหนักตัวเป็นกิโลกรัมต่อวัน ถ้าอาการดีขึ้นจึงค่อยลดยาลง แต่หากไม่ดีขึ้นควรส่งพบแพทย์ผิวหนังต่อไป
Intrahepatic cholestasis of pregnancy (ICP) เป็นภาวะที่พบได้ไม่บ่อย มักเกิดในช่วงท้ายของการตั้งครรภ์ สาเหตุเกิดจาก การคั่งของน้ำดี ที่เป็นผลมาจากการเปลี่ยนแปลงของฮอร์โมนในระหว่างการตั้งครรภ์ มีผลทำให้เซลล์ตับลดการดูดกลับน้ำดี23โดยที่ผู้ป่วยจะไม่มีรอยโรคที่ผิวหนัง แต่จะมาด้วยอาการคันบริเวณฝ่ามือฝ่าเท้าและลามไปทั่วตัว อาจพบการเปลี่ยนแปลงทางผิวหนังจากการแกะเกา หรือพบตุ่มคันที่บริเวณแขนขา ส่งผลต่อทารกในครรภ์ ทำให้มีความเสี่ยงต่อ intrauterine fetal demise (IUFD), spontaneous preterm delivery, non-reassuring fetal status, และ meconium staining ซึ่งสัมพันธ์กับระดับของ Bile acid23
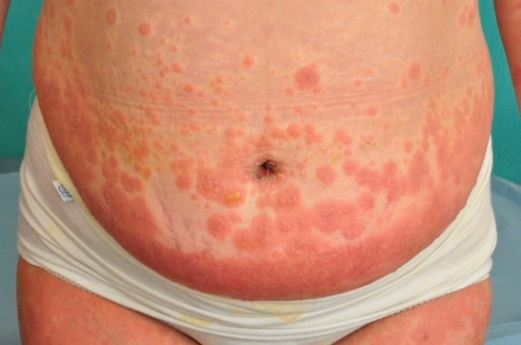
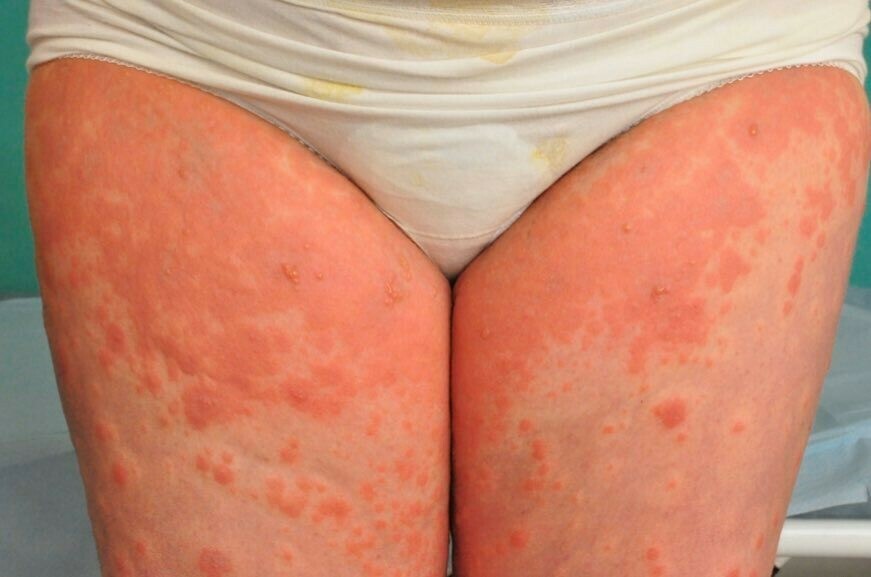
รูปที่ 9 Pemphigoid gestationis (ที่มา uptodate 2018: dermatoses of pregnancy)
การวินิจฉัยอาศัยการตรวจทางห้องปฏิบัติการ ส่งตรวจการทำงานของตับ จะพบการเพิ่มขึ้นของระดับ Total serum bile acid level การรักษาเพื่อต้องการลดระดับ serum bile acid ให้สามารถดำเนินการตั้งครรภ์ต่อไปได้ และลดอัตราการเกิดภาวะแทรกซ้อนต่อทารก การลดอาการคัน โดยใช้ยา Ursodeoxycholic acid ขนาด 15 มิลลิกรัมต่อน้ำหนักตัวเป็นกิโลกรัมต่อวัน ถือเป็น first-line treatment นอกจากนี้ต้องมีการติดตามสุขภาพของทารกในครรภ์อย่างใกล้ชิด23
การดูแลสตรีตั้งครรภ์ที่มีปัญหารอยโรคผิวหนังในระหว่างตั้งครรภ์ พบได้ทั้งโรคผิวหนังทั่วไป และโรคผิวหนังชนิดจำเพาะที่เกิดในสตรีตั้งครรภ์ การดูแลรักษาขึ้นอยู่กับอาการของสตรีตั้งครรภ์เป็นสำคัญ ซึ่งสูติแพทย์สามารถให้การดูแลรักษาเบื้องต้นได้ หากอาการรุนแรงมากขึ้น ควรส่งพบแพทย์เฉพาะทางต่อไป
เอกสารอ้างอิง
- F. Gary. Cunningham, Kenneth J. Leveno, Steven L. Bloom, Jodi S. Dashe, Barbara L. Hoffman, Brian M. Casey, et al. Williams Obstetrics. 25 ed ed. New York: McGraw-Hill Education; 2018.
- Ambros-Rudolph CM, Müllegger RR, Vaughan-Jones SA, Kerl H, Black MM. The specific dermatoses of pregnancy revisited and reclassified: results of a retrospective two-center study on 505 pregnant patients. Journal of the American Academy of Dermatology. 2006;54(3):395-404.
- Bastola PD, Rijal A, Upreti D. Study of pregnancy dermatoses in patients attending outpatient of BP Koirala Institute of Health Sciences, Dharan, Nepal. Nepal Journal of Dermatology, Venereology & Leprology. 2015;13(1):38-44.
- Bilgili MA, Bilvanisi SK, Bilgili SG, Okyay AG, Dursun R, Karadag AS. Specific and Non-Spesicific Dermatoses Of Pregnancy In The Emergency Department. Eastern Journal of Medicine. 2019;24(2):176-81.
- Masood S, Rizvi DA, Tabassum S, Akhtar S, Alvi RU. Frequency and clinical variants of specific dermatoses in third trimester of pregnancy: a study from a tertiary care centre. Journal of the Pakistan Medical Association. 2012;62(3):244.
- Obstetricians ACo, Gynecologists. Management of herpes in pregnancy. ACOG practice bulletin. 2007;8.
- Patel R, Kennedy OJ, Clarke E, Geretti A, Nilsen A, Lautenschlager S, et al. 2017 European guidelines for the management of genital herpes. International journal of STD & AIDS. 2017;28(14):1366-79.
- Straface G, Selmin A, Zanardo V, De Santis M, Ercoli A, Scambia G. Herpes simplex virus infection in pregnancy. Infectious Diseases in Obstetrics and Gynecology. 2012;2012.
- Hayward K, Cline A, Stephens A, Street L. Management of herpes zoster (shingles) during pregnancy. Journal of Obstetrics and Gynaecology. 2018;38(7):887-94.
- Obstetricians ACo, Gynecologists. Practice bulletin no. 151: Cytomegalovirus, parvovirus B19, varicella zoster, and toxoplasmosis in pregnancy. Obstetrics and gynecology. 2015;125(6):1510.
- Kesson A, Grimwood K, Burgess M, Ferson M, Gilbert G, Hogg G, et al. Acyclovir for the prevention and treatment of varicella zoster in children, adolescents and pregnancy. Journal of paediatrics and child health. 1996;32(3):211-7.
- จงกลนี วศ์ปิยะบวร. โรคผิวหนังที่เกี่ยวข้องกับระบบภูมิคุ้มกัน. พิมพ์ครั้งที่ 1 ed. กรุงเทพมหานคร: บริษัท หนังสือดีวัน จำกัด; 2561.
- Koutroulis I, Papoutsis J, Kroumpouzos G. Atopic dermatitis in pregnancy: current status and challenges. Obstetrical & gynecological survey. 2011;66(10):654-63.
- Weatherhead S, Robson SC, Reynolds NJ. Eczema in pregnancy. Bmj. 2007;335(7611):152-4.
- Kar S, Krishnan A, Preetha K, Mohankar A. A review of antihistamines used during pregnancy. Journal of pharmacology & pharmacotherapeutics. 2012;3(2):105.
- Kadar L, Kivity S. Urticaria and angioedema in pregnancy. Current Dermatology Reports. 2013;2(4):236-42.
- Lawlor F. Urticaria and angioedema in pregnancy and lactation. Immunology and allergy clinics of North America. 2014;34(1):149-56.
- Alves GF, Zanetti VT, Viegas RMF. Dermatology and pregnancy. Dermatology in Public Health Environments: Springer; 2018. p. 661-74.
- Sävervall C, Sand FL, Thomsen SF. Dermatological diseases associated with pregnancy: pemphigoid gestationis, polymorphic eruption of pregnancy, intrahepatic cholestasis of pregnancy, and atopic eruption of pregnancy. Dermatology research and practice. 2015;2015.
- Adil M, Arif T, Amin SS. A comprehensive review on the pregnancy dermatoses. British Journal of Medical Practitioners. 2016;9(1).
- Resende C, Braga A, Vieira A, Brito C. Atopic eruption of pregnancy: A recent, but controversial classification. Austin J Dermatol. 2014;1:4.
- Sävervall C, Sand FL, Thomsen SF. Pemphigoid gestationis: current perspectives. Clinical, cosmetic and investigational dermatology. 2017;10:441.
- Williamson C, Geenes V. Intrahepatic cholestasis of pregnancy. Obstetrics & Gynecology. 2014;124(1):120-33.