Ultrasonography in Obstetric Emergencies
การตรวจคลื่นเสียงความถี่สูงในภาวะฉุกเฉินทางสูติศาสตร์
พ.ญ. ภัทรามาส เลิศชีวกานต์
อาจารย์ที่ปรึกษา อ.พ.ญ. สุชยา ลือวรรณ
บทนำ
การตรวจด้วยคลื่นเสียงความถี่สูงมีบทบาทสำคัญต่อการดูแลผู้ป่วยทางสูติศาสตร์ คลื่นเสียงความถี่สูงมีประโยชน์ในการวินิจฉัยการตั้งครรภ์ทั้งการตั้งครรภ์ที่ปกติและการตั้งครรภ์ที่มีภาวะแทรกซ้อน ตรวจติดตามการเจริญเติบโตและสุขภาพของทารก ตรวจคัดกรองความพิการและความผิดปกติทางพันธุกรรมของทารก รวมทั้งความผิดปกติของรกและน้ำคร่ำ
ปัจจุบันเครื่องตรวจคลื่นเสียงความถี่สูงมีประสิทธิภาพดีขึ้นและมีใช้อย่างแพร่หลายในเกือบทุกโรงพยาบาล นอกจากนี้ยังสามารถทำการตรวจได้ทันทีและสามารถเคลื่อนย้ายมาตรวจข้างเตียงผู้ป่วยได้ สูตินรีแพทย์และแพทย์ทั่วไปสามารถเรียนรู้และฝึกฝนให้มีความชำนาญในการตรวจและแปลผลได้ จึงมีความเหมาะสมที่จะนำมาใช้ในการดูแลและวางแผนการรักษาผู้ป่วยที่มีภาวะฉุกเฉินทางสูติศาสตร์เป็นอย่างยิ่ง
หลักการเบื้องต้นของการตรวจด้วยคลื่นเสียงความถี่สูงทางสูติศาสตร์
การตรวจด้วยคลื่นเสียงความถี่สูงในไตรมาสแรก
สามารถตรวจได้ทั้งทางหน้าท้อง(Transabdominal ultrasonography, TAS) และทางช่องคลอด(Transabvaginal ultrasonography, TVS) การตรวจทางช่องคลอดจะได้ภาพที่ชัดเจนกว่าในช่วงอายุครรภ์ที่น้อยกว่า 10 สัปดาห์ โดยเฉพาะในรายที่มดลูกคว่ำหลัง ผู้ป่วยอ้วนหรือมีผนังหน้าท้องหนา (1)
ลักษณะคลื่นเสียงความถี่สูงในการตั้งครรภ์ปกติในไตรมาสแรก มีรายละเอียดดังตารางที่ 1
ตารางที่ 1: ลักษณะที่ตรวจพบจากการตรวจคลื่นเสียงความถี่สูงในไตรมาสแรกของการตั้งครรภ์
|
อายุครรภ์ (สัปดาห์)
|
การตรวจพบทางคลื่นเสียงความถี่สูง
|
|
4+3– 5+0
5+1– 5+5
5+6– 6+0
6+1– 6+6
7+0– 7+6
|
– พบถุงการตั้งครรภ์ขนาด 2-5 มิลลิเมตร รูปร่างกลม ขอบชัด อยู่ใกล้ยอดมดลูกค่อนไปทางด้านใดด้านหนึ่ง
– มองเห็นถุงไข่แดง (yolk sac) อยู่ภายใน chorionic cavity ซึ่งควรจะพบทุกรายเมื่อค่าเฉลี่ยของถุงการตั้งครรภ์มากกว่า 10 มิลลิเมตร ถ้าไม่พบโอกาสที่จะเป็นตัวอ่อนตายในครรภ์สูง ควรตรวจซ้ำอีก 1 สัปดาห์ถัดมา เพื่อยืนยันการวินิจฉัย
– พบตัวอ่อนยาวประมาณ 2 – 4 มิลลิเมตรและการเต้นของหัวใจ ควรจะเห็นตัวอ่อนเมื่อค่าเฉลี่ยของเส้นผ่านศูนย์กลางมากกว่า 20 มิลลิเมตร ถ้าไม่พบโอกาสที่จะเป็นตัวอ่อนตายในครรภ์สูง ควรตรวจซ้ำอีก 1 สัปดาห์ถัดมา
– ตัวอ่อนจะมีรูปร่างคล้ายรูปไตหรือถั่ว และเห็นถุงไข่แดงและ vitelline duct แยกออกจากตัวอ่อนชัดเจน ตัวอ่อนยาวประมาณ 4 – 10 มิลลิเมตร ถ้าไม่เห็นหัวใจเด็กสามารถวินิจฉัยว่าเป็นต้วอ่อนตายในครรภ์ได้
– ความยาวของตัวอ่อนจากหัวถึงก้น (Crown Rump Length) ประมาณ 11 – 16 มิลลิเมตร เห็นสมองส่วน rhombencephalon เป็นช่องว่างรูปสี่เหลี่ยมขนมเปียกปูน แยกส่วนหัวและส่วนก้นออกจากกันได้ชัดเจน กระดูกสันหลังเห็นเป็นเส้นเข้มทึบ 2 เส้นขนานกัน เห็น amniotic membrane ซึ่งแบ่ง amniotic cavity ออกจาก chorionic cavity ได้ชัดเจน นอกจากนี้ยังเห็นสายสะดือด้วย
|
ตารางที่ 1. ลักษณะที่ตรวจพบจากการตรวจคลื่นเสียงความถี่สูงในไตรมาสแรกของการตั้งครรภ์
|
อายุครรภ์ (สัปดาห์)
|
การตรวจพบทางคลื่นเสียงความถี่สูง
|
|
8+0– 8+6
|
– ความยาวของตัวอ่อนจากหัวถึงก้น (Crown Rump Length) ประมาณ 17 – 23 มิลลิเมตร กะโหลกและสมองส่วน forebrain, midbrain และ hindbrain แยกจากกันได้ชัดเจน เริ่มเห็นตุ่มของแขนและขา บริเวณท้องตำแหน่งของสายสะดือจะมีไส้เลื่อนยื่นออกมา ซึ่งเป็นภาวะปกติในช่วงนี้ amniotic cavity ขยายออก สายสะดือและ vittelline duct ยืดยาวขึ้น
|
องค์กร American Institute of Ultrasound in Medicine แนะนำให้รายงานผลการตรวจขั้นพื้นฐาน ดังนี้
- )ตำแหน่งของถุงการตั้งครรภ์ เพื่อแยกการตั้งครรภ์นอกโพรงมดลูก ลักษณะถุงการตั้งครรภ์ ถุงไข่แดง(Yolk sac) ตัวอ่อนและความยาวของตัวอ่อน (Crown Rump Length)
- การเต้นของหัวใจตัวอ่อน จำนวนตัวอ่อน ถ้าเป็นครรภ์แฝดต้องระบุ Amnionicity และ Chorionicity
- ลักษณะของมดลูก รวมถึงอวัยะวอื่น ๆ ในอุ้งเชิงกราน
- ถ้าเป็นไปได้ให้ประเมินบริเวณต้นคอของทารกที่มีชีวิตด้วย
การตรวจคลื่นเสียงความถี่สูงในไตรมาสที่สองและสาม
โดยทั่วไปจะทำการตรวจผ่านทางหน้าท้องโดยใช้หัวตรวจที่มีความถี่ 4-6 เมกะเฮิรตซ์ในช่วงไตรมาสที่สอง
และความถี่ 2-5 เมกะเฮิรตซ์ในช่วงไตรมาสที่สาม โดยองค์กร American Institute of Ultrasound in Medicine แนะนำให้รายงานผลการตรวจขั้นพื้นฐาน ดังนี้
- จำนวนทารก ในกรณีที่เป็นครรภ์แฝดควรรายงาน Amnionicity, Chorionicity, ขนาดทารก, ปริมาณน้ำคร่ำและเพศของทารก
- ส่วนนำ (Presentation)
- การเต้นของหัวใจ
- ตำแหน่งและลักษณะของรก ระยะห่างจากปากมดลูกด้านใน (Internal cervical os)
- ปริมาณน้ำคร่ำ
- การประเมินอายุครรภ์
- การคะเนน้ำหนักทารก
- ประเมินมดลูก, ปีกมดลูกและปากมดลูก
- ลักษณะความผิดปกติของทารกในครรภ์
นอกจากนี้อาจมีการตรวจเพิ่มเติมเฉพาะส่วนในกรณีที่สงสัยความผิดปกติ เช่น ตรวจดูตำแหน่งรกในกรณีที่มีเลือดออกผิดปกติทางช่องคลอด, การตรวจดูท่าทารกในระยะคลอด เป็นต้น
การตรวจด้วยคลื่นเสียงความถี่สูงสำหรับภาวะฉุกเฉินในขณะตั้งครรภ์
ภาวะการมีเลือดออกในไตรมาสแรกของการตั้งครรภ์ (First Trimester Bleeding)
การมีเลือดออกทางช่องคลอดของหญิงตั้งครรภ์ในไตรมาสแรกเป็นปัญหาที่พบได้บ่อย โดยพบประมาณร้อยละ 20-30 ของสตรีที่ทราบว่าตั้งครรภ์ ซึ่งมักจะมีสาเหตุมาจาก
1. ภาวะแท้ง ซึ่งแบ่งออกได้เป็น
1.1. แท้งคุกคาม (Threatened abortion) ซึ่งตัวอ่อนหรือทารกในครรภ์ยังมีชีวิตอยู่
1.2. แท้งไม่ครบ (Incomplete abortion)
1.3. แท้งครบ (Complete abortion)
2. การตั้งครรภ์ในโพรงมดลูกที่ผิดปกติ (Abnormal intrauterine pregnancy) ประกอบด้วย
2.1. ถุงการตั้งครรภ์ที่ไม่มีตัวอ่อน (Blighted ovum)
2.2. ตัวอ่อนหรือทารกเสียชีวิตในครรภ์ระยะแรก (Early fetal death)
2.3. ครรภ์ไข่ปลาอุก (Molar pregnancy)
3. การตั้งครรภ์นอกมดลูก (Ectopic pregnancy)
ในกรณีที่มีภาวะเลือดออกผิดปกติในไตรมาสแรกของการตั้งครรภ์ การตรวจด้วยคลื่นเสียงความถี่สูงเป็นวิธีการตรวจวินิจฉัยที่มีความถูกต้องแม่นยำสูง สามารถแยกภาวะอื่นๆ ที่อาจจะให้ลักษณะทางคลินิกคล้ายภาวะแท้งคุกคามได้ ซึ่งภาวะเหล่านั้นหากวินิจฉัยได้ล่าช้าอาจทำให้เกิดภาวะแทรกซ้อนที่รุนแรงตามมาได้ โดยส่วนใหญ่จะสามารถให้การวินิจฉัยได้ในการตรวจครั้งแรก ซึ่งแต่ละภาวะจะมีลักษณะที่พบจากการตรวจด้วยคลื่นเสียงความถี่สูงดังนี้
1. ภาวะแท้ง
1.1 ภาวะแท้งคุกคาม (Threatened abortion)
ภาวะแท้งคุกคามเป็นภาวะแทรกซ้อนของการตั้งครรภ์ที่พบได้บ่อย ประมาณร้อยละ 20-25 ของการตั้งครรภ์ เมื่อตรวจด้วยคลื่นเสียงความถี่สูงจะพบตัวอ่อนหรือทารกที่มีการเต้นของหัวใจชัดเจน หรืออาจจะไม่พบในการตรวจครั้งแรกในกรณีที่อายุครรภ์น้อยเกินไปแต่สามารถตรวจพบได้ในการตรวจติดตามในสัปดาห์ถัดมา ถ้าทำการตรวจแล้วพบว่าทารกยังมีชีวิตอยู่จะมีโอกาสดำเนินการตั้งครรภ์ต่อไปอย่างปกติสูงถึงร้อยละ 90-97 (2-4)
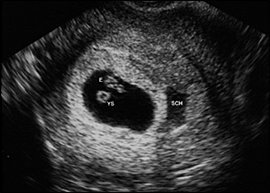
รูปที่ 1: แสดงถุงการตั้งครรภ์ที่เห็น yolk sac ภายในและ Subchorionic hemorrhage
(ที่มา: http://www.aafp.org)
1.2 แท้งไม่ครบ (Incomplete abortion)
การให้การวินิจฉัยภาวะแท้งไม่ครบสามารถทำได้ด้วยการตรวจร่างกายแล้วพบว่าปากมดลูกเปิดอยู่และยังคงมีเลือดไหลออกจากปากช่องคลอด หรือพบว่ามีชิ้นส่วนของรกหรือทารกค้างอยู่ที่ปากมดลูก แต่พบว่ามีผู้ป่วยร้อยละ
5-8 ที่ตรวจพบปากมดลูกปิดแต่ยังแท้งไม่ครบ (4, 5) ในกรณีนี้การตรวจด้วยคลื่นเสียงความถี่สูงจะพบว่ามีชิ้นส่วนของรกหรือทารกบางส่วนค้างอยู่ในโพรงมดลูก ซึ่งจะเห็นเนื้อรก ลักษณะสีขาว ความเข้มเสียงมาก (Hyperechoic content) ขอบเขตไม่เรียบ อาจมีของเหลวหรือเลือดอยู่ภายใน
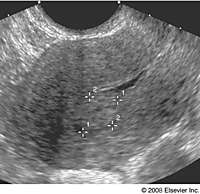
รูปที่ 2: แสดงให้เห็นชิ้นส่วนของรกหรือทารกบางส่วนค้างอยู่ในโพรงมดลูก ลักษณะสีขาว ความเข้มเสียงมาก
(ที่มา: http://imaging.consult.com)
1.3 แท้งครบ (Complete abortion)
การให้การวินิจฉัยภาวะแท้งครบสามารถทำได้ด้วยการตรวจร่างกายแล้วพบว่าปากมดลูกปิด เลือดหยุดไหล ขนาดมดลูกเล็กกว่าอายุครรภ์แต่อาจจะยังลดขนาดลงมาไม่เท่ากับคนปกติ ในกรณีที่ไม่แน่ใจสามารถทำการตรวจด้วยคลื่นเสียงความถี่สูงจะพบว่าเยื่อบุโพรงมดลูก จะเห็นเป็นแนวเส้นสีขาวเข้ม บางและ เรียบตลอดแนว หรือ มีของเหลวที่เป็นเลือดอยู่ภายในเล็กน้อยและไม่พบชิ้นส่วนของการตั้งครรภ์เหลืออยู่
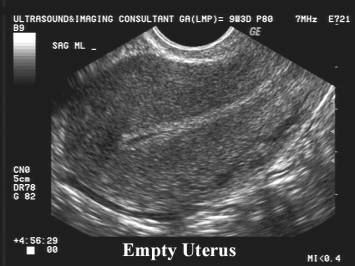
รูปที่ 3: แสดงโพรงมดลูกที่ว่างเปล่า เห็นเป็นแนวเส้นสีขาวเข้ม บางและเรียบตลอดแนว
(ที่มา: http://www.fetalultrasound.com/online)
2. การตั้งครรภ์ในโพรงมดลูกที่ผิดปกติ
2.1 ถุงการตั้งครรภ์ที่ไม่มีตัวอ่อน (Blighted ovum)
Blighted ovum หมายถึงการตั้งครรภ์ที่ไม่มีตัวอ่อนหรือตัวอ่อนสลายไปตั้งแต่ระยะเริ่มแรก การวินิจฉัยภาวะนี้จากการตรวจด้วยคลื่นเสียงความถี่สูง มีเกณฑ์ดังต่อไปนี้ (6, 7)
– Mean Sac Diameter(MSD) มากกว่า 10 มิลลิเมตรจากการตรวจทางช่องคลอด หรือมากกว่า 20 มิลลิเมตรจากการตรวจทางหน้าท้องแต่ยังไม่พบ Yolk sac
– Mean Sac Diameter(MSD) มากกว่า 18 มิลลิเมตรจากการตรวจทางช่องคลอด หรือมากกว่า 25 มิลลิเมตรจากการตรวจทางหน้าท้องแต่ยังไม่พบตัวอ่อน (Embryo)
– ถุงน้ำของการตั้งครรภ์ (Gestational sac) มีรูปร่างผิดปกติอย่างชัดเจน (deformed)
นอกจากนี้ยังอาจพบลักษณะอื่นๆ ที่บ่งชี้ว่ามีความเป็นไปได้สูงที่จะเป็น Blighted ovum แต่ไม่เสมอไป อาทิเช่น
– Choriodecidual reaction หนาน้อยกว่า 2 มิลลิเมตรหรือมีความเข้มเสียงต่ำ (echo lucent)
– ไม่พบ double decidual sac sign ชัดเจน
– รูปร่างของถุงการตั้งครรภ์ (Gestational sac) ไม่สม่ำเสมอหรือขรุขระ
– ถุงการตั้งครรภ์เคลื่อนลงไปต่ำหรืออยู่ในส่วน Lower segment ของมดลูก
ในกรณีที่ผลการตรวจก้ำกึ่งดังที่กล่าวมานี้หรือภาพไม่ชัดเจนควรทำการตรวจติดตามอีกครั้ง เนื่องจากมีโอกาสเป็นครรภ์ปกติได้อยู่ และเมื่อพบลักษณะที่เข้าได้ตามเกณฑ์การวินิจฉัยหรือพบว่าเมื่อผ่านไป 1-2 สัปดาห์ แล้วไม่พบการเจริญเติบโตของถุงการตั้งครรภ์ก็สามารถสรุปได้ว่าเป็น Blighted ovum
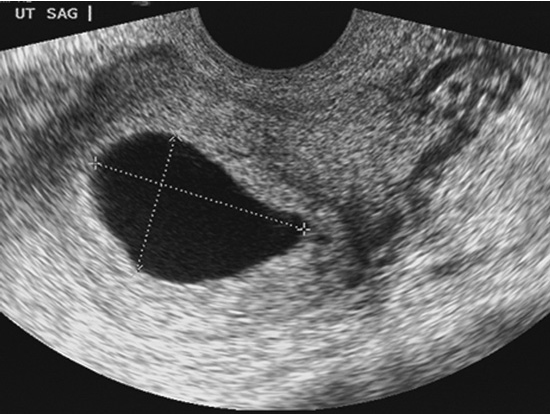
รูปที่ 4: ถุงการตั้งครรภ์ที่ไม่มีตัวอ่อน (Blighted ovum) (8)
2.2 ตัวอ่อนหรือทารกตายในครรภ์ระยะแรก (Early fetal death)
การตรวจด้วยคลื่นเสียงความถี่สูงถ้าเห็นตัวอ่อนชัดเจนแล้วไม่เห็นหัวใจเต้นสามารถให้การวินิจฉัยได้ว่าตัวอ่อนเสียชีวิตแล้ว สำหรับตัวอ่อนขนาดเล็กมากอาจใช้เกณฑ์ช่วยในการวินิจฉัยดังนี้ (9, 10)
– ตรวจไม่พบการเต้นของหัวใจ เมื่อขนาดของตัวอ่อน หรือ Crown Rump Length (CRL) มากกว่า 5 มิลลิเมตรจากการตรวจทางช่องคลอด หรือมากกว่า 9 มิลลิเมตรจากการตรวจทางหน้าท้อง
– ในกรณีที่ผู้ตรวจไม่แน่ใจว่าที่เห็นใช่ตัวอ่อนหรือไม่ให้ทำการตรวจซ้ำในอีก 1 สัปดาห์ ถ้ายังพบลักษณะเช่นเดิมก็สามารถให้การวินิจฉัยได้ว่าตัวอ่อนเสียชีวิตแล้ว
2.3 ครรภ์ไข่ปลาอุก (Molar pregnancy)
ครรภ์ไข่ปลาอุกแบ่งออกเป็น 2 กลุ่มคือ
1. ครรภ์ไข่ปลาอุกโดยสมบูรณ์ (Complete hydratidiform mole) ซึ่งจะไม่มีทารกมีแต่เพียงเนื้อรกที่ผิดปกติ
2. ครรภ์ไข่ปลาอุกแบบไม่สมบูณ์ (Partial hydratidiform mole) มีเนื้อเยื่อของทารกหรือรกปกติร่วมด้วย บางครั้งทารกในครรภ์สามารถเจริญเติบโตต่อไปได้ แต่มักจะมีความผิดปกติหลายอย่างร่วมกับภาวะการเจริญเติบโตช้า
ในปัจจุบันการตรวจด้วยคลื่นเสียงความถี่สูงในสตรีตั้งครรภ์ที่มาด้วยเลือดออกในไตรมาสแรกของการตั้งครรภ์ช่วยให้การวินิจฉัยครรภ์ไข่ปลาอุกได้เร็วขึ้น และสามารถให้การรักษาได้ตั้งแต่ยังไม่มีภาวะแทรกซ้อนอื่นๆ ร่วมด้วย
ลักษณะทางคลื่นเสียงความถี่สูงในไตรมาสแรก
มีลักษณะที่ไม่จำเพาะ ภาพคลื่นเสียงแปรปรวนหลายรูปแบบ บางครั้งจะเห็นภาพคล้ายเนื้อรกที่เสื่อมสภาพเนื่องจาก chorionic villi ยังมีขนาดเล็กมาก ซึ่งจะมีลักษณะเป็น complex echogenic mass และมีถุงน้ำเล็กๆ กระจายอยู่ภายใน บางครั้งให้ภาพลักษณะคล้ายกับถุงน้ำที่ไม่มีตัวอ่อนอยู่เหมือนกับ blighted ovum แต่ถ้าเป็น partial hydratidiform mole อาจจะเห็น yolk sac หรือ fetal echo ร่วมด้วย นอกจากนี้อาจจะพบถุงน้ำที่รังไข่ (Theca luteal cyst) แต่จะพบได้ไม่บ่อยเหมือนในไตรมาสที่สอง จะเห็นว่าการวินิจฉัยโดยอาศัยเพียงลักษณะของคลื่นเสียงความถี่สูงนั้นแยกได้ยากจากภาวะแท้งค้าง ถ้าไม่ได้ส่งชิ้นเนื้อตรวจทางพยาธิวิทยาอาจให้การวินิจฉัยที่ผิดพลาดได้ ดังนั้นการตรวจติดตามระดับ hCG แล้วพบว่าสูงขึ้นหรือทำการตรวจด้วยคลื่นสียงความถี่สูงซ้ำอาจช่วยในการวินิจฉัยแยกโรคจากภาวะแท้งค้างได้ (11)
ลักษณะทางคลื่นเสียงความถี่สูงในไตรมาสที่สอง (12)
ในกรณีที่เป็นการตั้งครรภ์ไข่ปลาอุกแบบสมบูรณ์จะพบลักษณะจำเพาะคือไม่มีทารก ในกรณีที่ขนาดใหญ่ขึ้นจะเห็นก้อนเนื้อในโพรงมดลูกที่มีความเข้มเสียงปานกลาง ภายในประกอบด้วยถุงน้ำเล็กๆ กระจัดกระจายทั่วก้อน (Numerous cystic pattern) ถ้าถุงน้ำมีขนาดเล็กมากจะเห็นเป็นเกล็ดหิมะกระจายสม่ำเสมอ (Snow storm pattern) แต่ถ้าก้อนเล็กอาจเห็นเป็นก้อนที่มีความเข้มเสียงสูงล้อมรอบด้วยกล้ามเนื้อมดลูกที่มีความเข้มเสียงต่ำกว่าหรือดูคล้ายรกบรรจุอยู่เต็มโพรงมดลูก (Placental like pattern) นอกจากนี้จะพบถุงน้ำที่รังไข่ (Theca luteal cyst) ร่วมด้วยร้อยละ 20-50 ส่วนใหญ่เป็นทั้งสองข้าง มีได้หลายขนาด เป็นก้อนที่ไม่มีความเข้มเสียง (Anechoic) มีแผ่นกั้นแบ่งช่องภายในหลายช่อง นอกจากนี้การตรวจด้วยคลื่นสียงความถี่สูงยังมีประโยชน์ในการวินิจฉัยและประเมินการรักษาเนื้องอกของเนื้อรกที่เกิดตามหลังการตั้งครรภ์ไข่ปลาอุกได้
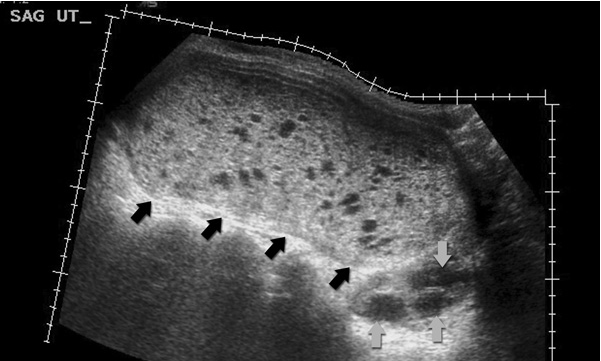
รูปที่ 5 : ครรภ์ไข่ปลาอุกโดยสมบูรณ์ เห็นก้อนเนื้อในโพรงมดลูกที่มีความเข้มเสียงปานกลาง ภายในประกอบด้วยถุงน้ำเล็กๆ กระจัดกระจายทั่วก้อน (Numerous cystic pattern) และพบถุงน้ำที่รังไข่ (Theca luteal cyst) ร่วมด้วย (8)
3. การตั้งครรภ์นอกมดลูก (Ectopic pregnancy)
การวินิจฉัยการตั้งครรภ์นอกมดลูกให้ได้ตั้งแต่เริ่มแรกนั้นยังคงเป็นปัญหาสำคัญ เนื่องจากมีหลายภาวะที่อาจจะมีอาการและอาการแสดงเหมือนกับการตั้งครรภ์นอกมดลูก ในปัจจุบันได้มีการพัฒนาแนวทางในการสืบค้นเพื่อวินิจฉัยภาวะการตั้งครรภ์นอกมดลูก โดยอาศัยเทคนิคการตรวจต่างๆ ร่วมกันดังนี้
- 1)การตรวจด้วยคลื่นเสียงความถี่สูง
- 2)การตรวจวัดระดับซีรั่ม beta hCG
- 3)การตรวจวัดระดับซีรั่ม progesterone
- 4)การขูดมดลูก (Uterine curettage)
- 5)การตรวจด้วยการส่องกล้องดูภายในช่องท้อง (Laparoscopy)
การตรวจด้วยคลื่นเสียงความถี่สูงจะใช้ในการตรวจผู้ป่วยที่ผลการทดสอบการตั้งครรภ์เป็นบวกและมีอาการและอาการแสดงของการตั้งครรภ์นอกมดลูก ซึ่งเหมาะจะตรวจในผู้ป่วยที่มีสัญญาณชีพคงที่ การตรวจด้วยคลื่นเสียงความถี่สูงจะช่วยตรวจหาตำแหน่งของการตั้งครรภ์และช่วยในการวินิจฉัยแยกออกจากภาวะอื่น ซึ่งการตรวจจะให้ผลดังนี้ (12)
1. แยกภาวะการตั้งครรภ์นอกมดลูก
ถ้าตรวจด้วยคลื่นเสียงความถี่สูงพบมีหลักฐานการตั้งครรภ์ภายในโพรงมดลูกชัดเจนก็สามารถแยกการตั้งครรภ์นอกมดลูกออกไปได้ แม้ว่าการตั้งครรภ์ที่พบร่วมกันทั้งภายในและภายนอกมดลูก (Heterotopic pregnancy) อาจเกิดขึ้นได้แต่ก็พบน้อยมากประมาณ 1 ต่อ 80,000 ของการตั้งครรภ์ (13)
2. ยืนยันการวินิจฉัยตั้งครรภ์นอกมดลูก
ลักษณะที่สำคัญเมื่อตรวจด้วยคลื่นเสียงความถี่สูง คือ ไม่พบถุงการตั้งครรภ์ในโพรงมดลูกและตรวจพบถุงการตั้งครรภ์บริเวณอื่น ในกรณีที่มีการตั้งครรภ์บริเวณท่อนำไข่ จะมีลักษณะเป็นวงแหวนทึบเสียงล้อมรอบบริเวณที่มีความเข้มเสียงต่ำที่เรียกว่า tubal ring ซึ่งเกิดจากผนังของท่อนำไข่ถูกขยายใหญ่ขึ้นเนื่องจากภายในบรรจุด้วยถุงการตั้งครรภ์นอกมดลูก และอาจพบตัวอ่อน, yolk sac หรือการเต้นของหัวใจของทารกด้วยซึ่งจะทำให้การวินิจฉัยแม่นยำมากขึ้น ในกลุ่มนี้สามารถพิจารณาให้การรักษาได้ทันที
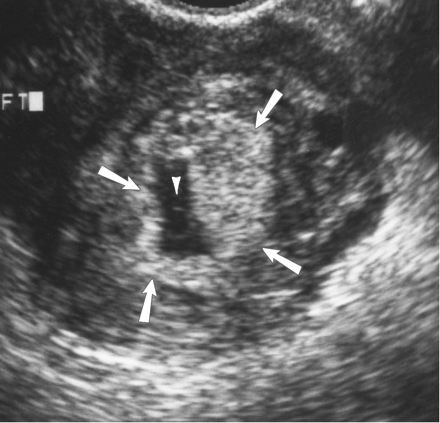
รูปที่ 6 : ท่อนำไข่ด้านซ้ายที่มีถุงการตั้งครรภ์ (Tubal ring) และเห็น yolk sac อยู่ภายใน (14)
3. สงสัยการตั้งครรภ์นอกมดลูก
ลักษณะบ่งชี้ทางอ้อมซึ่งน่าจะเป็นการตั้งครรภ์นอกมดลูกมีดังต่อไปนี้
3.1) มดลูกว่างเปล่า (Empty uterus)
จากการตรวจด้วยคลื่นเสียงความถี่สูงไม่พบถุงการตั้งครรภ์ในโพรงมดลูก เยื่อบุโพรงมดลูกอาจจะหนาหรือบางก็ได้ บางครั้งพบลักษณะเป็นถุงการตั้งครรภ์เทียม (Pseudo sac) ซึ่งเป็นเลือดหรือน้ำที่ค้างอยู่ในโพรงมดลูก มีความแตกต่างจากถุงการตั้งครรภ์ปกติดังมีรายละเอียดดังตารางที่ 2
ตารางที่ 2 : ความแตกต่างระหว่างถุงการตั้งครรภ์ปกติกับถุงการตั้งครรภ์เทียม (15)
|
ลักษณะที่พบ
|
ถุงการตั้งครรภ์เทียม
|
ถุงการตั้งครรภ์ปกติ
|
|
ตำแหน่ง
|
กลางโพรงเยื่อบุโพรงมดลูก
|
ฝังในเนื้อเยื่อบุโพรงมดลูกที่ค่อนไปด้านใดด้านหนึ่ง
|
|
ขอบเขต
|
ไม่มี Double decidual sac และขรุขระ
|
มี Double decidual sac
|
|
รูปร่างและขนาด
|
อาจเปลี่ยนได้ในขณะตรวจครั้งเดียวกันหรือใกล้ๆ กัน
|
ค่อนข้างคงที่ทั้งรูปร่างและตำแหน่ง
|
|
องค์ประกอบภายใน
|
ไม่มีตัวอ่อน ไม่มี yolk sac อาจมีเศษตะกอนขุ่นๆ ภายใน
|
หลัง 5 สัปดาห์จะเห็น yolk sac และตัวอ่อน
|
|
ลักษณะการไหลเวียนเลือดรอบถุงการตั้งครรภ์
|
ไม่มีหรืออาจมีได้เล็กน้อย
|
มีปริมาณมาก
|
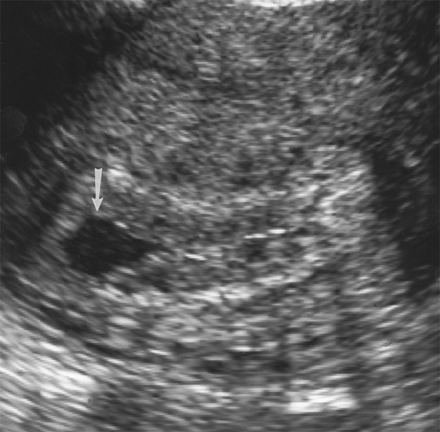
รูปที่ 7 : ถุงการตั้งครรภ์เทียม (Pseudo sac) ซึ่งเป็นเลือดหรือน้ำที่ค้างอยู่ในโพรงมดลูก (14)
3.2) ก้อนที่ปีกมดลูก (Complex mass)
ก้อนที่ปีกมดลูกอาจเกิดขึ้นจากเนื้อเยื่อการตั้งครรภ์และก้อนเลือดบริเวณปีกมดลูก ซึ่งเกิดจากเลือดที่ออกภายในท่อนำไข่ ทำให้เห็นท่อนำไข่ขยายโตขึ้นและมีเลือดออกมาทางปลายท่อนำไข่หรือเกิดจาก Tubal abortion ซึ่งมีการขับเอาครรภ์นอกมดลูกออกไปทาง fimbria เข้าสู่ช่องท้อง ในบางรายอาจเกิดจากครรภ์นอกมดลูกแตกจนมีเลือดและชิ้นส่วนของตัวอ่อนและถุงการตั้งครรภ์เข้าไปอยู่ในช่องท้อง
ลักษณะภาพคลื่นเสียงความถี่สูง มีของเหลวปนเนื้อเยื่อในช่องท้อง ซึ่งคือก้อนเลือดปนกับเนื้อเยื่อและเลือดที่ยังไม่แข็งตัว ในกรณีที่เลือดออกมากจะเห็นเลือดเซาะแทรกไปตามอวัยวะต่างๆ ในอุ้งเชิงกราน ภาพที่เป็นจึงมีลักษณะไม่จำเพาะเห็นเป็น complex mass ที่มีขอบเขตไม่แน่นอน มีทั้งความเข้มเสียงต่ำหรือสูงไม่สม่ำเสมอปะปนกัน
3.3) น้ำในอุ้งเชิงกราน (Pelvic fluid)
ตรวจพบบริเวณที่ไม่มีความเข้มเสียงในอุ้งเชิงกราน โดยเฉพาะถ้าตรวจที่บริเวณ Cul-de-sac แล้วพบว่าแอ่งใหญ่ที่สุดมีขนาดเกิน 0.5-1 เซนติเมตรขึ้นไปถือว่าผิดปกติ นอกจากนี้ถ้าพบน้ำปริมาณมากล้อมตัวมดลูกหรือเซาะแทรกขึ้นไปยังช่องท้องส่วนบน และถ้าน้ำมีลักษณะขุ่น (Echogenic fluid) ยิ่งมีโอกาสเกิดจากเลือดที่ออกจากครรภ์นอกมดลูกสูงมาก (16, 17)
ในผู้ป่วยกลุ่มนี้แนะนำให้ตรวจค้นเพิ่มเติมเพื่อการวินิจฉัยที่แน่นอนโดยเร็ว เช่น การตรวจด้วยการส่องกล้องดูภายในช่องท้อง หรือเจาะดูระดับ beta hCG ถ้าหากสูงเกินระดับวิกฤตอาจให้การวินิจฉัยได้เลย
3.4) ไม่พบลักษณะผิดปกติ
ซึ่งอาจจะเป็นได้ทั้งการตั้งครรภ์นอกมดลูกที่มีขนาดเล็กหรือครรภ์ในมดลูกระยะเริ่มแรกที่ตรวจไม่พบด้วยคลื่นเสียงความถี่สูง ในกรณีนี้อาจต้องวัดระดับซีรั่ม beta hCG และ/หรือระดับซีรั่ม progesterone ในการช่วยวินิจฉัยและวางแผนการดูแลรักษา โดยทั่วไปถ้าระดับ beta hCG เกิน 2,000 หรือ 6,000 มิลลิยูนิต/มิลลิลิตร แล้วตรวจไม่พบถุงการตั้งครรภ์ภายในโพรงมดลูกด้วยการตรวจคลื่นเสียงความถี่สูงทางช่องคลอดหรือทางหน้าท้องตามลำดับมีโอกาสเป็นครรภ์นอกมดลูกสูงมาก บางท่านเชื่อว่าสามารถให้การวินิจฉัยครรภ์นอกมดลูกได้เลย แต่ในกรณีที่ระดับซีรั่ม beta hCG ยังสูงไม่ถึงระดับที่คาดว่าน่าจะเห็นถุงการตั้งครรภ์ให้ตรวจระดับซีรั่ม beta hCG ในอีก 48 ชั่วโมง ถ้าไม่ขึ้นตามปกติให้ทำการขูดมดลูก แต่ถ้าขึ้นตามปกติให้ตรวจติดตามด้วยคลื่นเสียงความถี่สูงเมื่อซีรั่ม beta hCG สูงถึงระดับที่คาดว่าจะเห็นถุงการตั้งครรภ์
ภาวะการมีเลือดออกในไตรมาสที่สองหรือสามของการตั้งครรภ์
(Second and Third Trimester Bleeding)
การมีเลือดออกในไตรมาสที่สองและสามของการตั้งครรภ์นับเป็นปัญหาสำคัญที่ผู้ป่วยต้องได้รับการดูแลอย่างเร่งด่วนและการดูแลรักษาขึ้นอยู่กับสาเหตุที่ทำให้มีเลือดออกและสุขภาพของทารกในครรภ์ การตรวจด้วยคลื่นเสียงความถี่สูงสามารถนำมาใช้เพื่อช่วยในการวินิจฉัยและวางแผนการดูแลรักษาได้เป็นอย่างดี ซึ่งการที่มีเลือดออกในระยะนี้ของการตั้งครรภ์นั้นมักมีสาเหตุมาจาก
1. รกเกาะต่ำ (Placenta previa)
2. รกลอกตัวก่อนกำหนด (Placental abruption)
3. สายสะดือเกาะที่เยื่อหุ้มเด็กโดยผ่านปากมดลูกด้านใน (Vasa previa)
4. เลือดออกบริเวณขอบรก (Marginal sinus separation)
ซึ่งสาเหตุส่วนใหญ่เกิดจากความผิดปกติของรก การตรวจด้วยคลื่นเสียงความถี่สูงเพื่อหาความผิดปกติที่เกิดขึ้นกับรกจึงมีความสำคัญ บางครั้งสามารถให้การวินิจฉัยและเฝ้าระวังได้ก่อนที่จะมีเลือดออก โดยการตรวจรกนั้นควรจะบันทึกรายละเอียดของ ตำแหน่ง ขนาด รูปร่าง เนื้อรก และลักษณะบริเวณด้านหลังรก
การตรวจด้วยคลื่นเสียงความถี่สูงในกรณีที่มีภาวะเลือดออกในไตรมาสที่สองหรือสามมีลักษณะดังต่อไปนี้
1. รกเกาะต่ำ (Placenta previa)
รกเกาะต่ำ หมายถึง รกเกาะบริเวณส่วนล่างของโพรงมดลูก ตำแหน่งที่ใกล้หรือปิดปากมดลูก เป็นสาเหตุหลักของการมีเลือดออกในไตรมาสหลังของการตั้งครรภ์ โดยมีอุบัติการณ์ประมาณ 1 ต่อ 200-250 การตั้งครรภ์ (18) และมีอันตรายต่อทั้งมารดาและทารก จำแนกความรุนแรงของรกเกาะต่ำออกได้ 4 ระดับ ดังนี้
- รกเกาะส่วนล่างของมดลูก (Low lying placenta) หมายถึง ขอบรกอยู่ห่างจากปากมดลูกด้านในน้อยกว่า 2 เซนติเมตร
- รกเกาะต่ำชนิดเกาะขอบ (Marginal previa) หมายถึง ขอบรกอยู่ชิดกับขอบของปากมดลูกด้านใน แต่ไม่คลุมปากมดลูก
- รกเกาะต่ำชนิดสมบูรณ์ (Complete previa) หมายถึง รกเกาะคลุมปากมดลูกด้านในทั้งหมด
- รกเกาะต่ำชนิดบางส่วน (Partial previa) หมายถึง รกเกาะคลุมปากมดลูกด้านในเพียงบางส่วน มักจะใช้ในการวินิจฉัยเมื่อมีการเปิดของปากมดลูกแล้ว

รูปที่ 8: (A) รกเกาะต่ำชนิดเกาะขอบ, (B) รกเกาะต่ำชนิดบางส่วน, (C) รกเกาะต่ำชนิดสมบูรณ์
ปัจจุบันนี้การตรวจด้วยคลื่นเสียงความถี่สูงถือเป็นเทคนิคมาตรฐานในการวินิจฉัยรกเกาะต่ำ และควรทำการตรวจทุกรายที่มีปัญหาตกเลือดก่อนคลอดเพื่อแยกภาวะรกเกาะต่ำให้ได้ก่อนที่จะทำการตรวจภายในหรือเริ่มการรักษา
ลักษณะทางคลื่นเสียงความถี่สูง (12)
การตรวจด้วยหัวตรวจคลื่นเสียงความถี่สูงทางช่องคลอดสามารถวินิจฉัยตำแหน่งของรกและขอบรกได้แม่นยำกว่าการตรวจทางหน้าท้อง โดยเฉพาะในกรณีที่รกเกาะอยู่ทางด้านหลังและมีส่วนนำของของทารกบังขอบรกอยู่ และเชื่อว่ามีความปลอดภัยในการตรวจเมื่อทำการตรวจด้วยความนุ่มนวล
ในกรณีทั่วไปขั้นตอนการตรวจควรเริ่มด้วยการตรวจทางหน้าท้องก่อน โดยตรวจในแนวยาวตามลำตัว ขณะที่กระเพาะปัสสาวะโป่ง ดูที่ตำแหน่งส่วนล่างของมดลูกและให้ดูระยะห่างระหว่างปากมดลูกด้านในกับรก และวินิจฉัยตามเกณฑ์ข้างต้น ในกรณีที่รกเกาะส่วนล่างของมดลูกและยังเห็นปากมดลูกไม่ชัดเจนให้ทำการตรวจทางช่องคลอดหรือทางปากช่องคลอด โดยให้ผู้ป่วยปัสสาวะทิ้งก่อนตรวจจะให้ภาพที่เห็นปากมดลูกด้านในและขอบรกได้ดีขึ้น
ผู้ตรวจควรทำการตรวจและรายงานผลว่าชายรกห่างจากขอบรกมากน้อยเพียงใดและมีขอบเขตสิ้นสุดบริเวณไหน มีภาวะรกติด (Placenta adherence) ร่วมด้วยหรือไม่ เพราะการทราบขอบเขตรกและความผิดปกติของการฝังตัวของรกมีประโยชน์อย่างมากในการวางแผนการผ่าตัด ในกรณีที่วินิจฉัยภาวะรกเกาะต่ำในไตรมาสที่สองของการตั้งครรภ์โดยเฉพาะในกรณีที่ไม่ปิดคลุมปากมดลูกทั้งหมดจะต้องมีการตรวจติดตามตำแหน่งของรก เนื่องจากอาจจะพบมีการเคลื่อนตัวของรกไปทางด้านบนที่เรียกว่า Placenta migration และต้องตรวจว่ามีเส้นเลือดทอดผ่านถุงน้ำคร่ำบริเวณปากมดลูกหรือไม่ (Vasa previa) ก่อนที่จะตัดสินใจเลือกวิธีการคลอด
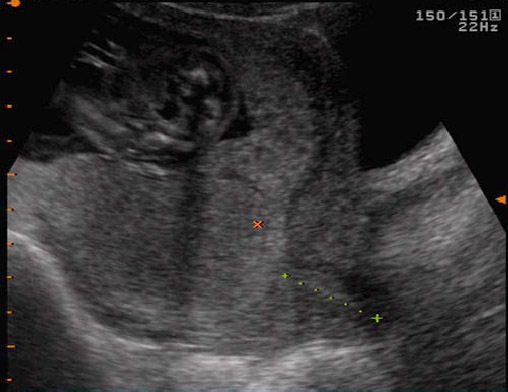
รูปที่ 9 : ภาพการตรวจด้วยคลื่นเสียงความถี่สูงทางหน้าท้องแสดงภาวะรกเกาะต่ำชนิดสมบูรณ์ (19)
นอกจากนี้ควรทำการตรวจให้รอบคอบเพราะอาจมีการแปลผลผิดพลาดได้ โดยมีผลบวกลวงซึ่งมักเกิดจากการที่มีกระเพาะปัสสาวะโป่งมากจนอาจกดผนังด้านหน้ามดลูกส่วนล่างจนตีบลงให้ชิดกับผนังด้านหลัง ทำให้ดูคล้ายปากมดลูกด้านในที่จะอยู่สูงกว่าตำแหน่งปกติ อาจแปลผลได้ว่ารกเกาะต่ำ ทำให้เกิดผลบวกลวงขึ้น ในกรณีเช่นนี้แนะนำให้ผู้ป่วยปัสสาวะทิ้งบางส่วนแล้วทำการตรวจซ้ำ บางครั้งการหดรัดตัวของมดลูกส่วนล่างทำให้กล้ามเนื้อหนาตัวขึ้นจนแปลผลผิดว่าเป็นรกได้ ถ้าสงสัยภาวะนี้ให้ทำการตรวจซ้ำในอีก 30 นาที (20) สำหรับผลลบลวงนั้นอาจเกิดขึ้นได้จากการที่มีศีรษะทารกบดบังทำให้เห็นภาพของปากมดลูกและผนังมดลูกไม่ชัดเจน ในกรณีนี้ให้ทำการตรวจเพิ่มเติมทางช่องคลอด
2. สายสะดือเกาะที่เยื่อหุ้มเด็กโดยผ่านปากมดลูกด้านใน (Vasa previa)
สายสะดือเกาะที่เยื่อหุ้มเด็กโดยผ่านปากมดลูกด้านในเป็นภาวะที่มีเส้นเลือดทอดผ่านถุงน้ำคร่ำโดยไม่มีรกหรือ Wharton’s jelly ปกคลุม อยู่ต่ำกว่าส่วนนำของทารกและใกล้กับปากมดลูกด้านใน ถ้าเกิดมีการแตกของถุงน้ำคร่ำจะทำให้เกิดการฉีกขาดของเส้นเลือดทำให้ทารกเสียเลือดจนถึงแก่ชีวิตได้ การวินิจฉัยภาวะ vasa previa ให้ได้ก่อนคลอดสามารถทำได้ด้วยการตรวจคลื่นเสียงความถี่สูง
ลักษณะทางคลื่นเสียงความถี่สูง
การวินิจฉัยด้วยคลื่นเสียงความถี่สูงทางช่องคลอดและทางปากช่องคลอดจะมีประสิทธิภาพดีกว่าการตรวจทางหน้าท้อง ลักษณะภาพคลื่นเสียงความถี่สูงจะเห็นเส้นเลือดเส้นเดี่ยวหรือหลายส้นทอดผ่านเยื่อหุ้มเด็กบริเวณปากมดลูก บางครั้งอาจจะเห็นการเต้นเป็นจังหวะตามชีพจรทารก ในรายที่สงสัย vasa previa ควรยืนยันการตรวจด้วย Doppler flow และต้องแยกภาวะ Funic presentation ซึ่งเป็นภาวะที่สายสะดืออยู่ต่ำกว่าส่วนนำของทารกและใกล้ปากมดลูก การวินิจฉัยแยกจากภาวะ Funic presentation สามารถทำได้ด้วยการดันส่วนนำของทารกให้เคลื่อนขึ้นร่วมกับการกดบริเวณส่วนล่างของตัวมดลูกจะพบว่าสายสะดือจะมีการเคลื่อนตาม ซึ่งต่างจาก vasa previa จะไม่พบการเคลื่อนตัวของเส้นเลือด
3. รกลอกตัวก่อนกำหนด (Placental abruption)
รกลอกตัวก่อนกำหนดเป็นภาวะที่มีการลอกตัวของรกในตำแหน่งปกติก่อนทารกคลอด ทำให้มีเลือดออกในชั้นใต้รก โดยออกมาจากเส้นเลือด Spiral arteries ซึ่งอาจจะมีเลือดออกทางช่องคลอด (Reveal type) หรือคั่งสะสมอยู่หลังรกหรือเยื่อหุ้มเด็ก (Conceal type) การวินิจฉัยอาศัยอาการและอาการแสดงทางคลินิกคือเลือดออกทางช่องคลอด มดลูกหดรัดตัวและกดเจ็บ แต่มีประมาณร้อยละ 10 เป็นชนิด concealed จะไม่มีเลือดออกทางช่องคลอด การตรวจวินิจฉัยด้วยคลื่นเสียงความถี่สูงมีประโยชน์ค่อนข้างน้อย เนื่องจากมีความไวในการวินิจฉัยไม่ถึงร้อยละ 50 (21) แต่ยังคงมีประโยชน์ในกรณีที่มีลักษณะทางคลินิกไม่ชัดเจนและจำเป็นต้องแยกกับภาวะรกเกาะต่ำ
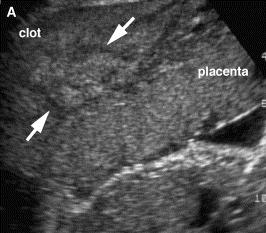
รูปที่ 10 : รกลอกตัวก่อนกำหนดเห็นก้อนเลือดอยู่หลังรก (22)
ลักษณะทางคลื่นเสียงความถี่สูง
เมื่อทำการตรวจด้วยเครื่องเสียงความถี่สูงจะพบว่ารกมีการแยกตัวจากชั้นเยื่อบุโพรงมดลูก และมีเลือดออกหลังรกบริเวณ subchorionic และ retroplacenta ลักษณะเลือดที่ออกอาจจะเห็นเป็นบริเวณความเข้มเสียงต่ำหรือความเข้มเสียงสูงต่ำปนกัน เมื่อเป็นก้อนเลือดคั่งใหม่จะมีความเข้มเสียงมากขึ้น ในรายที่เลือดออกใหม่อาจจะเห็นเป็นบริเวณ echogenic ซึ่งให้ลักษณะภาพคล้ายกับเนื้อรกปกติได้ทำให้เห็นเป็นเพียงเนื้อรกที่ดูหนาขึ้น แต่ก้อนเลือดที่คั่งอยู่สักระยะหนึ่งจะเริ่มมีการสลายตัวและมีความเข้มเสียงไม่สม่ำเสมอทำให้แยกออกจากเนื้อรกได้ชัดเจนขึ้น นอกจากนี้กล้ามเนื้อมดลูกที่มีการหดรัดตัว เนื้องอกกล้ามเนื้อมดลูกและ vascular plexus ที่อยู่หลังรกจะให้ภาพคล้ายกับเลือดออกหลังรกได้ จึงควรระมัดระวังในการแปลผลซึ่งมีข้อสังเกตในการวินิจฉัยดังนี้
– รกจะหนามากกว่าปกติ ทั้งเป็นเพราะมีก้อนเลือดอยู่ใต้ต่อตำแหน่งรก
– อาจมีแนวของกล้ามเนื้อมดลูกให้เห็นตลอดแนวหลังรก[S1] เป็นแนวเรียบ ซึ่งจะเห็นก้อนเลือดวางอยู่บนแนวนี้
– ความเข้มเสียงมักจะไม่สม่ำเสมอเท่ากับกล้ามเนื้อมดลูก (มีความเข้มเสียงต่ำ) และรก (มีความเข้มเสียงสูงกว่า)
– แนวต่อระหว่างรกกับก้อนเลือดมีลักษณะไม่เรียบ
– รกถูกยกตัวขึ้นบางบริเวณที่มีเลือดคั่งอยู่ข้างใต้ และจะมีบริเวณที่หนาเท่าปกติให้เห็นปะปนอยู่ด้วย
– อาจเห็นรอยแยกระหว่างแนวของรกและกล้ามเนื้อมดลูกในตำแหน่งที่มีผิวสัมผัสติดกันตามปกติ แยกออกจากกันที่ตำแหน่งของก้อนเลือด
นอกจากนี้แพทย์ผู้ทำการตรวจควรระบุตำแหน่งและขนาดของก้อนเลือดที่คั่งใต้รก ซึ่งเป็นปัจจัยสำคัญที่ส่งผลต่อสุขภาพของมารดาและทารกในครรภ์
4. เลือดออกบริเวณขอบรก (Marginal sinus separation)
เลือดที่ออกบริเวณขอบรกเชื่อว่ามาจากเส้นเลือดดำที่ขอบรก อาจจะเห็นเป็นก้อนเลือดที่ขอบรก ก้อนเลือดสามารถแผ่ขยายออกห่างจากรกโดยแทรกไปในชั้นใต้ Chorion ซึ่งมีความต้านทานต่ำ เลือดที่ออกในลักษณะนี้มีอันตรายน้อยกว่าเลือดที่ออกหลังรกเพราะรบกวนการทำงานของรกไม่มาก
ลักษณะทางคลื่นเสียงความถี่สูง
เมื่อตรวจด้วยคลื่นเสียงความถี่สูงจะพบก้อนที่มีรูปร่างเหมือนพระจันทร์เสี้ยว (Crescent shape) บริเวณขอบรก มีความเข้มเสียงต่ำถ้าเลือดออกมาได้ไม่นานและเห็นขอบรกยกสูงขึ้นเล็กน้อย
การตรวจด้วยคลื่นเสียงความถี่สูงสำหรับภาวะฉุกเฉินในระยะคลอด
ภาวะมดลูกปริและแตก (Uterine dehiscence and rupture)
ถึงแม้ว่าภาวะมดลูกปริหรือแตกจะพบได้ในหญิงตั้งครรภ์ปกติทั่วไปก็ตาม แต่ส่วนใหญ่แล้วพบในหญิงที่มีแผลบริเวณมดลูกจากการผ่าตัดคลอดในครรภ์ก่อนได้บ่อยที่สุด ภาวะที่มีรอยแยกของผนังมดลูกโดยที่ผิวชั้นนอก (Serosa) ยังคงติดกันอยู่และยังไม่มีส่วนของถุงน้ำคร่ำหรือทารกออกไปอยู่นอกมดลูกเรียกว่า ภาวะมดลูกปริ (Uterine dehiscence) สามารถทำให้มีเลือดออกในช่องท้องและช่องคลอดได้ในปริมาณไม่มากนัก แต่ถ้ามีการแยกของผนังมดลูกทุกชั้นจนมีส่วนของถุงน้ำคร่ำหรือทารกออกไปอยู่ในช่องท้องแล้วจะเรียกว่า ภาวะมดลูกแตก (Uterine rupture) ซึ่งภาวะนี้ทำให้มีอัตราการบาดเจ็บและเสียชีวิตของทั้งทารกและมารดาค่อนข้างสูง เป็นภาวะฉุกเฉินที่ต้องได้รับการวินิจฉัยอย่างเร่งด่วน การประเมินความเสี่ยงไว้ก่อนล่วงหน้าและเฝ้าระวังในระยะคลอดและหลังคลอดเป็นอย่างดี ร่วมกับการตรวจร่างกายและการตรวจด้วยคลื่นเสียงความถี่สูงเมื่อสงสัยจะนำไปสู่การวินิจฉัยได้อย่างรวดเร็ว
ลักษณะทางคลื่นเสียงความถี่สูง
เมื่อมีการแตกของมดลูกเกิดขึ้นอาจจะเห็นลักษณะภาพทางคลื่นเสียงความถี่สูงดังนี้ (23)
- พบบางส่วนของทารกอยู่นอกมดลูก
- พบบางส่วนของถุงน้ำคร่ำโป่งนูนผ่านรอยแยกของผนังมดลูก
- พบรอยแยกของเยื่อบุโพรงมดลูกและผนังกล้ามเนื้อมดลูก
- พบก้อนเลือดและเลือดออกอยู่ในช่องท้องภายนอกมดลูก
- บางครั้งอาจพบเลือดออกภายในถุงน้ำคร่ำร่วมด้วย
นอกจากนี้ยังมีผู้ศึกษาวิจัยถึงการใช้การตรวจด้วยคลื่นเสียงความถี่สูงทางช่องคลอดมาช่วยในการตรวจหารอยแยกของแผลผ่าตัดคลอดเดิมในระยะก่อนเจ็บครรภ์คลอดเพื่อเป็นข้อมูลประกอบในการตัดสินใจเลือกวิธีการคลอด พบว่ามีความไวในการตรวจพบรอยแผลบริเวณมดลูกได้ร้อยละ 87 และมีความจำเพาะร้อยละ 100 (24) และมีรายงานการศึกษาอีกฉบับหนึ่งพบว่าการตรวจด้วยคลื่นเสียงความถี่สูงทางหน้าท้องขณะอายุครรภ์ 36-38 สัปดาห์ ในรายที่พบว่าผนังมดลูกส่วนล่างมีความหนาน้อยกว่า 1.5 -3.5 มิลลิเมตรมีความเสี่ยงต่อการเกิดมดลูกแตกสูงขึ้น (25)
ภาวะรกติด (Placental accreta)
ภาวะรกติดถือเป็นความผิดปกติในการฝังตัวของรก โดยที่ Chorionic villi ฝังตัวบุกรุกลึกเข้าไปถึงชั้น decidual basalis และสัมผัสกับกล้ามเนื้อมดลูก เชื่อว่าเกิดจากการที่ชั้น Neitabuch layer ของ decidual หายไปหรือมีน้อย ถ้ามีการบุกรุกเข้าไปในกล้ามเนื้อมดลูกด้วยเรียกว่า Placenta increta และอาจมีการฝังตัวทะลุผ่านชั้นกล้ามเนื้อมดลูกออกไปถึงชั้น serosa เรียกว่า Placenta percreta มีการศึกษาพบว่าภาวะรกติดมีความสัมพันธ์กับประวัติการผ่าตัดคลอด การขูดมดลูกและการมีภาวะรกเกาะต่ำ ภาวะนี้เป็นภาวะที่อันตรายเนื่องจากทำให้เกิดการตกเลือดในระยะคลอดและหลังคลอด มีอัตราการตายสูง การวินิจฉัยก่อนคลอดอาจมีประโยชน์ในการวางแผนการดูแลรักษา ให้คำปรึกษาแก่ผู้ป่วยและเตรียมความพร้อมในการคลอด เนื่องจากอาจจะต้องทำการตัดมดลูกภายหลังการคลอด
ลักษณะทางคลื่นเสียงความถี่สูง
การวินิจฉัยก่อนคลอดของภาวะรกติดด้วยคลื่นเสียงความถี่สูงค่อนข้างยาก แต่ก็มีลักษณะทางคลื่นเสียงความถี่สูงที่บ่งชี้ถึงความเป็นไปได้ที่จะมีโอกาสเกิดภาวะรกติดในระยะคลอดดังนี้
– แถบความเข้มเสียงต่ำของชั้น Decidual basalis หายไป และมีการขยายขนาดของเส้นเลือดดำ
– เมื่อมีการตรวจติดตามพบว่าแถบความเข้มเสียงต่ำบริเวณหลังรกบางลงและพบมีแอ่งเลือดของรก (Placental lake) แผ่ขยายจากเนื้อรกเข้าไปในกล้ามเนื้อมดลูก ซึ่งเรียกลักษณะที่พบนี้ว่า “Swiss cheese” appearance (26)
เนื้อรกบุกรุกขยายเลยชั้นผิวนอกของมดลูกหรือบุกรุกออกไปชิดอวัยวะข้างเคียงโดยเฉพาะกระเพาะปัสสาวะ (27)
– แถบความเข้มเสียงต่ำของกล้ามเนื้อมดลูกที่อยู่ระหว่างรกและชั้นเยื่อบุผิวนอกของมดลูก (Serosa) หรือกระเพาะปัสสาวะหายไปหรือบางมาก เส้นเลือดของมดลูกที่อยู่ใกล้รกขยายใหญ่ขึ้น บางบริเวณไม่สามารถหากล้ามเนื้อมดลูกได้ (28)
– จากการตรวจด้วย Doppler พบว่ามีการไหลเวียนของเลือดอย่างรวดเร็วหรือมี turbulent blood flow ในแอ่งเลือดของรก (Placental Lake) ที่กินลึกเข้าไปในกล้ามเนื้อมดลูก (29)
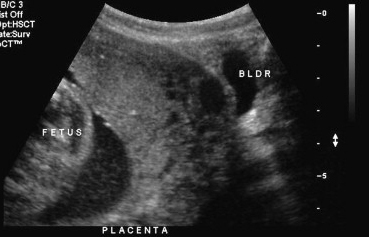
รูปที่ 11 : แสดงแถบความเข้มเสียงต่ำบริเวณหลังรกบางลงและพบมีแอ่งเลือดของรก (Placental lake) แผ่ขยายจากเนื้อรกเข้าไปในกล้ามเนื้อมดลูก ซึ่งเรียกลักษณะที่พบนี้ว่า “Swiss cheese” appearance
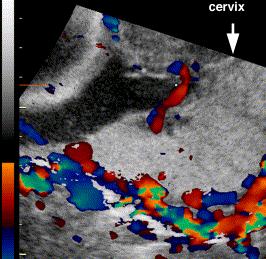
รูปที่ 12 : การตรวจด้วย Doppler พบว่ามีแถบความเข้มเสียงต่ำบริเวณหลังรกบางลงและพบมีแอ่งเลือดของรกที่มี turbulent blood flow ภายใน (22)
ในรายที่ไม่สามารถบอกขอบเขตของการบุกรุกของรกได้แน่นอน ในรายที่สงสัยอาจตรวจด้วย MRI ซึ่งบอกขอบเขตของการบุกรุกได้ดีกว่า
การตรวจด้วยคลื่นเสียงความถี่สูงสำหรับภาวะฉุกเฉินในระยะหลังคลอด
ภาวะตกเลือดหลังคลอด (Postpartum hemorrhage)
ภาวะตกเลือดหลังคลอดถือเป็นภาวะฉุกเฉินทางสูติศาสตร์ที่เป็นสาเหตุสำคัญของการเสียชีวิตของสตรีตั้งครรภ์ ซึ่งภาวะตกเลือดหลังคลอดเกิดขึ้นได้จากหลายสาเหตุ การมีรกค้างและรกติดก็เป็นสาเหตุหนึ่งที่ทำให้เกิดการตกเลือดหลังคลอดและต้องได้รับการประเมินเพื่อวินิจฉัยและทำการรักษาเพิ่มเติมอย่างเร่งด่วน
1. ภาวะรกค้าง (Retain piece of placenta)
ปัจจัยเสี่ยงที่ทำให้คลอดรกออกมาได้ไม่ครบได้แก่ การมีรกน้อย (Placenta succenturia) และการมีรกติด การมีเศษชิ้นรกค้างอยู่ในโพรงมดลูกสามารถวินิจฉัยได้จากการตรวจรกที่คลอดออกมาว่าครบหรือไม่ และทำการตรวจด้วยคลื่นเสียงความถี่สูงก่อนที่จะทำการขูดมดลูกเพิ่มเติม
ลักษณะทางคลื่นเสียงความถี่สูง
ลักษณะภาพที่เห็นจะมีลักษณะไม่จำเพาะ ก้อนเลือดและเศษชิ้นรกให้ภาพที่มีลักษณะคล้ายกันได้ โดยจะเห็นเป็นก้อนที่มีความเข้มเสียงสูง (Echogenic mass) อยู่ในโพรงมดลูก ในบางครั้งอาจเห็นเป็นก้อนที่มีความเข้มเสียงไม่สม่ำเสมอ (Heterogeneous mass) แต่โดยมากถ้าตรวจพบก้อนลักษณะแบบนี้มักจะเป็นก้อนเลือดที่ค้างอยู่ ในกรณีที่ตรวจด้วยคลื่นเสียงความถี่สูงและพบว่าโพรงมดลูกเรียบดีหรือมีแถบความเข้มเสียงสูงอยู่ในโพรงมดลูกโดยที่ไม่พบก้อนมักจะไม่พบว่ามีเศษชิ้นรกเหลืออยู่ (30)
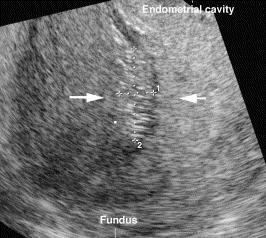
รูปที่ 13 : ภาวะรกค้างเห็นเป็นก้อนที่มีความเข้มเสียงสูง (Echogenic mass) อยู่ในโพรงมดลูก (22)
2. ภาวะรกติด (Placental accreta)
สำหรับภาวะรกติดมีลักษณะทางคลื่นเสียงความถี่สูงดังที่กล่าวไว้ในหัวข้อก่อนหน้านี้
สรุป
การตรวจด้วยคลื่นเสียงความถี่สูงมีประโยชน์สำหรับการวินิจฉัยและวางแผนการดูแลรักษาผู้ป่วยที่มีภาวะฉุกเฉินทางสูติศาสตร์ และมีการใช้กันอย่างแพร่หลาย สูติแพทย์และแพทย์ทั่วไปที่ต้องดูแลสตรีตั้งครรภ์ควรเรียนรู้และฝึกฝนให้เกิดความชำนาญ
เอกสารอ้างอิง
- Cullen MT, Green JJ, Reece EA, Hobbins JC. A comparison of transvaginal and abdominal ultrasound in visualizing the first trimester conceptus. J Ultrasound Med. 1989 Oct;8(10):565-9.
- Tongsong T, Srisomboon J, Wanapirak C, Sirichotiyakul S, Pongsatha S, Polsrisuthikul T. Pregnancy outcome of threatened abortion with demonstrable fetal cardiac activity: a cohort study. J Obstet Gynaecol (Tokyo 1995). 1995 Aug;21(4):331-5.
- Wilson RD, Kendrick V, Wittmann BK, McGillivray B. Spontaneous abortion and pregnancy outcome after normal first-trimester ultrasound examination. Obstet Gynecol. 1986 Mar;67(3):352-5.
- Mantoni M. Ultrasound signs in threatened abortion and their prognostic significance. Obstet Gynecol. 1985 Apr;65(4):471-5.
- Stabile I, Campbell S, Grudzinskas JG. Ultrasonic assessment of complications during first trimester of pregnancy. Lancet. 1987 Nov 28;2(8570):1237-40.
- Tongsong T, Wanapirak C, Srisomboon J, Sirichotiyakul S, Polsrisuthikul T, Pongsatha S. Transvaginal ultrasound in threatened abortions with empty gestational sacs. Int J Gynaecol Obstet. 1994 Sep;46(3):297-301.
- Nyberg DA, Laing FC, Filly RA. Threatened abortion: sonographic distinction of normal and abnormal gestation sacs. Radiology. 1986 Feb;158(2):397-400.
- Williams Obstetrics. United States of America: McGraw-Hill Companies; 2010.
- Levi CS, Lyons EA, Zheng XH, Lindsay DJ, Holt SC. Endovaginal US: demonstration of cardiac activity in embryos of less than 5.0 mm in crown-rump length. Radiology. 1990 Jul;176(1):71-4.
- Pennell RG, Needleman L, Pajak T, Baltarowich O, Vilaro M, Goldberg BB, et al. Prospective comparison of vaginal and abdominal sonography in normal early pregnancy. J Ultrasound Med. 1991 Feb;10(2):63-7.
- Romero R, Kadar N, Jeanty P, Copel JA, Chervenak FA, DeCherney A, et al. Diagnosis of ectopic pregnancy: value of the discriminatory human chorionic gonadotropin zone. Obstet Gynecol. 1985 Sep;66(3):357-60.
- ทองสง ธ, editor. คลื่นเสียงความถี่สูงทางสูติศาสตร์. กรุงเทพฯ: พี.บี. ฟอเรน บุ๊คส์ เซนเตอร์; 2000.
- Reece EA, Petrie RH, Sirmans MF, Finster M, Todd WD. Combined intrauterine and extrauterine gestations: a review. Am J Obstet Gynecol. 1983 Jun 1;146(3):323-30.
- Kaakaji Y, Nghiem HV, Nodell C, Winter TC. Sonography of obstetric and gynecologic emergencies: Part II, Gynecologic emergencies. AJR Am J Roentgenol. 2000 Mar;174(3):651-6.
- Hill LM, Kislak S, Martin JG. Transvaginal sonographic detection of the pseudogestational sac associated with ectopic pregnancy. Obstet Gynecol. 1990 Jun;75(6):986-8.
- Nyberg DA, Hughes MP, Mack LA, Wang KY. Extrauterine findings of ectopic pregnancy of transvaginal US: importance of echogenic fluid. Radiology. 1991 Mar;178(3):823-6.
- Wachsberg RH. Sonographic detection of echogenic fluid and correlation with culdocentesis in the evaluation of ectopic pregnancy. AJR Am J Roentgenol. 1999 Jan;172(1):244-5.
- Oyelese Y, Smulian JC. Placenta previa, placenta accreta, and vasa previa. Obstet Gynecol. 2006 Apr;107(4):927-41.
- Mukherjee S, Bhide A. Antepartum haemorrhage. OBSTETRICS, GYNAECOLOGY AND REPRODUCTIVE MEDICINE. [Review]. 2008;18(12):5.
- Townsend RR, Laing FC, Nyberg DA, Jeffrey RB, Wing VW. Technical factors responsible for “placental migration”: sonographic assessment. Radiology. 1986 Jul;160(1):105-8.
- Oyelese Y, Ananth CV. Placental abruption. Obstet Gynecol. 2006 Oct;108(4):1005-16.
- Lazebnik N, Lazebnik RS. The role of ultrasound in pregnancy-related emergencies. Radiol Clin North Am. 2004 Mar;42(2):315-27.
- Di Salvo DN. Sonographic imaging of maternal complications of pregnancy. J Ultrasound Med. 2003 Jan;22(1):69-89.
- Armstrong V, Hansen WF, Van Voorhis BJ, Syrop CH. Detection of cesarean scars by transvaginal ultrasound. Obstet Gynecol. 2003 Jan;101(1):61-5.
- Rozenberg P, Goffinet F, Philippe HJ, Nisand I. Thickness of the lower uterine segment: its influence in the management of patients with previous cesarean sections. Eur J Obstet Gynecol Reprod Biol. 1999 Nov;87(1):39-45.
- Hoffman-Tretin JC, Koenigsberg M, Rabin A, Anyaegbunam A. Placenta accreta. Additional sonographic observations. J Ultrasound Med. 1992 Jan;11(1):29-34.
- Finberg HJ, Williams JW. Placenta accreta: prospective sonographic diagnosis in patients with placenta previa and prior cesarean section. J Ultrasound Med. 1992 Jul;11(7):333-43.
- Jauniaux E, Toplis PJ, Nicolaides KH. Sonographic diagnosis of a non-previa placenta accreta. Ultrasound Obstet Gynecol. 1996 Jan;7(1):58-60.
- Lerner JP, Deane S, Timor-Tritsch IE. Characterization of placenta accreta using transvaginal sonography and color Doppler imaging. Ultrasound Obstet Gynecol. 1995 Mar;5(3):198-201.
- Hertzberg BS, Bowie JD. Ultrasound of the postpartum uterus. Prediction of retained placental tissue. J Ultrasound Med. 1991 Aug;10(8):451-6.