Basic steps in simple vaginal hysterectomy for general gynecologists
Basic steps in simple vaginal hysterectomy for general gynecologists
พญ.สุปรีชญา พันธุ์เสนีย์
อ.พญ.ศศิวิมล ศรีสุโข
การผ่าตัดมดลูก (Hysterectomy) เป็นหัตถการที่พบบ่อยเป็นอันดับสองรองจากการผ่าตัดคลอดทางหน้าท้องในการผ่าตัดทางสูติศาสตร์และนรีเวช สามารถทำได้หลากหลายช่องทาง ได้แก่ การผ่าตัดการผ่าตัดมดลูกผ่านช่องคลอด (Vaginal Hysterectomy) การผ่าตัดมดลูกผ่านหน้าท้อง (Abdominal Hysterectomy) การผ่าตัดมดลูกผ่านการส่องกล้องช่องท้อง (Laparoscopic Hysterectomy) การผ่าตัดมดลูกผ่านการส่องกล้องช่องท้องโดยใช้หุ่นยนต์ช่วย (Robotic-assisted Hysterectomy) จากรายงานหลายฉบับพบว่า การผ่าตัดการผ่าตัดมดลูกผ่านช่องคลอดมีความปลอดภัยและคุ้มทุนมากที่สุดเมื่อเปรียบเทียบกับช่องทางอื่น1 ระยะเวลานอนโรงพยาบาลสั้นกว่า การฟื้นตัวเร็วกว่าและโอกาสการติดเชื้อน้อยกว่าเมื่อเทียบกับการผ่าตัดผ่านหน้าท้อง เวลาที่ใช้ในการผ่าตัดสั้นกว่าการผ่าตัดผ่านการส่องกล้องช่องท้อง อย่างไรก็ตามการผ่าตัดผ่านหน้าท้องได้รับความนิยมมากกว่าการผ่าตัดผ่านช่องคลอดมาก อาจเนื่องจากหลายปัจจัย เช่น ความต้องการของผู้ป่วยหรือความชำนาญของแพทย์ผู้ผ่าตัด เป็นต้น สถิติของโรงพยาบาลมหาราชนครเชียงใหม่ในปี ค.ศ. 2004-2013 มีผู้เข้ารับการผ่าตัดมดลูกจำนวน 1,035 ราย คิดเป็นผ่าตัดผ่านหน้าท้องร้อยละ 94 ผ่านช่องคลอดร้อยละ 1.2 และผ่านการส่องกล้องช่องท้องร้อยละ 4.82 จะเห็นได้ว่า ถึงแม้การผ่าตัดผ่านช่องคลอดจะเป็นวิธีที่ปลอดภัย แต่เป็นวิธีที่ทำน้อยมากเมื่อเทียบกับการผ่าตัดผ่านหน้าท้อง รวมถึงน้อยกว่าการผ่าตัดผ่านการส่องกล้องช่องท้องซึ่งเป็นวิธีที่ทันสมัยกว่า ซึ่งการเลือกช่องทางการผ่าตัดมดลูกส่วนใหญ่ขึ้นอยู่กับการตกลงระหว่างแพทย์และผู้ป่วย
ข้อบ่งชี้ (Indication)3,4
- เนื้องอกกล้ามเนื้อมดลูก (Uterine fibroids)
- เลือดออกผิดปกติทางช่องคลอด (Abnormal Uterine Bleeding) โดยอาจจะมาจากหลายสาเหตุ เช่น Adenomyosis, endometrial hyperplasia เป็นต้น
- ภาวะอุ้งเชิงกรานหย่อน (Genital prolapse) ในรายที่ต้องด้วยการผ่าตัดและไม่ต้องการมีบุตรอีก การผ่าตัดมดลูกผ่านช่องคลอดเป็นทางเลือกแรก เนื่องจากสามารถทำหัตถการอื่นๆ ได้ไปในคราวเดียวกัน เช่น pelvic floor repair, sacrospinous colpopexy เป็นต้น
- Neoplasia ส่วนมากจะแนะนำการผ่าตัดผ่านหน้าท้องมากกว่า อย่างไรก็ตามสามารถผ่าตัดมดลูกผ่านช่องคลอดได้ในบางราย เช่น carcinoma in-situ of the cervix, cervical cancer stage IA1 หรือ Early Endometrial cancer stage 1 โดยเฉพาะในคนไข้ที่อ้วนมากหรือมีโรคหัวใจหรือปอด โดยอาจทำพร้อมกับการเลาะต่อมน้ำเหลืองผ่านการส่องกล้อง (Laparoscopic lymphadenectomy) การศึกษาของ Ingiulla พบว่า Survival rate ในผู้ป่วยมะเร็งเยื่อบุโพรงมดลูกที่ผ่าตัดมดลูกผ่านช่องคลอดสูงกว่าการผ่าตัดผ่านหน้าท้อง 5
- Miscellaneous เช่น ปวดท้องน้อยเรื้อรัง (Chronic pelvic pain) หรือ Benign adnexal pathology โดยจะเลือกในรายที่มั่นใจว่าไม่ใช่มะเร็งและก้อนรังไข่เคลื่อนที่ได้ง่าย
ข้อบ่งห้าม (Contraindication) 3,6,7
สำหรับข้อบ่งห้ามในการผ่าตัดมดลูกทางช่องคลอดนั้นยังเป็นข้อถกเถียงกันอยู่ ผู้เชี่ยวชาญบางรายแนะนำบางภาวะที่ไม่เหมาะสมกับการผ่าตัดผ่านช่องคลอด แต่บางรายก็แนะนำว่าสามารถผ่าตัดได้ ดังนั้น ขณะนี้ยังไม่มีข้อบ่งห้ามของการผ่าตัดทางช่องคลอดชัดเจน อาจพอสรุป relative contraindication ได้ดังนี้
- มดลูกขนาดใหญ่มากกว่า 12 สัปดาห์หรือปริมาตรเกิน 300 ลูกบาศก์เซนติเมตร สามารถผ่าตัดผ่านช่องคลอดได้ โดยการลดขนาดของมดลูกขณะผ่าตัด เช่น wedge morcellation, uterine bisection และ intramyometrial coring หรือการให้ยากลุ่ม GnRH analogue ลดขนาดก้อนก่อนการผ่าตัดก็ได้ 2
- ภาวะที่ทำให้การเข้าถึงมดลูกเป็นไปได้ยาก ได้แก่ Undescended/immobilized uterus, narrow vagina, narrow pubic arch (น้อยกว่า 90 องศา) อย่างไรก็ตาม หากสามารถเข้าถึง Uterosacral ligament และ cardinal ligament ผ่านทางช่องคลอดได้ ก็สามารถผ่าตัดมดลูกผ่านช่องคลอดได้เช่นกัน
- รอยโรคนอกมดลูก เช่น ก้อนที่ปีกมดลูกและรังไข่ พังผืดในช่องท้อง เยื่อบุโพรงมดลูกเจริญผิดที่ การใช้ Laparoscopic examination ประเมินรอยโรคเพื่อช่วยเลือกช่องทางการผ่าตัดมดลูก พบถึงร้อยละ 91 ที่สามารถผ่าตัดผ่านช่องคลอดได้ในผู้ป่วยกลุ่มนี้ 8
- นอกจากนี้ยังมีปัจจัยอื่นที่ทำให้แพทย์กังวล เช่น ผู้ป่วยที่ไม่เคยคลอดบุตรทางช่องคลอดมาก่อนหรือเคยผ่าตัดคลอด แต่ในผู้ป่วยกลุ่มนี้สามารถผ่าตัดทางช่องคลอดได้เช่นกัน9,10
การตัดท่อนำไข่และรังไข่ (Elective Salpingo-oophorectomy)
ในผู้ป่วยที่ต้องการตัดท่อนำไข่และรังไข่พร้อมกับการตัดมดลูกโดยที่ไม่มีรอยโรค ไม่มีผลต่อการตัดสินใจในการเลือกช่องทางการผ่าตัด ดังนั้น สามารถผ่าตัดผ่านช่องคลอดได้ รายงานการผ่าตัดมดลูกพร้อมท่อนำไข่และรังไข่ผ่านช่องคลอดประสบความสำเร็จถึงร้อยละ 65-97.5 สำหรับการใช้การส่องกล้องทางช่องคลอด (Transvaginal Natural Orifice Transluminal Endoscopic Surgery ; NOTES) เพื่อช่วยในการผ่าตัดนั้นอาจมีประโยชน์ในรายที่มดลูกไม่มีการหย่อนหรือการ exposure ทางช่องคลอดทำได้ยาก การส่องกล้องอาจช่วยลดโอกาสเกิดภาวะแทรกซ้อนในการเกิด adjacent organ injury เนื่องจาก identify anatomy ให้ชัดเจนขึ้น
Preoperative preparation2,11
- Anesthesia วิธีที่เหมาะสมที่สุดคือ การระงับความรู้สึกเฉพาะส่วนโดยการฉีดยาชาเข้าทางช่องไขสันหลังหรือ spinal anesthesia ซึ่งเป็นวิธีที่รวดเร็วและปลอดภัย
- Patient position จัดให้ผู้ป่วยอยู่ในท่าขึ้นขาหยั่ง (lithotomy) บริเวณขาอาจใช้ candy cane stirrups หรือ boot-type stirrups เพื่อช่วยให้การผ่าตัดง่ายขึ้น แต่ต้องระมัดระวังการเกิดแผลกดทับ การบาดเจ็บของเส้นประสาทและ compartment syndrome
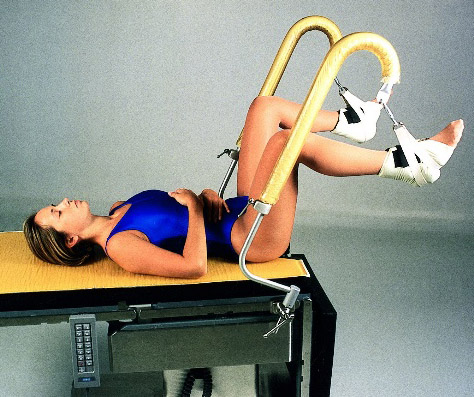
รูปที่ 1 แสดงผู้ป่วยในท่า dorsal lithotomy และ candy cane stirrups

รูปที่ 2 แสดง boot-type stirrups
- Abdomino-vaginal preparation ทำความสะอาดหน้าท้องและช่องคลอดด้วย providone-iodine หรือ chlorhexidine-alcohol ไม่จำเป็นต้องโกนขนหัวหน่าว
- Bladder catheter insertion เพื่อป้องกันกระเพาะปัสสาวะหย่อนลงมาบังพื้นที่การผ่าตัด ช่วงเวลาที่จะสวนขึ้นอยู่กับแพทย์ผู้ผ่าตัด โดยอาจสวนก่อนเริ่มการผ่าตัดหรือหลังจากเข้าสู่ Cul-de-sac ด้านหน้า หรือในบางครั้งอาจใช้ indigo carmine หรือ methylene blue ฉีดเข้าไปในกระเพาะปัสสาวะก่อน ซึ่งการสวนหลังเข้า Cul-de-sacและการฉีดสี จะช่วยให้แพทย์ผู้ผ่าตัดทราบหากมีการบาดเจ็บต่อกระเพาะปัสสาวะ แต่ไม่ลดโอกาสการบาดเจ็บต่อกระเพาะปัสสาวะ
- Prophylactic antibiotics ผู้ป่วยที่ได้รับการผ่าตัดมดลูกทางช่องคลอดควรได้รับการป้องกันการติดเชื้อด้วยยาปฏิชีวนะทางหลอดเลือดดำ (Intravenous) สำหรับยาปฏิชีวนะที่เหมาะสม คือ กลุ่ม 1st generation cephalosporin เช่นเดียวกับการผ่าตัดมดลูกทางหน้าท้อง12
Procedure2, 9, 13, 14
Cervix incision
การทำ cervical incision เพื่อช่วยรักษาความยาวของช่องคลอด แพทย์ผู้ผ่าตัดบางรายอาจไม่ทำก็ได้ ก่อนการทำ cervical incision จะฉีดสารน้ำโดยรอบบริเวณ cervical mucosae เพื่อลดการเสียเลือดและยังช่วยเรื่อง hydrodissection สารที่นิยมใช้คือยาชาเฉพาะที่ เช่น lidocaine หรือ bupivacaine ร่วมกับ epinephrine และน้ำ จากนั้นจะกรีดเปิดโดยรอบของ vaginal rugae บริเวณรอยต่อจากปากมดลูกทั้งทางด้านหน้าและด้านหลัง โดยใช้ใบมีดหรือจี้ไฟฟ้า แล้วใช้นิ้วดันเพื่อแยกชั้น vaginal mucosa ลดการบาดเจ็บต่อกระเพะปัสสาวะ
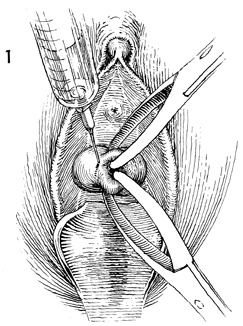
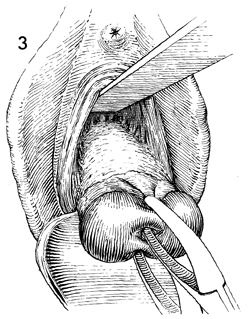
รูปที่ 3 แสดงการฉีด vasoconstrictor รอบ cervical mucosae
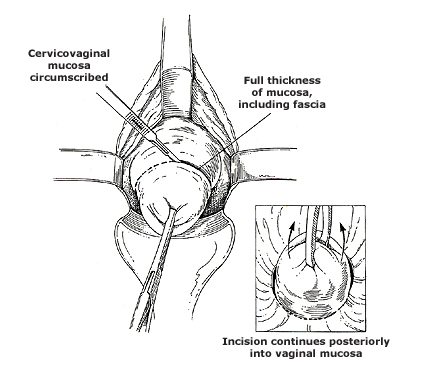
รูปที่ 4 แสดงการกรีดเปิดปากมดลูก
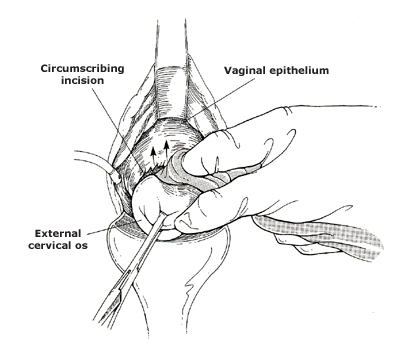
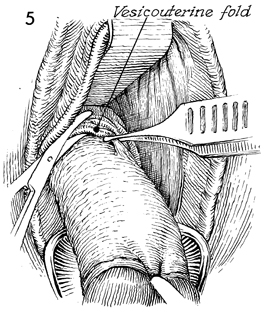
รูปที่ 5 แสดงการแยกชั้น vaginal mucosa กับ cervix โดย blunt dissection
Entry into the peritoneal cavity
หลังจากกรีดเปิด vaginal mucosae จะเห็น cul-de-sac อยู่ด้านใน และทำการกรีดเปิดเพื่อเข้าสู่ช่องท้อง
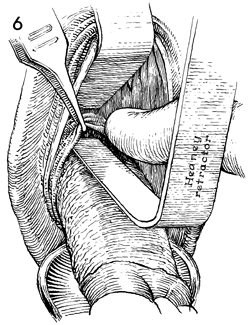
- Posterior cul-de-sac entry ใช้ tenaculum จับที่ปากมดลูกแล้วดึงไปด้านหน้า อาจใช้ retractor ดึงช่องคลอดด้านหลัง เพื่อทำให้เห็น cul-de-sac ด้านหลังและ peritoneum ได้ชัดเจนมากขึ้น ใช้ forceps จับที่ cul-de-sac และดึงเข้าหาตัว จากนั้นใช้กรรไกร mayo ตัดเหนือ forceps ในแนวขวางหรือในลักษณะ “T appearance” ในกรณีที่ไม่เห็น peritoneum ได้ชัด โดยพยายามตัดให้ชิดด้านปากมดลูกมากที่สุด เพื่อป้องกัน bowel injury หลังจากตัด peritoneum แล้ว อาจเห็นน้ำในช่องท้องได้ 70-100 มิลลิลิตร จากนั้นให้วาง right-angle Heaney retractor ในช่องที่เปิดไว้
รูปที่ 6 แสดงการตัด posterior cul-de-sac
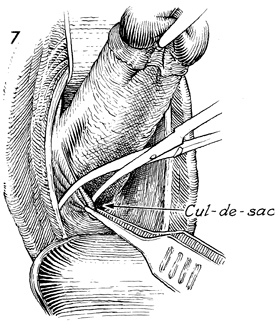
รูปที่ 7 แสดงการวาง Heaney retractor ใน posterior peritoneum cavity
- Anterior cul-de-sac entry ใช้ tenaculum จับที่ปากมดลูกแล้วดึงลงด้านหลังและใช้ right-angle retractor ดึงช่องคลอดไปด้านหน้า เพื่อป้องกันการบาดเจ็บต่อกระเพาะปัสสาวะและหา vesicouterine fold ลักษณะเป็นแถบสีขาวในแนวขวางต่อมดลูกส่วนล่าง (lower uterine segment) ซึ่งเป็นบริเวณที่จะตัดเพื่อเข้าสู่ช่องท้อง ในรายที่มีพังผืดยึดมดลูก เช่น เคยผ่าตัดคลอดมาก่อน มีภาวะเยื่อบึโพรงมดลูกเจริญผิดที่ เป็นต้น อาจหา vesicouterine fold ได้ยาก ใช้ forceps จับบริเวณ vesicouterine fold แล้วยกขึ้น จากนั้นตัดด้วยกรรไกร mayo แล้ววาง right-angle Heaney retractor ในช่องที่เปิดไว้
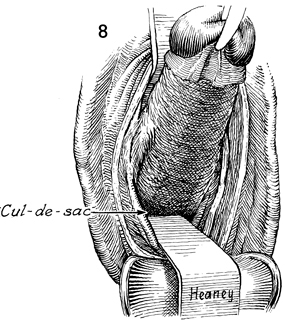
รูปที่ 8 แสดงการวาง right angle retractor ที่ anterior vaginal wall
รูปที่ 9 แสดงการตัด anterior cul-de-sac
รูปที่ 10 แสดงการวาง Heaney retractor ใน anterior peritoneum cavity
Hysterectomy
ที่นิยมทำคือ Heaney technique โดยเริ่มจากการตัดแล้วผูก uterosacral ligament ไปจนถึง utero-ovarian ligament แล้วดึงมดลูกออก อีกวิธีเรียกว่า Döderlein-Krönig technique ซึ่งไม่เป็นที่นิยม โดยทำการเปิดช่องท้องด้านหน้าอย่างเดียว แล้วดึงมดลูกส่วน fundus ออกทางช่องคลอด แล้วตัด vascular pedicle ขั้นตอนเหมือนการตัดมดลูกผ่านช่องท้อง (total abdominal hysterectomy) ซึ่งมีข้อดีคืออัตราการสูญเสียเลือดน้อยกว่า Heaney technique15
เทคนิคการตัดแล้วผูก คือ ใช้ clamp หนีบบริเวณที่ต้องการ โดยอาจใช้ 1 ตัวหรือ 2 ตัวก็ได้ จากนั้นใช้กรรไกร mayo หรือ metzenbaum ตัดโดยเหลือเนื้อเยื่อประมาณ 0.5 เซนติเมตรใต้ต่อ clamp แล้วเย็บผูกโดยวิธี transfixation suture หรือ ligation suture แล้วแต่ตำแหน่งที่ตัด นอกจากนี้ยังสามารถใช้เครื่องจี้คลื่นความถี่วิทยุ (radiofrequency bipolar vessel-sealing) หรือที่รู้จักโดยทั่วไปว่า LigaSure แทนได้ มีผลลัพธ์ไม่แตกต่างกัน
- Uterosacral ligament ดึงปากมดลูกไปด้านหน้าเบ้ออกด้านตรงข้ามกับด้านที่ต้องการตัด ใช้ clamp หนีบ uterosacral ligament ซึ่งอยู่ด้านหน้าต่อ rectocervical fold โดยหนีบให้ชิดการปากมดลูกเพื่อป้องกันการบาดเจ็บของท่อไต จากนั้นตัดแล้วเย็บผูกด้วย transfixation suture โดยยึดกับผนังช่องคลอดด้านข้าง หรือ double ligation แล้วเหลือปลายไหมไว้ใช้ดึงเพื่อให้ผ่าตัดง่ายขึ้นหรือทำหัตถการ suspension
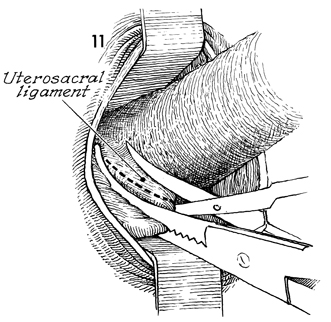
รูปที่ 11 แสดงการหนีบและตัด uterosacral ligament
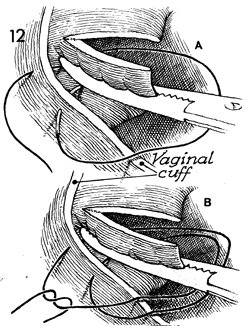
รูปที่ 12 แสดงการเย็บ transfixation suture
- Cardinal ligament หลังจากเย็บผูก Uterosacral ligament แล้ว เหนือจากนั้นจะเห็น cardinal ligament ที่อยู่ใกล้กับ lower uterine segment ใช้ clamp หนีบ ตัดและเย็บผูก ligation suture ไม่ใช้วิธี transfixtion suture เพราะเพิ่มโอกาสเกิด hematoma ได้
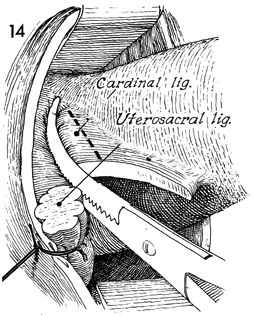
รูปที่ 13 แสดงการหนีบและตัด cardinal ligament
รูปที่ 14 แสดงการเย็บ ligation suture
- Uterine vessel และ Broad ligament uterine artery ทอดผ่านใน Broad ligament ตอนดึงปากมดลูกต้องใช้ความระมัดระวังเพราะเป็นส่วนที่เลือดออกได้ง่าย ใช้ clamp 1 ตัวหนีบชิดกับ uterus ตัดแล้วเย็บผูกด้วย double ligation suture บางกรณีอาจใช้ clamp 2 ตัวหนีบก็ได้ (double clamp technique) แต่มีโอกาสบาดเจ็บท่อไตมากขึ้น
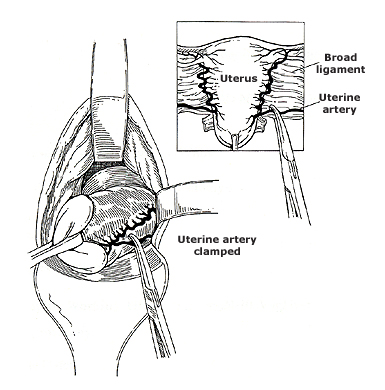
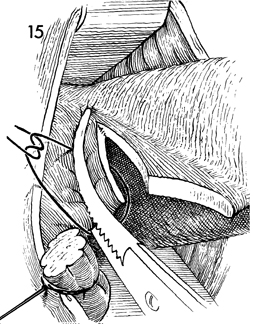
รูปที่ 15 แสดงตำแหน่ง uterine artery ใน broad ligament

รูปที่ 16 แสดงการหนีบและตัด broad ligament
- Utero-ovarian pedicle ดึงปากมดลูกและมดลูกเข้าหาตัว จะเห็น tubo-ovarian ligament, round ligament และ fallopian tube ใช้ double clamp หนีบบริเวณดังกล่าวชิดกับมดลูกบริเวณ fundus ตัดแล้วผูกสองครั้ง โดย technique ดังรูป ในบางรายที่ไม่สามารถ double clamp ได้ เช่น พื้นที่ไม่เพียงพอ บัง filed ผ่าตัด เป็นต้น อาจใช้ clamp ตัวเดียว แต่เย็บผูกสองครั้ง
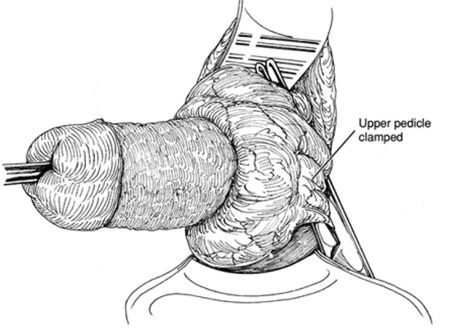
รูปที่ 17 แสดงการหนีบที่ utero-ovarian pedicle
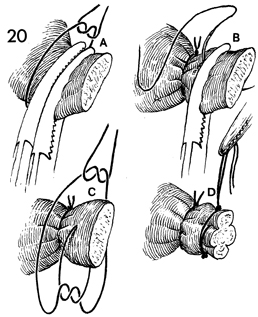
รูปที่ 18 แสดงการทำ double clamp และ double ligation
ในผู้ป่วยที่มดลูกขนาดเล็ก สามารถใช้เครื่องมือจับบริเวณด้านหลังมดลูกจนถึงส่วนยอดมดลูก เพื่อคลอดมดลูกออกทาง cul-de-sac ด้านหลัง แล้วเริ่มต้นขั้นตอนการหนีบ ตัดและผูก Utero-ovarian pedicle ดังกล่าวข้างต้น
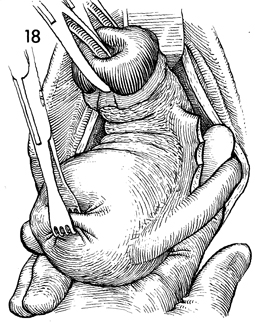
รูปที่ 19 แสดงการคลอดมดลูกส่วน fundus และวางมือในตำแหน่ง tubo-ovarian-round ligament
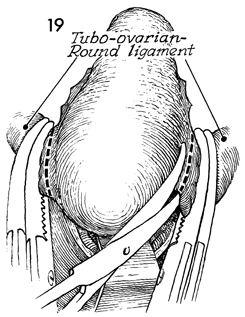
รูปที่ 20 แสดงการหนีบและตัด tubo-ovarian-round ligament (double clamp technique)
- Remove uterus หากมดลูกขนาดเล็กสามารถทำคลอดมดลูกได้เลย แต่ในรายที่มดลูกขนาดใหญ่ ต้องทำ uterine size reduction ซึ่งมีหลายวิธี ได้แก่ uterine morcellation, bivalve resection (hemisection), wedge resection และ myomectomy แต่ต้องมั่นใจว่าเป็น benign condition เนื่องจากว่าหากเป็น malignancy อาจทำให้มีการแพร่กระจายของมะเร็งในช่องท้อง
Adnexal surgery when indicate
สามารถทำ salpingo-oophorectomy ผ่านทางช่องคลอดได้ ทำหลังจากตัดมดลูกออกแล้วหรือทำพร้อมกันก็ได้ ในรายที่ตัดท่อนำไข่และรังไข่พร้อมมดลูก สามารถทำได้โดยหลังจากตัด Broad ligament แล้ว ให้หนีบ ตัดแล้วผูก ที่ round ligament ก่อน จากนั้นหา infundibulopelvic ligament และหนีบ ตัดแล้วผูกแบบเดียวที่ทำกับ utero-ovarian pedicle ในรายที่ไม่สามารถ identified ปีกมดลูก ได้ หรือประเมินแล้วการทำ salpingo-oophorectomy ทำได้ยาก เช่น การหย่อนของอุ้งเชิงกรานตาม Pelvic Organ Prolapse Quantification System (POP–Q) Stage 0-II อาจใช้การส่องกล้องมาช่วยผ่าตัดต่อไป
Apical support procedures when indicated แล้วแต่ชนิดและความรุนแรงของการหย่อน
Closure of the vaginal cuff
ก่อนทำการเย็บปิด ต้องตรวจจุดเลือดออกให้ดีทั้งส่วนของ pedicle ที่ตัดไปและขอบของช่องคลอด หากพบต้องทำการหยุดเลือดโดยการจี้ไฟฟ้าหรือการเย็บผูกแล้วแต่ความเหมาะสม การเย็บปิด vaginal cuff มีหลายเทคนิค โดยอาจเย็บปิดทั้งหมดหรือเย็บให้มีรูเปิดก็ได้ หรืออาจมีการวาง mesh เพื่อป้องกันการหย่อนของ vaginal vault ด้วยก็ได้ ส่วนการจัดท่าผู้ป่วย แนะนำท่า trendelenburg จะลดการรบกวนของลำไส้
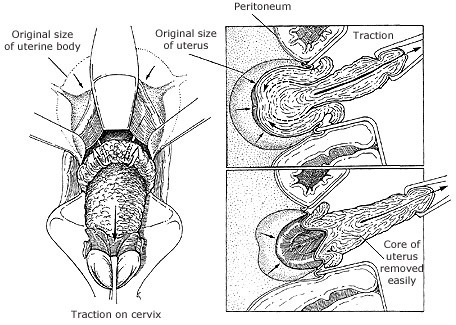
รูปที่ 21 แสดง uterine morcellation/coring
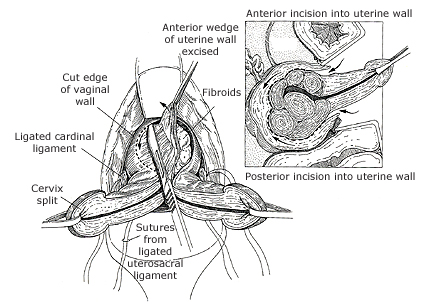
รูปที่ 22 แสดง bivalve resection (ซ้าย) myomectomy (ขวา)
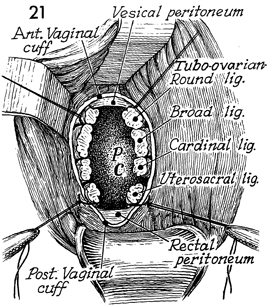
รูปที่ 23 vaginal cuff และ pedicles หลังตัดมดลูก
- การเย็บปิด vaginal cuff ทั้งหมด ใช้ absorbable material เย็บแบบ interrupted, continuous หรือ continuous locking ก็ได้ แนวเย็บแนวดิ่ง (vertical) สามารถรักษาความยาวช่องคลอดได้มากกว่าเย็บแนวขวาง (horizontal)
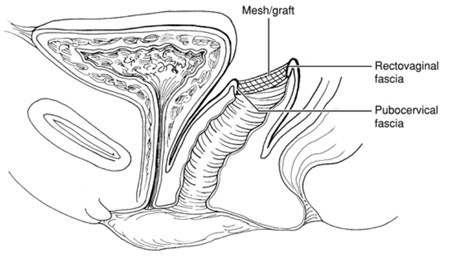
รูปที่ 24 แสดงการวาง mesh ที่ vaginal cuff หลังตัดมดลูก ด้านหน้าติดเย็บกับ pubocervical fascia ดันหลังเย็บติดกับ rectovaginal fascia
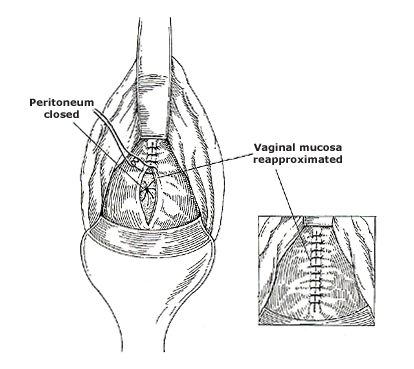
รูปที่ 25 การเย็บปิด vaginal cuff ในแนว vertical
- การเย็บแบบมีรูเปิด เพื่อระบายเลือดหรือน้ำในช่องท้อง เพื่อป้องกันการเกิดฝีหนอง ขั้นตอนแรกคือ reperitonealization เป็นการเย็บบริเวณ peritoneum และ pedicle ด้วย pursestring suture เริ่มจากเย็บขอบ peritoneum ที่ 12 นาฬิกา ผ่าน tubo-ovarian pedicle จนถึง uterosacral ligament จากนั้นเย็บต่อจนถึง peritoneum ด้านหลัง แล้วเย็บด้านตรงข้ามจาก uterosacral ligament จนถึง tubo-ovarian pedicle สิ้นสุดตำแหน่ง peritoneum ที่ 12 นาฬิกา จากนั้นดึงปลายไหมทั้งสองด้านและผูกเข้าด้วยกัน ขั้นตอนที่สองคือการเย็บขอบของช่องคลอด โดย continuous locking ซึ่งควรเย็บรวบ cardinal และ uterosacral ligament ด้วยเพื่อป้องกันการเกิด enterocele เย็บจนครบวงแล้วผูก ส่วนปลายไหมที่เย็บ suspension ระหว่าง uterosacral ligament กับ vaginal mucosae ในขั้นตอน hysterectomy ให้นำทั้งสองข้างมาผูกกันเพื่อป้องกันการเกิด enterocele เช่นกัน
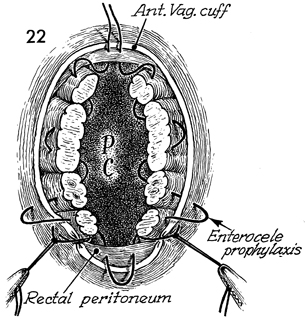
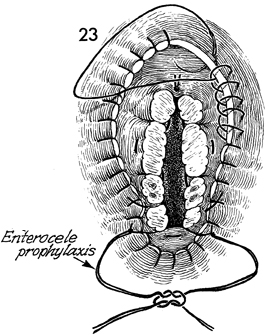
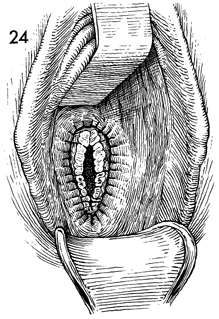
รูปที่ 26 การเย็บปิด vaginal cuff (ซ้าย)เย็บ pedicles ด้วย pursestring technique (กลาง)เย็บ continuous locking ที่ vaginal edge (ขวา)หลังเย็บเสร็จจะมีรูระบายสานน้ำในช่องท้อง
ภาวะแทรกซ้อนจากการผ่าตัด (Complications)
Intraoperative complications
- Hemorrhage
การเสียเลือดมากเกิดได้ไม่บ่อย ส่วนใหญ่เกิดได้ 2 กรณี คือ 1. เย็บ pedicle หลวม 2. การบาดเจ็บต่ออวัยวะภายใน ในกรณีที่เลือดออกจาก pedicle แล้วไม่สามารถห้ามเลือดได้ จำเป็นต้องใช้การส่องกล้องช่วยผ่าตัดต่อไป - Bladder injury/Ureter injury
Bladder injury เกิดได้ประมาณร้อยละ 2 พบบ่อยตอนการเปิด cul-de-sac ด้านหน้า ส่วน ureter injury พบได้น้อยกว่าร้อยละ 1 ซึ่งเป็นไปได้ทั้ง transection, crush หรือ anatomic distortion สำหรับในบางสถาบันแนะนำให้ routine cystoscopy16 เนื่องจากเพิ่ม intraoperative detection rate ของ urinary tract injuries ได้ - Bowel injury
หากเกิดขึ้นควรปรึกษาศัลยแพทย์เพื่อเย็บซ่อมแซม - Nerve injury
เกิดจากการจัดท่าไม่เหมาะสม อาจมีการกดทับเส้นประสาทได้ ทั้ง sciatic, peroneal และ femoral nerve
Postoperative complications
- Hematoma above the vaginal vault เกิดได้บ่อย มักไม่รุนแรง อาจทำให้เกิดอาการไข้ได้ แต่ในบางรายจำเป็นต้องผ่าตัดซ้ำเพื่อหยุดเลือด อย่างไรก็ตาม ไม่จำเป็นต้องทำคลื่นเสียงความถี่สูงหรือส่องกล้องช่องท้องหลังผ่าตัดทุกรายเพื่อวินิจฉัยภาวะดังกล่าว
- Fever พบได้บ่อย
- Bleeding อาจมีเลือดออกกะปริดกะปรอยทางช่องคลอดได้หลังผ่าตัด 1-2 สัปดาห์ แต่ถ้าหากมีเลือดออกมากหรือเป็นสีแดงสด ควรรีบหาสาเหตุ อาจเกิดจาก vaginal cuff dehiscent หรือ pedicle หลวมได้
- อื่น ๆ ได้แก่ vaginal cuff abscess/pelvic abscess, urinary retention, urinary incontinence, fistula, venous thromboembolism, Vaginal vault evisceration, Vault prolapse
เอกสารอ้างอิง
- Nieboer TE, Johnson N, Lethaby A, Tavender E, Curr E, Garry R, van Voorst S, Mol BW, Kluivers KB. Surgical approach to hysterectomy for benign gynaecological disease. Cochrane Database Syst Rev. 2009 Jul 8.
- Jitkunnatumkul A, Tantipalakorn C, Charoenkwan K, Srisomboon J. Subsequent Oophorectomy and Ovarian Cancer after Hysterectomy for Benign Gynecologic Conditions at Chiang Mai University Hospital. Asian Pac J Cancer Prev. 2016;17(8):3845-8.
- Berek, Jonathan S., E. Y. Adashi, Paula Adams Hillard, and Howard W. Jones. 1996. Novak’s gynecology. Baltimore: Williams & Wilkins.
- Sheth SS. Vaginal hysterectomy. Best Pract Res Clin Obstet Gynaecol. 2005 Jun;19(3):307-32
- Ingiulla C. Vaginal hysterectomy for the treatment of carcinoma endometrium. Am J Obstet Gynecol 1968; 100: 541–543.
- ACOG Committee Opinion No. 444: choosing the route of hysterectomy for benign disease. Obstet Gynecol. 2009 Nov;114(5):1156-8.
- Paparella P., Sizzi O., Rossetti A., et al: Vaginal hysterectomy in generally considered contraindications to vaginal surgery. Arch Gynecol Obstet 2004; 270: pp. 104-109.
- Stovall TG, Ling FW, Crawford DA. Hysterectomy for chronic pelvic pain of presumed uterine etiology. Obstet Gynecol 1990; 75:676
- Tohic AL, Dhainaut C, Yazbeck C, et al. Hysterectomy for benign uterine pathology among women without previous vaginal delivery. Obstet Gynecol 2008; 111:829.
- Sheth SS, Malpani AN. Vaginal hysterectomy following previous cesarean section. Int J Gynaecol Obstet 1995; 50:165.
- Thompson, John D., John A. Rock, Richard W. Te Linde, and Richard F. Mattingly. 1992. Te Linde’s operative gynecology. Philadelphia: Lippincott.
- ACOG Practice Bulletin No. 74. Antibiotic prophylaxis for gynecologic procedures. Obstet Gynecol. 2006 Jul;108(1):225-34.
- Clifford R. Wheeless, Jr., M.D. and Marcella L. Roenneburg, M.D. n.d. atlasofpelvicsurgery. Accessed january 2017.http://www.atlasofpelvicsurgery.com/5Uterus/9TotalVaginalHysterectomy/chap5sec9.html
- Lori R Berkowitz, MDCaroline E Foust-Wright, MD, MBA. n.d. UpToDate. Accessed january 2017.https://www.uptodate.com
- Paul F. KAMINSKI, Edward Podczaski. The Doderlein Vaginal Hysterectomy: A Useful Approach for the Neophyte Vaginal Surgeon. Journal of Gynecologic Surgery 6(2):123-128. 1990 January.
- Teeluckdharry B., Gilmour D., and Flowerdew G.: Urinary Tract Injury at Benign Gynecologic Surgery and the Role of Cystoscopy: A Systematic Review and Meta-analysis. Obstet Gynecol 2015; 126: pp. 1161-1169.

