โรคเบาหวานขณะตั้งครรภ์ (Gestational Diabetes Mellitus)
โรคเบาหวานขณะตั้งครรภ์ (Gestational Diabetes Mellitus)
นพ.ธรรมพจน์ จีรากรภาสวัฒน์
อาจารย์ที่ปรึกษา รศ.พญ.สุพัตรา ศิริโชติยะกุล
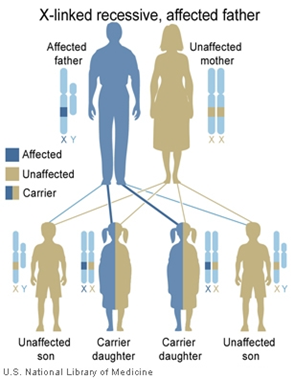
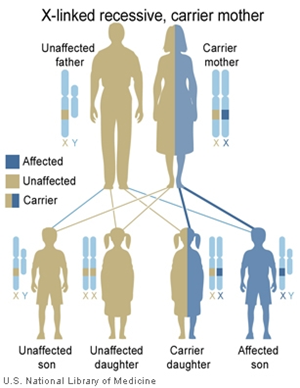
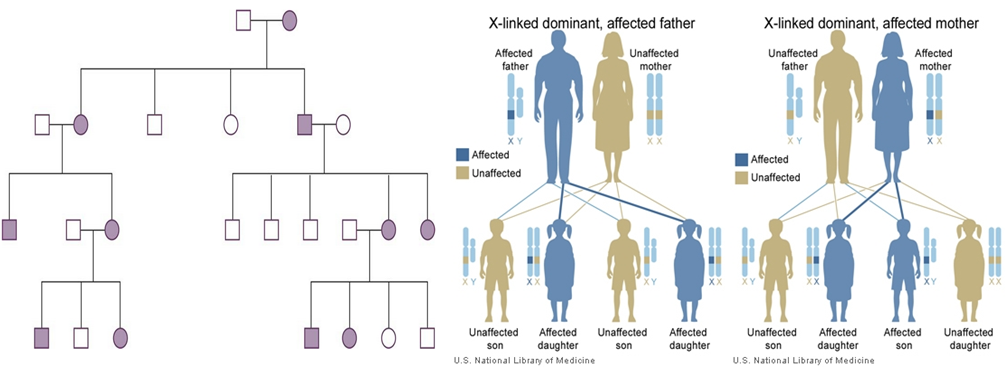
คือโรคเบาหวานที่วินิจฉัยขณะตั้งครรภ์ และจะหายไปภายหลังการคลอด ซึ่งเป็นภาวะแทรกซ้อนทางอายุรศาสตร์ที่ส่งผลกระทบต่อสตรีตั้งครรภ์และทารกในครรภ์ ความชุก (Prevalence) ประมาณร้อยละ 6 – 7 ในสตรีตั้งครรภ์(1) ซึ่งก่อให้เกิดภาวะแทรกซ้อนต่างๆ อาทิเช่น ภาวะความดันโลหิตสูงขณะตั้งครรภ์(Gestational hypertension), เพิ่มโอกาสคลอดทางหน้าท้องมากขึ้น (Caesarean delivery),ภาวะทารกตัวโต (Macrosomia), ภาวะคลอดติดไหล่ (Shoulder dystocia), เพิ่มอัตราตายปริกำเนิด (Perinatal death), ภาวะทารกน้ำตาลในเลือดต่ำภายหลังการคลอด (Neonatal hypoglycemia) เป็นต้น นอกจากนั้นในสตรีที่เป็นโรคเบาหวานขณะตั้งครรภ์ ยังเสี่ยงต่อการเกิดโรคเบาหวานในอนาคตเพิ่มขึ้นถึง 7เท่า และพบว่าร้อยละ 50จะเป็นโรคเบาหวานภายใน 22 – 28 ปีภายหลังการตั้งครรภ์และในด้านทารกเองยังเพิ่มความเสี่ยงของการเกิดโรคเบาหวานในอนาคตเพิ่มขึ้นด้วย (1)
สรีรวิทยาของการตั้งครรภ์ที่สัมพันธ์กับการเกิดโรคเบาหวานขณะตั้งครรภ์
ขณะตั้งครรภ์รกมีการสร้างฮอร์โมน human placental lactogen (hPL) ก่อให้เกิดภาวะดื้ออินซูลิน (insulin resistance) และเพิ่มการใช้พลังงานจากไขมัน เพื่อสงวนพลังงานจากน้ำตาลนั้นไว้ให้กับทารกในครรภ์ ส่งผลให้ในการตั้งครรภ์ปกตินั้นจะตรวจพบว่ามีภาวะfasting hypoglycemia และภาวะpostprandial hyperglycemia และภาวะhyperinsulinemia ซึ่งฮอร์โมน human placental lactogen จะเพิ่มปริมาณมากขึ้นเรื่อยๆ ตามอายุครรภ์และเพิ่มสูงในช่วงอายุครรภ์ 24 – 28 สัปดาห์และสูงสุดที่ช่วงอายุครรภ์ 34 – 36 สัปดาห์(2)
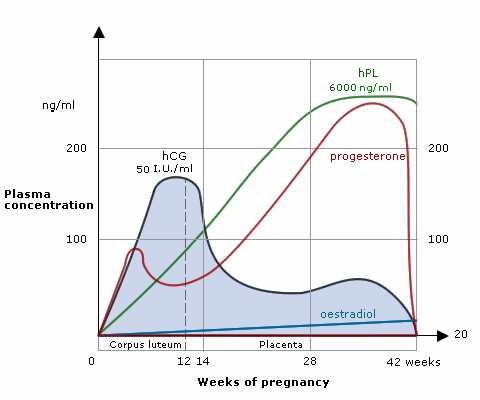
รูปที่ 1 แสดงระดับฮอร์โมน hPL(ที่มา :http://e-safe-anaesthesia.org/sessions/08_01/d/ANAE_Session/377/tab_566.html)
ผลของโรคเบาหวานต่อการตั้งครรภ์
ด้านสตรีตั้งครรภ์
- ภาวะความดันโลหิตสูงขณะตั้งครรภ์ (Gestational hypertension) หรือครรภ์เป็นพิษ (Preeclampsia)
- เพิ่มอัตราการคลอดทางหน้าท้อง (Caesarean delivery)
- เพิ่มความเสี่ยงการเป็นโรคเบาหวานในอนาคต
ด้านทารกในครรภ์
- ไม่เพิ่มโอกาสการเกิดทารกพิการในครรภ์ เมื่อเทียบกับสตรีที่เป็นโรคเบาหวานก่อนการตั้งครรภ์
- .หากควบคุมไม่ให้เกิดภาวะ postprandrial hyperglycemia ได้ จะสามารถลดอัตราการตายของทารกในครรภ์ได้
- หากระดับ fasting blood glucose > 105 mg/dl จะเพิ่มอัตราตายของทารกในครรภ์ ในช่วง 4 – 8สัปดาห์สุดท้ายก่อนคลอด(2)
- ภาวะทารกตัวโต (Macrosomia) เป็นภาวะที่พบบ่อยในสตรีที่เป็นโรคเบาหวานขณะตั้งครรภ์ ซึ่งเกิดจากระดับน้ำตาลในเลือดของมารดาที่สูงขึ้น ส่งผลให้เกิดภาวะอินซูลินเกิน (hyperinsulinemia) ทำให้เพิ่มอัตราการเจริญเติบโตของทารกในครรภ์ มีการสะสมของไขมันบริเวณไหล่และท้องของทารกในครรภ์ ซึ่งนำไปสู่ความเสี่ยงของการคลอดติดไหล่ที่สูงขึ้นรวมถึงการบาดเจ็บระหว่างการคลอด
- ภาวะทารกน้ำตาลในเลือดต่ำภายหลังการคลอด (Neonatal hypoglycemia) โดยพบว่าค่าระดับน้ำตาลกลูโคสในเลือด ต่ำกว่า 35 mg/และหากมีการต่ำของระดับน้ำตาลในเลือดของทารกอย่างฉับพลันนั้นเพิ่มโอกาสเนื้อเยื่อสมองถูกทำลาย จนเกิดภาวะ Cerebral palsy ได้(2)
การจำแนกประเภทของโรคเบาหวานขณะตั้งครรภ์
ในปี 1994American College of Obstetricians and Gynecologists (ACOG) : Management of Diabetes Mellitus in Pregnancy ยังมีการอ้างอิงถึงการจำแนกประเภทของโรคเบาหวานในสตรีตั้งครรภ์ตาม White Classification (1986 – 1994)ที่มีการจำแนกเป็นประเภท A1 และ A2 ตามระดับของ Fasting blood glucose ซึ่งภายหลังเป็นที่นิยมลดลง และใน ACOG Practice Bulletin ปี 2013ไม่ได้กล่าวถึงการจำแนกโรคเบาหวานในสตรีตั้งครรภ์ตาม White Classification แล้ว (1)
ในปัจจุบันมีการแนะนำให้จำแนกประเภทของโรคเบาหวานในสตรีตั้งครรภ์ตาม American Diabetes Association (ADA) ปี 2012ดังนี้ (3)
{tabulizer:style[gr.alterora.elemental_1_blue.css]}
| Gestational Diabetes : โรคเบาหวานที่ได้รับการวินิจฉัยระหว่างตั้งครรภ์ และไม่สามารถจำแนกได้ชัดเจนว่าเป็นโรคเบาหวานก่อนการตั้งครรภ์มาก่อนหรือไม่ | |
| Type I Diabetes : ซึ่งเกิดจากเซลล์เบตาในตับอ่อนถูกทำลาย มักพบว่ามีภาวะพร่องอินซูลินโดยสมบูรณ์ | Type II Diabetes : ซึ่งเกิดจากการหลั่งฮอร์โมนอินซูลินไม่เพียงพอ ร่วมกับมีภาวะดื้ออินซูลิน |
| a.ไม่มีภาวะแทรกซ้อนเกี่ยวกับหลอดเลือด | c.ไม่มีภาวะแทรกซ้อนเกี่ยวกับหลอดเลือด |
| b.มีภาวะแทรกซ้อนเกี่ยวกับหลอดเลือด | d.มีภาวะแทรกซ้อนเกี่ยวกับหลอดเลือด |
| Other type of diabetes : เกี่ยวกับพันธุกรรม, สัมพันธ์กับโรคของตับอ่อน, ผลจากยาหรือสารเคมี | |
ตารางที่ 1 : แสดงการจำแนกชนิดของโรคเบาหวานในสตรีตั้งครรภ์ตาม American Diabetes Association (ADA) ปี 2012
ทั้งนี้การวินิจฉัยโรคเบาหวานขณะตั้งครรภ์ เป็นไปเพื่อการเฝ้าระวังภาวะแทรกซ้อนทางสูติศาสตร์ระหว่างการฝากครรภ์และการดำเนินการคลอด ตลอดจนการติดตามเฝ้าระวังโอกาสการกลายเป็นโรคเบาหวานในอนาคต ทั้งในสตรีที่เคยได้รับการวินิจฉัยโรคเบาหวานขณะตั้งครรภ์และทารกในครรภ์นั้นๆด้วย
การคัดกรองและวินิจฉัยโรคเบาหวานขณะตั้งครรภ์ ในสตรีที่มารับการฝากครรภ์
- การคัดกรองโรคเบาหวานขณะตั้งครรภ์ในสตรีทุกรายที่มาฝากครรภ์สามารถทำได้ โดยแนะนำให้ทำการตรวจคัดกรองที่อายุครรภ์ 24 – 28 สัปดาห์ (universal screening) หรือ
- การประเมินความเสี่ยงต่อการเกิดโรคเบาหวานขณะตั้งครรภ์ในกลุ่มสตรีที่มาฝากครรภ์ ตั้งแต่ครั้งแรกที่เข้ารับการฝากครรภ์
a. แนวทางของ Fifth International Workshop-Conference on Gestational Diabetes : Recommended screening Strategy Based on Risk Assessment for Detecting Gestational Diabetes (ตารางที่ 2 )(2)
{tabulizer:style[gr.alterora.elemental_1_blue.css]}
| Low Risk :
ไม่จำเป็นต้องตรวจคัดกรองทุกราย หากมีความเสี่ยงต่ำต่อการเกิดโรคเบาหวานขณะตั้งครรภ์ครบทุกข้อ |
|
| Average Risk :
ตรวจคัดกรอง ที่อายุครรภ์ 24 – 28 สัปดาห์ |
|
| High Risk :
แนะนำให้คัดกรองเร็วที่สุด หากมีความเสี่ยงสูงต่อการเกิดโรคเบาหวานขณะตั้งครรภ์ตั้งแต่1ข้อขึ้นไปและหากไม่ได้รับการวินิจฉัยว่าเป็นโรคเบาหวานขณะตั้งครรภ์ ให้คัดกรองซ้ำอีกครั้ง ที่อายุครรภ์ 24 – 28 สัปดาห์ |
|
ตารางที่ 2 : แสดงการจำแนกกลุ่มความเสี่ยงของการเกิดโรคเบาหวานในขณะตั้งครรภ์ตามแนวทางของ Fifth International Workshop-Conference on Gestational Diabetes
b. แนวทางของหน่วยเวชศาสตร์มาดารและทารก คณะแพทยศาสตร์ มหาวิทยาลัยเชียงใหม่ (ตารางที่ 3)
{tabulizer:style[gr.alterora.elemental_1_blue.css]}
| ความเสี่ยง | แนวทางการคัดกรองและการตรวจวินิจฉัย | |
| กลุ่มความเสี่ยงสูง |
|
ตรวจคัดกรองด้วย 50 g GCT ทันทีโดยไม่คำนึงถึงอายุครรภ์
|
| กลุ่มความเสี่ยงปานกลาง |
|
ตรวจคัดกรองด้วย 50 g GCT ที่อายุครรภ์ 24 – 28 สัปดาห์ |
ตารางที่ 3 แสดงแนวทางการคัดกรองโรคเบาหวานขณะตั้งครรภ์ ของคณะแพทยศาสตร์ มหาวิทยาลัยเชียงใหม่
*BMI : Body mass index, FBS : Fasting Blood Sugar, 50 g GCT : 50 g Glucose Challenge Test, 100 g OGTT : 100 g Oral Glucose Tolerance Test
แนวทางการคัดกรองโรคเบาหวานขณะตั้งครรภ์
1.วิธีตรวจแบบ 1ขั้นตอน ( One – step)
- คัดกรองด้วยการทำ 75 g Oral Glucose Tolerance Test ( 75 g, 2 hours OGTT) ให้การวินิจฉัยโรคเบาหวานขณะตั้งครรภ์เมื่อค่าระดับน้ำตาลกลูโคสในเลือดค่าใดค่าหนึ่งมากกว่าหรือเท่ากับ (fasting value, 92 mg/dL; 1-hour value, 180 mg/dL; and 2-hour value, 153 mg/dL)
- ในปี 2010International Association of Diabetes and Pregnancy Study Group (IADPSG) ได้แนะนำการคัดกรองแบบ 1ขั้นตอนนี้ไว้ โดยอ้างอิงจากการศึกษาเรื่อง Hyperglycemia and Adverse Pregnancy Outcome study data ประกอบกับองค์การอนามัยโลก (WHO) ได้ปรับเปลี่ยนแนวทางการคัดกรองใหม่ในปี 2013ได้อ้างอิงเกณฑ์และแนวทางการคัดกรองจาก IADPSG(4) ซึ่งงานวิจัยต่อมาภายหลังพบว่าการคัดกรองด้วยเกณฑ์การวินิจฉัยนี้ทำให้อุบัติการณ์ของโรคเบาหวานขณะตั้งครรภ์สูงขึ้นอย่างมีนัยสำคัญทางสถิติ ซึ่ง ก่อให้เกิดคำถามเกี่ยวกับความคุ้มค่าในการรักษาพยาบาล ต่อมาACOG Practice Bulletin 2013 : Gestational Diabetes (1) แนะนำว่ายังต้องมีการศึกษาเพิ่มเติมต่อไปเนื่องจากยังไม่มีงานวิจัยในรูปแบบของ Randomized clinical trials (RCTs) ออกมารองรับ และล่าสุดจากการศึกษาของ R. Klara Feldman และคณะ(5)ที่ตีพิมพ์ในปี2016กล่าวว่าการตรวจคัดกรองโรคเบาหวานในขณะตั้งครรภ์ แบบ 1ขั้นตอนตามแนวทางของ IADPSG นั้นไม่ช่วยลดภาวะทารกตัวโต ทั้งยังเพิ่มอัตราการคลอดทางหน้าท้องอย่างมีนัยสำคัญทางสถิติ และไม่ให้การสนับสนุนการคัดกรองในแนวทางนี้อีกด้วย
2.วิธีตรวจแบบ 2 ขั้นตอน ( Two – step screening)
ขั้นตอนที่ 1:50g Glucose Challenge Test (50 g GCT)
เป็นการคัดกรองโรคเบาหวานขณะตั้งครรภ์ โดยเจาะเลือดหลังรับประทานน้ำตาลกลูโคส 50กรัม ที่ 1ชั่วโมง โดยไม่ต้องงดน้ำและอาหารก่อนการตรวจ หากผิดปกติให้ส่งตรวจเพิ่มเติมขั้นตอนที่ 2
ซึ่งการคัดกรองด้วย 50 g GCT นี้มีเกณฑ์การวัดผลที่หลากหลายตั้งแต่ 130, 135, และ 140 mg/dLซึ่งยังไม่มีข้อมูลจากงานวิจัยในรูปแบบ RCTs ออกมารองรับ แต่มีงานวิจัยรูปแบบ cohort study ที่ที่ให้ข้อมูลว่าการใช้เกณฑ์การวัดผล ที่ 140 mg/dLนั้นสามารถลดผลบวกลวง (False positive) ได้ ทั้งยังสามรถเพิ่มค่า positive predictive value เมื่อใช้เกณฑ์นี้คัดกรองในหลากหลายกลุ่มชาติพันธุ์ ทั้งยังช่วยลดค่าใช้จ่ายในการคัดกรองขั้นตอนที่ 2ด้วย 3 hours OGTT ที่ไม่จำเป็นได้อีกด้วย (1, 6) โดยสรุปทางด้าน ACOG Practice Bulletin 2013 ได้ให้ข้อแนะนำว่า การเลือกใช้เกณฑ์การวัดผลค่าใดค่าหนึ่งนั้น ให้พิจารณาจากความชุกของโรคเบาหวานขณะตั้งครรภ์ในพื้นที่นั้นๆเป็นสำคัญ(1)
ขั้นตอนที่ 2 : 100 g, 3 hours Oral Glucose Tolerance Test (100 g 3-h OGTT)
เป็นการตรวจเพิ่มเติมเพื่อการวินิจฉัยโรคเบาหวานขณะตั้งครรภ์ ในรายที่ 50 g GCT ผิดปกติ โดยแนะนำให้ผู้ป่วยงดน้ำและอาหารมาก่อนอย่างน้อย 8- 14ชั่วโมง แล้วเจาะเลือด Fasting blood sugar (FBS) แล้วจึงให้รับประทานน้ำตาลกลูโคส 100กรัม แล้วจึงเจาะเลือดซ้ำ ที่ 1, 2, และ 3 ชั่วโมงหลังรับประทาน โดยในปัจจุบันมีเกณฑ์วัดผลอยู่ 2เกณฑ์ คือ แนวทางของ Carpenter and Coustan และ แนวทางของ National Diabetes Data Group ดังตารางที่ 4และหากมีค่าผิดปกติตั้งแต่ 2ค่าขึ้นไปให้วินิจฉัยโรคเบาหวานขณะตั้งครรภ์
{tabulizer:style[gr.alterora.elemental_1_blue.css]}
| Plasma or serum glucose levelCarpenter and Coustan(mg/dL) | Plasma glucose levelNational Diabetes Data Group(mg/dL) | |
| Fasting | 95 | 105 |
| 1 – hour | 180 | 190 |
| 2 – hour | 155 | 165 |
| 3 –hour | 140 | 145 |
ตารางที่ 4:แสดงเกณฑ์การวินิจฉัยโรคเบาหวานขณะตั้งครรภ์
ซึ่งจากเกณฑ์การวัดผลค่าระดับน้ำตาลกลูโคสในพลาสมา ตามแนวทางของ Carpenter and Coustan นั้นมีค่าต่ำกว่า เกณฑ์วัดผลตามแนวทางของ National Diabetes Data Group ซึ่งทำให้อุบัติการณ์ของโรคเบาหวานขณะตั้งครรภ์สูงขึ้น และมีบางงานวิจัยรายงานว่า การอ้างอิงเกณฑ์วัดผลตามแนวทางของ Carpenter and Coustan นั้นเพิ่มอุบัติการณ์สูงกว่าค่าเฉลี่ยถึงร้อยละ 50ต่อมาในปี 2009Yvonne W. Chengและคณะ (7)ได้ทำการศึกษาเปรียบเทียบแบบย้อนหลัง เกี่ยวกับผลลัพธ์ของการคัดกรองโรคเบาหวานขณะตั้งครรภ์ โดยพิจารณาจากทั้งเกณฑ์ของ Carpenter and Coustan และ National Diabetes Data Group พบว่าสตรีตั้งครรภ์ที่ได้รับการวินิจฉัยโรคเบาหวานขณะตั้งครรภ์ตามเกณฑ์ของCarpenter and Coustanแต่ไม่ได้รับการวินิจฉัยตามเกณฑ์ของNational Diabetes Data Group มีความเสี่ยงสูงขึ้นต่อการใช้หัตถการช่วยคลอดทางช่องคลอด ภาวะทารกตัวโต ภาวะคลอดติดไหล่ อย่างมีนัยสำคัญทางสถิติ นอกจากนั้นตำรามาตรฐานทางสูติศาสตร์และเวชศาสตร์มารดาและทารกจะอ้างอิงตามแนวทางของ Carpenter and Coustan เป็นส่วนมาก(2, 8)แต่ทาง ACOG Practice Bulletin 2013 แนะนำว่าในโรงพยาบาลหนึ่งๆควรเลือกอ้างอิงเกณฑ์การวัดผลเพียงแนวทางเดียว โดยเลือกให้เหมาะสมกับ ความชุกของโรคเบาหวาน และกลุ่มประชากรในเขตพื้นที่ด้วย(1)
การเฝ้าระวังภาวะแทรกซ้อนจากโรคเบาหวานขณะตั้งครรภ์
สตรีตั้งครรภ์ที่ได้รับการวินิจฉัยโรคเบาหวานในขณะตั้งครรภ์ทุกราย ควรให้การรักษาด้วยการควบคุมอาหารทุกราย และมีการติดตามเจาะเลือดวัดค่าระดับน้ำตาลกลูโคสในเลือด ซึ่งเป็นตัวแปรสำคัญที่ก่อให้เกิดภาวะแทรกซ้อนจากโรคเบาหวานในขณะตั้งครรภ์
โดยหลักเกณฑ์ในการควบคุมระดับน้ำตาลกลูโคสในเลือดนั้นในการประชุม Fifth International Workshop-Conference on Gestational Diabetes in 2007แนะนำให้ (1, 2, 8)
- ค่า Fasting blood glucose น้อยกว่า 95 mg/dL
- ค่า 1 hour postprandial blood glucose น้อยกว่า 140 mg/dL
- ค่า2 hour postprandial blood glucose น้อยกว่า 120 mg/dL
โดยพบว่าค่า postprandial blood glucose ที่ควบคุมไม่ได้ตามเป้าหมาย ส่งผลให้เกิดภาวะแทรกซ้อนต่อสตรีตั้งครรภ์และทารกในครรภ์สูงขึ้นโดยมีรายงานว่าหากค่า 2 hour postprandial blood glucose มากกว่า 160 mg/dLเพิ่มอัตราการเกิดภาวะทารกตัวโต สูงขึ้นร้อยละ 35และมักเกิดขึ้นในช่วงอายุครรภ์ 29 – 32 สัปดาห์แต่อย่างไรก็ตามในรายที่สามารถควบคุมค่าระดับน้ำตาลกลูโคสในเลือดได้ตามเป้าหมาย ก็ยังมีโอกาสการเกิดภาวะทารกตัวโตได้เช่นกัน(8)
นอกจากนี้ในสตรีตั้งครรภ์ที่มีค่าเฉลี่ยระดับน้ำตาลกลูโคสในเลือดสูงกว่า 110 mg/dLนั้นส่งผลให้ค่าระดับ phosphatidylglycerolในน้ำคร่ำ ตรวจพบได้ล่าช้ากว่าอายุครรภ์ปกติที่ควรตรวจพบออกไป 1.5สัปดาห์ ส่งผลให้การพัฒนาของปอดทารกในครรภ์ล่าช้านานไปถึงอายุครรภ์ 39สัปดาห์ ซึ่งในรายที่ทารกคลอดก่อน อายุครรภ์ 39สัปดาห์มีความเสี่ยงของภาวะ Respiratory distress syndrome (RDS ) ได้มากกว่าสตรีที่ไม่เป็นโรคเบาหวานขณะตั้งครรภ์ (8)
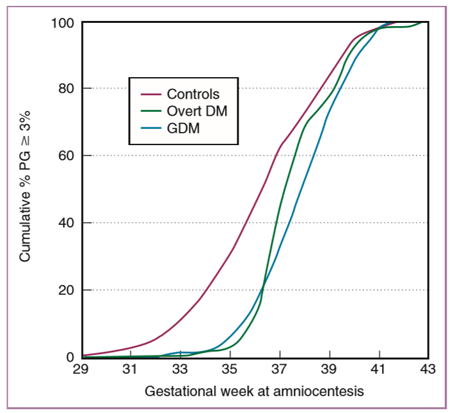
รูปที่ 2 แสดงภาวะ Delay in fetal pulmonary phosphatidylglycerol ที่ได้จาการเจาะตรวจน้ำคร่ำ ซึ่งระดับ phosphatidylglycerolเป็นค่าที่บ่งบอกการพัฒนาของปอดของทารกในครรภ์ เทียบกับอายุครรภ์ ใน 3กลุ่มตัวอย่าง(8, 9)
แนวทางการดูแลรักษาสตรีที่เป็นโรคเบาหวานขณะตั้งครรภ์
1. การควบคุมอาหาร (Diet control)
ในสตรีตั้งครรภ์ที่ได้รับการวินิจฉัยเป็นโรคเบาหวานขณะตั้งครรภ์ ควรได้รับการดูแลด้วยการควบคุมอาหารทุกราย หากมีโอกาสผู้ป่วยควรได้รับการแนะนำการควบคุมอาหารจากนักโภชนาการ โดยคำนวณจากค่าส่วนสูง น้ำหนัก และดัชนีมวลกาย (Body Mass Index,BMI) ก่อนการตั้งครรภ์
หลักการการควบคุมอาหาร อ้างอิงตามพยาธิกำเนิดที่ว่า ร่างกายจะหลั่งฮอร์โมนอินซูลินได้ไม่เพียงพอภายหลังการรับประทานอาหาร ดังนั้นควรปฏิบัติดังนี้(8)
- หลีกเลี่ยงอาหารมื้อใหญ่ มื้อเดี่ยวโดยควรแบ่งเป็น 3มื้อหลัก สลับมื้ออาหารว่าง 3มื้อ
- หลีกเลี่ยงการรับประทานอาหารจำพวกSimple carbohydrateเนื่องจากร่างกายจะดูดซึมระดับน้ำตาลได้เร็วทำให้ ค่าระดับ postprandial blood glocseสูงขึ้นอย่างรวดเร็ว
- รับประทานอาหารที่ให้พลังงานจากกลุ่มโปรตีน ไขมัน หรือComplex carbohydrate โดย แบ่งสัดส่วนอาหารเป็น คาร์โบไฮเดรต : โปรตีน : ไขมัน เท่ากับ 40 : 20 : 40 (2)
- American Diabetes Association แนะนำการคำนวณพลังงานที่ควรได้รับจาก ดัชนีมวลกาย (BMI) ก่อนการตั้งครรภ์(3)
- น้ำหนักปกติ BMI 20-25 kg/m2 30 kcal/kg
- น้ำหนักเกิน BMI > 24-34 kg/m2 25 kcal/kg
- ภาวะอ้วน BMI > 34 kg/m2 20 kcal/kg
– แนะนำให้รับประทานอาหารว่างมื้อก่อนนอน ซึ่งควรมีส่วนประกอบของ Complex carbohydrate อย่างน้อย 25มิลลิกรัมเพื่อหลีกเลี่ยงภาวะน้ำตาลในเลือดต่ำขณะนอนหลับ (Nocturnal hypoglycemia) โดยเฉพาะในรายที่ได้รับการรักษาด้วยอินซูลิน
2. การควบคุมการเพิ่มของน้ำหนัก ( Weight gain)
ในปี 2009 องค์กร Institute of Medicine (IOM) ได้ปรับปรุงเป้าหมายช่วงน้ำหนักที่แนะนำให้เพิ่มขึ้นในระหว่างการตั้งครรภ์ ตามค่าดัชนีมวลกายจากงานวิจัยของ Cheng และคณะ(10)โดยพบว่าหากน้ำหนักเพิ่มขึ้นมากกว่าค่าแนะนำของ IOM เพิ่มความเสี่ยงภาวะทารกตัวโตและเพิ่มอัตราการคลอดทางหน้าท้อง อย่างมีนัยสำคัญทางสถิติ
{tabulizer:style[gr.alterora.elemental_1_blue.css]}
| BMI (kg/m2) | ช่วงน้ำหนักที่เพิ่มขึ้น(kg) | อัตราการเพิ่มขึ้นของน้ำหนักในช่วงไตรมาสที่ 2และ 3(kg/wk) | |
| น้ำหนักต่ำกว่าเกณฑ์ | < 18.5 | 12.7 – 18.0 | 0.5 (0.5 – 0.6) |
| น้ำหนักปกติ | 18.5 – 24.9 | 11.3 – 15.8 | 0.5 (0.4 – 0.5) |
| น้ำหนักเกิน | 25.0 – 29.9 | 6.8 – 11.3 | 0.27 (0.2 – 0.3) |
| อ้วน | > 30 | 5.0 – 9.0 | 0.22 (0.2 – 0.3) |
ตารางที่ 5 แสดงช่วงน้ำหนักที่แนะนำให้เพิ่มขึ้นในระหว่างการตั้งครรภ์ ตามค่าดัชนีมวลกายก่อนการตั้งครรภ์ (11)
3. การให้การรักษาด้วยยาเพื่อควบคุมระดับน้ำตาลในเลือด
ตามปกติทารกในครรภ์จะมีอัตราความเร็วในการเจริญเติบโต (growth velocity) และการสะสม
ไขมันสูงที่ชุดในช่วงอายุครรภ์ 28 – 34 สัปดาห์ ซึ่งหากสตรีตั้งครรภ์ที่ได้รับการวินิจฉัยว่าเป็นโรคเบาหวานขณะตั้งครรภ์ และได้รับการรักษาด้วยการควบคุมอาหาร แต่ตรวจวัดค่าระดับน้ำตาลในเลือดยังไม่เป็นตามเป้าหมาย ดังที่กล่าวข้างต้นมาแล้ว แพทย์ไม่ควรพิจารณาล่าช้าในเริ่มการรักษาด้วยฮอร์โมนอินซูลินหรือยาลดระดับน้ำตาลในเลือด จากงานวิจัยของ McFarland และคณะ(12)พบว่าร้อยละ 50 ของผู้ป่วยที่ได้รับการควบคุมอาหาร จะสามารถควบคุมระดับตาลในเลือดได้ตามเป้าหมาย ภายใน 2สัปดาห์แรก และติดตามต่อไปครบสัปดาห์ที่ 4จะพบเพียงร้อยละ 10ของผู้ป่วยที่ควบคุมอาหารจนสามารถควบคุมระดับน้ำตาลในเลือดได้ตามเป้าหมาย
พิจารณาเริ่มการรักษาด้วยฮอร์โมนอินซูลินเป็นอันดับแรก เนื่องจากอินซูลินไม่ถ่ายทอดผ่านรกไปสู่ทารกในครรภ์ โดยทั่วไปเริ่มให้ Short acting insulin ที่ 0.7 – 1.0 units/kg/day โดยแบ่งมื้อให้ฉีดก่อนอาหารเช้า และเย็น ในบางรายอาจพิจารณาให้ Intermediate acting insulin ร่วมด้วยเพื่อเพิ่มประสิทธิภาพในการควบคุมระดับ Fasting blood glucose โดยแนะนำให้ฉีดช่วงเวลา 22.00 – 23.00 น.(1, 2)นอกจากนั้นชนิดของอินซูลินยังมีผลต่อการควบคุมระดับน้ำตาลในเลือด พบว่า Insulin aspartและ Insulin lisproระยะเวลาในการเริ่มออกฤทธิ์เร็วกว่า regular insulin ในทางทฤษฎีเชื่อว่าสามารถควบคุมระดับ Postprandial blood glucose ได้ดีกว่า (2)
ส่วนการให้การรักษาด้วยยาลดระดับน้ำตาลในเลือดชนิดรับประทาน มีรายงานการศึกษาวิจัยทั้งในรูปแบบของ RCTs และ systematic review พบว่าประสิทธิภาพในการควบคุมระดับน้ำตาลในเลือดให้ได้ตามเป้าหมายเทียบเท่าการฉีดอินซูนลิน และไม่มีหลักฐานที่บ่งชี้ถึงการเพิ่มขึ้นของภาวะแทรกซ้อนต่อมารดาและทารกในครรภ์ แต่รายงานวิจัยของ Moore และคณะ(2)พบว่า การรับประทานยาลดระดับน้ำตาลในเลือดเพียงอย่างเดียว ไม่สามารถควบคุมคุมระดับน้ำตาลในเลือดได้ตามเป้าหมาย และจำเป็นต้องเพิ่มการฉีดอินซูลินร่วมด้วย
โดยมียาลดระดับน้ำตาลในเลือดชนิดรับประทาน2กลุ่มที่มีการศึกษาวิจัย และนิยมใช้ในการรักษาสตรีตั้งครรภ์ที่เป็นโรคเบาหวานขณะตั้งครรภ์ แม้ว่าองค์กรFood and Drug Administration (FDA) ของสหรัฐอเมริกายังไม่ได้รับรองการใช้ยานี้ คือ
- Metforminแนะนำให้เริ่มที่ 500 mg ทุก 12ชั่วโมง และสามารถปรับเพิ่มได้สูงสุด 2500 mg ต่อวัน (8)
- Glyburideแนะนำให้เริ่มที่ 5 mg รับประทานก่อนอาหาร 30 – 60 นาที โดยให้รับประทานสูงสุดไม่เกิน 20 mg ต่อวัน และไม่ควรให้เกินกว่า 7.5 mg ต่อมื้อเพราะอาจทำให้เกิดภาวะน้ำตาลในเลือดต่ำได้(8)
แนวทางการติดตามสุขภาพทารกในครรภ์และประเมินช่วงเวลาการคลอดและช่องทางการคลอด
1.การติดตามสุขภาพทารกในครรภ์ (Fetal surveillance)
- เป้าหมายเพื่อป้องกันภาวะทารกตายปริกำเนิด ภาวะทารกขาดออกซิเจนขณะคลอด รวมถึงการประเมินโอกาสการคลอดทางช่องคลอดได้อย่างปลอดภัย ในช่วงไตรมาสที่ 3
- แนะนำให้เริ่มติดตามสุขภาพทารกในครรภ์ดังนี้(8)
- อายุครรภ์ 28 สัปดาห์ให้เริ่มนัดลูกดิ้น (Fetal movement count) และตรวจประเมินน้ำหนักทารกในครรภ์ด้วยคลื่นเสียงความถี่สูงตามข้อบ่งชี้
- ในรายที่ควบคุมระดับน้ำตาลในเลือดไม่ได้ตามเป้าหมายควรได้รับการติดตามสุขภาพทารกในครรภ์ด้วยการตรวจ Non stress test (NST) 1 – 2 ครั้งต่อสัปดาห์ตั้งแต่อายุครรภ์ 28สัปดาห์ หรือพิจารณาเป็นการตรวจ Contraction stress test (CST) หรือ Biophysical profile เป็นรายๆไป
- ในรายที่ควบคุมระดับน้ำตาลในเลือดได้ตามเป้าหมาย พิจารณาตรวจ NST 1- 2 ครั้งต่อสัปดาห์ โดยเริ่มที่อายุครรภ์ 34 – 36 สัปดาห์
2.การประเมินน้ำหนักทารกในครรภ์ ก่อนคลอด
ตาม ACOG Practice Bulletin 2013 แนะนำให้ทำคลอดทางหน้าท้อง หากตรวจประเมินน้ำหนักทารกในครรภ์ด้วยคลื่นความถี่สูงแล้ว พบว่าน้ำหนักมากกว่า 4,500กรัม เพื่อลดความเสี่ยงการคลอดติดไหล่ การบาดเจ็บของเส้นประสาท brachial plexus (1)
แนวทางการดูแลรักษาหลังคลอด
1. ด้านสตรีตั้งครรภ์
- งดการให้ยาฉีดอินซูลิน หรือยาลดระดับน้ำตาลในเลือดหลังคลอด แนะนำให้เจาะตรวจติดตามระดับน้ำตาลในเลือดเป็นระยะ ในช่วง 1 – 3 วันแรกหลังคลอด
- ตรวจคัดกรองโรคเบาหวานด้วยการตรวจ 75 g OGTT ภายหลังการคลอด 6 – 12 สัปดาห์
- การแปลผล ตาม American Diabetes Association 2013 ดังนี้
{tabulizer:style[gr.alterora.elemental_1_blue.css]}
| ค่าปกติ(mg/dL) | Impaired Glucose Tolerance (mg/dL) | เบาหวาน(mg/dL) | |
| Fasting | < 100 | 100 – 125 | ≥ 126 |
| 2 hours | < 140 | 140 -199 | ≥ 200 |
- หากผลการคัดกรองปกติ ให้เฝ้าระวังการเกิดโรคเบาหวานในอนาคต ด้วยการตรวจติดตาม ตามแนวทางของ Fifth International Workshop-Conference ดังนี้
{tabulizer:style[gr.alterora.elemental_1_blue.css]}
| ช่วงเวลาในการตรวจติดตาม | วิธีการตรวจ |
| หลังคลอด 1- 3 วัน | Fasting / Random blood glucose |
| หลังคลอด 6 – 12 สัปดาห์ | 75 g, 2 hour OGTT |
| หลังคลอด 1 ปี | 75 g, 2 hour OGTT |
| ทุก 1ปี | Fasting blood glucose |
| ทุก 3ปี | 75 g, 2 hour OGTT |
2. ด้านทารกแรกเกิด
ควรได้รับการติดตามระดับน้ำตาลกลูโคสในเลือด เนื่องจากมีความเสี่ยงต่อภาวะน้ำตาลในเลือดต่ำนำไปสู่อาการชัก ภาวะสมองถูกทำลาย และเสียชีวิตได้
เอกสารอ้างอิง
- Obstetricians ACo, Gynecologists. ACOG practice bulletin no. 137: gestational diabetes. Obstet Gynecol. 2013;122:406-16.
- Cunningham FG. Williams Obstetrics 24th edition McGraw-Hill Education. Diabetes Mellitus: Medical; 2014.
- Association AD. Executive summary: Standards of medical care in diabetes–2012. Diabetes care. 2012;35:S4.
- Organization WH. Diagnostic criteria and classification of hyperglycaemia first detected in pregnancy. 2013.
- Feldman RK, Tieu RS, Yasumura L. Gestational diabetes screening: the international association of the diabetes and pregnancy study groups compared with Carpenter-Coustan screening. Obstetrics & Gynecology. 2016;127(1):10-7.
- Esakoff TF, Cheng YW, Caughey AB. Screening for gestational diabetes: different cut-offs for different ethnicities? American journal of obstetrics and gynecology. 2005;193(3):1040-4.
- Cheng YW, Block-Kurbisch I, Caughey AB. Carpenter-Coustan criteria compared with the national diabetes data group thresholds for gestational diabetes mellitus. Obstetrics & Gynecology. 2009;114(2, Part 1):326-32.
- Creasy RK, Resnik R, Iams JD, Lockwood CJ, Greene MF, Moore TR. Creasy and Resnik’s maternal-fetal medicine: principles and practice: Elsevier Health Sciences; 2013.
- Moore TR. A comparison of amniotic fluid fetal pulmonary phospholipids in normal and diabetic pregnancy. American journal of obstetrics and gynecology. 2002;186(4):641-50.
- Cheng YW, Chung JH, Kurbisch-Block I, Inturrisi M, Shafer S, Caughey AB. Gestational weight gain and gestational diabetes mellitus: perinatal outcomes. Obstetrics & Gynecology. 2008;112(5):1015-22.
- Pregnancy WGD. Reexamining the Guidelines. Institute of Medicine (US) and National Research Council (US) Committee to Reexamine IOM Pregnancy Weight Guidelines; Rasmussen KM, Yaktine AL, eds. Rasmussen KM, Yaktine AL. 2009.
- McFarland MB, Langer O, Conway DL, Berkus MD. Dietary therapy for gestational diabetes: how long is long enough? Obstetrics & Gynecology. 1999;93(6):978-82.