Stress urinary incontinence in menopause
พญ.เพ็ญพรรณ บุตรชัยงาม
อาจารย์ที่ปรึกษา ผศ.นพ.ชัยเลิศ พงษ์นริศร
บทนำ
วัยทองเป็นวัยที่มีการเสื่อมถอยอย่างมากในกระบวนการทางกายภาพ การเปลี่ยนแปลงนี้เกิดขึ้นกับอวัยวะทุกระบบ รวมถึงระบบขับถ่ายปัสสาวะ(Urogenital system)(1) อวัยวะเพศสตรีและทางเดินปัสสาวะส่วนล่าง เจริญมาจากต้นกำเนิดทาง embryology เดียวกันคือ urogenital sinus ซึ่งจะเจริญต่อมาเป็น vagina, urethra, bladder และ pelvic floor อวัยวะทั้งหมดนี้มี estrogen receptor อยู่มากมาย(1-4) การเจริญและความสมบูรณ์ของอวัยวะเหล่านี้ต้องอาศัยฮอร์โมน estrogen พบว่าในส่วนของ lower urinary organs มีการเปลี่ยนแปลง cytological และ urodynamic ในแต่ละช่วงของวงรอบประจำเดือน การตั้งครรภ์ และหลังจากหมดประจำเดือนเช่นเดียวกับมดลูก ปากมดลูก และช่องคลอดด้วย(4)
หลังจาก menopause ระดับของ estrogen ในกระแสเลือดจะลดต่ำลงอย่างรวดเร็ว แต่กว่าจะมีผลต่อการเปลี่ยนแปลงของ urogenital function ต่อเมื่อระดับของ estrogen ลดลงอย่างมากซึ่งกินเวลา 4-5 ปีขึ้นไป คือช่วงอายุ 55-65 ปี(4, 5) การเปลี่ยนแปลงของช่องคลอดจะเห็นได้ก่อนและมีอาการชัดเจนกว่า จากนั้นจึงเห็นการเปลี่ยนแปลงและอาการของกระเพาะปัสสาวะ และท่อปัสสาวะ(4) อาการที่พบบ่อยของ urogenital tract ใน menopause ได้แก่ อาการปัสสาวะแสบ ขัด ปัสสาวะลำบาก อาการทางเดินปัสสาวะอักเสบบ่อย กลุ่มอาการปัสสาวะเล็ด (Urinary Incontinence) คันปากช่องคลอด ช่องคลอดอักเสบบ่อย ๆ มีอาการเจ็บจากมีเพศสัมพันธ์ (1, 4, 6)
มีการศึกษาพบความสัมพันธ์ระหว่างภาวะวัยหมดประจำเดือนและ Stress Urinary Incontinence อย่างชัดเจน(7) ซึ่งการปัสสาวะเล็ดราด ขณะออกแรงหรือไอ จาม (Stress Urinary Incontinence) เข้าห้องน้ำไม่ทัน เป็นปัญหาก่อให้เกิดผลเสียต่อคุณภาพชีวิตของผู้ป่วย ไม่กล้าเดินทาง ไม่สามารถมีกิจกรรมนอกบ้าน สูญเสียความมั่นใจในการดําเนินกิจวัตรประจําวัน มีปัญหาทางสังคม นอกจากนั้นยังอาจจะเกิดปัญหาโรคแทรกซ้อนเช่น ผื่น ผิวหนังอักเสบ ทางเดินปัสสาวะอักเสบ(4, 8) การศึกษาผลกระทบต่อคุณภาพชีวิต ในผู้สูงอายุไทยพบว่า ผู้สูงอายุหญิงในช่วงวัยหมดประจําเดือนที่รับการติดตามในคลินิกวัยทองพบว่าผู้ป่วยกลุ่มนี้มีคุณภาพชีวิตที่เลวลงอย่างชัดเจน โดยเฉพาะผู้ที่มีสาเหตุ เนื่องจาก overactive bladder หรือเป็นทั้งจาก stress incontinence ร่วมกับ overactive bladder (9, 10)
ความหมาย
Urinary incontinence (UI) ตามนิยามของ International Continence Society (ICS) หมายถึง ภาวะที่มีปัสสาวะไหลเล็ดออกมาโดยควบคุมไม่ได้ ‘any involuntary leakage of urine’ (11, 12)
Stress urinary incontinence (SUI) หมายถึง ภาวะที่มีปัสสาวะเล็ดออกมาโดยควบคุมไม่ได้ขณะออกแรงเบ่ง ไอ หรือจาม ซึ่งเป็นอาการที่นำผู้ป่วยมาพบแพทย์มากที่สุด(12, 13) (ภาพที่ 1)
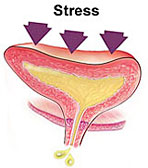
ภาพที่ 1 : แสดงการเกิด Stress urinary incontinence (ที่มา : www.mayoclinic.org)
ระบาดวิทยา
ความชุกของอาการปัสสาวะเล็ด (urinary incontinence) ในวัยทองแตกต่างกันไปจากการศึกษาแต่ละที่ เพราะมีมากรายที่มีอาการแต่ไม่ไปรับการรักษา ตัวเลขแต่ละที่จึงได้แตกต่างกัน (14) ในทวีปเอเชียความชุกของหญิงที่มี urinary incontinence อยู่ในช่วงร้อยละ 4 – 17 ความชุกในประเทศไทยร้อยละ 17 (15) ความชุกของ stress urinary incontinence ในหญิงไทยพบมากร้อยละ 41(16) ความชุกของภาวะปัสสาวะเล็ดในหญิงวัยหมดประจำเดือนของประเทศไทยจากรายงานของคลินิกวัยทองโรงพยาบาลศรีนครินทร์คณะแพทยศาสตร์มหาวิทยาลัยขอนแก่น พบร้อยละ 38.86 เป็น stress urinary incontinence ร้อยละ 12.36 ผลการศึกษานี้ยังพบว่าการคลอดทางช่องคลอด ภาวะหมดประจำเดือนก่อนอายุ 50 ปี และการไม่ได้รับฮอร์โมนรักษาในสตรีวัยหมดประจำเดือนเป็นปัจจัยที่ทำให้เพิ่มความเสี่ยงต่อการเกิดภาวะปัสสาวะเล็ด(17) และการศึกษาที่ในคลินิกวัยทอง ของโรงพยาบาลพระมงกุฎเกล้า พบความชุกของ urinary incontinence ร้อยละ 75.3 เป็น stress incontinence ร้อยละ 18.3 และพบว่าหญิงวัยหมดประจำเดือนมีเพียง 3.6% ที่เคยได้รักษาเรื่อง urinary incontinence(18)
สรีรวิทยาของการปัสสาวะ
การ control urinary storage และ voiding ของมนุษย์ค่อนข้างซับซ้อน เพราะเป็น interaction ระหว่าง autonomic , neurogenic , behavioral และระดับอื่น ๆ ซึ่งรวมถึงการ support ของ bladder outlet ด้วย(4) โดยทั่วไปแบ่งการทํางานของกระเพาะปัสสาวะ เป็น 3 ระยะคือ Filling/storage phase, Initiation phase และ Emptying/voiding phase โดยทั้ง 3 ระยะจะหมุนเวียนสลับกันไปเป็นวงจร (micturition cycle) ดังนี้(19)
Filling/storage phase
มีการกักเก็บปัสสาวะ ปริมาตรของกระเพาะปัสสาวะเพิ่มขึ้นเรื่อยๆโดยความดันภายในกระเพาะปัสสาวะไม่เปลี่ยนแปลง (normal compliance) จากความสามารถในการพองตัวเพิ่มขนาดของกระเพาะปัสสาวะ และมีการรับรู้ความรู้สึกเป็นปกติ Bladder neck และ sphincter ปิดสนิทแม้ว่าจะมีการเพิ่มขึ้นของความดันในช่องท้อง และไม่มีการบีบตัวของ detrusor muscle (involuntary contraction)
Initiation phase
เป็นระยะที่จะเปลี่ยนเป็น non-voiding stage หรือ micturition เมื่อความต้องการจะถ่ายปัสสาวะมีมากก็ยังสามารถห้ามการบีบตัวของกระเพาะปัสสาวะต่อไปได้โดยอยู่ภายใต้การควบคุมของสมอง ( voluntary) เมื่อถึงเวลา ท่าทาง และสถานที่ที่เหมาะสม จึงมีการเปลี่ยนแปลงแรงดันของกระเพาะปัสสาวะ
Emptying/voiding phase
มีการบีบตัวของกล้ามเนื้อเรียบที่ผนังของกระเพาะปัสสาวะอยางสัมพันธ์กัน โดยมีความแรงและระยะเวลาเพียงพอที่จะขับเอาน้ำปัสสาวะออกจากกระเพาะปัสสาวะ มีการคลายตัวของ sphincter สัมพันธ์กับการบีบตัวของกล้ามเนื้อเรียบของกระเพาะปัสสาวะ
การทํางานของกระเพาะปัสสาวะถูกควบคุมโดยระบบประสาทอัตโนมัติทั้ง sympathetic (Hypogastric nerve, T10-L2, predominate in storage phase) และ parasympathetic (pelvic nerve, S2-4, predominate in emptying phase) โดยมี micturition reflex center อยู่ที่ไขสันหลังระดับ S2-4 และ pontine micturition center จะควบคุมทําให้การบีบตัวของกระเพาะปัสสาวะและการคลายตัวของ sphincter สัมพันธ์กัน ระบบประสาท somatic (pudendal nerve, S2-4)จะควบคุม External urethral sphincter (voluntary) สัญญาณประสาทจากสมองจะสงลงมา inhibit micturition reflex เปรียบเหมือนสวิชเปิดปิดอนุญาตให้มีการปัสสาวะในสถานที่และเวลาที่เหมาะสม(20) (ภาพที่ 2)
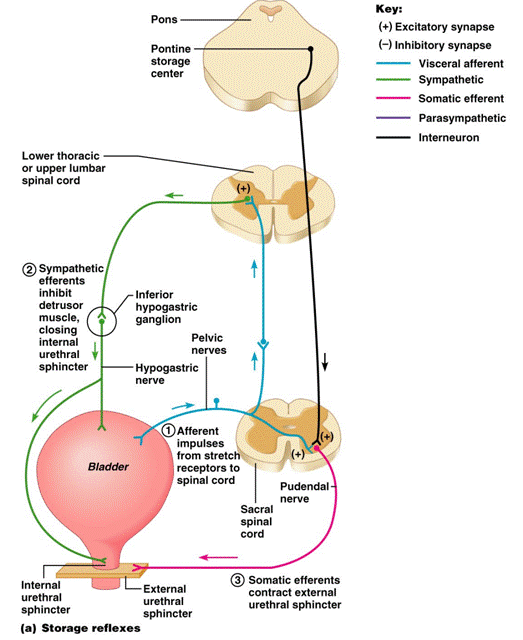
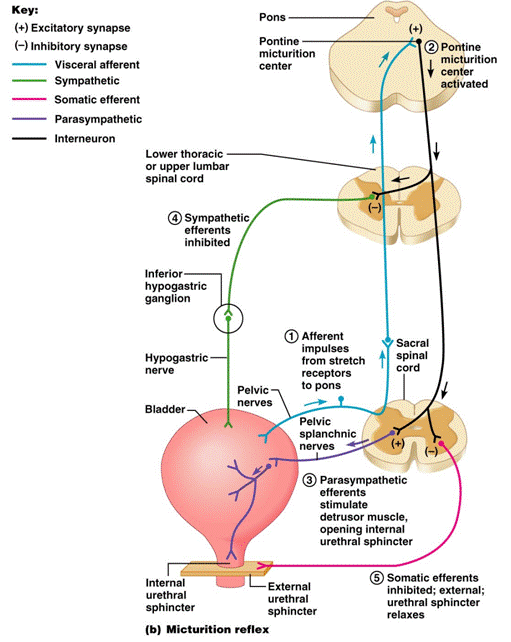
ภาพที่ 2 : แสดงการทํางานของกระเพาะปัสสาวะ
ที่มา http://classes.midlandstech.edu/carterp/Courses/bio211/chap25/chap25.htm
ทฤษฎีการเกิด Stress urinary incontinence
ในระยะเวลาที่ผ่านมามีหลายทฤษฎีที่พยายามอธิบายพยาธิสรีรวิทยาของการเกิด Stress urinary incontinence มีทฤษฎีที่ได้รับการยอมรับและนำมาประยุกต์ใช้ในการรักษา(20) ได้แก่
- 1.ALTERATIONS IN THE URETHROVESICAL AXIS
ปี ค.ศ.1913 Howard Kelly ทฤษฎีว่าการกลั้นปัสสาวะได้ Urethra ต้องมีตำแหน่งอยู่เหนือ Pelvic floor ทำให้แรงดันที่ Bladder เท่ากับที่ Urethra ซึ่ง Stress urinary incontinence เกิดจากความผิดปกติทางกายภาพมีภาวะกระบังลมหย่อนทำให้การพยุง และตำแหน่งของ Urethra เคลื่อนเปลี่ยนมากเกิน(Urethral hypermobility) จะเกิดการเปิดของ vesical neck เกิดปัสสาวะเล็ด(20-22) (ภาพที่ 3)
- 2.INTRINSIC SPHINCTER DEFICIENCY (ISD)
ปี ค.ศ.1976 Edward McGuire ได้เสนอทฤษฎีว่า Stress urinary incontinence (SUI) เกิดจากกล้ามเนื้อหูรูดท่อปัสสาวะอ่อนแรงเอง(Deficient sphincteric mechanism) โดยที่บริเวณ bladder neck และ proximal urethra มีการพยุงและอยู่ในตำแหน่งที่ปกติไม่มีการเลื่อนต่ำลง(23-25) (ภาพที่ 3,4)โดยระบบนี้สรุปว่า SUI ที่มี Valsalva leak-point pressure (VLPP) < 60 cmH2O น่าจะเกิดจาก Intrinsic sphincter deficiency (ISD) ถ้า VLPP > 90 cmH2O SUI น่าจะเกิดจากสาเหตุ anatomical มากกว่า ISD ถ้า SUI ในผู้ป่วยที่มีค่า VLPP 60 – 90 cmH2O น่าจะเกิดจากทั้ง anatomical defects และ ISD(26)
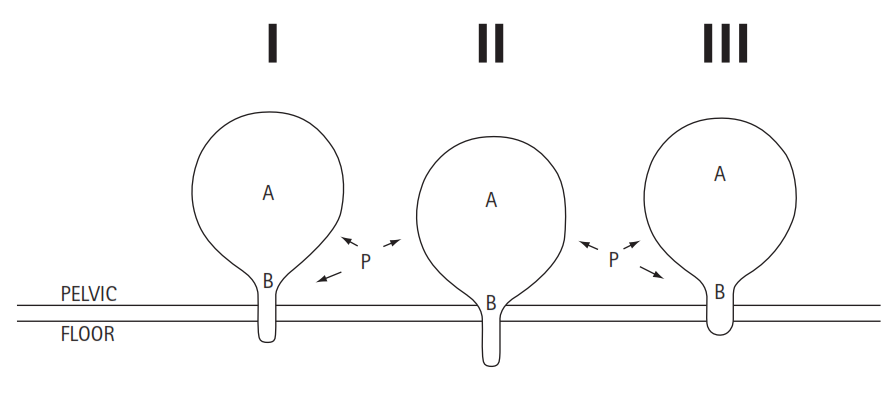
ภาพที่ 3 : แสดงทฤษฎี The Urethral Position. Increases in intra-abdominal pressure (p) จะส่งความดันไปที่ bladder neck และ proximal urethra ในรูป I หญิงปกติการเพิ่ม P จะส่งความดันไปเท่าๆกันที่บริเวณ bladder neck และ proximal urethra, ในรูป II Urethral hypermobility เมื่อเพิ่ม P ที่บริเวณ bladder neck และ proximal urethra ตำแหน่ง B จะเลื่อนต่ำลงและอยู่นอก abdominal cavity จะมีการกระจายของความดันไปที่ bladder neck และ proximal urethra อย่างไม่สมดุลทำให้เกิด SUI, ในรูป III Intrinsic sphincter deficiency (ISD) ที่บริเวณ bladder neck และ proximal urethra ตำแหน่ง B มีการพยุงที่ปกติไม่มีการเลื่อนต่ำลง แต่ bladder neck และ proximal urethra อ่อนแรงเอง( nonfunction) ทำให้เกิด SUI ที่มา : ดัดแปลงจากเอกสารประกอบที่ 20
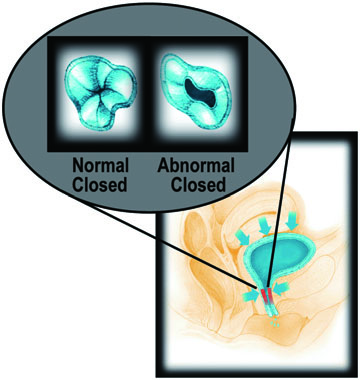
ภาพที่ 4 : แสดง Intrinsic sphincter deficiency (ISD), ท่อปัสสาวะ (urethra) อ่อนแรงไม่มีแรงต้านที่จะ กลั้นปัสสาวะได้
ที่มา : ดัดแปลงจากเอกสารประกอบที่ 20
- 3.HAMMOCK THEORY
ปี ค.ศ.1994, Dr John Delancey กล่าวถึงการสูญเสียความยืดหยุ่นแข็งแรงของพื้นที่รองรับท่อปัสสาวะ ซึ่งก็คือ Endopelvic fascia และ ผนังช่องคลอดด้านหน้า (Anterior vaginal wall) ที่ขึงติดกับ Arcus tendineus fascia และ levator ani muscle ทำให้เมื่อมีการเพิ่มขึ้นของแรงดันในช่องท้องกดทับลงบนท่อปัสสาวะที่วางอยู่บนพื้นรองรับที่นุ่มขาดแรงต้าน ท่อปัสสาวะก็ไม่มาสารถปิดได้อย่างสมบูรณ์ (27) (ภาพที่ 5,6)
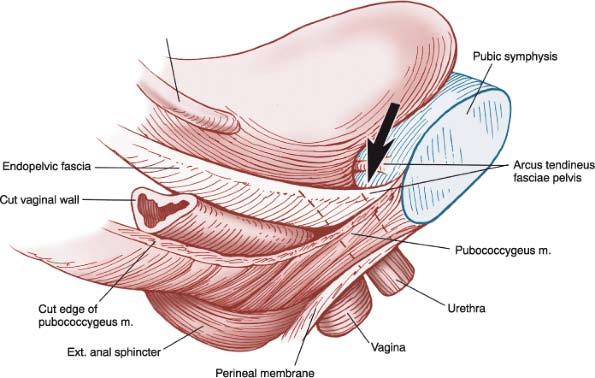
ภาพที่ 5 : แสดง The ‘hammock’ hypothesis, Urethra วางอยู่บน supportive layer ที่ประกอบด้วย endopelvic fascia และ anterior vaginal wall เมื่อมีแรงจากการไอหรือจามกดลง (ลูกศร) Urethra จะปิด ที่มา : เอกสารประกอบที่ 28 (28)
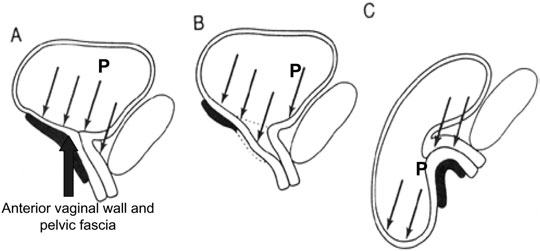
ภาพที่ 6 : แสดง The ‘hammock’ hypothesis. A, The anterior vaginal wall และ pelvic fascia ทำหน้าที่เป็น‘hammock’ กด Urethra เมื่อมีการเพิ่มขึ้นของ intra-bdominal pressure (P). B, ถ้าขาด ‘hammock’(เส้นประ) เมื่อมีการเพิ่มขึ้นของ intra-bdominal pressure (P)ทำให้เกิดSUI. C,แสดง ‘hammock’ support, จะทำให้เกิดcystourethrocele อย่างเดียวและไม่ทำให้มี SUI เมื่อมีการเพิ่มขึ้นของ intra-bdominal pressure (P) จะเพิ่ม urethral resistance. ที่มา : ดัดแปลงจากเอกสารประกอบที่ 20
- 4.INTEGRAL THEORY
ปี ค.ศ. 1990 Petros and Ulmsten เสนอทฤษฎีว่า Anterior vaginal wall หย่อนทำให้เกิดการกระตุ้น stretch receptors ที่ bladder neck และ proximal urethra ทำให้เกิด micturition reflex ที่ไม่สมบูรณ์เกิด detrusor overactivity และเกิด Stress urinary incontinence จากการกระจายของแรงปิดท่อปัสสาวะ (dissipation of urethral closure pressures) ในสภาวะปกติ anterior pubococcygeus muscle จะยก anterior vaginal wall ให้กดกับ urethra และ bladder neck จะถูกปิด การหย่อยตัวของ pubourethral ligament และ anterior vaginal wall ทำให้เกิด hypermobility ของ bladder neck และ dissipation of pressure ทำให้เกิด SUI(29)
- 5.THE TRAMPOLINE THEORY
ปี ค.ศ.2006 Firouz Daneshgari และ Courtenay Moore เสนอว่าสรีระวิทยาของการกลั้นปัสสาวะเกิดจากหลายปัจจัย Stress urinary incontinence (SUI) ก็เป็นผลจากหลายปัจจัยทั้งกายวิภาคและพยาธิสรีระวิทยา ‘complex anatomical and physiological’ ที่เป็นผลมาจากกลไกการควบคุมทั้ง central และ peripheral control ไม่สามารถอธิบายได้ด้วยทฤษฎีใดเพียงอย่างเดียว(20) (ภาพที่ 7)
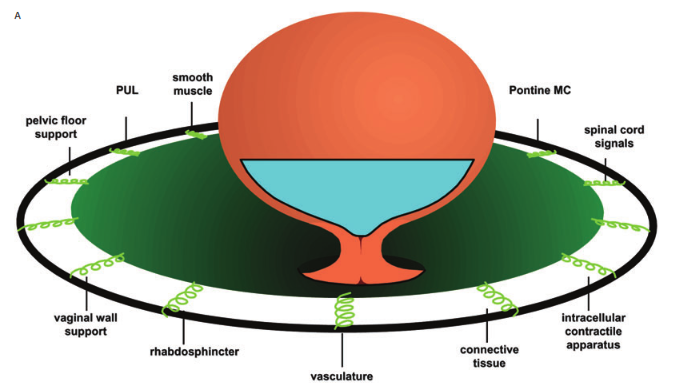
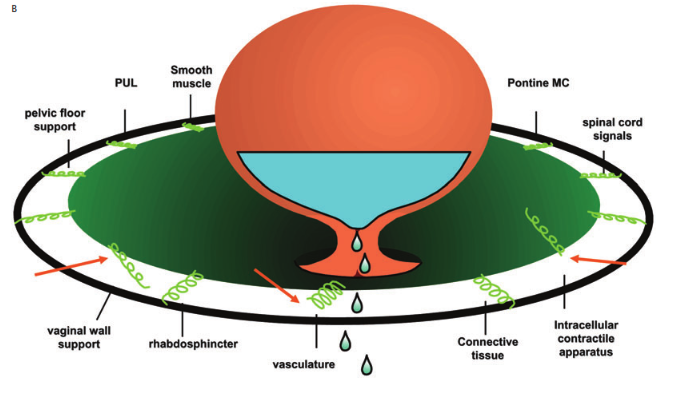
ภาพที่ 7 : แสดง The ‘Trampoline’ theory. A , Intact ‘trampoline’; ฐานทั้งหมดทำงานได้ดีจะไม่เกิด SUI.
B , การทำงานได้ไม่ดี( malfunction) ของหลายปัจจัยทำให้เกิด SUI ที่มา : ดัดแปลงจากเอกสารประกอบที่ 20
พยาธิสรีรวิทยาของการเกิด Stress urinary incontinence ในสตรีวัยหมดประจำเดือน
เมื่อ estrogen ลดลงจะมีการเปลี่ยนแปลงของ Urethra และ bladder มี epithelium แบบ transitional epithelium (ยกเว้นบริเวณใกล้ urethral orifice ซึ่งเป็น stratified epithelium เช่นเดียวกับ vagina) epithelium เหล่านี้มี estrogen receptor และมีการเปลี่ยนแปลงตามวงรอบของประจำเดือน เมื่อขาด estrogen ทำให้ mucosa ของ urethra และ periurethral tissue (ซึ่งเป็นกล้ามเนื้อ , connective tissue และเส้นเลือด) บางตัวลง ทำให้ mechanism การปิดของ urethra เสียไป ทำให้เกิด stress incontinence และ prolapse ของ urethral mucosa ที่ urethral meatus mucosa ของ bladder และตัว bladder เองก็บางลงเช่นกัน ความต้านทาน infection ลดลง ทำให้เกิดภาวะ trigone hypersensitivity และ unstable ประกอบกับการหย่อนตัวของ pelvic floor ทำให้ anatomy บริเวณ bladder neck เสียไป ความสามารถของการกลั้นปัสสาวะจึงเสียไปด้วยเหตุต่าง ๆ ดังกล่าว ทำให้เกิด stress incontinence , urgency incontinence และ dysuria ได้ ความผิดปกติที่มี mucosa atrophy , recurrent urinary tract infection และ cystourethral dysfunction นี้มีชื่อเรียกว่า Urogenital Estrogen Deficiency Syndrome (UGEDS ) (4) ( ตารางที่ 1 )
1. Mucosal Atrophy:
- Dysuria (painful micturition)
- Dryness of the mucous membranes. Dyspareunia (painful coitus)
- Itching and soreness around the urethral and vaginal orifices
- Vaginal bleeding
2. Recurrent Urinary Tract infection
3. Bladder and Urethral Dysfunction:
- Urinary incontinence:
– Stress incontinence (involuntary loss of urine during exercise (physical activity, coughing, sneezing, etc)
– Urge incontinence (involuntary loss of urine in association with a strong desire to void)
– Mixed incontinence (A mixture of stress and urge incontinence)
- Urgency
- Frequent micturition
- Nocturia
ตารางที่ 1 : Urogenital estrogen deficiency ที่มา : ดัดแปลงจากเอกสารประกอบที่ 4
ใน Aging Bladder พบว่าอายุมีความสัมพันธ์กับ bladder capacity ทำให้ไม่สามารถยับยั้งการ contractions, ลด urinary flow rate และเพิ่ม post void residual volume (30)
การวินิจฉัย
ต้องซักประวัติ และตรวจร่างกายเพื่อวินิจฉัย Stress urinary incontinence แยกจาก Urinary incontinence สาเหตุอื่นเพราะการรักษาแตกต่างกัน(31)
การซักประวัติ
ผู้ป่วยจะมีประวัติปัสสาวะเล็ดออกมาโดยควบคุมไม่ได้ขณะออกแรงเบ่ง ไอ หรือจาม โดยไม่ได้มีความรู้สึกอยากถ่ายปัสสาวะ จำนวนปัสสาวะที่ออกมามีปริมาณน้อย อาการมักจะหายไปในท่านอน ควรซักประวัติและประเมินสภาพทั่วไป การผ่าตัดในอุ้งเชิงกราน ปริมาณน้ำดื่มในแต่ละช่วงของวัน ปริมาณปัสสาวะราดในแต่ละครั้ง ความถี่ของปัสสาวะราด จํานวนแผ่นผ้าอ้อมที่ใช้ในแต่ละวัน อาการร่วมขณะถ่ายปัสสาวะ ลักษณะการไหลของปัสสาวะที่พุ่งออกมา กิจกรรมที่ผู้ป่วยกําลังกระทําขณะที่มีปัสสาวะราด ไม่สามารถกลั้นปัสสาวะได้ ต้องเข้าห้องน้ำทันทีที่ปวดปัสสาวะ (Urgency) ปัสสาวะเล็ดราด ขณะออกแรงหรือไอ จาม (Stress Urinary Incontinence) ปัสสาวะกลางคืนมากกว่า 1 ครั้งต่อคืน (Nocturia) ปัสสาวะบ่อยกว่าปกติ ( มากกว่า 8 ครั้งใน 24 ชั่วโมง) (Increased Daytime Frequency) เจ็บปวดขณะปัสสาวะ (Painful Urination) ปัสสาวะไหลรั่วตลอดเวลา (Continuous Incontinence) การคั่งค้างของปัสสาวะหรือปัสสาวะลำบาก (Urinary Retention with overflow)(13) การประเมินคุณภาพชีวิตของผู้ป่วยและญาติผู้ดูแล การใช้ฮอร์โมนทดแทน อาการวัยหมดประจำเดือน อาการของความผิดปกติอื่นๆที่พบร่วม ประวัติการตั้งครรภ์และการคลอด ประวัติโรคประจำตัวโดยเฉพาะโรคเบาหวาน ระบบหลอดเลือด ทางเดินหายใจ การไอ จามตลอด ระบบประสาท ยาหรือสารเคมีที่ได้รับ ยาบางชนิดก็มีผลต่ออาการ เช่น ยาขับปัสสาวะ ยาลดความดันโลหิต
การตรวจร่างกาย
ตรวจร่างกายทั่วไปรวมถึงการตรวจอวัยวะเพศภายนอก/ภายใน(per vagina examination) การตรวจทางทวารหนัก(per rectum examination) และระบบประสาท
Simple Tests
Voiding diary หรือ Bladder diary
การตรวจประเมินความรุนแรงโดยให้ผู้ป่วยประเมินตนเองจากการทำบันทึกการถ่ายปัสสาวะ (Bladder diary หรือ simple frequency/volume chart) (ตารางที่ 2)
การตรวจปัสสาวะและเพาะเชื้อ (Urine analysis and culture)
การตรวจปัสสาวะ ตรวจเพื่อแยกโรคการติดเชื้อในระบบปัสสาวะซึ่งเป็นสาเหตุของอาการปัสสาวะผิดปกติ ถ้าตรวจพบเม็ดเลือดแดงออกผิดปกติควรส่องกล้องตรวจในกระเพาะปัสสาวะต่อไป
Cough stress test (Bonney’s test)
Cough stress test เป็นการตรวจทีใช้กันอย่างแพร่หลาย เนื่องจากใช้ได้ง่ายและไม่สิ้นเปลืองค่าใช้จ่ายและ จากผลการศึกษาพบว่าถ้าทําได้ถูกต้อง การตรวจ stress test จะมีความไว (sensitivity)ดีและมีความจําเพาะ (specificity) ต่อภาวะนี้มากกว่าร้อยละ 90(32) ตรวจผู้ป่วยในท่า Lithotomy และท่ายืนตรวจในขณะผู้ป่วยมีปริมาณปัสสาวะเต็มกระเพาะปัสสาวะ และให้ผู้ป่วยไอเพื่อประเมินปัสสาวะที่เล็ด ซึ่ง Stress Urinary Incontinence จะมีปัสสาวะเล็ดทันทีเวลาไอ ออกมาปริมาณไม่มาก และหยุดทันที หากมีปัสสาวะราดหลังจากการไอผ่านไปช่วงระยะเวลาหนึ่ง (delayed leakage) บ่งถึงพยาธิ สภาพชนิด Over active bladderที่อาจถูกกระตุ้นโดยการเบ่ง ดังนั้นขณะกําลังจะตรวจ stress test ถ้าผู้ป่วยมีอาการปวดปัสสาวะขึ้นมากะทันหัน (urgency) ก็ไม่ควรทําการตรวจ เพราะอาจทําให้เกิดผลบวกลวงได้ ในบางกรณี อาจทําให้เกิดผลลบลวงได้เช่น มีปริมาณปัสสาวะในกระเพาะปัสสาวะไม่มากพอ ไอไม่แรงพอ กล้ามเนื้อ perineal ไม่ผ่อนคลายมากพอ หรือมี cystocele ขนาดใหญ่เมื่ออยู่ในท่าหัวสูงจะทําให้ท่อปัสสาวะพับงอ
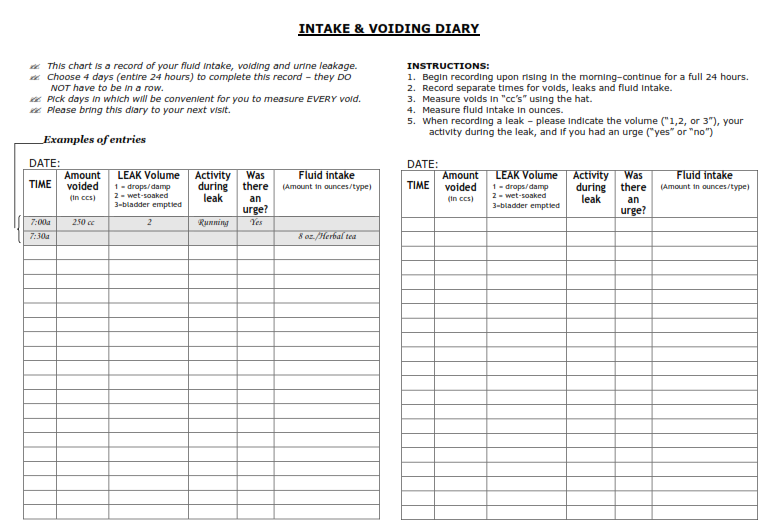
ตารางที่ 2 : แสดงตัวอย่างการทำบันทึกการถ่ายปัสสาวะ ที่มา:www.usadelaware.com/medical…/voiding_diary.pdf
Pad test
เป็นการให้ผู้ป่วยใส่แผ่นรองซับเพื่อประเมินปัสสาวะเล็ด โดยชั่งน้ำหนักแผ่นรองซับก่อน แล้วออกกำลังเมื่อครบ 1 หรือ 24 ชั่วโมง จึงนำแผ่นรองซับมาชั่ง สามารถวินิจฉัยภาวะปัสสาวะเล็ดขณะไอหรือจาม หาก 1-hour pad test น้ำหนักเพิ่มเกิน 1 กรัม และ 24-hour pad test น้ำหนักเพิ่มเกิน 8 กรัม
Cotton swab test (Q-tip test)
เป็นการวัดมุมที่เปลี่ยนไปของท่อปัสสาวะในขณะที่ไอ หรือเบ่ง ถ้ามุมระหว่างพื้นราบกับปลายไม้พันสำลีมากกว่า 30 องศา แสดงว่ามีการเปลี่ยนตำแหน่งมากเกินของท่อปัสสาวะ
การวัดปริมาณปัสสาวะตกค้าง (Postvoid ResidualVolume)
อาจวัดได้โดยตรงจากการใส่ Catheterization หรือจาก Ultrasound ถ้าเหลือมากกว่า 30% ของปริมาตรกระเพาะปัสสาวะหรือมากกว่า 200 ml ถือว่าผิดปกติ
Advanced Testing
Urodynamics evaluation
การตรวจทางยูโรไดนามิกจะทำในสตรีที่การวินิจฉัยยังไม่ชัดเจน อาการไม่ดีขึ้นหลังจากรักษาแบบอนุรักษ์และใช้ประเมินก่อนหรือหลังการผ่าตัด
- 1.Uroflowmetry เป็นการตรวจอัตราความเร็วของการไหลพุ่งของปัสสาวะ ค่าปกติมากกว่า 15 ml/sec มักใช้ในการประเมินภาวะทางเดินปัสสาวะอุดตัน ความผิดปกติในการบีบตัวของกล้ามเนื้อdetrusor และภาวะ external sphincter dyssynergia
- 2.Cystoscopy เป็นการส่องกล้องเพื่อดูพยาธิสภาพในกระเพาะปัสสาวะ ใช้ในกรณีตรวจพบเม็ดเลือดแดงในปัสสาวะ ซึ่งอาจเกิดจากนิ่วหรือเนื้องอกในกระเพาะปัสสาวะ
- 3.Urodynamic study เป็นการวัดความดันในกระเพาะปัสสาวะระหว่างที่มีน้ำไหลเข้าตัวกระเพาะปัสสาวะ ขณะกําลังถ่ายปัสสาวะ อาการปัสสาวะราดขณะที่มีน้ำไหลเข้ากระเพาะปัสสาวะ และผลจากการเบ่งปัสสาวะ bladder sensitivity และ external sphincter activity
- 4.การตรวจชนิดอื่นๆได้แก่ cystometography, pressure voiding study, electromyography
การรักษา
- 1.การรักษาเชิงพฤติกรรม (Behavioral Therapy)
ปรับเปลี่ยนพฤติกรรมที่ทำให้อาการเป็นรุนแรงขึ้น เช่น การลดน้ำหนัก การควบคุมปริมาณน้ำที่ดื่ม หลีกเลี่ยงเครื่องดื่มที่มีแอลกอฮอล์ การหยุดสูบบุหรี่ และหยุดดื่มกาแฟ เป็นต้น
- 2.การบริหารกล้ามเนื้ออุ้งเชิงกราน (Pelvic Floor Exercise or Kegal exercise)
เป็นวิธีที่นิยมมากในการรักษาแบบ conservative นอกจากนี้ยังมีการกระตุ้นกล้ามเนื้ออุ้งเชิงกรานด้วยไฟฟ้า (Electrical stimulation) มีข้อเสียคือความสม่ำเสมอและความถี่ในการบริหารจะลดลงเมื่อเวลาผ่านไป
- 3.การรักษาโดยการใช้ยา ( Pharmacological Therapy)
3.1 Estrogen
การที่ให้ estrogen แล้วอาการ stress incontinence ดีขึ้นในบางรายนั้น นอกจากฮอร์โมนจะช่วยให้ urethra หนาตัวขึ้นแล้ว ยังทำให้ collagen tissue ซึ่งเป็นตัว support bladder และ urethra มีความยืดหยุ่นแข็งแรงมากขึ้น เพราะ cell เหล่านี้มี receptor ของ estrogen ด้วย(33) ในรายที่มี anatomical defect เช่น vaginal relaxation , uterine prolapse การแก้ไขด้วย hormone replacement therapy อย่างเดียวยัง controversy และในบางครั้งจะต้องใช้การผ่าตัดช่วยด้วย ก่อนการรักษาควรพิจารณาว่า menopause ตั้งแต่เมื่อไร มีการใช้ hormone อยู่หรือเปล่า มีการรักษาวิธีอื่นมาก่อนหรือเปล่า ผลของอาการต่อการมีเพศสัมพันธ์และคุณภาพชีวิตประจำวัน การถามอาการอย่างละเอียดมีความสำคัญในการประเมิน เพื่อดูว่ามีความจำเป็นที่จะรักษาผู้ป่วยอย่างไรมากขนาดไหน ควรตรวจดูความรุนแรงของ mucosal atrophy และดูว่ามีร่วมกับ urogenital prolapse ด้วยหรือไม่ ก่อนการตรวจละเอียดดังกล่าวอาจให้ estrogen เฉพาะที่ 3-4 สัปดาห์ เพื่อดูว่าขณะที่ไม่ขาดฮอร์โมนลักษณะ เป็นอย่างไร และควรตรวจดูด้วยว่ามีการติดเชื้อเกิดขึ้นหรือไม่ ถ้ามีควรให้การรักษาการติดเชื้อร่วมไปด้วย (4) หลักการรักษาคือให้ estrogen ในระดับที่ต่ำที่สุดที่จะแก้ปัญหาได้ เช่นเดียวกับการให้ฮอร์โมนรักษาภาวะหมดประจำเดือนทั่ว ๆ ไป hormone estrogen ทุกชนิดไม่ว่าจะให้ทางใด (รับประทาน ทา สอดช่องคลอด) ก็ถูกดูดซึมเข้าร่างกาย และมีผลทาง systemic ได้ทั้งสิ้นถ้าให้ในขนาดที่มากพอ แต่เนื่องจากช่องคลอดและทางเดินปัสสาวะส่วนล่าง มี receptor ต่อ estrogen มาก โดยเฉพาะถ้าอยู่ในภาวะ atrophic(34) จะ sensitive ต่อ estrogen มาก สามารถได้ผลเมื่อรักษาด้วย estrogen ในขนาดที่รักษา postmenopause ทั่วๆไปหรือในขนาดที่ต่ำกว่า optimum dose โดยทั่ว ๆ ไป เช่น 0.01 mg. ethinyl estradiol , 0.3-0.625 mg. conjugated estrogen , 0.5-1 mg. estradiol โดยการรับประทานวันละครั้ง นาน 1-3 เดือนก็จะได้ผล หลังจากนั้นให้เป็น intermittent dose คือสัปดาห์ละ 1-2 ครั้งก็พอ แต่ต้องให้ติดต่อกันไป ถ้าหยุดให้ยาอาการจะเกิดขึ้นมาใหม่ภายใน 6 เดือน หรือในกรณีที่เราไม่ต้องการ systemic effect ของ estrogen ทำให้ short acting estrogen คือ estradiol เริ่มต้นรับประทาน 2 mg/วัน นาน 2 สัปดาห์ต่อด้วย 1 mg/วัน อีก 2-3 เดือน หลังจากนั้น 1 mg. 2 ครั้ง/สัปดาห์ หรือจะให้เป็น estrogen เฉพาะที่ในขนาดน้อย ๆ ซึ่งมีหลายอย่างให้เลือก เช่น estradiol estrogen vaginal tablet 0.01-0.025 mg/วัน ( Vagifem ) conjugated estrogen vaginal cream 0.5-1 gm/วัน ( Premarin cream ) , estriol vaginal cream 0.5 gm/วัน , ฮอร์โมนให้เฉพาะที่เหล่านี้ recommend ให้ครั้งแรกทุกวันนาน 2 สัปดาห์ จากนั้นให้ 1-2 ครั้ง/สัปดาห์ ในรายที่มี Uterine prolapse การใช้ estrogen released vaginal ring ก็ได้ผลดี(4) ยาเฉพาะที่มีประโยชน์ในกรณีที่เราไม่ต้องการให้ยามีผลต่อร่างกายหรือ endometrium ในรายที่มี relative contraindication ต่อ estrogen เช่น ตับหรือไตทำงานไม่ดี มีปัญหา หรือความโน้มเอียงที่จะเป็นมะเร็งเต้านม แต่มีอาการทาง urogenital organs อย่างไรก็ตามถ้าให้ขนาดมาก ๆ ก็มีการดูดซึมเข้า systemic ได้ทุกชนิด
3.2 Serotonin noradenaline reuptake inhibitor (Duloxetine)
เป็นกลุ่มยาที่ใช้รักษาอาการภาวะซึมเศร้ามีหลักฐานว่ามีประโยชน์ชัดเจนในการลดความถี่ของการกลั้นไม่อยู่ และที่มีรายงานถึงประสิทธิภาพองการรักษาดี
3.3 Alpha one adrenoreceptor agonists
ทำให้มีการหดรัดตัวของกล้ามเนื้อเรียบของท่อปัสสาวะช่วยรักษาภาวะปัสสาวะเล็ดได้ แต่จาก Cochrene review พบว่ามีผลไม่ต่างจากยาหลอก (35)และมีผลข้างเคียงทำให้ความดันโลหิตต่ำลงได้
3.4 Imipramine
เป็นยาที่ใช้รักษาอาการภาวะซึมเศร้าทำให้มีการหดรัดตัวของกล้ามเนื้อเรียบของหูรูดท่อปัสสาวะ ผลข้างเคียงทำให้เกิดอาการง่วงซึม
- 4.การรักษาด้วยการผ่าตัด (Surgical Therapy)
เนื่องจากมีหลายทฤษฎีพยายามอธิบายกลไกในการเกิด Stress urinary incontinence จึงมีการรักษาที่หลากหลาย(20) (ตารางที่ 3)

ตารางที่ 3 : แสดงวิธีการรักษา SUI ที่มา : ดัดแปลงจากเอกสารประกอบที่ 20
RETROPUBIC SUSPENSIONS FOR CORRECTING URETHRAL POSITION
จากทฤษฎีตำแหน่งของท่อปัสสาวะที่ต้องอยู่เหนือ Pelvic floor จึงจะไม่เกิด Stress urinary incontinence การจะผ่าตัดแก้ไข SUI คือยกท่อปัสสาวะให้อยู่เหนือ Pelvis การตรึงคอปัสสาวะไม่ให้เคลื่อนตาม เวลามีการไอหรือจามจึงจะกลั้นปัสสาวะได้(36) Marshall-MarchettiKrantz (MMK) vesico-urethral suspension คือการเย็บ fascia ข้างท่อปัสสาวะ(urethral and periurethral vaginal wall) กับ periosteum ด้านหลัง pubis มีการผ่าตัดหลายอย่างดัดแปลงมาจาก Marshall-MarchettiKrantz (MMK) ล่าสุดคือ Burch colpocystourethropexy จะเย็บ fascia ข้างท่อปัสสาวะ (urethrovaginal tissue) กับ Cooper’s Ligaments
BULKING AGENTS FOR ISD
จากทฤษฎี ISD Stress urinary incontinence เกิดจากกล้ามเนื้อหูรูดท่อปัสสาวะอ่อนแรงเอง (Deficient sphincteric mechanism) ก็ได้มีการฉีด Bulking agents บริเวณ periurethral submucosa เพื่อไปแก้ไขให้ท่อปัสสาวะปิด สาร Bulking agents ที่ใช้มีหลายชนิด(37) เช่น bovine collagen (Contigen, Bard, UK);pyrolytic carbon-coated zirconium oxide beads (Durasphere TM or Durasphere-EXP TM) sodium carboxylmethylcellulose (trade name,Coaptite®) และ ethylene vinyl alcohol copolymer suspended in dimethyl sulphoxide (Tegress® solution) การศึกษาของประสิทธิภาพของสารที่ใช้แต่ละตัวก็หลากหลายตามแต่ละงานวิจัย(38)
NEEDLE SUSPENSIONS, PUBOVAGINAL SLINGS FOR THE HAMMOCK THEORY
Needle suspensions ได้ถูกออกแบบเพื่อแก้ไข SUI ที่สัมพันธ์กับ poorly supported และ hypermobile urethra โดยใช้ hammock support บริเวณตำแหน่ง bladder neck มีหลายวิธี วิธีที่ ลด complication rates ได้คือ Pereyra procedure(39) เป็นการเย็บ paraurethral fascia กับ anterior rectus fascia โดยใช้ Non-absorbable suture
Pubovaginal slings ดั้งเดิมจะใช้ autograft fascia วางที่ bladder neck และยึดกับ rectus muscle บ้างก็ดัดแปลงใช้ vaginal wall แทน autograft tissue และยึดกับ symphysis pubis หรือหลังต่อ symphysis rami แทน
MID-URETHRAL SLINGS FOR INTEGRAL THEORY
Suburethral slings ใช้เมื่อมีการล้มเหลวจากวิธีอื่นมาก่อน หรือมีความเสี่ยงในการกลับเป็นซ้ำสูง หลักการจะวาง mesh บริเวณ mid-urethral area เพื่อทำหน้าที่พยุงคล้าย pubourethral ligament TVT (Tansion free Vaginal Tape) เป็นเทคนิคที่ใช้เทปสอดลอดใต้ท่อปัสสาวะ ช่วยค้ำจุนโดยมุ่งหวังให้ท่อปัสสาวะกลับมาอยู่ในตำแหน่งปกติ TVT เป็นเทคนิคที่มีประสิทธิภาพสูง การศึกษาในหญิงไทยพบว่า ค่า Valsalva leak point pressure (VLPP) ต่ำกว่า 60 cm H2O มีความสัมพันธ์ เป็น 0.6 เท่าของโอกาสที่จะหายขาดหลังการผ่าตัด TVT (40) TOT (Trans – Obturator Tape) เป็นวิธีใส่ Polypropylene Sling ใต้ mid-urethral area โดยสอดเข็มรอบ Ischiopubic ramus ผ่าน Obturator foramens ทั้งสองข้าง
TECHNOLOGICAL ADVANCES
Stress urinary incontinence มีสาเหตุจากหลายปัจจัย หลักๆจาก urethral hypermobility หรือ intrinsic sphincter deficiency (ISD) หรือทั้งสองอย่าง บริเวณ mid-urethra ประกอบด้วยกล้ามเนื้อลายทั้ง muscle fibers type I และ type II ประกอบเป็น external urethral sphincter (EUS) หรือที่เรียกว่า rhabdosphincter การรักษา Stress urinary incontinence ที่สามารถกระตุ้นการสร้างและซ่อมแซม (regeneration) rhabdosphincter ได้ คือการใช้ stem cells therapy ซึ่งแหล่งของ stem cells ได้จากทั้งจาก embryonic stem cells (ESCs) ซึ่งมีข้อจำกัดทางด้านจริยธรรม และ autologous adult stem cells ที่ได้จาก Bone-marrow stromal cells, muscle-derived stem cells (MDSCs) และ adipose-derived stem cells (ADSCs) การเก็บ autologous multipotent stem cells จาก bone marrow stromal cells เป็นวิธีที่รุกล้ำ สร้างความเจ็บปวดมากกว่า muscle-derived stem cells (MDSCs) และ adipose-derived stem cells (ADSCs) (41-43)
พบว่า skeletal muscle-derived cells (SkMDCs) สามารถซ่อมแซม sphincter musculature ได้ specific cell type ของ SkMDCs อยู่ที่ myoblasts, satellite cells, muscle progenitor cells หรือ muscle-derived stem cells ได้มีหลายการศึกษาเกี่ยวกับ stem cellsในการรักษา SUI โดยทดลองกับหนู โดยมีทั้ง Transurethral injection of stem cell, Periurethral injection และ Intravenous injection และประเมินผลการรักษาพบว่าได้ผลดี(44) และมีการศึกษาในคนแต่เป็นจำนวนที่น้อยและยังต้องมีการศึกษา พัฒนาต่อไป(43, 45)
Referance
1. Rogerio A. Lobo JK, Robert Marcus. Menopause:Biology And Pathobiology. California, USA; 2000.
2. Cardozo LD, Kelleher CJ. Sex hormones, the menopause and urinary problems. Gynecol Endocrinol. 1995 Mar;9(1):75-84.
3. Iosif CS. Effects of protracted administration of estriol on the lower genito urinary tract in postmenopausal women. Arch Gynecol Obstet. 1992;251(3):115-20.
4. Tamrongterakul T. Urogenital Health During Midlife Second Phramongkutklao Menopause Training Course 2000 10 – 11 February 2000.
5. Molander U, Milsom I, Ekelund P, Mellstrom D, Eriksson O. Effect of oral oestriol on vaginal flora and cytology and urogenital symptoms in the post-menopause. Maturitas. 1990 Jun;12(2):113-20.
6. Sukwatana P, Meekhangvan J, Tamrongterakul T, Tanapat Y, Asavarait S, Boonjitrpimon P. Menopausal symptoms among Thai women in Bangkok. Maturitas. 1991 Sep;13(3):217-28.
7. Salinas Casado J, Virseda Chamorro M, Teba del Pino F, Vazquez Alba D, Adot Zurbano JM. [Urinary incontinence in menopause]. Arch Esp Urol. 2000 May;53(4):349-54.
8. Cheater FM, Castleden CM. Epidemiology and classification of urinary incontinence. Baillieres Best Pract Res Clin Obstet Gynaecol. 2000 Apr;14(2):183-205.
9. Bunyavejchevin S. The impact of overactive bladder, stress and mixed urinary incontinence on quality of life in Thai postmenopausal women. J Med Assoc Thai. 2006 Mar;89(3):294-8.
10. Wattanayingcharoenchai R, Manonai J, Vannatim N, Saritapirak S, Imsomboon C, Chittacharoen A. Impact of stress urinary incontinence and overactive bladder on quality of life in Thai women attending the urogynecology clinic. J Med Assoc Thai. 2007 Jan;90(1):26-31.
11. Abrams P CL, Fall M. . The standardization of terminology of lower urinary tract function : report from the standardization subcommittee of the International Continence
Society. Neurourol Urodyn p. 167-78.
12. Abrams P, Cardozo L, Fall M, Griffiths D, Rosier P, Ulmsten U, et al. The standardisation of terminology of lower urinary tract function: report from the Standardisation Sub-committee of the International Continence Society. Neurourol Urodyn. 2002;21(2):167-78.
13. Matthew Parsons LC. The classfication of urinary incontinence. Gynaecological Practice [Reviews ]. 2003 14 April 2003;3:57-64.
14. Jolleys JV. Reported prevalence of urinary incontinence in women in a general practice. Br Med J (Clin Res Ed). 1988 May 7;296(6632):1300-2.
15. Lapitan MC, Chye PL. The epidemiology of overactive bladder among females in Asia: a questionnaire survey. Int Urogynecol J Pelvic Floor Dysfunct. 2001;12(4):226-31.
16. Kinchen K GJ, Obenchain R, Bump R. Prevalence and frequency of stress urinary incontinence among community-dwelling women. Presented at the European Association in Urology (EAU).Annual Meeting; Febuary 2002; Birmingham, UK. Eur Urol. 2002(1):85.
17. Sakondhavat C, Choosuwan C, Kaewrudee S, Soontrapa S, Louanka K. Prevalence and risk factors of urinary incontinence in Khon Kaen menopausal women. J Med Assoc Thai. 2007 Dec;90(12):2553-8.
18. Panugthong P, Chulyamitporn T, Tanapat Y. Prevalence and risk factors of urinary incontinence in Thai menopausal women at Phramongkutklao Hospital. J Med Assoc Thai. 2005 Nov;88 Suppl 3:S25-30.
19. Stuart L Stanton AKM. Clinical Urogynaecology. 2 ed. Hilton P, editor. UK; 2000.
20. Daneshgari F, Moore C. Advancing the understanding of pathophysiological rationale for the treatment of stress urinary incontinence in women: the ‘trampoline theory’. BJU Int. 2006 Sep;98 Suppl 1:8-14; discussion 5-6.
21. Kelly H. Incontinence of urine in women. . Urol Cutan Rev. 1913;17: 291-3.
22. Bonney V. On diurnal incontinence of urine in women. . J Obstet Gynaecol Br Emp. 1923;30:358-65.
23. Blaivas JG. Incontinence. J Urol. 1993 Nov;150(5 Pt 1):1455.
24. McGuire EJ. The effects of sacral denervation on bladder and urethral function. Surg Gynecol Obstet. 1977 Mar;144(3):343-6.
25. McGuire EJ. Urodynamic findings in patients after failure of stress incontinence operations. Prog Clin Biol Res. 1981;78:351-60.
26. McGuire EJ, Fitzpatrick CC, Wan J, Bloom D, Sanvordenker J, Ritchey M, et al. Clinical assessment of urethral sphincter function. J Urol. 1993 Nov;150(5 Pt 1):1452-4.
27. DeLancey JO. Structural support of the urethra as it relates to stress urinary incontinence: the hammock hypothesis. Am J Obstet Gynecol. 1994 Jun;170(6):1713-20; discussion 20-3.
28. Delancey J. Structural support of the urethra as it relates to stress urinary incontinence: the hammock hypothesis. Am J Obstet Gynecol EndocrinoI. 1994;170:1718.
29. Petros PE, Ulmsten UI. An integral theory of female urinary incontinence. Experimental and clinical considerations. Acta Obstet Gynecol Scand Suppl. 1990;153:7-31.
30. Siroky MB. The aging bladder. Rev Urol. 2004;6 Suppl 1:S3-7.
31. Bunyavejchevin S. Role of general Obstetricians-Gynecologists in the treatment of stress urinary incontinence in Thai woman. Thai Journal of Obstetrics and Gynaecology. 2010; 18(October 2010):145-7.
32. Kong TK MJ, Robinson JM, Brocklehurst JC Predicting urodynamic dysfunction from clinical features in incontinent elderly women. Age Ageing 1990;19 257-63.
33. Fantl JA, Wyman JF, Anderson RL, Matt DW, Bump RC. Postmenopausal urinary incontinence: comparison between non-estrogen-supplemented and estrogen-supplemented women. Obstet Gynecol. 1988 Jun;71(6 Pt 1):823-8.
34. Nilsson K, Heimer G. Low-dose oestradiol in the treatment of urogenital oestrogen deficiency–a pharmacokinetic and pharmacodynamic study. Maturitas. 1992 Oct;15(2):121-7.
35. Alhasso A, Glazener CM, Pickard R, N’Dow J. Adrenergic drugs for urinary incontinence in adults. Cochrane Database Syst Rev. 2003(2):CD001842.
36. Enhorning G. Simultaneous recording of intravesical and intra-urethral pressure. A study on urethral closure in normal and stress incontinent women. Acta Chir Scand Suppl. 1961;Suppl 276:1-68.
37. Rechberger T, Donica H, Baranowski W, Jakowicki J. Female urinary stress incontinence in terms of connective tissue biochemistry. Eur J Obstet Gynecol Reprod Biol. 1993 May;49(3):187-91.
38. Appell RA, Dmochowski RR, Herschorn S. Urethral injections for female stress incontinence. BJU Int. 2006 Sep;98 Suppl 1:27-30; discussion 1.
39. Ulmsten U, Falconer C. Connective tissue in female urinary incontinence. Curr Opin Obstet Gynecol. 1999 Oct;11(5):509-15.
40. Bunyavejchevin S. Can pre-operative urodynamic study predict the successful outcome of tension free vaginal tape (TVT) operation in Thai women with stress urinary incontinence? J Med Assoc Thai. 2005 Nov;88(11):1493-6.
41. Chancellor DNaMB. Stem Cell Therapy for Stress Urinary Incontinence. Neurourology and Urodynamics 2010 15 April 2010 29:S36-S41.
42. Chancellor MCSMB. Muscle derived stem cell therapy for stress urinary incontinence. World J Urol 2008 10 May 2008;26:327-32.
43. MINERVA MEDICA MCS, M. L. CHEN, M. B. CHANCELLOR Stem cell therapy for urethral sphincter regeneration. MINERVA UROL NEFROL. 2009 March 2009;61(1):27-40.
44. Lin CS, Lue TF. Stem Cell Therapy for Stress Urinary Incontinence: A Critical Review. Stem Cells Dev. Jan 13.
45. Carr LK SD, Steele S, et al. 1-year follow-up of autologous musclederived stem cell injection pilot study to treat stress urinary incontinence. Int Urogynecol J Pelvic Floor Dysfunct. 2008;19:881-3.


