การติดเชื้อระบบทางเดินปัสสาวะในหญิงตั้งครรภ์
Urinary tract infection in pregnancy
พญ.แพรทิพย์ พรายแก้ว
อาจารย์ที่ปรึกษา พญ. เฟื่องลดา ทองประเสริฐ
บทนำ
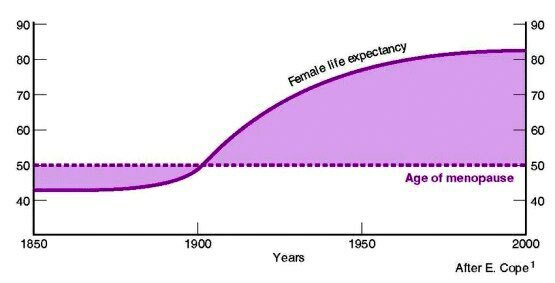
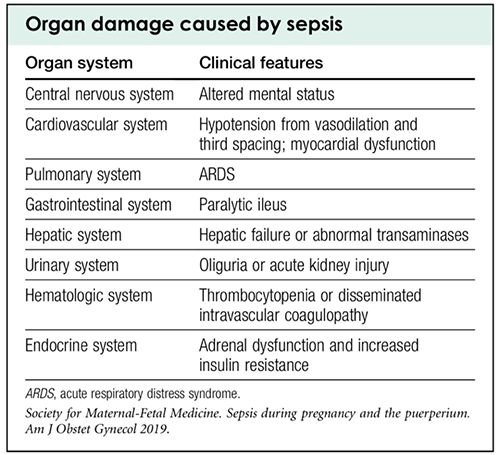
การติดเชื้อระบบทางเดินปัสสาวะเป็นปัญหาที่พบได้บ่อยในหญิงตั้งครรภ์ โดยเฉพาะ ในระหว่างการตั้งครรภ์การติดเชื้อในทางเดินปัสสาวะ ทำให้เกิดภาวะแทรกซ้อนจากการ ติดเชื้อที่รุนแรง ส่งผลกระทบทั้งมารดาและทารกได้ หากไม่ได้รับการรักษาที่เหมาะสม
พยาธิสรีรวิทยาของโรค
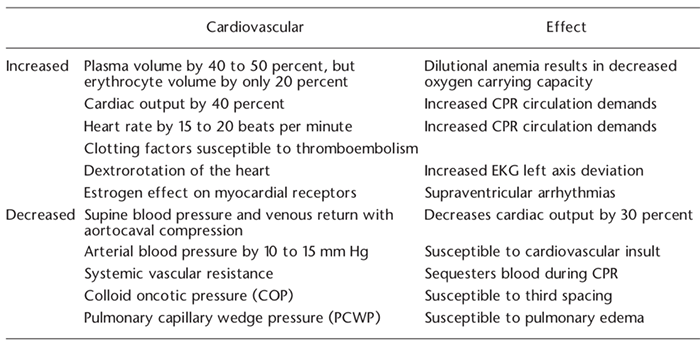
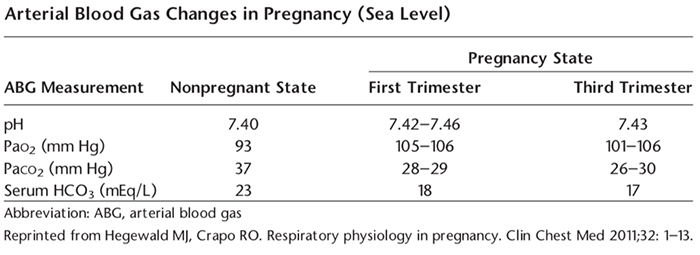
เกิดจากการติดเชื้อพวกแบคทีเรียบริเวณปากช่องคลอดหรือทวารหนักใกล้ท่อปัสสาวะ ย้อนกลับขึ้นไป (Ascending infection) ร่วมกับการเปลี่ยนแปลงโครงสร้างและการทำงานของ ระบบทางเดินปัสสาวะขณะตั้งครรภ์ จากผลของฮอร์โมนโปรเจสเตอโรน (Progesterone) และการขยายตัวของขนาดมดลูก เป็นปัจจัยเพิ่มความเสี่ยงต่อการติดเชื้อระบบทางเดิน ปัสสาวะได้ โดยการเปลี่ยนแปลงทางสรีรวิทยามีดังนี้
Kidneys
- increase renal plasma flow
- increase GFR
- increase urine output
Renal pelvis and ureters
- calyceal and ureteral dilatation
- decreased peristalsis
- increase obstruction by enlarged uterus
Bladder
- smooth muscle relaxation
- increase residual urine
- urinary stasis
การติดเชื้อระบบทางเดินปัสสาวะ (Urinary tract infection; UTI)
เป็นการอักเสบของเยื่อบุผิวของระบบทางเดินปัสสาวะ เกิดจากการติดเชื้อแบคทีเรีย สามารถแบ่งได้เป็นการติดเชื้อทางเดินปัสสาวะแบบไม่มีอาการ (Asymptomatic bacteriuria) พบได้ประมาณ 2-15% และแบบที่มีอาการแสดง (Symptomatic UTI) พบได้ 1-2% ในหญิงตั้งครรภ์
ปัจจัยเสี่ยงสำคัญ
- Young age pregnancy
- Late ANC
- Smoking
- Primigravida
- Pregestational DM
เชื้อก่อโรคที่สำคัญ ได้แก่ E.coli พบได้ถึง 70-80% ของการติดเชื้อทั้งหมด, Group B Streptococcus, Stapylococcus saprophyticus,Klebsiella spp,Enterobacter spp, Proteus spp, Enterococcus sppetc.
ภาวะแทรกซ้อน
ผลต่อมารดา
- Pyelonephritis
- Anemia
- Septicemia
- Respiratory distress syndrome
- ARDS
- Acute renal failure
- Chorioamnionitis
- Preeclampsia
- Primary cesarean section rate
ผลต่อทารก
- Preterm delivery
- Low birth weight
- Stillbirth/ neonatal death
Asymptomatic bacteriuria
มักตรวจพบได้จากการคัดกรองโรค หากไม่ได้รับการรักษา ผู้ป่วยประมาณ 20-40% จะสามารถพัฒนาไปเป็น Pyelonephritis ได้ ภาวะแทรกซ้อนที่สำคัญ คือ การคลอดก่อน อายุครรภ์ 37 สัปดาห์ พบได้ถึง 20-50% ทารกแรกเกิดน้ำหนักน้อยหรือภาวะทารกโตช้าในครรภ์
การวินิจฉัยการติดเชื้อทางเดินปัสสาวะแบบไม่ปรากฏอาการ
- ตรวจพบเชื้อแบคทีเรียโดยวิธีการเก็บตรวจปัสสาวะ 2 ครั้ง (2 consecutive voided urine specimens) โดยพบเชื้อแบคทีเรียก่อโรคชนิดเดียวกัน ปริมาณเชื้อมากกว่า หรือเท่ากับ 〖10〗^5 cfu/mL
- ตรวจพบเชื้อแบคทีเรียโดยวิธีการสวนผ่านท่อปัสสาวะ(catheterized urine specimens) ผลการเพาะเชื้อ พบเชื้อแบคทีเรียก่อโรคชนิดเดียว ปริมาณเชื้อมากกว่า หรือเท่ากับ 〖10〗^2 cfu/mL
วิธีเก็บสิ่งส่งตรวจควรแนะนำให้หญิงตั้งครรภ์ทำความสะอาดบริเวณอวัยวะเพศก่อนทุกครั้ง เมื่อปัสสาวะออกไปก่อนระยะหนึ่ง แล้วจึงเก็บปัสสาวะช่วงกลางของการปัสสาวะเพื่อส่งตรวจ (midstream clean-catch specimen) จะช่วยลดการปนเปื้อน ไม่แนะนำให้เก็บปัสสาวะส่งตรวจ ด้วยวิธีสวนท่อปัสสาวะ เนื่องจากเป็นการเพิ่มโอกาสติดเชื้อ
การตรวจปัสสาวะด้วยวิธีอื่น
Urianalysis
การตรวจวิเคราะห์ปริมาณเม็ดเลือดขาว เม็ดเลือดแดง และโปรตีนในปัสสาวะ แต่หากพบว่ามี squamous epithelial cells มากกว่า15-20 /HPF ให้พิจารณาเก็บส่งตัวอย่างอีกครั้งเนื่องจาก contamination
Urine dipstick
การตรวจ nitrite, leukocyte esterase หากพบว่าให้ผลบวก sensitivity และ specificity คิดเป็น 75% และ 82 %ตามลำดับ
ถ้าการตรวจ nitrite ให้ผลเป็นบวก บ่งบอกการติดเชื้อในกลุ่มแกรมลบ เช่น E.coli, Klebsiella, Proteus หรือ Enterobacter และจะให้ผลลบในกรณีที่เป็นเชื้อในกลุ่มแกรมบวก เช่น Enterococci, Staphylococcus, Streptococcus หรือ Acinatobactor
ถ้าการตรวจ leukocyte esterase ให้ผลเป็นบวก บ่งบอกถึงการเพิ่มขึ้นของเม็ดเลือดขาว
อย่างไรก็ตามทั้งสองวิธีนี้ มีผลลบลวง(false negative) สูงและมีค่าทำนายผลบวก(Positive predictive value) ต่ำ ซึ่งไม่ไวพอสำหรับการวินิจฉัย
คำแนะนำสำหรับการคัดกรองสำหรับผู้ป่วยแบบไม่แสดงอาการ
The American Academy of Family Physicians(AAFP) และ The U.S. Preventive Service Task Force(USPSTF)
แนะนำให้หญิงตั้งครรภ์ที่มีอายุครรภ์ในช่วง 12-16 สัปดาห์หรือมาฝากครรภ์ครั้งแรกใน กรณีที่มาฝากครรภ์ช้า ควรเก็บปัสสาวะส่งตรวจการเพาะเชื้อทุกราย
The Infectious Disease Society of America(IDSA)
แนะนำคัดกรองโดยส่งเพาะเชื้อจากปัสสาวะ อย่างน้อย 1 ครั้งช่วงแรกของการตั้งครรภ์ หากพบการติดเชื้อแบคทีเรียให้ส่งตรวจซ้ำหลังการรักษา ในกรณีที่ครั้งแรกไม่พบเชื้อยังไม่มีข้อ กำหนดที่ชัดเจนเรื่องการตรวจคัดกรองซ้ำ
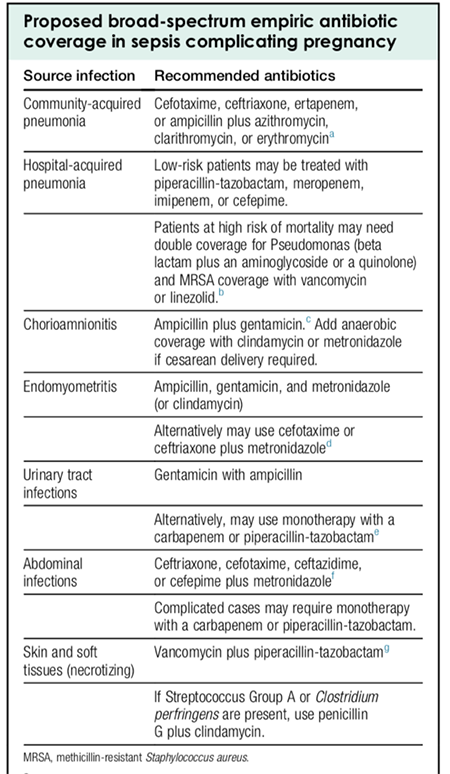
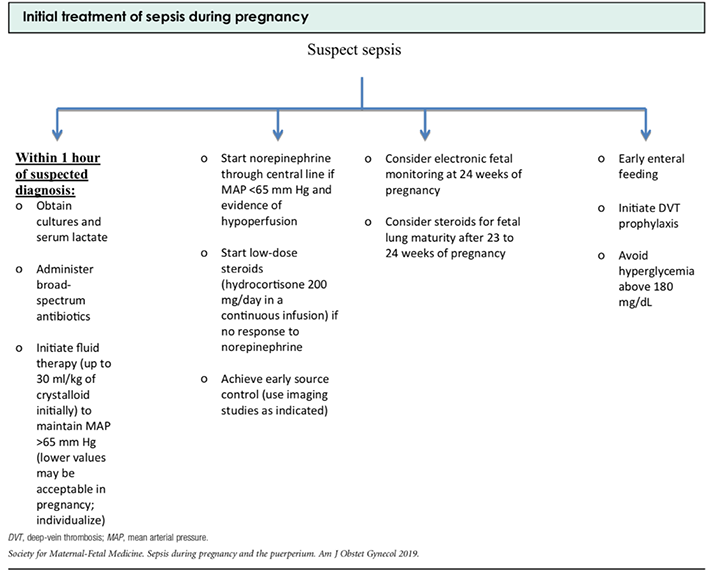
การรักษา
หญิงตั้งครรภ์ที่ได้รับการวินิจฉัยว่ามีการติดเชื้อในทางเดินปัสสาวะควรได้รับการรักษาทุกรายโดยไม่คำนึงว่าจะมีอาการแสดงหรือไม่ เพื่อลดการภาวะแทรกซ้อนรุนแรงจากกรวยไตอักเสบ
ชนิดของยาปฏิชีวนะที่แนะนำให้ใช้เป็นดังนี้ (รูปที่ 1 และ 2)

รูปที่ 1 แสดงการพิจารณาใช้ยาปฏิชีวนะสำหรับ Asymptomatic bacteriuria
(ที่มา : Williams Obstetrics, 25e. F. Gary Cunningham, Kenneth J. Leveno, Steven L. Bloom, Jodi S. Dashe, Barbara L. Hoffman, Brian M. Casey, Catherine Y. Spong.)

รูปที่ 2 แสดงการพิจารณาใช้ยาปฏิชีวนะสำหรับ Asymptomatic bacteriuria
(ที่มา : เอกสารการประชุมวิชาการกลางปี พ.ศ. 2561 ราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย)
การพิจารณาใช้ยาปฏิชีวนะตามเชื้อ
E.coli
แนะนำ Fosfomycin มากกว่า เนื่องจากรายงานผู้ป่วยที่ติดเชื้อนี้ส่วนหนึ่ง 20-40% ดื้อต่อยา Ampicillin และ Amoxicillin
Group B streptococcus (GBS)
แนะนำยาในกลุ่ม Penicillin ; Ampicillin, Cefazolin จำเป็นต้องได้รับยาฆ่าเชื้อทาง หลอดเลือดดำ เนื่องจากมีความสัมพันธ์กับการติดเชื้อจากมารดาสู่ทารกด้วย (Vertical transmission) โดยผู้ป่วยควรได้รับยาปฏิชีวนะก่อนที่จะคลอดอย่างน้อย 4 ชั่วโมง
การติดตามอาการ
หลังการรักษาด้วยยาปฏิชีวนะจนครบ ผู้ป่วยควรได้รับการส่งตรวจ urine culture ภายใน 1-2 สัปดาห์ หากผลเพาะเชื้อยังพบเชื้อแบคทีเรียก่อโรคตัวเดียวกัน (persisitent bacteriuria)
ผู้ป่วยควรได้รับยาปฏิชีวนะเป็น Nitrofurantoin 100 mg รับประทานก่อนนอน เป็นระยะเวลา 21 วัน
จากการศึกษาพบว่าหลังการรักษาหญิงตั้งครรภ์มีโอกาสติดเชื้อได้อีก (recurrent bacteriuria) คิดเป็นร้อยละ 30 ดังนั้นแนะนำให้ตรวจเพาะเชื้อหลังการรักษาซ้ำเป็นระยะ เพื่อป้องกันการกลับเป็นซ้ำ และอาจพิจารณาให้ยาปฏิชีวนะเพื่อควบคุมตลอดการตั้งครรภ์ โดยการเลือกยาปฏิชีวนะตามผลเพาะเชื้อแบคทีเรีย ในหญิงตั้งครรภ์แนะนำให้ Nitrofurantoin 100 mg รับประทานก่อนนอน
Symptomatic UTI
การติดเชื้อระบบทางเดินปัสสาวะส่วนล่าง ได้แก่ กระเพาะปัสสาวะอักเสบ (Cystitis) หรือท่อปัสสาวะอักเสบ (Urethritis) คือ อาการแสดงที่พบได้บ่อย ได้แก่ ถ่ายปัสสาวะแล้วรู้สึกแสบขัด (dysuria) , อาการปวดปัสสาวะเป็นทันทีและไม่สามารถรอได้ (urgency) ปัสสาวะบ่อย
(frequent urination) หรืออาจมาด้วย อาการปวดเหนือบริเวณหัวหน่าว (suprapubic pain)
การติดเชื้อระบบทางเดินปัสสาวะส่วนบน ได้แก่ กรวยไตอักเสบ (Pyelonephritis) อาการแสดงที่พบได้บ่อย ได้แก่ ไข้หนาวสั่น (fever with chill) , ปวดเอว (Frank pain) , คลื่นไส้อาเจียน (nausea & vomiting) หากไม่ได้รับการรักษาอย่างเหมาะสม มีโอกาสเกิด ภาวะแทรกซ้อนรุนแรงได้
Acute cystitis
หญิงตั้งครรภ์ที่ติดเชื้อที่มีอาการผิดปกติ มักพบ microscopic hematuria ในปัสสาวะ หากไม่ได้รับการรักษาอย่างเหมาะสม อาจมีภาวะแทรกซ้อนจากกรวยไตอักเสบได้ร้อยละ 40 แนวทางการรักษาและยาปฏิชีวนะที่แนะนำเช่นเดียวกับการรักษา Asymptomatic bacteriuria โดยให้ยาปฏิชีวนะเป็นเวลา 3 วันสำหรับการติดเชื้อครั้งแรก หากมีการติดเชื้อซ้ำซ้อน (recurrent infection) แนะนำให้เป็นเวลา 7-10 วัน หลังการรักษาผู้ป่วยร้อยละ 90 อาการจะดีขึ้นภายใน 72 ชั่วโมง
การติดตามอาการ
หลังการรักษาด้วยยาปฏิชีวนะจนครบ ผู้ป่วยควรได้รับการส่งตรวจ urine culture ภายใน 1-2 สัปดาห์
หากพบว่าหญิงตั้งครรภ์มีการติดเชื้อซ้ำซ้อน (recurrent infection) อย่างน้อย 3 ครั้งใน 12 เดือน แนะนำให้ยาปฏิชีวนะเพื่อควบคุมตลอดการตั้งครรภ์ โดยให้ Nitrofurantoin หรือ TMP-SMX รับประทานก่อนนอน
Acute pyelonephritis
เป็นการติดเชื้อระบบทางเดินปัสสาวะชนิดรุนแรง ทำให้เกิดภาวะแทรกซ้อน เช่น การติดเชื้อรุนแรง การติดเชื้อแบคทีเรียในกระแสเลือด ระบบทางเดินหายใจล้มเหลว ไตวายฉับพลัน เป็นต้น
การรักษา
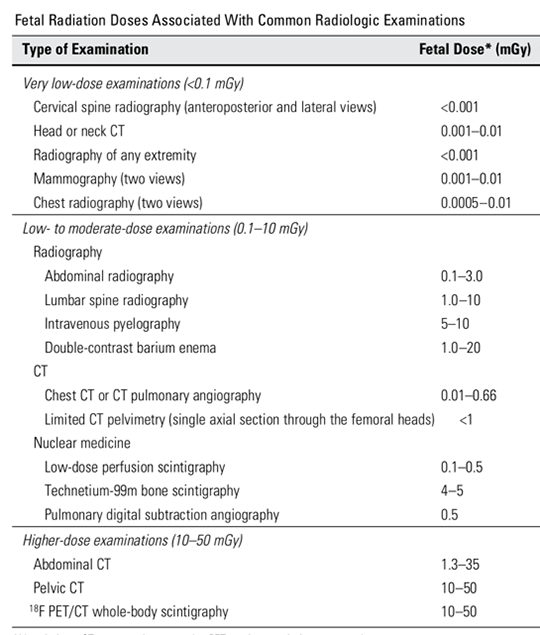
หญิงตั้งครรภ์ที่ได้รับการวินิจฉัยควรได้รับการรักษาในโรงพยาบาลทุกกรณี โดยให้ยา ปฏิชีวนะทางหลอดเลือดดำ(รูปที่ 3) จนกระทั่งไข้ลดลงอย่างน้อย 48 ชั่วโมง จึงพิจารณาเปลี่ยน เป็นยาปฏิชีวนะแบบกินต่อเนื่อง 10-14 วัน หากผู้ป่วยไม่ตอบสนองต่อการรักษา ควรส่งตรวจ เพิ่มเติมเรื่องการอุดกั้นระบบทางเดินปัสสาวะหรือภาวะแทรกซ้อนอื่นจากการติดเชื้อ เช่น perinephric abscess เป็นต้น
หญิงตั้งครรภ์ที่ได้รับการรักษาควรได้รับการส่งตรวจเพิ่มเติมดังนี้ Urine culture, CBC Hemoculture, Cr, Electrolye, และอาจส่ง film chest x-ray ถ้าผู้ป่วยมีอาการเหนื่อยร่วมด้วย
การวินิจฉัยแยกโรค
- Chorioamnionitis
- Appendicitis
- Placenta abruption
- Infarcted leiomyoma
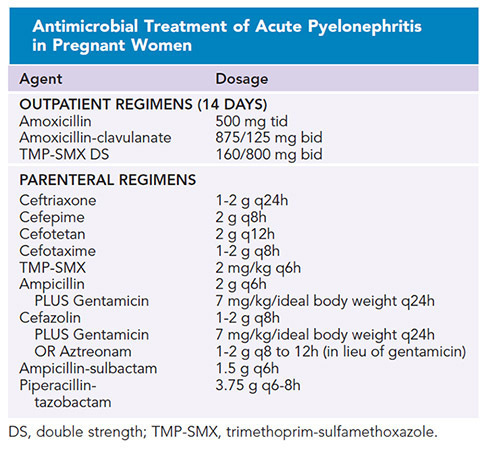
รูปที่ 3 แสดงการพิจารณาใช้ยาปฏิชีวนะสำหรับ Acute pyelonephritis
(ที่มา :Creasy and Resnik’s. Chapter 51, Maternal and fetal infection; p.813-820)
การติดตามอาการ
หลังการได้รับการรักษา 24-48 ชั่วโมง ผู้ป่วยควรได้รับการส่งตรวจเลือดซ้ำ ได้แก่ CBC, Cr, Electrolyte เพื่อประมินผลการรักษาร่วมกับการสังเกตอาการผู้ป่วย หากได้รับการพิจารณา ให้กลับบ้านควรนัดผู้ป่วยมาติดตามอาการและเก็บปัสสาวะส่งตรวจการเพาะเชื้อซ้ำอีกครั้งภายใน 1-2 สัปดาห์
อย่างไรก็ตาม หญิงตั้งครรภ์ส่วนหนึ่งมีกรวยไตติดเชื้อซ้ำซ้อนได้ร้อยละ 6-8 จึงแนะนำให้ยาปฏิชีวนะ เพื่อควบคุมตลอดการตั้งครรภ์ ได้แก่ Nitrofurantoin ขนาด 50-100 mg หรือ Cephalexin ขนาด 250-500 mg รับประทานก่อนนอน
เอกสารอ้างอิง
- William Obstetrics. 25th ed. Chapter 53, Renal and urinary tract disorder; p 1026-30.
- Creasy and Resnik’s. Chapter 51, Maternal and fetal infection; p.813-820.
- Little PJ. The incidence of urinary infection in 5000 pregnant women. Lancet 1966; 2:925-8.
- New England Journal Medicine. 2012 Mar15; 366(11):1028-37.
- Moore A, Doull M, Grad R, et al. Recommendations on screening for asymptomatic bacteriuria in pregnancy. CMAJ. 2018;190(27):E823–E830.
- Szweda H, Jóźwik M. Urinary tract infections during pregnancy – an updated overview. Dev Period Med. 2016;20(4):263–72.
- Wing DA, Fassett MJ, Getahun D. Acute pyelonephritis in pregnancy: an 18-year retrospective analysis. Am J Obstet Gynecol. 2014;210(3):219. e1-219.e6.
- McCormick, T. , Ashe, R. G. and Kearney, P. M. (2008), Urinary tract infection in pregnancy. The Obstetrician & Gynaecologist, 10: 156-162.
- Lindsay E Nicolle, Kalpana Gupta, Suzanne F Bradley, Richard Colgan, Gregory P DeMuri, Dimitri Drekonja, Linda O Eckert, Suzanne E Geerlings, Béla Köves, Thomas M Hooton, Manisha Juthani-Mehta, Shandra L Knight, Sanjay Saint, Anthony J Schaeffer, Barbara Trautner, Bjorn Wullt, Reed Siemieniuk, Clinical Practice Guideline for the Management of Asymptomatic Bacteriuria: 2019 Update by the Infectious Diseases Society of America, Clinical Infectious Diseases, Volume 68, Issue 10, 15 May 2019, Pages e83–e110