Current Management of Gestational Trophoblastic Neoplasia
พญ.อสมา วาณิชตันติกุล
ศ.นพ.จตุพล ศรีสมบูรณ์
Gestational trophoblastic neoplasms (GTN) เป็นโรคที่เกิดจากการเจริญแบ่งตัวผิดปกติของเซลล์เนื้อรก (placental villous and extravillous trophoblast) ซึ่งแบ่งตามลักษณะทางพยาธิวิทยาคลินิก ออกเป็น 4 ชนิด ได้แก่ (1)
- Invasive mole แบ่งออกเป็น complete hydatidiform mole (CHM) หรือ partial hydatidiform mole (PHM)
- Choriocarcinoma (CCA)
- Placental-site trophoblastic tumor (PSTT)
- Epithelioid trophoblastic tumor (ETT)
Invasive mole และ CCA เป็นลักษณะที่พบบ่อยของมะเร็งชนิดนี้ ซึ่งมักจะตรวจพบค่า human chorionic gonadotropin (hCG) สูง และมักตอบสนองดีต่อยาเคมีบำบัด ในขณะที่ PSTT และ ETT พบน้อย ตรวจพบค่า hCG น้อยกว่า แต่มักไม่ค่อยตอบสนองต่อยาเคมีบำบัด ดังนั้นจึงนิยมให้ยาเคมีบำบัดเฉพาะกรณีที่มะเร็งมีการกระจายไปแล้วเท่านั้น (1)
PATHOLOGY
Invasive mole
- เกิดจากการที่ molar villi มีขนาดใหญ่ มีการแบ่งตัวจำนวนมากและทะลุเข้าชั้นกล้ามเนื้อมดลูก (myometrium)
- Complete hydatidiform mole (CHM) จะกลายเป็นมะเร็งในมดลูก (local invasion) 15% และมีการแพร่กระจาย (metastases) 5% ซึ่งเป็นการกระจายโดยตรง (direct extension) ผ่านทางเส้นเลือดดำ (venous channels) (2)
- Partial hydatidiform mole (PHM) กลายเป็นมะเร็งเพียง 3 – 5% ซึ่งส่วนใหญ่จะอยู่เฉพาะที่มดลูก(2)
- การวินิจฉัย postmolar GTN ขึ้นกับระดับ hCG มากกว่าพยาธิวิทยา (การวินิจฉัยภาวะนี้จากการขูดมดลูกมักทำได้ยากเพราะมีส่วนน้อยที่จะพบการลุกลามของ chorionic villi เข้าไปในกล้ามเนื้อมดลูก) ดังนั้นสามารถรักษาด้วยยาเคมีบำบัดได้โดยไม่จำเป็นต้องวินิจฉัยจากพยาธิวิทยา (histopathology)
Choriocarcinoma (CCA)
- ทางพยาธิวิทยาจะพบลักษณะ hyperplastic และ anaplastic syncytioblasts/cytotrophoblasts ไม่มี chorionic villi, hemorrhage หรือ tissue necrosis (1)
- มีการกระจายแบบ direct invasion ผ่าน vascular channels มักกระจายไปที่ปอด ปีกมดลูก ช่องคลอด ตับ ไต ลำไส้เล็ก
- พบว่าประมาณ 50% ของ choriocarcinoma เกิดตามหลังครรภ์ไข่ปลาอุก, 25% เกิดตามหลังการแท้งบุตรหรือท้องนอกมดลูก และ 25% เกิดตามหลังการตั้งครรภ์ปกติ(3) โดยมะเร็งเนื้อรกที่เกิดตามหลังครรภ์ที่ไมใช่ครรภ์ไข่ปลาอุกมักมีการพยากรณ์โรคแย่กว่า และเกือบทั้งหมดผลทางพยาธิวิทยาเป็น choriocarcinoma
Placental-site trophoblastic tumor (PSTT)
- เป็นมะเร็งชนิดที่พบได้น้อยมาก สาเหตุเกิดจาก placental implantation และประกอบไปด้วย mononuclear intermediate trophoblasts โดยไม่มี chorionic villi ที่ทะลุเข้าชั้น myometrium (1)
- ทางพยาธิวิทยาจะพบลักษณะ deep myometrial invasion, high mitotic index, coagulative tumor necrosis และ tumor cell with clear cytoplasm(4) การย้อม immunohistochemical staining แสดงลักษณะ diffuse ของ cytokeratin และ human placental lactogen (hPL) ส่วน hCG พบเพียงเฉพาะจุด (focal) เท่านั้น (1)
- การกระจายมักเป็น lymphatic metastases ไม่สัมพันธ์กับ vascular invasion, necrosis หรือ hemorrhage เหมือน CCA
- เนื้องอกชนิดนี้สร้าง hCG ปริมาณน้อย ทำให้ตรวจพบได้ช้าและมักพบก้อนขนาดใหญ่ โดยพบว่าส่วนใหญ่จะมีเนื้องอกอยู่ที่มดลูก โดยมีการแพร่กระจายประมาณ 30% และมักไม่ค่อยตอบสนองต่อยาเคมีบำบัด
Epithelioid trophoblastic tumor (ETT)
- ETT เป็นอีกภาวะหนึ่งของ PSTT ที่พบได้ไม่บ่อย
- เจริญมากจาก neoplastic transformation ของ chorionic-type extravillous trophoblast ซึ่ง ETT มีลักษณะคล้ายกับ PSTT คืออาจเกิดตามหลังการคลอดครบกำหนดหลายปีได้(5, 6)
CLINICAL PRESENTATION
GTN มีการแสดงออกทางคลินิกที่หลากหลายขึ้นอยู่กับการตั้งครรภ์ การกระจายของโรคและลักษณะทางพยาธิวิทยา
Postmolar GTN
(มักเป็น invasive mole, หรืออาจเป็น CCA) เป็นลักษณะที่พบได้บ่อย หลังการตั้งครรภ์ไข่ปลาอุกที่มีมดลูกโต กว่าอายุครรภ์และระดับ hCG สูงกว่า 100,000 mIU/mL โดยมักมีมดลูกขนาดใหญ่ ส่วนใหญ่มีเลือดออกทางช่องคลอดและอาจตรวจพบรังไข่ขนาดใหญ่ขึ้นได้ (มักพบในกรณีที่ระดับ hCG สูง) โดย การวินิจฉัย postmolar GTN ถือตาม FIGO ดังนี้
The Cancer Committee of the International Federation of Gynecologists and Obstetricians (FIGO) (7)
- Four values or more of hCG plateaued over at least 3 weeks
- An increase in hCG of 10% or greater for 3 or more values over at least 2 weeks
- The histologic diagnosis of CCA
- Persistence of hCG 6 months after molar evacuation
Choriocarcinoma
Non-metastasis : เลือดออกผิดปกติทางช่องคลอด, theca lutein cysts, มดลูกยังคงมีขนาดใหญ่ (subinvolution)
Metastasis : มะเร็งเนื้อรกแพร่กระจายได้อย่างรวดเร็วทางหลอดเลือด มักมีลักษณะเลือดมาเลี้ยงมากและเลือดออกง่าย (1)
- Lungs metastasis (80%)
มาด้วยอาการเจ็บหน้าอก ไอ เหนื่อย หายใจลำบาก ไอเป็นเลือด หรือตรวจพบพยาธิสภาพในปอดจากการตรวจรังสีทรวงอก ได้แก่ snowstorm pattern หรือ alveolar pattern, discrete rounded densities, pleural effusion, embolic pattern เป็นต้น
- Vaginal metastasis (30%) มักกระจายมาที่ตำแหน่ง fornices และ suburethral
มาด้วยอาการเลือดออกผิดปกติหรือมีหนองไหลออกทางช่องคลอด ตรวจภายในอาจพบติ่งก้อนแดงๆ มีเส้นเลือดมาเลี้ยงมาก เลือดออกง่าย ดังนั้นไม่มีความจำเป็นต้องตัดชิ้นเนื้อมาตรวจทางพยาธิวิทยา
- Liver metastasis (10%) มักพบในรายที่มะเร็งลุกลามมากแล้ว การพยากรณ์โรคไม่ดี
มาด้วยอาการเจ็บใต้ชายโครงขวาหรือบริเวณลิ้นปี่ เนื่องจากก้อนมะเร็งยืดขยายเยื่อหุ้มตับ
- Brain metastasis (10%) มักพบในกรณีมะเร็งลุกลามมากแล้ว
มาด้วยอาการชัก หมดสติ และความผิดปกติทางระบบประสาทเฉพาะที่
(โดยผู้ป่วยที่มีการแพร่กระจายไปที่สมองเกือบทุกรายจะมีการแพร่กระจายไปที่ปอดหรือช่องคลอดร่วมด้วย)
เนื่องจากการกระจายของโรค ผู้ป่วยจึงอาจมาด้วยอาการที่ไม่ชัดเจนได้ ขึ้นอยู่กับตำแหน่งที่มะเร็งแพร่กระจาย ทำให้ยากต่อการวินิจฉัยและมักทำให้การรักษาล่าช้า ซึ่งมีผลต่อการพยากรณ์โรค ดังนั้น แนะนำให้ตรวจ hCG ในหญิงวัยเจริญพันธ์ทุกรายที่มาด้วยเลือดออกผิดปกติทางช่องคลอดหรือในรายที่พบการกระจายของมะเร็งที่ไม่ทราบสาเหตุ
PSTTs และ ETTs
ผู้ป่วยส่วนใหญ่มักจะเกิดขึ้นตามหลังการตั้งครรภ์ปกตินานหลายปี
- • เลือดออกผิดปกติทางช่องคลอด หรือ ขาดประจำเดือน (amenorrhea) (3) ร่วมกับ ตรวจภายในมดลูกมีขนาดโต
- • Ultrasound พบก้อนในโพรงมดลูก (hyperechoic intrauterine mass) และอาจพบการลุกลามเข้าไปในเนื้อมดลูก
WORKUP
เมื่อวินิจฉัย GTN แล้ว ควรมีการตรวจเพิ่มเติมเพื่อหาการกระจายของโรค เพื่อประเมินระยะของโรคตาม anatomic staging system (FIGO) และ prognostic scoring system (WHO) (7, 8)
- ซักประวัติ, ตรวจร่างกายละเอียด, เจาะระดับ hCG ในเลือด, เจาะ CBC, hepatic และ renal function test
- ตรวจลักษณะทางพยาธิวิทยาซ้ำ (Review of all available pathologic specimens)
- Pelvic ultrasonography เพื่อประเมินการกระจายและลักษณะของ uterine involvement เพื่อประเมินความเสี่ยงต่อการเกิด uterine perforation และประโยชน์จาก tumor-debulking hysterectomy
- Chest radiograph เพื่อประเมินการกระจายไปที่ปอด หรืออาจพิจารณาส่งตรวจ computed tomography (CT) scan เนื่องจาก 40% ของผู้ป่วยที่ CXR ปกติ สามารถพบการกระจายไปที่ปอดจาก CT scan ได้ อย่างไรก็ตามการตรวจรอยโรคที่ซ่อนอยู่นั้นไม่มีผลต่อการเปลี่ยนแผนการรักษา
* ในรายที่ตรวจไม่พบการกระจายไปที่ปอด ไม่มีความจำเป็นต้อง imaging ของอวัยวะอื่นๆ เนื่องจากโอกาสเกิด distant metastases น้อยมาก (1)
- Magnetic resonance imaging (MRI) of the brain and abdominopelvic CT scan เพื่อหาการกระจายของโรคไปที่สมอง ตับและอวัยวะในช่องท้อง ซึ่งแนะนำในกรณีที่มีการกระจายไปที่ปอดแล้วเท่านั้น(1)
- ขูดมดลูกซ้ำอีกครั้งเมื่อมี excessive uterine bleeding ที่สัมพันธ์ retained molar tissue
- Cerebrospinal fluid : plasma hCG ratio อาจช่วยประเมิน cerebral involvement(1)
* แนะนำให้ตรวจตามข้อ 1-4 ในผู้ป่วย GTN ทุกราย (สำหรับข้อ 5-7 ให้พิจารณาเป็นรายๆ ไป)
STAGING AND RISK ASSESSMENT
1. FIGO staging : Anatomical classification
2. Modified WHO Prognostic Scoring System
3. Hammond / The National Cancer Institute (NCI) classification(9) : Clinical classification
ในปี 2002 ได้มีการรวม anatomic staging และ and modified WHO risk-factor scoring system ในการ staging GTN (สำหรับ PSTTs และ ETTs มีการแบ่งระยะที่แตกต่างออกไป) (7, 8)

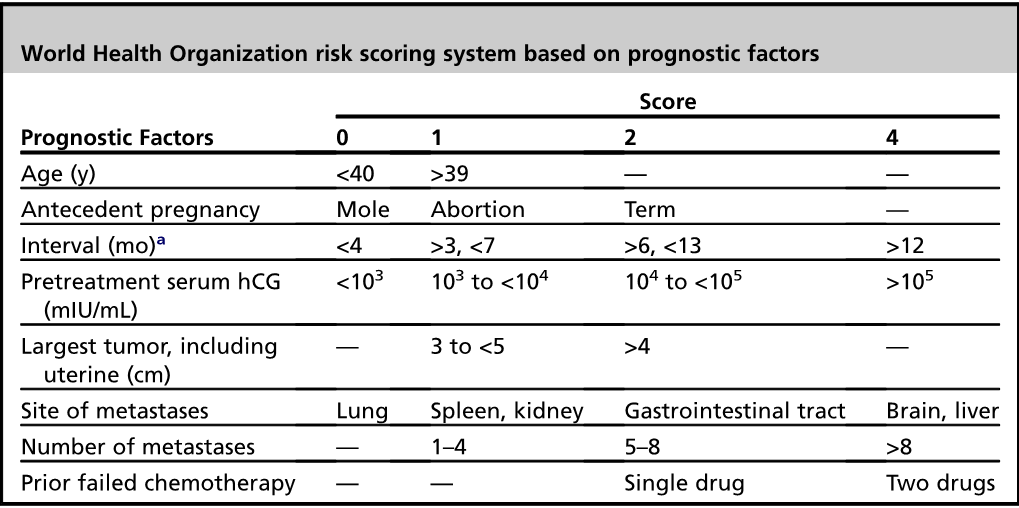
a : Interval (in months) between end of antecedent pregnancy (where known) or onset of symptoms
MANAGEMENT
การรักษา GTN ขึ้นอยู่กับ WHO risk score ซึ่งเป็นตัวบอกความเสี่ยงในการเกิดการดื้อยา
- WHO scores < 7 ถือเป็นกลุ่มที่มีความเสี่ยงต่ำ (low risk)
- WHO scores > 7 ถือเป็นผู้ที่มีความเสี่ยงสูง (high risk)
- ผู้ป่วยที่เป็น nonmetastatic disease (Stage I) หรือ low-risk metastatic GTN (Stages II and III, score <7) สามารถเริ่มต้นรักษาด้วย single-agent chemotherapy โดยมี cure rates ประมาน 80-90%(1)
- ผู้ป่วยที่เป็น high-risk metastatic disease (Stage IV and Stages II–III with scores > 7) แนะนำให้รักษาด้วยยาหลายชนิด(multiagent chemotherapy) จึงจะมี cure rates ประมาน 80-90% เท่ากันโดยอาจพิจารณา adjuvant radiation หรือ surgery ร่วมด้วย(1)
อย่างไรก็ตาม มีรายงาน(10) ในผู้ป่วย low-risk GTN ที่มีก้อนขนาดใหญ่, hCG levels มากกว่า 100,000 mIU/mL หรือมี prognostic scores 5 – 6 สัมพันธ์กับการเพิ่มความเสี่ยงในการเกิดการดื้อยา ดังนั้นอาจเริ่มต้นด้วย multiagent chemotherapy
TREATMENT OF LOW-RISK GTN (1, 11-13)
Single-agent chemotherapy (ดังตาราง)

GTN กลุ่มที่มีความเสี่ยงต่ำ แนะนำรักษาด้วยยาเคมีบำบัด 1 ชนิด อาจพิจารณาให้ methotrexate (MTX) หรือ actinomycin-D (actD) ในกรณีที่ไม่หายขาดก็ยังสามารถรักษาโดยการเปลี่ยนชนิดยาเคมีบำบัดหรือใช้ยาเคมีบำบัดร่วมกันหลายชนิด (combination chemotherapy)
การให้ยา single agent chemotherapy มีหลาย protocols (ดังตาราง) โดยผลการรักษาส่วนใหญ่ใกล้เคียงกัน โดย primary remission rates ขึ้นกับขนาดยา, ระยะเวลาการให้ยา, วิธีการให้ยา และการเลือกผู้ป่วยที่เหมาะสม (1) อย่างไรก็ตามผู้ป่วย low-risk GTN ทุกคนที่ได้รับการรักษาอย่างถูกต้องมีโอกาสหายขาดเกือบ 100%(1)
การให้ MTX ทุกสัปดาห์หรือ actD ทุก 2 สัปดาห์ พบว่ามีประสิทธิภาพด้อยกว่าการให้ 5-day Mtx / actD regimens หรือ 8-day Mtx/FA protocol (1) สำหรับการเลือกใช้ยา 1st line chemotherapy ในผู้ป่วย low-risk GTN นั้น จาก Cochrane review 2009(13) พบว่า pulse actinomycin-D มีประสิทธิภาพดีกว่า Mtx weekly (โดยแนะนำให้ศึกษาเปรียบเทียบกับ 8-day Mtx/FA protocol ต่อไป) อย่างไรก็ตามจากการศึกษาล่าสุดที่ New England Trophoblastic Disease Center (NETDC) (14, 15) พบว่า 8-day Mtx/FA protocol มีประสิทธิภาพและมีความคุ้มค่ามากกว่า 5-day actD regimens นอกจากนี้การให้ MTX ยังมีผลข้างเคียงน้อยกว่า actinomycin-D ในเรื่องการคลื่นไส้/อาเจียนรุนแรง, ผมร่วง และผื่นคันตามตัว อย่างไรก็ตาม actinomycin-D แนะนำให้ในผู้ป่วยที่มีปัญหาเรื่องตับผิดปกติหรือมีประวัติว่ามีผลข้างเคียงจาก MTX มากหรือเคยดื้อต่อ MTX เป็นต้น(1, 12) โดยทั่วไปการรักษาจะให้ต่อเนื่องห่างกันทุก 2-3 สัปดาห์ จนกว่าจะวัดระดับ hCG ไม่ได้ 3 สัปดาห์ติดต่อกัน อย่างไรก็ตาม ในผู้ป่วย Stage I GTN ที่ FIGO scores ต่ำ (<3) ถ้าสามารถตรวจติดตามอย่างใกล้ชิดได้ อาจไม่จำเป็นต้องให้ยาต่อในกรณี hCG ลดลงมากกว่า 1 log ภายในเวลา 18 วัน (1, 12) ทั้งนี้เพื่อให้ผู้ป่วยได้รับผลข้างเคียงจากยาน้อยที่สุดในขณะที่ได้รับการรักษาที่มีประภาพมากที่สุด
ในกรณีที่ผู้ป่วยมีประวัติดื้อยาหรือดื้อยา single-agent อาจเริ่มให้ยา multiagent therapy ได้แก่ MAC (Mtx, actD, cyclophosphamide) หรือ EMA/CO (etoposide, Mtx, actD, cyclophosphamide, vincristine) และอาจแนะนำผ่าตัดมดลูกร่วมด้วย สำหรับผู้ป่วยที่ต้องการเก็บมดลูกไว้แนะนำให้ทำ local uterine resection แทน(1, 12) โดยปัจจัยที่มีผลต่อการดื้อยา ได้แก่ การที่มีระดับ hCG เริ่มต้นสูง, เป็น nonmolar pregnancy หรือมี clinicopathologic diagnosis of CCA เป็นต้น(9, 16) สำหรับผู้ป่วยผู้ป่วย low-risk GTN ที่มีก้อนขนาดใหญ่, hCG levels มากกว่า 100,000 mIU/mL หรือมี prognostic scores 5 – 6 อาจเริ่มต้นด้วย multiagent chemotherapy(10)
Hysterectomy
ในผู้ป่วยที่ไม่ต้องการมีบุตรแล้ว แนะนำให้ตัดมดลูกร่วมด้วย ทั้งนี้เพื่อป้องกันและรักษาภาวะแทรกซ้อน ได้แก่ hemorrhage, perforation, หรือ infection เป็นต้น อย่างไรก็ตามการผ่าตัดมดลูกไม่ใช่การรักษาหลัก เนื่องจากยังมีความเสี่ยงของ occult metastasis จึงแนะนำให้ chemotherapy ต่อหลังผ่าตัดทุกราย โดยพบว่าการผ่าตัดมดลูกสามารถลดระยะเวลาการให้ multiagent ในผู้ป่วยที่ดื้อต่อ single-agent therapy (1, 17)
สำหรับการขูดมดลูกซ้ำ (repeat dilatation and curettage) ไม่แนะนำ เนื่องจากเพิ่มความเสี่ยงต่อเลือดออกและการติดเชื้อเพิ่มขึ้น ในขณะที่ไม่ช่วยลดการให้ adjuvant chemotherapy(12)
สรุป ในผู้ป่วย nonmetastatic และ low-risk metastatic GTN มีโอกาสหายขาดเกือบ 100% ถ้ารักษาด้วย single-agent Mtx หรือ actD (หรือ multiagent therapy กรณีที่ดื้อต่อ single-agent therapy) โดยแนะนำ 8-day Mtx/FA protocol อย่างไรก็ตามมีประมาณ 10-30% ของผู้ป่วยกลุ่ม low-risk GTN ที่จะดื้อต่อยา single-agent ซึ่ง 15-20% จำเป็นต้องได้ multiagent therapy ต่อ ได้แก่ MAC หรือ EMA/CO สำหรับการตัดมดลูกนั้นแนะนำในผู้ป่วยที่ไม่ต้องการมีบุตรแล้ว
TREATMENT OF HIGH-RISK GTN
Multiagent chemotherapy
ผู้ป่วย high-risk metastatic GTN (FIGO Stage IV and Stages II–III, score >7) แนะนำเริ่มรักษาด้วย multiagent chemotherapy ได้แก่ MAC, EMA/CO, EMA-EP เป็นต้น (ดังตาราง)
ในช่วงปี 1970-1980 แนะนำ MAC regimen เป็น first-line multiagent treatment ซึ่งมี cure ประมาน 50-71%.(1, 18)หลังจากนั้น พบว่า EMA/CO regimen แนะนำมากกว่า เนื่องจาก remission rate 80-90%(1, 19, 20) ดังนั้นจึงแนะนำ EMA/CO regimen เป็น first-line drug อย่างไรก็ตามการใช้ etoposide อาจเพิ่มความเสี่ยงต่อมะเร็งชนิดอื่น ได้แก่ leukemia, breast cancer, colon cancer หรือ melanoma ตามมาได้ สำหรับกรณีที่มีการดื้อยากลุ่ม EMA/CO แนะนำให้ใช้ EMA/EP regimen (etoposide, Mtx, actD, cisplatin/carboplatin และ etoposide) อย่างไรก็ตาม การให้ยาหลายชนิดร่วมกันอาจเกิดผลข้างเคียงจากยาได้ ดังนั้นแนะนำตรวจติดตามเป็นระยะระหว่างรักษา
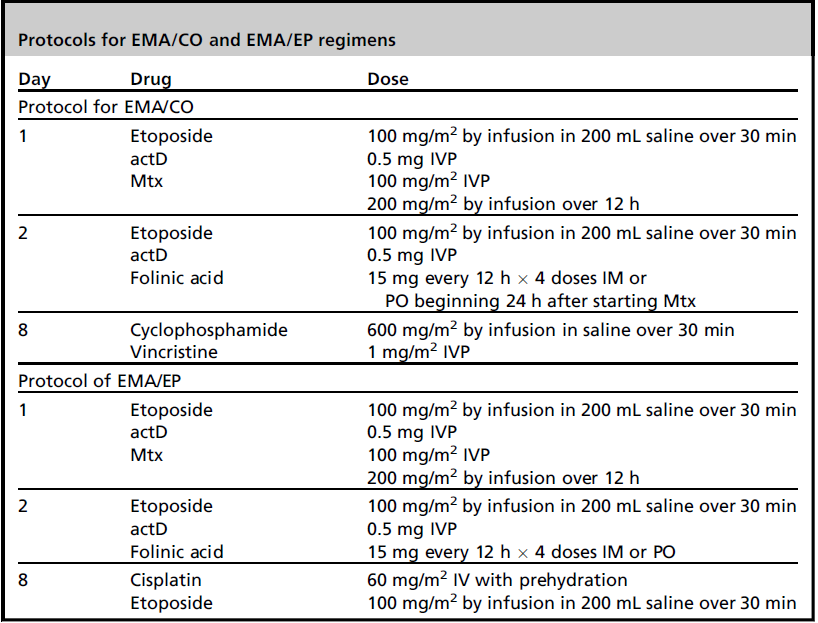
MAINTENANCE CHEMOTHERAPY
หลังจากการรักษาด้วยยาเคมีบำบัดจนระดับ hCG ลดลงมาในระดับปกติ จำเป็นต้องให้ยาเคมีบำบัดต่อไปอีกเพื่อให้แน่ใจว่าหายขาดและไม่กลับเป็นซ้ำอีก เนื่องจากการที่ระดับของ hCG <1 หน่วย/ลิตร ไม่ได้แสดงว่าผู้ป่วยหายขาด (complete remission)
หลักการให้ maintenance chemotherapy (21)
Nonmetastatic GTT (ระยะที่ 1) : ให้ยาเคมีบำบัดต่ออีก 1 รอบ
มะเร็งไข่ปลาอุกแบบความเสี่ยงต่ำ (คะแนน < 7) : ให้ยาเคมีบำบัดต่ออีก 2 รอบ
มะเร็งไข่ปลาอุกแบบความเสี่ยงสูง (คะแนน >7) : ให้ยาเคมีบำบัดต่ออีก 3 รอบ
MANAGEMENT OF STAGE IV GTN AND METASTASES(1, 12)
สำหรับผู้ป่วยกลุ่ม stage IV GTN เริ่มต้นรักษาด้วย multiagent chemotherapy ทุกราย โดยแนะนำ EMA/CO เป็นหลัก และอาจฉายแสงหรือผ่าตัดเพิ่มเติมเป็นรายๆไป
CENTRAL NERVOUS SYSTEM METASTASES
- Chemotherapy : แนะนำ EMA/CO หรือ EMA/EP regimen โดยแนะนำเพิ่มขนาด Mtx ในวันแรกเป็น 1 g/m2 เพื่อเพิ่มยาผ่าน blood-brain barrier(1, 12, 22)
- Whole brain irradiation (3000 cGy in 200 cGy fractions) : NETDC แนะนำในผู้ป่วย GTN ที่ brain metastasis ทุกราย
- Surgical excision : แนะนำในกรณีที่รอยโรคเป็นก้อนเดี่ยว(solitary) และอยู่ด้านข้าง(peripheral)(22, 23) โดยผู้ป่วยส่วนใหญ่ที่รักษาหายเป็นผู้ป่วยที่ไม่มี residual tumor เหลืออยู่
PULMONARY METASTASES
• Surgery : ในการรักษา solitary pulmonary nodules แนะนำการผ่าตัดร่วมกับยาเคมีบำบัด โดยเฉพาะกรณีที่พบว่ามีการดื้อต่อการให้ยาเคมีบำบัดแล้ว(24-26) มีรายงานพบว่า(26) ผู้ที่สามารถผ่าตัดได้, primary malignancy ที่ควบคุมได้ดี, ไม่มี metastatic ที่อื่น, pulmonary metastasis ที่ปอดเพียงข้างเดียวและระดับ hCG <1,000 mIU/mL มีการตอบสนองดีต่อ pulmonary resection ถึง 90% นอกจากนี้การตรวจไม่พบ hCG ใน 2 สัปดาห์หลังผ่าตัด มีผลการรักษาดี อย่างไรก็ตามแม้ว่า pulmonary resection อาจมีประโยชน์ แต่ thoracotomy มักไม่จำเป็น เนื่องจากรอยโรคที่ปอดส่วนใหญ่มักตอบสนองดีต่อยาเคมีบำบัด(24, 25, 27)
HEPATIC METASTASES
ในผู้ป่วยที่มีการกระจายของโรคไปที่ตับ การให้ยาเคมีบำบัดเพียงอย่างเดียวตอบสนองค่อนข้างดี (1) การผ่าตัดแนะนำเฉพาะในรายที่มีปัญหา acute bleeding หรือมีรอยโรคด้านข้าง (peripheral lesion) ที่ดื้อยา สำหรับ hepatic arterial occlusion ด้วย embolization มีประโยชน์ในแง่ของ hemorrhage แต่ผลการรักษากรณีดื้อยาไม่ชัดเจน (1)
MANAGEMENT OF COMPLICATIONS
ในผู้ป่วยที่มาด้วยอาการของภาวะแทรกซ้อนจากตัวโรคซึ่งอาจมีความจำเป็นต้องรีบผ่าตัดหรือฉายรังสี โดยภาวะที่พบบ่อยที่สุดคือเลือดออกมาจากมดลูก ดังนั้นแนะนำผ่าตัดมดลูก (Hysterectomy) ในภาวะดังกล่าวเพื่อควบคุมเลือดออกและการติดเชื้อตามมา(1, 28)
การกระจายไปที่ช่องคลอด รอยโรคมักมีเลือดมาเลี้ยงมากจึงเลือดออกได้ง่าย แนะนำ vaginal packing เพื่อหยุดเลือด อาจพิจารณา wide local excision หรือ angiographic embolization of hypogastric vessels(12)
สำหรับภาวะเลือดออกที่ตับ อาจพิจารณาผ่าตัด (Hepatic resection) หรือ embolization(1)
MANAGEMENT OF RECURRENT AND CHEMORESISTANT GTN
Chemoresistant disease มักเกิดในผู้ป่วย Stage IV หรือ high-risk Stage III GTN โดยพบว่ามีผู้ป่วยเกือบ 40% ตอบสนองไม่ดี (incomplete response) ต่อ first-line chemotherapy หรือมีการกลับเป็นซ้ำหลังหายจากโรค (relapse after remission) (29-31) มีการศึกษา(32) พบว่า ในผู้ป่วย high-risk disease มีการกลับเป็นซ้ำ (recurrence rates) ถึง 13% และจาก NETDC(8) พบว่าการกลับเป็นซ้ำใน stage I-IV GTN เป็น 2.9, 8.3, 4.3 และ 9.1% ตามลำดับ โดยการกลับเป็นซ้ำอาจมาด้วยอาการที่มะเร็งมีการกระจายไปที่ต่างๆ ซึ่งอาจมีความจำเป็นต้องแบ่งระยะของโรคใหม่ สำหรับการรักษา นอกเหนือจากการให้ยาเคมีบำบัด อาจผ่าตัดหรือฉายรังสีร่วมด้วย (multimodality treatment) ยาเคมีบำบัดที่นิยมใช้กรณีที่มีการกลับเป็นซ้ำ ได้แก่ EMA/EP, TP/TE (paclitaxel, etoposide, และ cisplatin), PVB (cisplatin, vinblastine, and bleomycin) เป็นต้น(1)
โดยสรุป พบว่า cure rates ของ high-risk GTN ประมาน 80-90% ซึ่งโดยส่วนใหญ่ตอบสนองดีต่อการรักษาด้วย multimodal therapy คือการให้ยาเคมีบำบัด ร่วมกับการผ่าตัดหรือฉายรังสี โดยสูตร EMA/CO เป็นสูตรที่นิยมนำมาใช้ก่อน เนื่องจากผลข้างเคียงน้อย, โอกาสหาย (complete response rates) สูง และอัตราการอยู่รอด (overall survival) สูง(33) อย่างไรก็ตาม พบว่า มีประมาณ 20% ที่ไม่ตอบสนองต่อการรักษาด้วย EMA/CO ดังนั้นแนะนำให้ EMA/EP ต่อไป(33)
MANAGEMENT OF PSTT AND ETT
การรักษาผู้ป่วย PSTT และ ETT ใกล้เคียงกับการรักษา GTN ทั่วไป แต่แนะนำการตัดมดลูก (Hysterectomy) the first-line treatment มากกว่าการให้ยาเคมีบำบัด ในผู้ป่วย PSTT/ETT ที่เป็น nonmetastatic disease เนื่องจากมะเร็งชนิดนี้มักดื้อต่อการรักษาด้วยยาเคมีบำบัด (relatively chemoresistant)(1, 12)
Hysterectomy
แนะนำให้ผ่าตัดมดลูกทุกราย โดยการผ่าตัด แนะนำให้ทำ surgery pelvic lymph nodes sampling ร่วมด้วย เนื่องจากมะเร็งชนิดนี้มีการกระจายผ่านทางน้ำเหลือง (lymphatic spread) ซึ่งแตกต่างจาก CCA ที่ผ่านทางหลอดเลือด โดยอัตราการอยู่รอด (survival rate) ของผู้ป่วย nonmetastatic disease กลุ่มนี้ ที่รักษาด้วยการตัดมดลูกอย่างเดียว สูงเกือบ 100% อย่างไรก็ตาม กรณี metastatic disease แนะนำ multiagent chemotherapy ร่วมด้วย (34-36)
Chemotherapy
กรณี metastatic disease แนะนำ multiagent chemotherapy ร่วมด้วย โดยปัจจัยที่มีโอกาสเกิดการกระจาย ได้แก่ ผู้ป่วย ที่มีระยะห่างจากการตั้งครรภ์เป็นเวลานานกว่า 2 ปี, มี deep myometrial invasion, tumor necrosis, และ mitotic count > 6/10 hpf เป็นต้น ยาเคมีบำบัดที่แนะนำ คือ platinum-containing regimen ได้แก่ EMA/EP ซึ่งมี survival rates สูงถึง 50-60%.(36, 37)
FOLLOW-UP AFTER TREATMENT OF GTN
Serum hCG(12)
หลังจากให้ยาเคมีบำบัดจนระดับ hCG ลงมาสู่ระดับปกติและผู้ป่วยได้รับยาเคมีบำบัดแบบ maintenance ตามคำแนะนำแล้วให้ตรวจหาระดับ hCG ทุกสัปดาห์ จนกระทั่งปกติ 3 สัปดาห์ติดต่อกัน หลังจากนั้นให้ตรวจทุกเดือน 12 เดือนติดต่อกัน ใน GTN ระยะที่ 1-3 สำหรับในระยะที่ 4 แนะนำให้ตรวจทุกเดือนนานถึง 24 เดือน (เนื่องจากมีโอกาสกลับเป็นซ้ำสูง) ในระหว่างที่ติดตามการรักษาให้คุมกำเนิดเป็นเวลา 1 ปี โดยทั่วไป โอกาสการกลับเป็นซ้ำในปีแรก ประมาน 3- 9% หลังรักษา ซึ่งพบน้อยมากหลัง 12 เดือน ที่ระดับ hCG กลับสู่ปกติแล้ว
Physician examinations แนะนำให้ตรวจร่างกายทุกๆ 3 เดือน ในช่วงที่ยังตรวจติดตามระดับ hCG
Contraception แนะนำคุมกำเนิด 12 เดือน (ในระยะที่ 1-3) หรือ 24 เดือน (ในระยะที่ 4) โดยแนะนำเป็นยาเม็ดคุมกำเนิด และควรหลีกเลี่ยง Intrauterine devices จนกว่าจะตรวจไม่พบค่า hCG ในเลือด
โอกาสเกิด GTN ในครรภ์หน้า ประมาน 1- 2% ดังนั้นจึงแนะนำ pelvic ultrasound ในครรภ์ถัดไป ที่อายุครรภ์ประมาน 10 สัปดาห์ นอกจากนี้ในกรณีที่ครรภ์ถัดไปเป็นการแท้ง แนะนำให้ตรวจชิ้นเนื้อโดย pathologist ร่วมด้วย
SUBSEQUENT PREGNANCY
ผู้ป่วยที่มีประวัติ molar pregnancy หรือ GTN อุบัติการณ์ของภาวะมีลูกยากไม่ได้สูงขึ้น โดยทั่วไปจะสามารถตั้งครรภ์ใหม่ได้ตามปกติ แต่มีความเสี่ยงต่อการเกิดครรภ์ไข่ปลาอุกซ้ำ 1 – 2% (จาก ปกติ 1 ใน 1000) แม้จะเปลี่ยนคู่ครองก็ตาม(38) กรณีที่มีการตั้งครรภ์เกิดขึ้นในช่วง 1 ปีแรกที่ตรวจติดตาม ซึ่งจะตรวจพบระดับ hCG สูงขึ้น ควรตรวจ ultrasound โดยเร็ว เพื่อแยกสาเหตุการตั้งครรภ์ใหม่กับการกลับเป็นซ้ำ อย่างไรก็ตาม มีรายงาน(39) พบว่า การตั้งครรภ์ภายใน 6 เดือนหลัง remission จะเพิ่มความเสี่ยงต่อการเกิด spontaneous miscarriages, stillbirths และการเกิด moles ซ้ำได้สูงขึ้น สำหรับทารกที่เกิดจากมารดาที่เคยได้รับยาเคมีบำบัดในการรักษา GTT มาก่อน มีรายงานพบว่าความพิการโดยกำเนิดหรือโครโมโซมผิดปกติไม่ได้สูงขึ้นอย่างมีนัยสำคัญ การพัฒนาการด้านสติปัญญาและการเจริญเติบโตไม่แตกต่างจากเด็กทั่วไป(4)
PSYCHOSOCIAL CONSEQUENCES OF GTN
ผู้ป่วย GTN ส่วนใหญ่มีอายุน้อย มักมีปัญหา mood disturbance, ปัญหาคู่ครอง, ปัญหาเรื่องเพศสัมพันธ์ และความกังวลเกี่ยวกับการตั้งครรภ์ครั้งหน้าได้มากขึ้น(40) ดังนั้นควรให้กำลังใจและทำให้ผู้ป่วยมั่นใจว่าการรักษาและการตรวจติดตามอย่างสม่ำเสมอมีโอกาสหายขาดได้สูง
REFERENCES
- Goldstein DP, Berkowitz RS. Current management of gestational trophoblastic neoplasia. Hematol Oncol Clin North Am. Feb;26(1):111-31.
- Berkowitz RS, Goldstein DP. Clinical practice. Molar pregnancy. N Engl J Med. 2009 Apr 16;360(16):1639-45.
- Baergen RN, Rutgers JL, Young RH, Osann K, Scully RE. Placental site trophoblastic tumor: A study of 55 cases and review of the literature emphasizing factors of prognostic significance. Gynecol Oncol. 2006 Mar;100(3):511-20.
- Berkowitz RS, Im SS, Bernstein MR, Goldstein DP. Gestational trophoblastic disease. Subsequent pregnancy outcome, including repeat molar pregnancy. J Reprod Med. 1998 Jan;43(1):81-6.
- Allison KH, Love JE, Garcia RL. Epithelioid trophoblastic tumor: review of a rare neoplasm of the chorionic-type intermediate trophoblast. Arch Pathol Lab Med. 2006 Dec;130(12):1875-7.
- Shih IM, Kurman RJ. Epithelioid trophoblastic tumor: a neoplasm distinct from choriocarcinoma and placental site trophoblastic tumor simulating carcinoma. Am J Surg Pathol. 1998 Nov;22(11):1393-403.
- Kohorn EI. Negotiating a staging and risk factor scoring system for gestational trophoblastic neoplasia. A progress report. J Reprod Med. 2002 Jun;47(6):445-50.
- Goldstein DP, Zanten-Przybysz IV, Bernstein MR, Berkowitz RS. Revised FIGO staging system for gestational trophoblastic tumors. Recommendations regarding therapy. J Reprod Med. 1998 Jan;43(1):37-43.
- Hammond CB, Borchert LG, Tyrey L, Creasman WT, Parker RT. Treatment of metastatic trophoblastic disease: good and poor prognosis. Am J Obstet Gynecol. 1973 Feb 15;115(4):451-7.
- Lurain JR. Pharmacotherapy of gestational trophoblastic disease. Expert Opin Pharmacother. 2003 Nov;4(11):2005-17.
- Aghajanian C. Treatment of low-risk gestational trophoblastic neoplasia. J Clin Oncol. Mar 1;29(7):786-8.
- May T, Goldstein DP, Berkowitz RS. Current chemotherapeutic management of patients with gestational trophoblastic neoplasia. Chemother Res Pract.2011:806256.
- Alazzam M, Tidy J, Hancock BW, Osborne R. First line chemotherapy in low risk gestational trophoblastic neoplasia. Cochrane Database Syst Rev. 2009(1):CD007102.
- Growdon WB, Wolfberg AJ, Goldstein DP, Feltmate CM, Chinchilla ME, Lieberman ES, et al. Evaluating methotrexate treatment in patients with low-risk postmolar gestational trophoblastic neoplasia. Gynecol Oncol. 2009 Feb;112(2):353-7.
- Petrilli ES, Morrow CP. Actinomycin D toxicity in the treatment of trophoblastic disease: a comparison of the five-day course to single-dose administration. Gynecol Oncol. 1980 Feb;9(1):18-22.
- Hammond CB, Soper JT. Poor-prognosis metastatic gestational trophoblastic neoplasia. Clin Obstet Gynecol. 1984 Mar;27(1):228-39.
- Hammond CB, Weed JC, Jr., Currie JL. The role of operation in the current therapy of gestational trophoblastic disease. Am J Obstet Gynecol. 1980 Apr 1;136(7):844-58.
- DuBeshter B, Berkowitz RS, Goldstein DP, Cramer DW, Bernstein MR. Metastatic gestational trophoblastic disease: experience at the New England Trophoblastic Disease Center, 1965 to 1985. Obstet Gynecol. 1987 Mar;69(3 Pt 1):390-5.
- Bolis G, Bonazzi C, Landoni F, Mangili G, Vergadoro F, Zanaboni F, et al. EMA/CO regimen in high-risk gestational trophoblastic tumor (GTT). Gynecol Oncol. 1988 Nov;31(3):439-44.
- Bower M, Newlands ES, Holden L, Short D, Brock C, Rustin GJ, et al. EMA/CO for high-risk gestational trophoblastic tumors: results from a cohort of 272 patients. J Clin Oncol. 1997 Jul;15(7):2636-43.
- Soper JT, Mutch DG, Schink JC. Diagnosis and treatment of gestational trophoblastic disease: ACOG Practice Bulletin No. 53. Gynecol Oncol. 2004 Jun;93(3):575-85.
- Newlands ES, Holden L, Seckl MJ, McNeish I, Strickland S, Rustin GJ. Management of brain metastases in patients with high-risk gestational trophoblastic tumors. J Reprod Med. 2002 Jun;47(6):465-71.
- Bakri Y, Berkowitz RS, Goldstein DP, Subhi J, Senoussi M, von Sinner W, et al. Brain metastases of gestational trophoblastic tumor. J Reprod Med. 1994 Mar;39(3):179-84.
- Edwards JL, Makey AR, Bagshawe KD. The role of thoracotomy in the management of the pulmonary metastases of gestational choriocarcinoma. Clin Oncol. 1975 Dec;1(4):329-39.
- Fleming EL, Garrett L, Growdon WB, Callahan M, Nevadunsky N, Ghosh S, et al. The changing role of thoracotomy in gestational trophoblastic neoplasia at the New England Trophoblastic Disease Center. J Reprod Med. 2008 Jul;53(7):493-8.
- Tomoda Y, Arii Y, Kaseki S, Asai Y, Gotoh S, Suzuki T, et al. Surgical indications for resection in pulmonary metastasis of choriocarcinoma. Cancer. 1980 Dec 15;46(12):2723-30.
- Wang YA, Song HZ, Xia ZF, Sun CF. Drug resistant pulmonary choriocarcinoma metastasis treated by lobectomy: report of 29 cases. Chin Med J (Engl). 1980 Nov;93(11):758-66.
- Clark RM, Nevadunsky NS, Ghosh S, Goldstein DP, Berkowitz RS. The evolving role of hysterectomy in gestational trophoblastic neoplasia at the New England Trophoblastic Disease Center. J Reprod Med. May-Jun;55(5-6):194-8.
- Ngan HY, Tam KF, Lam KW, Chan KK. Relapsed gestational trophoblastic neoplasia: A 20-year experience. J Reprod Med. 2006 Oct;51(10):829-34.
- Powles T, Savage PM, Stebbing J, Short D, Young A, Bower M, et al. A comparison of patients with relapsed and chemo-refractory gestational trophoblastic neoplasia. Br J Cancer. 2007 Mar 12;96(5):732-7.
- Yang J, Xiang Y, Wan X, Yang X. Recurrent gestational trophoblastic tumor: management and risk factors for recurrence. Gynecol Oncol. 2006 Nov;103(2):587-90.
- Mutch DG, Soper JT, Babcock CJ, Clarke-Pearson DL, Hammond CB. Recurrent gestational trophoblastic disease. Experience of the Southeastern Regional Trophoblastic Disease Center. Cancer. 1990 Sep 1;66(5):978-82.
- Tewari KS, Monk BJ. American Society of Clinical Oncology 2011 Annual Meeting update: summary of selected gynecologic cancer abstracts. Gynecol Oncol. Aug;122(2):209-12.
- Feltmate CM, Genest DR, Goldstein DP, Berkowitz RS. Advances in the understanding of placental site trophoblastic tumor. J Reprod Med. 2002 May;47(5):337-41.
- Palmer JE, Macdonald M, Wells M, Hancock BW, Tidy JA. Epithelioid trophoblastic tumor: a review of the literature. J Reprod Med. 2008 Jul;53(7):465-75.
- Papadopoulos AJ, Foskett M, Seckl MJ, McNeish I, Paradinas FJ, Rees H, et al. Twenty-five years’ clinical experience with placental site trophoblastic tumors. J Reprod Med. 2002 Jun;47(6):460-4.
- Hassadia A, Gillespie A, Tidy J, Everard RGNJ, Wells M, Coleman R, et al. Placental site trophoblastic tumour: clinical features and management. Gynecol Oncol. 2005 Dec;99(3):603-7.
- Garrett LA, Garner EI, Feltmate CM, Goldstein DP, Berkowitz RS. Subsequent pregnancy outcomes in patients with molar pregnancy and persistent gestational trophoblastic neoplasia. J Reprod Med. 2008 Jul;53(7):481-6.
- Matsui H, Iitsuka Y, Suzuka K, Yamazawa K, Tanaka N, Mitsuhashi A, et al. Early pregnancy outcomes after chemotherapy for gestational trophoblastic tumor. J Reprod Med. 2004 Jul;49(7):531-4.
- Cagayan MS, Llarena RT. Quality of life of gestational trophoblastic neoplasia survivors: a study of patients at the Philippine General Hospital trophoblastic disease section. J Reprod Med. Jul-Aug;55(7-8):321-6.
 งานคืนสู่เหย้าชาวสูติฯเชียงใหม่ วันที่ 15-16 มีนาคม 2555 ณ โรงแรมดิเอ็มเพรส เชียงใหม่ ประชุมวิชาการ update quidline in OB&GYN clinical practice 2 วัน และสังสรรค์ในหมู่พี่น้อง 1 คืน เยี่ยมรำลึกถึงพี่ ๆ น้อง ๆ หลากหลายรุ่นได้จากเมนู gallery : วิชาการและงานสังสรรค์วันคืนสู่เหย้าฯ
งานคืนสู่เหย้าชาวสูติฯเชียงใหม่ วันที่ 15-16 มีนาคม 2555 ณ โรงแรมดิเอ็มเพรส เชียงใหม่ ประชุมวิชาการ update quidline in OB&GYN clinical practice 2 วัน และสังสรรค์ในหมู่พี่น้อง 1 คืน เยี่ยมรำลึกถึงพี่ ๆ น้อง ๆ หลากหลายรุ่นได้จากเมนู gallery : วิชาการและงานสังสรรค์วันคืนสู่เหย้าฯ