Ovarian sex cord stromal tumors
พญ.กฤตยา ภิรมย์
อาจารย์ที่ปรึกษา รศ.พญ.ประภาพร สู่ประเสริฐ
บทนำ
เนื้องอกรังไข่ชนิด sex cord stroma เกิดจากเซลล์ sex cord และ stroma ของรังไข่ โดยเนื้องอกชนิดนี้ประกอบขึ้นจากเซลล์หลายชนิดต่อไปนี้ร่วมกันได้แก่ Sex cord ที่มาจากเพศหญิงคือ granulosa cells และ theca cells ส่วน sex cord ที่มาจากเพศชายคือ Sertoli cells และ Leydig cells ส่วน stroma คือ fibroblast หรือ precursors ของเซลล์เหล่านี้ (1)
รูปที่ 1 ชนิดของเนื้องอกรังไข่ตามเซลล์ต้นกำเนิด(2)
อุบัติการณ์
เนื้องอกชนิดนี้พบได้ประมาณร้อยละ 5-8 ของเนื้องอกรังไข่ทั้งหมด ส่วนใหญ่ของเนื้องอกชนิดนี้เป็นเนื้องอกธรรมดา (benign) หรือ กลุ่มเนื้องอกที่มีโอกาสการเป็นมะเร็งน้อย (low malignant potential)(1) เนื้องอกชนิดนี้มักวินิจฉัยได้ตั้งแต่ระยะเริ่มต้น โดยวินิจฉัยจากลักษณะทางพยาธิวิทยาของชิ้นเนื้อ ส่วนใหญ่ของเนื้องอกกลุ่มนี้เป็น granulosa-theca cell tumor ส่วนกลุ่ม Sertoli-Leydig cell tumor พบได้น้อย (1,3)
เนื้องอกกลุ่มนี้จะพบในอายุที่น้อยกว่าเมื่อเทียบกับเนื้องอกรังไข่ชนิดเยื่อบุผิว อายุโดยเฉลี่ยของเนื้องอกรังไข่ชนิด sex cord stroma อยู่ที่ 50 ปี โดยร้อยละ 12 พบในกลุ่มอายุน้อยกว่า 30 ปี และร้อยละ 50 พบในกลุ่มอายุ 30-59 ปี ในขณะที่อายุโดยเฉลี่ยของเนื้องอกรังไข่ชนิดเยื่อบุผิวอยู่ที่ 61 ปี(3)
กลุ่มที่มีความเสี่ยงต่อการเป็นเนื้องอกชนิดนี้ คือ ภาวะที่มีระดับ FSH สูง เช่น วัยเด็กก่อนมีประจำเดือน หรือวัยหมดประจำเดือน การใช้ยากระตุ้นไข่ตก เชื้อชาติผิวดำมากกว่าผิวขาว โรคอ้วน โรคทางพันธุกรรมบางชนิดที่มักพบร่วมกัน เช่น Peutz-Jeghers มีประวัติครอบครัวเป็นมะเร็งเต้านมหรือมะเร็งรังไข่ ในขณะที่กลุ่มที่สูบบุหรี่ กลุ่มที่ใช้ยาคุมกำเนิด และมีบุตร จะลดความเสี่ยงของโรคนี้ลง (4)
ลักษณะอาการทางคลินิก
ส่วนใหญ่จะมาด้วย ก้อนโตในอุ้งเชิงกราน ท้องมาน ปวดท้อง เนื้องอกบางชนิดสามารถสร้างฮอร์โมนเพศได้ เช่น เอสโตรเจน หรือ แอนโดรเจน โดยร้อยละ 90 ของเนื้องอกรังไข่ที่สร้างฮอร์โมนอยู่ในเนื้องอกรังไข่กลุ่มนี้ ทำให้ผู้ป่วยมีอาการผิดปกติทางต่อมไร้ท่อ เช่น ภาวะวัยสาวก่อนกำหนด ระดูผิดปกติ เลือดออกผิดปกติทางช่องคลอด เลือดออกหลังวัยหมดระดู เยื่อบุโพรงมดลูกหนาตัว มะเร็งเยื่อบุโพรงมดลูก ภาวะบุรุษเพศ เช่น ขาดระดู ขนดก เต้านมฝ่อ มีสิว เสียงห้าว(5)
การตรวจวินิจฉัยเพิ่มเติม(5,6)
การตรวจต่อไปนี้สามารถช่วยในการวินิจฉัย
สารบ่งชี้มะเร็ง (tumor marker): มีประโยชน์ในการช่วยวินิจฉัยแยกโรคและใช้ในการตรวจติดตามหลังการรักษา(5)
ตารางที่ 1 แสดง tumor marker ที่สร้างโดย ovarian sex cord stromal tumors(6)
|
AFP |
Estradiol |
Inhibin |
Testosterone |
Androstenedione |
DHEA |
AMH |
|
| Thecoma- Fibroma |
– |
– |
– |
– |
– |
– |
– |
| Granulosa cell |
– |
± |
+ |
± |
– |
– |
+ |
| Sertoli-Leydig cell |
± |
± |
± |
± |
± |
± |
– |
การตรวจอัลตราซาวน์ (ultrasonography): เพื่อยืนยันการมีก้อนที่รังไข่ และดูลักษณะก้อนว่าเป็นน้ำหรือเนื้อตัน รวมถึงประเมินลักษณะการเปลี่ยนแปลงของเส้นเลือดที่มาเลี้ยงรังไข่เพื่อช่วยในการแยกว่าเป็นเนื้องอกธรรมดาหรือมะเร็ง ในผู้หญิงที่สงสัยเนื้องอกรังไข่ชนิด sex cord stroma ต้องประเมินเยื่อบุโพรงมดลูกด้วย เพื่อดูความหนาของเยื่อบุโพรงมดลูก เนื่องจากผลของฮอรโมนเอสโตรเจนจะทำให้มีเยื่อบุโพรงมดลูกหนาได้ นอกจากนี้ควรตรวจหาน้ำในช่องท้อง น้ำในเยื่อหุ้มปอดและอวัยวะโตในช่องท้องร่วมด้วย
การถ่ายภาพรังสีทรวงอก (chest x-ray): ช่วยประเมินการแพร่กระจายไปที่ปอดหรือเยื่อกั้นกลางช่องอกได้
การตรวจเอกเซรย์คอมพิวเตอร์ (computed tomography/ CT) หรือ การตรวจเอกซเรย์คลื่นแม่เหล็กไฟฟ้า (magnetic resonance imaging/ MRI): ช่วยประเมินเรื่องการแพร่กระจายภายในช่องท้องและการแพร่กระจายไปต่อมน้ำเหลืองหลังช่องท้อง
Endometrial sampling: พิจารณาเก็บชิ้นเนื้อเยื่อบุโพรงมดลูกในผู้หญิงวัยเจริญพันธุ์ที่มีเลือดออกผิดปกติทางช่องคลอด หรือวัยทองที่มีเยื่อบุโพรงมดลูกหนากว่า 4 มิลลิเมตร รวมถึงในรายที่สงสัยเนื้องอกรังไข่ชนิด granulosa cell เพื่อวินิจฉัยก่อนการผ่าตัด
การวินิจฉัย
การวินิจฉัยที่แน่นอนของเนื้องอกรังไข่ชนิด sex cord stroma ได้จากลักษณะทางพยาธิวิทยาของชิ้นเนื้อที่ได้จากการผ่าตัด ส่วนก่อนการผ่าตัด อาจสงสัยได้จากมีก้อนที่ปีกมดลูก ร่วมกับมีอาการแสดงของฮอรโมนเอสโตรเจนหรือแอนโดรเจนสูงและมีระดับสารบ่งชี้มะเร็ง
การแบ่งชนิดของ ovarian sex cord stromal tumors (1)
ตารางที่ 2 แสดงการแบ่งชนิดเนื้องอกรังไข่ชนิด Sex cord stromal ตาม WHO classification of tumors of the ovary (7)
| I. Granulosa -stromal cell tumors | II. Sertoli-stromal cell tumors |
| A. Granulosa cell tumor group
1. Adult-type granulosa cell tumor 2. Juvenile-type granulosa cell tumor B. Theca–fibroma group 1. Thecoma a. Typical b. Luteinized (partly luteinized theca cell tumor) c. Calcified 2. Fibroma 3. Cellular fibroma (cellular fibrous tumor of low malignant potential) 4. Fibrosarcoma 5. Stromal tumor with minor sex cord elements 6. Sclerosing stromal tumor 7. Signet-ring stromal tumor 8. Unclassified (fibrothecoma) |
A. Sertoli–Leydig cell tumor group (androblastoma)
1. Well differentiated 2. Intermediate differentiation Variant with heterologous elements 3. Poorly differentiated (sarcomatoid) Variant with heterologous elements 4. Retiform Variant with heterologous elements B. Sertoli cell tumor C. Stromal-Leydig cell tumor |
| III. Sex cord-stromal cell tumors of mixed or unclassified cell type | |
| A. Sex cord tumor with annular tubules
B. Gynandroblastoma (specify components) C. Sex cord-stromal tumor, unclassified |
|
| IV. Steroid cell tumors | |
| A. Stromal luteoma
B. Leydig cell tumor group a. Hilus cell tumor b. Leydig cell tumor, nonhilar type c. Leydig cell tumor, not otherwise specified C. Steroid cell tumor, not otherwise specified a. Well differentiated b. Malignant |
Granulosa-Stromal cell tumor
Granulosa-Stromal cell tumor ประกอบด้วย granulosa cell tumors, thecomas และ fibromas ซึ่ง granulosa cell tumors เป็นกลุ่มเนื้องอกที่มีโอกาสการเป็นมะเร็งน้อย (Low malignant potential) ส่วน thecomas และ fibroma เป็นเนื้องอกธรรมดา (benign) แต่มีส่วนน้อยมากที่เป็นมะเร็งเรียกว่า malignant thecoma และ fIbrosarcoma(1)
Granulosa cell tumors
พบได้ร้อยละ 1-2 ของเนื้องอกรังไข่ทั้งหมด และ ร้อยละ 5 ของมะเร็งรังไข่ มะเร็ง granulosa-Stromal cell พบได้บ่อยสุดในกลุ่มมะเร็งรังไข่ชนิด sex cord stroma โดยพบได้ร้อยละ 70 เนื้องอกกลุ่มนี้สามารถพบได้ตั้งแต่เด็กจนถึงผู้ใหญ่ โดยอายุเฉลี่ยคือ 52 ปี(5,8) ซึ่งแบ่งออกเป็น adult type และ juvenile type
1. Granulosa cell tumors : adult type
พบร้อยละ 95 ของ granulosa cell tumors พบในผู้หญิงอายุ 47-54ปี (8)
ลักษณะทางคลินิก: ก้อนโตในอุ้งเชิงกราน ท้องมาน ปวดท้อง อาการของเอสโตรเจนสูงจากการสร้างของก้อน เช่น ระดูผิดปกติ เลือดออกผิดปกติทางช่องคลอด คัดตึงเต้านม เยื่อบุโพรงมดลูกหนาตัว และส่วนน้อยจะพบภาวะบุรุษเพศ เช่น ขาดระดู ขนดก(9,10)
ลักษณะทางพยาธิวิทยา: ร้อยละ 95 พบที่รังไข่ข้างเดียว ก้อนโตเฉลี่ย 12 เซนติเมตร ลักษณะเป็น cystic หรือ เป็น solid แน่นหรือนุ่ม สีขาวเทาหรือเหลือง อาจมี necrosis หรือ hemorrhage ส่วนลักษณะของเซลล์ มีลักษณะรีหรือยาว สีซีด นิวเคลียสใหญ่มีร่องตรงกลางเหมือนเมล็ดกาแฟ การเรียงตัวมีหลายแบบ เช่น microfollicular ซึ่งพบมากที่สุด เซลล์เรียงตัวเป็น Rosette formation และมี eosinophilic fluid อยู่ภายใน เรียก Call- Exner bodies และแบบอื่นๆ ได้แก่ macrofollicular, trabecular, insular, water silk, gryriform, diffuse(2,5)
การพยากรณ์โรค: ผู้ป่วยมักจะอยู่ในระยะที่ 1 ร้อยละ 90 มีการพยากรณ์โรคดี อัตราการรอดชีวิตใน 10 ปีของระยะที่ 1 ร้อยละ 86-96 ส่วนของระยะอื่น อยู่ที่ร้อยละ 26-49 การกลับเป็นซ้ำในระยะยาว 5-30ปี โดยเฉลี่ยที่ 6 ปี และผู้ป่วยมักจะอยู่ได้ประมาณ 5.6 ปีหลังการกลับเป็นซ้ำ(9)
2. Granulosa cell tumors: juvenile type
พบร้อยละ 5 ของ granulosa cell tumors พบในวัยเด็กก่อนวัยเจริญพันธุ์ หรือผู้หญิงอายุน้อยกว่า 30 ปี(8)
ลักษณะทางคลินิก: ภาวะวัยสาวก่อนกำหนด ชนิด isosexual precocious pseudopuberty ก้อนโตในอุ้งเชิงกราน ท้องมาน ปวดท้อง
ลักษณะทางพยาธิวิทยา: ร้อยละ 95 พบที่รังไข่ข้างเดียว มองด้วยตาเปล่าจะเหมือนชนิด adult type โดยจะแยกได้จากfollicular ที่มีขนาดและรูปร่างแตกต่างกัน ไม่ค่อยพบ Call- Exner bodies ลักษณะของเซลล์ มีลักษณะกลม ติดสีเข้ม นิวเคลียสใหญ่ไม่มีร่องตรงกลาง มี vacuole หรือ eosinophilic cytoplasm(2,5)
การพยากรณ์โรค: การดำเนินโรครุนแรงกว่าแบบ adult type มักพบในระยะที่สูงกว่า การกลับเป็นซ้ำเร็วโดยเฉลี่ยที่ 3 ปี(9)
Thecoma
เป็นเนื้องอกธรรมดาของ theca cell พบได้ร้อยละ1 ของเนื้องอกรังไข่ พบได้ทุกกลุ่มอายุ ส่วนใหญ่อายุ 60-70 ปี เป็นเนื้องอกที่สร้างฮอร์โมนได้มากที่สุดในเนื้องอกรังไข่ชนิด sex cord stroma(5)
ลักษณะทางคลินิก: ก้อนโตในอุ้งเชิงกราน ปวดท้อง อาการของเอสโตรเจนสูงจากการสร้างของก้อน เช่น เลือดออกผิดปกติทางช่องคลอดพบได้ร้อยละ 60 ของผู้ป่วย เนื้องอกมดลูก เยื่อบุโพรงมดลูกหนาตัว ตื่งเนื้อของเยื่อบุโพรงมดลูก มะเร็งเยื่อบุโพรงมดลูก
ลักษณะทางพยาธิวิทยา: ก้อนขนาดใหญ่ ก้อนเนื้อตัน แข็ง กลม สีเทาเหลือง ลักษณะของเซลล์ ใส มี vacuole ใน cytoplasm นิวเคลียสกลมรี มี spindle cell เรียงตัวสานไปมา แทรกด้วยเนื้อเยื่อเกี่ยวพัน(2,5)
Fibroma
เป็นเนื้องอกธรรมดาของ stroma พบได้บ่อยสุด โดยพบร้อยละ 4 ของเนื้องอกรังไข่ พบได้ทุกอายุ มักพบอายุมากกว่า 30 ปี โดยอายุเฉลี่ยคือ 55 ปี เนื้องอกชนิดนี้ไม่สร้างฮอร์โมน
ลักษณะทางคลินิก: มักมีอาการปวดท้องน้อยและมีระดูผิดปกติ
มักมีความสัมพันธ์กับกลุ่มอาการ 2 กลุ่ม(1,5)
- Meigs’s syndrome ประกอบด้วย fibromatous ovarian tumor ร่วมกับ ascites พบได้ร้อยละ 10-15 ของก้อนที่มากกว่า 10 เซนติเมตร เกิดจากสารน้ำซึมผ่านก้อนเข้ามาในช่องท้อง และ hydrothorax โดยมักพบข้างขวา พบได้ร้อยละ 1 เกิดจากสารน้ำซึมผ่านท่อน้ำเหลือง
- Gorlin’s syndrome หรือ Nevoid basal cell carcinoma syndrome เป็นโรคที่ถ่ายทอดทางพันธุกรรมแบบ autosomal dominant ประกอบด้วย fibromatous ovarian tumor ร่วมกับ basal cell carcinoma และ keratocystic odontogenic tumors ที่ขากรรไกร
ลักษณะทางพยาธิวิทยา: มักเป็นข้างเดียว ขนาดหลากหลายตั้งแต่ 3 – 15 เซนติเมตร ก้อนเนื้อตัน หรืออาจมีถุงน้ำเล็กๆ มีสีขาวเทา ลักษณะของเซลล์ เป็นรูปกระสวย อาจมีเซลล์กล้ามเนื้อแทรกอยู่(2)
Sertoli-stromal cell tumors
เดิมชื่อ androblastoma หรือ arrhenoblastoma เป็นเนื้องอกของ Sertoli cell และ Leydig cell ซึ่งเป็นกลุ่มเซลล์จำเพาะของอัณฑะ เนื้องอกกลุ่มนี้แบ่งได้เป็น 3 กลุ่มย่อยตามชนิดของเซลล์ ได้แก่ Sertoli–Leydig cell tumor, Sertoli cell tumor และ Stromal-Leydig cell tumor(5)
Sertoli–Leydig cell tumor
เนื้องอกชนิดนี้พบได้น้อยมาก ร้อยละ 0.2 ของเนื้องอกรังไข่ พบได้ทุกกลุ่มอายุ มักพบในวัยเจริญพันธุ์ โดยอายุเฉลี่ย 25 ปี เนื้องอกมักสร้างแอนโดรเจน(12)
ลักษณะทางคลินิก: ก้อนโตในอุ้งเชิงกราน ปวดท้อง อาการแสดงของแอนโดรเจนสูง เช่น ขาดระดู ภาวะบุรุษเพศ เต้านมฝ่อ ขนดก มีสิว เสียงห้าว(1)
ลักษณะทางพยาธิวิทยา: มักเป็นข้างเดียว ก้อนเนื้อแน่นตัน สีเหลืองซีด อาจมีถุงน้ำแทรก ลักษณะของเซลล์ Sertoli cell ตัวกลมรี ไซโทพลาสซึมน้อย เรียงตัวเป็น tubule หรือ Cord แทรกด้วย Leydig cell รูปไข่ มีนิวเคลียสขนาดใหญ่กลางเซลล์ มี Crystalloid of Rinke(1,5)
การพยากรณ์โรค: มักพบในระยะที่1 การพยากรณ์โรคขึ้นกับระยะ และ differentiation อัตราการรอดชีวิตใน 5 ปี ร้อยละ 70-90 มักไม่พบ การกลับเป็นซ้ำ(12,13)
Sertoli cell tumor
พบได้น้อยกว่าร้อยละ 5 ของเนื้องอกชนิด Sertoli-stromal cell tumors พบในอายุเฉลี่ย 30 ปี สองในสามจะสร้างฮอร์โมนเอสโตรเจนได้ อาจพบเนื้องอกชนิดนี้ในกลุ่ม Peutz-Jeghers(12)
ลักษณะทางพยาธิวิทยา: มักพบที่รังไข่ข้างเดียว ก้อนเนื้อตันสีเหลือง ลักษณะเห็นเป็นท่อตันหรือเป็นโพรงบุด้วย Sertoli cell
การพยากรณ์โรค: เนื้องอกชนิดนี้มีความเป็นมะเร็งต่ำ การพยากรณ์โรคดี(5)
Stromal-Leydig cell tumor
เป็นเนื้องอกธรรมดาพบในกลุ่มอายุมาก โดยอายุเฉลี่ย 58 ปี
ลักษณะทางคลินิก: อาการแสดงของแอนโดรเจนสูง เช่น ขาดระดู ภาวะบุรุษเพศ เต้านมฝ่อ ขนดก มีสิว เสียงห้าว บางครั้งมีการสร้างฮอร์โมนเอสโตรเจนด้วย ทำให้เยื่อบุโพรงมดลูกหนาตัว หรือเป็นมะเร็งเยื่อบุโพรงมดลูกได้
ลักษณะทางพยาธิวิทยา: มักพบในรังไข่ข้างเดียว ขนาดเล็ก เฉลี่ย 2.7 เซนติเมตร ลักษณะเซลล์ Leydig cell รูปไข่ มีนิวเคลียสขนาดใหญ่กลางเซลล์ มี Crystalloid of Rinke(2)
การพยากรณ์โรค: เนื้องอกชนิดนี้มีความเป็นมะเร็งต่ำ การพยากรณ์โรคดี(5)
Sex cord-stromal cell tumors of mixed or unclassified cell type
Sex cord tumor with annular tubules
เป็นเนื้องอกที่มีลักษณะกึ่งกลางระหว่างเนื้องอกชนิด granulosa และเนื้องอกชนิด Sertoli พบในสตรีวัยกลางคน มักสร้างฮอร์โมนเอสโตรเจนและโปรเจสเตอโรน เนื้องอกชนิดนี้สัมพันธ์กับกลุ่มอาการ Peutz-Jeghers (14,15)
ลักษณะทางคลินิก: เลือดออกผิดปกติทางช่องคลอดหรือเลือดออกหลังวัยหมดประจำเดือน
ลักษณะทางพยาธิวิทยา: มักพบในรังไข่ข้างเดียว ลักษณะของเซลล์ Sertoli เรียงตัวเป็นท่อรูปวงแหวนพันทบไปมา ภายในท่อกลางมีสาร hyaline(2)
การพยากรณ์โรค: เนื้องอกที่มีกลุ่มอาการ Peutz-Jeghers ร่วมด้วยจะเป็นเนื้องอกธรรมดา ส่วนเนื้องอกที่ไม่มีกลุ่มอาการ Peutz-Jeghers ร่วมด้วยจะมีความเป็นมะเร็งสูงประมาณร้อยละ 20(15)
Gynandroblastoma
เป็นเนื้องอกที่ประกอบด้วยเซลล์ granulosa เซลล์ Theca เซลล์ Sertoli และเซลล์ Leydig พบน้อยมาก มักพบในสตรีวัยกลางคน สร้างฮอร์โมนเอสโตรเจนและแอนโดรเจน(16)
ลักษณะทางคลินิก: ระดูผิดปกติ เลือดออกผิดปกติทางช่องคลอด เยื่อบุโพรงมดลูกหนาตัว และภาวะบุรุษเพศ
ลักษณะทางพยาธิวิทยา: มักพบในรังไข่ข้างเดียว ลักษณะของเซลล์ granulosa มี Call- Exner bodies เซลล์ Theca เซลล์ Sertoli และ เซลล์ Leydig มี Crystalloid of Rinke(16)
การพยากรณ์โรค: เนื้องอกชนิดนี้มีความเป็นมะเร็งต่ำ
Sex cord-stromal tumor, unclassified
เป็นกลุ่มที่ไม่สามารถแยกได้ชัดเจนว่ามีลักษณะเป็นเซลล์ชนิดไหน พบได้ประมาณร้อยละ 10 ของเนื้องอกรังไข่ชนิด sex cord stroma มักพบขณะตั้งครรภ์(5)
Steroid cell tumors
เดิมชื่อ lipid cell tumor เป็นเนื้องอกของเซลล์ luteinized stromal cell, Leydig cell และ A\adrenocortical cell พบได้น้อยมา ร้อยละ 0.1 ของเนื้องอกรังไข่ พบได้ทุกกลุ่มอายุ แบ่งได้ 3 กลุ่มย่อย คือ stromal luteoma, Leydig cell tumor group และ steroid cell tumor, not otherwise specified(1)
Stromal luteoma
เป็นเนื้องอกธรรมดา พบในผู้หญิงอายุมาก พบได้ร้อยละ 25 ของเนื้องอกกลุ่ม steroid cell tumor
ลักษณะทางคลินิก: เลือดออกผิดปกติทางช่องคลอด เยื่อบุโพรงมดลูกหนาตัว และภาวะบุรุษเพศ
ลักษณะทางพยาธิวิทยา: เนื้องอกมีขนาดเล็ก เนื้อตัน สีเหลือง ลักษณะของเซลล์ luteinized stromal cell เซลล์กลมใหญ่ ติดสีซีด พบ stromal hyperthecosis(5)
Leydig cell tumor group
เป็นเนื้องอกธรรมดา พบได้น้อยมาก พบในผู้หญิงทุกอายุโดยอายุเฉลี่ย 58 ปี
ลักษณะทางคลินิก: ภาวะบุรุษเพศ เช่น ขาดระดู ขนดก เต้านมฝ่อ มีสิว เสียงห้าว
ลักษณะทางพยาธิวิทยา: มักพบข้างเดียว เนื้องอกมีขนาดหลากหลาย ลักษณะของ Leydig cell รูปไข่ มีนิวเคลียสขนาดใหญ่กลางเซลล์ ไซโทพลาสซึมสีส้ม(5)
Steroid cell tumor, not otherwise specified
เป็นเนื้องอกที่มีความเป็นมะเร็งสูง เป็นกลุ่มที่พบมากที่สุดในกลุ่มนี้ พบได้ทุกวัยตั้งแต่วัยเด็กถึงสูงอายุโดยอายุเฉลี่ย 43 ปี เนื้องอกกลุ่มนี้สร้างฮอร์โมนแอนโดรเจน(5)
ลักษณะทางคลินิก: ภาวะวัยสาวก่อนกำหนดชนิด heterosexual precocity ภาวะบุรุษเพศ
ลักษณะทางพยาธิวิทยา: มักพบข้างเดียว ขนาดโดยเฉลี่ย 8.4 เซนติเมตร เนื้องงอกก้อนตัน สีส้มหรือเหลืองบางครั้งพบสีแดง น้ำตาลเข้มหรือดำ ขอบเขตชัด อาจมีลักษณะของnecrosis หรือ hemorrhage หรือ cystic degeneration ลักษณะของเซลล์กลม หลายเหลี่ยม ไซโทพลาสซึมมาก
การพยากรณ์โรค: เนื้องอกชนิดนี้มีความเป็นมะเร็งสูง และมีกรแพร่กระจายนอกรังไข่ถึงร้อยละ 43
การแพร่กระจาย(6)
- การแพร่กระจายภายในช่องท้อง (intraperitoneal spread) หรือ transcoelomic spread เหมือนกับมะเร็งรังไข่ชนิดเยื่อบุผิว
- การแพร่กระจายไปตามระบบน้ำเหลือง ซึ่งเกิดขึ้นได้บ่อยกว่ามะเร็งรังไข่ชนิดเยื่อบุผิว โดยเฉพาะเนื้องอกชนิด granulosa และ sex cord tumor with annular tubules
- การแพร่กระจายไปตามกระแสเลือด พบน้อย
การแบ่งระยะของมะเร็งรังไข่ ตาม FIGO’s staging classification 2014
ตารางที่ 3 การแบ่งระยะของมะเร็งรังไข่ตาม FIGO’s staging classification 2014 (17)
|
Stage I. Tumor confined to ovaries or fallopian tube(s) T1-N0-M0 IA: Tumor limited to one ovary (capsule intact) or fallopian tube; no tumor on ovarian or fallopian tube surface; no malignant cells in the ascites or peritoneal washing T1a-N0-M0 IB: Tumor limited to both ovaries (capsule intact) or fallopian tube; no tumor on ovarian or fallopian tube surface; no malignant cells in the ascites or peritoneal washing T1b-N0-M0 IC: Tumor limited to one or both ovaries or fallopian tubes, with any of the following: IC1: surgical spill T1c1-N0-M0 IC2: capsule ruptured before surgery or tumor on ovarian or fallopian tube surface T1c2-N0-M0 IC3: malignant cells in the ascites or peritoneal washings T1c3-N0-M0 |
|
Stage II. Tumor involves one or both ovaries or fallopian tubes with pelvic extension (below pelvic brim) or primary peritoneal cancer T2-N0-M0 IIA: extension and/or implants on uterus and/or fallopian tubes and/or ovaries T2a-N0-M0 IIB: extension to other pelvic intraperitoneal tissues T2b-N0-M0 |
|
Stage III. Tumor involves one or both ovaries or fallopian tubes, or primary peritoneal cancer, with cytologically or histologically confirmed spread to peritoneum outside the pelvis and/or metastasis to the retroperitoneal lymph nodes T1/T2-N1-M0 IIIA1: positive retroperitoneal lymph nodes only (cytologically or histologically proven): IIIA1(i) Metastasis up to 10 mm in greatest dimension IIIA1(ii) Metastasis more than 10 mm in greatest dimension IIIA2: microscopic extrapelvic(above the pelvic brim) peritoneal involvement with or without positive retroperitoneal lymph nodes T3a2-N0/N1-M0 IIIB: macroscopic peritoneal metastasis beyond the pelvis up to 2 cm in greatest dimension, with or without metastasis to the retroperitoneal lymph nodes T3b-N0/N1-M0 IIIC: macroscopic peritoneal metastasis beyond the pelvis more than 2 cm in greatest demension, with or without metastasis to the retroperitoneal lymph nodes(include extension of tumor to capsule of liver and spleen without parenchymal involvement of either organ) T3c-N0/N1-M0 |
|
Stage IV. Distant metastasis excluding peritoneal metastases Any T, any N, M1 IVA: pleural effusion with positive cytology IVB: parenchymal metastases and metastases to extra-abdominal organs(including inguinal lymph nodes and lymph nodes outside of the abdominal cavity) |
แนวทางการรักษา
แนวทางการดูแลรักษาขึ้นกับปัจจัยต่างๆ ได้แก่ ชนิดของเนื้องอก ระยะของโรค อายุ ความต้องการมีบุตรของผู้ป่วย โดยทั่วไปการผ่าตัดเพียงอย่างเดียวถือว่าพอในเนื้องอกรังไข่ชนิด sex cord stroma เนื่องจากส่วนใหญ่ของเนื้องอกชนิดนี้เป็นเนื้องอกธรรมดา (benign) หรือ กลุ่มเนื้องอกที่มีโอกาสการเป็นมะเร็งน้อย (low malignant potential) ภายหลังการผ่าตัดอาจพิจารณาการรักษาเพิ่มเติมถ้าเป็นระยะลุกลาม หรือมีความเป็นมะเร็งสูง(4,5,6)
1. การผ่าตัด เป็นวิธีการรักษาหลักเพื่อให้ได้การวินิจฉัยที่แน่นอน
การผ่าตัดแบบธำรงภาวะเจริญพันธุ์ (fertility-preserving surgery) คือ การตัดท่อรังไข่และรังไข่ข้างที่มีโรค พิจารณาในผู้ป่วยระยะ IA ในเด็กหรือสตรีวัยเจริญพันธุ์ และ ต้องการมีบุตร ภายหลังการผ่าตัดในเนื้องอกที่สร้าฮอรโมนเอสโตรเจนจะต้องทำการขูดมดลูกเพื่อวินิจฉัย มะเร็งเยื่อบุโพรงมดลูกหรือเยื่อบุโพรงมดลูกหนาตัวที่อาจพบร่วมได้(5,6)
การผ่าตัดกำหนกระยะ โรค(complete surgical staging พิจารณาในผู้ป่วยอายุมากหรือไม่ต้องการมีบุตรหรือโรคได้แพร่กระจายไปมากแล้ว โดยในผู้ป่วยที่มีเนื้องอกธรรมดา ได้แก่ thecomas, fibromas, sclerosing stromal cell tumor, gynandroblastomas, stromal luteomas, Leydig cell, Sertoli cell, well differentiated Sertoli–Leydig cell tumor และ sex cord tumor with annular tubulesที่มีกลุ่มอาการ Peutz-Jeghers ร่วม พิจารณาล้างน้ำในช่องท้องส่งตรวจเซลล์ ดูและคลำอวัยวะภายใน ผ่าตัดเฉพาะก้อนเนื้องอก ส่วนในผู้ป่วยที่มีลักษณะเป็นมะเร็ง ได้แก่ granulosa cell tumor, Immediate or poorly differentiated Sertoli Leydig cell tumor, steroid cell tumor not otherwise specified และ sex cord tumor with annular tubulesที่ไม่มีกลุ่มอาการ Peutz-Jeghers ร่วม พิจารณา ล้างน้ำในช่องท้องส่งตรวจเซลล์ ดูและคลำอวัยวะภายใน ตัดเยื่อแขวนกระเพาะในช่องท้อง (omentum) ผ่าตัดมดลูกและปีกมดลูกทั้ง 2 ข้าง เลาะต่อมน้ำเหลืองหลังช่องท้องที่มีขนาดใหญ่ผิดปกติ อย่างไรก็ตามการผ่าตัดกำหนดระยะในเนื้องอกรังไข่ชนิด sex cord stroma ยังไม่มีข้อพิสูจน์ชัดเจน และมีรายงานว่าการเลาะต่อมน้ำเหลืองไม่ค่อยมีประโยขน์เนื่องจากการแพร่กระจายไปต่อมน้ำเหลืองน้อย(5)
การผ่าตัดเพื่อจำกัดขนาดของเนื้อเยื่อ (cytoreductive surgery) ในกรณีที่มีการแพร่กระจายของโรคในผู้ป่วยระยะลุกลามหรือการกลับมาเป็นซ้ำ การผ่าตัดเพื่อจำกัดขนาดของเนื้อเยื่ออาจได้ผลดีในกลุ่มที่ก้อนอยู่เฉพาะที่ การผ่าตัดนี้มีประโยชน์ในการรักษาประคับประคอง และช่วยลดอาการของผู้ป่วยได้นาน เนื่องจากการดำเนินของโรคกลุ่มนี้มีการเจริญเติบโตช้า(5)
2. ยาเคมีบำบัด
พิจารณาให้ยาเคมีบำบัดหลังการผ่าตัดในกลุ่มผู้ป่วยระยะที่ 1 ที่มีปัจจัยเสี่ยงต่อการพยากรณ์โรคที่ไม่ดี และกลุ่มผู้ป่วยระยะที่ 2-4 ยาเคมีบำบัดที่แนะนำคือกลุ่มที่มี platinum เป็นยาตัวหลัก เช่น BEP regimen (bleomycin, etoposide, cisplatin)ซึ่งมีการตอบสนองสูงสุดและเป็นที่นิยมมากสุดในปัจจุบัน , PAC (cisplatin, doxorubicin, cyclophosphamide), PVB (cisplatin, vinblastin, bleomycin)(1,4,5)
3. รังสีรักษา
ยังไม่ทราบประสิทธิภาพที่ชัดเจน พิจารณาให้หลังการผ่าตัดในรายที่ตัดก้อนออกไม่หมด หรือกลับมาเป็นซ้ำ(5)
4. การรักษาอื่นๆ
ฮอร์โมนโปรเจสติน เช่น medroxyprogesterone acetate (DMPA), megestrol acetate หรือการรักษาด้วย tamoxifen, gonadotropin-releasing hormone (GnRH) antagonist หรือ aromatase inhibitor อาจมีบทบาทในเนื้องอกชนิด granulosa cell เนื่องจากร้อยละ 30 มี Receptor ของ estrogen และร้อยละ 100 จะมี receptor ของ progesterone
Targeted therapy อาจพิจารณาให้ยายับยั้งการสร้างหลอดเลือด เช่น bevacizumab ในรายที่กลับมาเป็นซ้ำ หรือพิจารณาใช้ยากลุ่ม tyrosine kinase inhibitor เช่น imatinib mesylate, nilotinib ในกลุ่มเนื้องอกชนิด granulosa cellที่กลับมาเป็นซ้ำ(5)
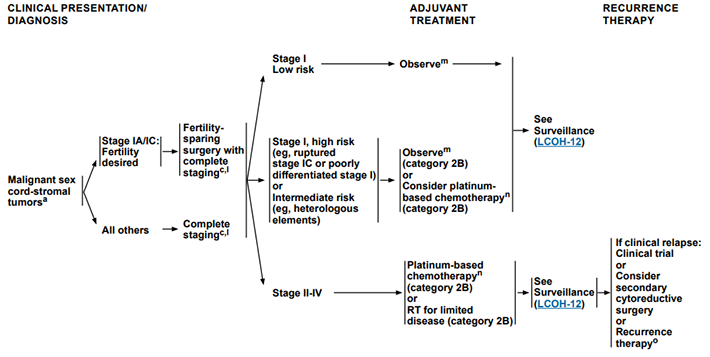
รูปที่ 2 แนวทางการรักษามะเร็งรังไข่ชนิด Sex cord stroma ตาม NCCN guideline (18)
ตารางที่ 3 การตรวจติดตามมะเร็งรังไข่ชนิด sex cord-stromal ตาม NCCN guideline(18)
|
|
Year |
||||
|
<1 |
1-2 |
2-3 |
3-5 |
>5 |
|
|
Physical exam |
Every 2-4 mo |
Every 6 mo |
|||
|
Tumor marker |
Every 2-4 mo |
Every 6 mo |
|||
|
Radiographic imaging |
Insufficient data to support routine use |
||||
|
Recurrence suspected |
CT scan and tumor markers |
||||
การตรวจติดตามหลังการรักษา(18)
NCCN clinical practice guidelines in oncology ปีค.ศ. 2017 แนะนำให้ทำการนัดผู้ป่วยมะเร็งรังไข่ชนิด sex cord stroma ทุก 2-4 เดือนใน 2 ปีแรกหลังสิ้นสุดการรักษา หากผลปกติให้นัดทุก 6 เดือน โดยในแต่ละครั้งจะต้องทำการซักประวัติ ตรวจร่างกายและตรวจภายในทุกครั้ง ส่วนการตรวจ tumor marker แนะนำให้ทำทุก 2-4 เดือนในช่วง 2 ปีแรก และ ทุก 6 เดือนหลังจากนั้น ส่วนการตรวจทางรังสี เช่น CXR, CT chest/abdomen/pelvis, MRI/PET scan ยังไม่มีข้อมูลที่เพียงพอ และหากสงสัยว่ามีการกลับเป็นซ้ำให้ตรวจ tumor marker และตรวจทางรังสีเพิ่มเติม
สรุป
เนื้องอกรังไข่ชนิด sex cord-stromal พบได้ประมาณร้อยละ 5-8 ของเนื้องอกรังไข่ทั้งหมด มักพบในผู้ป่วยทุกกล่มอายุส่วนใหญ่ของเนื้องอกชนิดนี้เป็นเนื้องอกธรรมดา เนื้องอกชนิดที่พบมากที่สุดในกลุ่มนี้คือ granulosa-theca cell tumor ส่วนกลุ่ม Sertoli-Leydig cell tumor พบได้น้อย อาการที่พบได้บ่อย คือ ก้อนโตในอุ้งเชิงกรานและปวดท้อง เนื้องอกบางชนิดสามารถสร้างฮอร์โมนเพศได้ ทำให้ผู้ป่วยมีอาการผิดปกติทางต่อมไร้ท่อ เช่น ภาวะวัยสาวก่อนกำหนด เลือดออกผิดปกติทางช่องคลอดและภาวะบุรุษ การรักษาหลักคือการผ่าตัด
เอกสารอ้างอิง
- Berek J, Friedlander M, Hacker N. Germ Cell and Nonepithelial Ovarian Cancer. 6 ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2015.
- Young RH. Sex cord-stromal tumors of the ovary and testis: their similarities and differences with consideration of selected problems. Mod Pathol 2005; 18 Suppl 2:S81.
- Quirk JT, Natarajan N. Ovarian cancer incidence in the United States, 1992-1999. Gynecol Oncol 2005; 97:519.
- Boyce EA, Costaggini I, Vitonis A, et al. The epidemiology of ovarian granulosa cell tumors: a case-control study. Gynecol Oncol 2009; 115:221.
- David M, Gershenson, Sean C. Dowdy, Robert H. Young. Ovarian Sex Cord Stromal Tumors. Principle and practice of gynecologic oncology. 7th ed. Philadelphia: Lippincott Williams&Wilkins; 2017:724-739.
- David M Gershenson, MD. Overview of sex cord-stromal tumors of the ovary. UPTODATE [Internet]. 2017. Available from: https://www.uptodate.com/contents/overview-of-sex-cord-stromal-tumors-of-the-ovary?source=history_widget
- Tavassoli FA, Devilee P, eds. Pathology and Genetics of Tumours of the Breast and Female Genital Tract. Lyon: IARC Press, 2003; Roth LM. Recent advances in the pathology and classification of ovarian sex cord-stromal tumors. Int J Gynecol Pathol. 2006;25:199–215.
- Boyce EA, Costaggini I, Vitonis A, et al. The epidemiology of ovarian granulosa cell tumors: A case-control study. Gynecol Oncol. 2009;115:221–225.
- Malmström H, Högberg T, Risberg B, et al. Granulosa cell tumors of the ovary: Prognostic factors and outcome. Gynecol Oncol. 1994; 52:50–55.
- Segal R, DePetrillo AD, Thomas G. Clinical review of adult granulosa cell tumors of the ovary. Gynecol Oncol. 1995;56:338–344.
- Cronje HS, Niemand I, Barn, RH, et al. Review of the granulosa– theca cell tumors from the Emil Novak ovarian tumor registry. Am J Obstet Gynecol. 1999;180:323–328.
- Roth LM, Anderson MC, Govan AD, et al. Sertoli-Leydig cell tumors: A clinicopathologic study of 34 cases. Cancer. 1981;48: 187–197.
- Tomlinson MW, Treadwell MC, Deppe G. Platinum based chemotherapy to treat recurrent Sertoli-Leydig cell ovarian carcinoma during pregnancy. Eur J Gynaecol Oncol. 1997;18:44–46.
- Shen K, Wu PC, Lang JH, et al. Ovarian sex cord tumor with annular tubules: a report of six cases. Gynecol Oncol 1993; 48:180.
- Westerman AM, Wilson JH. Peutz-Jeghers syndrome: risks of a hereditary condition. Scand J Gastroenterol Suppl 1999; 230:64.
- Fukunaga M, Endo Y, Ushigome S. Gynandroblastoma of the ovary: a case report with an immunohistochemical and ultrastructural study. Virchows Arch 1997; 430:77.
- Prat J. FIGO’s staging classification for cancer of the ovary, fallopian tube, and peritoneum: abridged republication. Gynecol Oncol. 2015;26:87-89.
- NCCN Guidelines Ovarian cancer including fallopian tube cancer and primary peritoneal cancer [Internet]. NCCN. 2017. Available from: www.nccn.org/


