Asthma in pregnancy
พญ.มัลลิกา วงศ์ชนะ
อาจารย์ที่ปรึกษา ร.ศ. พญ. เกษมศรี ศรีสุพรรณดิฐ
โรคปอดพบได้บ่อยในขณะตั้งครรภ์ ซึ่งโรคหอบหืดเรื้อรังหรือภาวะหอบ (Asthma) พบได้ 3-8%ของหญิงตั้งครรภ์(1) สำหรับปอดอักเสบติดเชื้อ(Pneumonia)ก็เป็นสาเหตุหนึ่งของการกลับมานอนโรงพยาบาลหลังคลอด ทั้งนี้การเปลี่ยนแปลงทางสรีรวิทยาของระบบทางเดินหายใจขณะตั้งครรภ์ก็เป็นปัจจัยหนึ่งที่มีผลกับความรุนแรงโรคปอดของหญิงตั้งครรภ์
การเปลี่ยนแปลงทางสรีรวิทยาของระบบทางเดินหายใจขณะตั้งครรภ์(2) มีดังนี้
- Vital capacity, inspiratory capacity เพิ่มขึ้นประมาณ 20 %ในช่วงระยะท้ายของการตั้งครรภ์
- Expiratory reserve volume ลดลงจาก 1300มิลลิลิตรเป็น 1100 มิลลิลิตร
- Tidal volume เพิ่มขึ้น 40 % ซึ่งเป็นผลจากฤทธิ์ของ progesterone
- Minute ventilation เพิ่มขึ้น 30-40 % เป็นผลเนื่องจาก tidal volume ที่เพิ่มขึ้น จึงทำให้ Po2เพิ่มขึ้นจาก 100 เป็น 105 mmHg
- Metabolic demand เพิ่มขึ้น ซึ่งมีผลทำให้เกิดการสร้าง CO2 เพิ่มขึ้น แต่เนื่องจากขณะตั้งครรภ์จะมีภาวะ hyperventilation เป็นผลให้มีการเพิ่มขึ้นของ diffusion capacity ทั้งหมดนี้ทำให้ Pco2ลดลงจาก 40 เป็น 32 mmHg
- Residual volume ลดลงประมาณ 20 % จาก 1500 มิลลิลิตร เป็น 1200 มิลลิลิตร
- ความสามารถในการเคลื่อนไหวของทรวงอกลดลงจากผลของมดลูกที่โตขึ้น รวมถึงความดันในช่องท้องที่เพิ่มขึ้น ส่งผลให้ Functional residual capacity ลดลง 25 %
การเปลี่ยนแปลงทั้งหมดส่งผลให้เกิด hyperventilationคือหายใจหอบลึกขึ้นแต่อัตราการหายใจไม่เปลี่ยนแปลงนอกจากนี้ oxygen consumption ที่เพิ่มขึ้นจาก 20 เป็น 40 ml/min ในช่วงครึ่งหลังของการตั้งครรภ์ส่งผลให้เกิดhyperventilation เช่นกัน
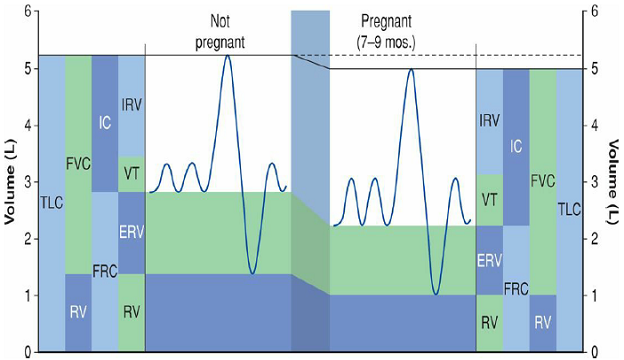
รูปที่ 1 แสดงการเปลี่ยนแปลงปริมาตรปอดขณะตั้งครรภ์ (ภาพจาก Williams obstetric24th edition, page143)
Pathophysiology
หอบหืด เป็นภาวะที่มีการอักเสบเรื้อรังของทางเดินหายใจ และมีการอุดตันของทางเดินหายใจแบบที่มีการกลับคืนมาบางส่วนหรือทั้งหมดโดยมีปัจจัยทางพันธุกรรมส่งเสริม พบว่ายีนบนโครโมโซม 5q (cytokine gene cluster,β-adrenergic and glucocorticoid receptor genes, T-cell antigen receptor gene) เกี่ยวข้องกับการเพิ่มขึ้นของการตอบสนองของระบบทางเดินหายใจ,การอักเสบของทางเดินหายใจ (airway responsiveness , persistent subacute inflammation)(2)นอกจากนี้ปัจจัยทางสิ่งแวดล้อม ได้แก่ เชื้อไข้หวัดใหญ่, ควันบุหรี่ ก็มีผลกระตุ้นอาการหอบหืดในผู้ป่วยบางรายด้วย
Clinical cause
อาการอาจเริ่มต้นเพียงแค่เล็กน้อย หายใจมีเสียงวี๊ดจนถึงขั้นที่หลอดลมตีบอย่างรุนแรง ทำให้ Forced expiratory volume in1 second(FEV1)/Forced vital capacity(FVC), Peak expiratory flow ลดลง
ความรุนแรงของโรคหอบหืดดังนี้
{tabulizer:style[gr.alterora.elemental_1_green.css]}
| Components of Severity | Classification of Asthma Severity ≥ 12 years of age | ||||
| Intermittent | Persistent | ||||
| Mild | Moderate | Severe | |||
| Impairment Normal FEV1/FVC: 8-19 yr : 85% 20-39 yr : 80% 40-59 yr : 75% 60-80 yr : 70% |
Symptoms | ≤ 2days/week | ≥ 2days/week but not daily | Daily | Throughout the day |
| Nighttime awakening | ≤ 2x/month | 3-4x/month | >1x/week but not nightly | Often 7x/week | |
| Short –acting beta2agonist use for symptom control(not prevention of EIB) | ≤ 2days/week | ≥ 2days/week but not daily, and not more than 1x on any day | Daily | Several times per day | |
| Interference with normal activity | None | Minor limitation | Some limitation | Extremely limited | |
| Lung function | Normal FEV1 between exacerbation FEV1>80% predicted FEV1/FVC normal | FEV1>80% predicted FEV1/FVC normal | FEV1>60% but<80% predicted=”” fev1=”” fvc=”” reduced=”” 5=”” td=””> | FEV1<60% predicted=”” fev1=”” fvc=”” reduced=””> 5% | |
ตารางที่ 1 แสดงการแบ่งระดับความรุนแรงของโรคหอบหืด จาก National Heart, Lung, and Blood institute, 2007(Expert panel report) (3)
หมายเหตุ: EIB: exercise-induced bronchoconstriction
สำหรับผู้ป่วยที่มีประวัติ exacerbation ≥ 2 ครั้งที่ได้รับ oral corticosteroid ภายใน 12 เดือน พิจารณาให้อยู่ในกลุ่ม persistent asthma(3)
ในกลุ่มอาการรุนแรง ที่มี persistentbronchial obstruction จะมีการ progression ดังนี้
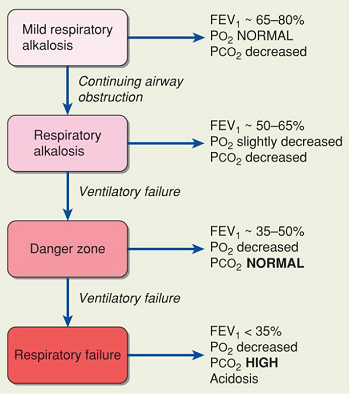
ภาพที่ 2 แสดงการเปลี่ยนแปลงเมื่อเกิด persistent bronchial obstruction ภาพจาก Williams obstetric24th edition , page 1012,2014
ซึ่งในหญิงตั้งครรภ์จะมี functional residual capacity น้อยกว่าและpulmonary shunting ที่เพิ่มขึ้น เมื่อเทียบกับหญิงที่ไม่ตั้งครรภ์ ทำให้ง่ายต่อการเกิด hypoxia, hypoxemia
หลักการรักษาโรคหอบหืดนั้น คือ ลดการอักเสบของหลอดลมซึ่งในหญิงตั้งครรภ์ก็เช่นเดียวกัน โดยพบว่าหญิงตั้งครรภ์ที่อยู่ในกลุ่ม mild, moderate well-controlled จะมีผลลัพธ์ของการตั้งครรภ์ที่ดี ส่วนกลุ่ม severe,poorly controlled asthma พบว่าอาจเกี่ยวข้องกับการเพิ่มขึ้นของภาวะprematurity, cesarean delivery, preeclampsia, growth restriction, maternal morbid-mortalityดังนั้นเป้าหมายหลักของการรักษาโรคหอบหืดในหญิงตั้งครรภ์ก็เพื่อดำรงภาวะoxygenation ของทารก โดยการป้องกันการเกิดภาวะ hypoxia ในมารดา ร่วมกับการใช้ยาให้น้อยที่สุดที่ยังสามารถควบคุมอาการได้(4)
Effects of pregnancy on asthma
ผลของการตั้งครรภ์ต่ออาการหอบหืดนั้น แบ่งผู้ป่วยได้เป็นสามกลุ่มคือ อาการดีขึ้น, แย่ลง, คงเดิม
ความรุนแรงก่อนการตั้งครรภ์ก็มีผลกับตอนตั้งครรภ์ พบว่า(5)
- Mild disease : 13% exacerbation, 2.3% admission
- Moderate disease : 26% exacerbation,7% admission
- Severe disease : 52% exacerbation, 27% admission
สำหรับ intrapartum exacerbation มีการศึกษาของ schatz,2003(5)พบว่าในกลุ่ม mild, moderate มีได้ 20% ส่วนการศึกษาของ Wendel and associates,1996(6)มีได้ 1%ดังนั้นการตรวจ PEFR, FEV1 ขณะตั้งครรภ์ มีความสำคัญพอๆกับการสังเกตอาการขณะตั้งครรภ์ (3)ดังนั้นการตรวจPeak expiratory flow rate(PEFR), FEV1ขณะตั้งครรภ์ มีความสำคัญพอๆกับการสังเกตอาการขณะตั้งครรภ์ (4)
Pregnancy outcome
ในกลุ่ม mild, moderate asthma จะมีผลการตั้งครรภ์ที่ดี
มีบางการศึกษาที่พบว่ามีความเสี่ยงในการเกิด preeclampsia, preterm, growth restriction, Low birth weightได้(7)ซึ่งได้มีการศึกษาพบว่ามีความสัมพันธ์กับค่าbaselineFEV1ซึ่งสัมพันธ์ไปทางเดียวกับbirth weight และมีความสัมพันธ์กลับกันกับอัตราการเกิด gestational hypertension, preterm delivery(8)
Fetal effect
หากมีการควบคุมอาการเป็นอย่างดี ผลลัพธ์ต่อทารกในครรภ์จะค่อนข้างดี แต่ในกลุ่ม severe asthma พบว่ามีfetal growth restriction มากขึ้น
สำหรับยาที่ใช้ในการรักษาหอบหืดในหญิงตั้งครรภ์ สามารถใช้ได้ทุกตัวเช่นเดียวกับคนที่ไม่ได้ตั้งครรภ์ ยังไม่พบหลักฐานว่ามีผลเสียต่อทารกในครรภ์(4)
Clinical evaluation
Pulmonary function test เป็นตัวช่วยในการดูแลผู้ป่วยทั้งแบบโรคหอบหืดเรื้อรังและที่มีอาการแบบฉับพลันซึ่งค่า FEV1,PEFRเป็นค่าที่บอกถึงความรุนแรงของโรคได้ดี หาก FEV1<1 ลิตร หรือ < 20% of predicted value จะสัมพันธ์กับภาวะhypoxia และการตอบสนองต่อการรักษาที่ไม่ดีนอกจากนี้ควรตรวจค่า PEFR เป็นพื้นฐานไว้เพื่อเปรียบเทียบกับเมื่อมีอาการ ซึ่งค่า PEFR นั้นจะไม่เปลี่ยนแปลงในการตั้งครรภ์ปกติ
Management of chronic asthma
ในกลุ่ม moderate, severe asthma ควรมีการวัดค่า FEV1หรือ PEFR สองครั้งต่อวัน โดย FEV1ควรมากกว่า 80% และPEFR ควรอยู่ในช่วง 380-550L/min
แนวทางการรักษาผู้ป่วยโรคหอบหืดตามระดับความรุนแรงของอาการ แสดงดังภาพด้านล่าง
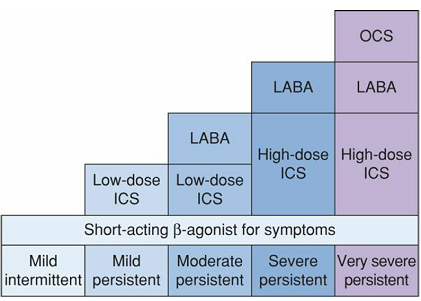
ภาพที่ 3 แสดงแนวทางการรักษาโรคหอบหืดตามระดับความรุนแรงของอาการ (Modified from Barnes,2012)(2) (ภาพจาก Williams obstetric24th edition , page 1014,2014)
{tabulizer:style[gr.alterora.elemental_1_green.css]}
|
severity |
treatment |
|
Mild intermittent asthma |
No daily medication, albuterol as need |
|
Mild persistent asthma |
Preferred : Low-dose inhaled corticosteroid Alternative : Cromolyn , Leukotriene receptor antagonist, or theophylline |
|
Moderate persistent asthma |
Preferred : Low-dose inhaled corticosteroid and salmeterol or medium- dose inhaled corticosteroidor (if needed) medium-dose inhaled corticosteroid and salmeterol Alternative : Low-dose inhaled corticosteroid or (if needed) medium-dose inhaled corticosteroid and either leukotriene receptor antagonist or theophylline |
|
Severe persistent asthma |
|
ตารางที่ 2 แสดงแนวทางการรักษาโรคหอบหืดตามระดับความรุนแรง จาก ACOG,2008(3)
หมายเหตุ : Theophylline serum level = 5-12 mcg/ml
แนวทางการให้Inhaled corticosteroids
{tabulizer:style[gr.alterora.elemental_1_green.css]}
|
Corticosteroid |
Amount |
Low Dose |
Medium Dose |
High Dose |
| Beclomethasone HFA | 40 mcg per puff
80 mcg per puff |
2-6 puffs
1-3 puffs |
More than 6-12 puffs
More than 3-6 puffs |
More than 12 puffs
More than 6 puffs |
| Budesonide | 200 mcg per inhalation | 1-3 puffs | More than 3-6 puffs | More than 6 puffs |
| Flunisolide | 250 mcg per puff | 2-4 puffs | 4-8 puffs | More than 8 puffs |
| Fluticasone HFA | 44 mcg per puff
110 mcg per puff 220 mcg per puff |
2-6 puffs
2 puffs
|
2-4 puffs 1-2 puffs |
More than 4 puffs More than 2 puffs |
| Fluticasone DPI | – 50 mcg per inhalation
– 100mcg per inhalation – 250 mcg per inhalation
|
2-6 puffs
1-3 puffs
1 puff |
3-5 puffs
2 puffs |
More than 5 puffs
More than 2 puffs |
| Momethasone | 200 mcg per inhalation | 1 puff | 2 puffs | More than 2 puffs |
| Triamcinolone | 75 mcg per puff | 4-10 puffs | 10-20 puffs | More than 20 puffs |
ตารางที่ 3 แนวทางการให้ Inhaled corticosteroids(4)
หมายเหตุ*Total daily puffs is usually divided into a twice-per-day regimen.
DPI : dry power inhaler; HFA: hydrofluoroalkane
Budesonide : pregnancy class B, Other ICS: class C
สำหรับ Inhaled corticosteroid (ICS)ที่นิยมให้คือ Budesonide (เนื่องจากหลายการศึกษาเลือกใช้)แต่อย่างไรก็ตามยังไม่มีข้อห้ามสำหรับ ICS ตัวอื่นๆ ในขณะตั้งครรภ์ นอกจากนี้มีการศึกษาของ Wendel and colleagues(1996)(6)พบว่า การให้ ICSควบคู่ β-agonist สามารถลดอัตราการกลับมานอนโรงพยาบาลในกลุ่มหญิงตั้งครรภ์ที่มี severe exacerbationได้
ยากลุ่มอื่นๆ
– Theophylline (pregnancy class C)
ออกฤทธิ์ anti-inflammation อาจใช้เป็น maintenance therapy ในกรณีที่ผลการรักษาของ ICS และ β-agonist จะ ไม่ดีพอแต่เนื่องจากมี narrow therapeutic index ทำให้พบผลข้างเคียงได้มากกว่า ได้แก่ insomnia, heartburn, palpitations, nausea ระดับยาในเลือดที่เหมาะสม คือ 5-12 mcg/mlได้มีการศึกษาเปรียบเทียบกับ ICS พบว่าไม่มีผลแตกต่างกันในเรื่องของ perinatal outcome(9)
– Antileukotrienes (pregnancy class B)ผลการศึกษาพบว่าทำให้ค่า FEV1ดีขึ้น(4)ใช้เป็น maintenanceควบคู่กับ ICS
– Cromolyn (pregnancy class B)
ออกฤทธิ์ยับยั้งการตอบสนองต่อallergenทั้งในระยะแรกและระยะหลัง และยังป้องกันการเกิด airway hyperresponsivenessจะเลือกใช้ใน chronic asthma แต่ประสิทธิภาพก็ยังไม่เทียบเท่า ICS(4)
– Oral corticosteroid (pregnancy class C)
มีหลายการศึกษาในมนุษย์ให้ผลขัดแย้งกัน บางรายงานพบว่าหากให้ใช้ในช่วง 1sttrimester มีโอกาสเกิด cleft lip ที่มีหรือไม่มี cleft palate ร่วมด้วย 3 เท่า(10) บางรายงานพบว่ามีโอกาสเกิดpleeclampsia ,low birth weight ได้(ซึ่งก็แยกได้ยากว่าเป็นผลจากยาหรือตัวโรคเอง) แนะนำใช้ในกลุ่ม severe asthma หรือ exacerbation ปริมาณยาที่แนะนำกรณี exacerbation
Methyl prednisolone , other corticosteroid: 120-180 mg/day (แบ่งให้ 3-4 ครั้ง)และให้เป็น oral corticosteroid 60-80 mg/day(4)
สำหรับในกลุ่มผู้ป่วยที่เคยรับการรักษาโดย allergen immunotherapy มาตั้งแต่ก่อนตั้งครรภ์สามารถให้ต่อเนื่องได้ หากเป็นการได้รับในครั้งแรกๆ ต้องเฝ้าระวังเรื่อง anaphylaxsisด้วย เนื่องจากมีระดับ allergen ค่อนข้างสูง(3)
Antenatal management
ผู้ป่วยกลุ่ม moderate-severe asthma มีโอกาสเกิดภาวะแทรกซ้อนในขณะตั้งครรภ์ ควรทำ daily peak flow monitor สำหรับการ surveillance ทารกในครรภ์ควรทำอัลตราซาวน์ดู growth, fetal activity ตั้งแต่ GA32 weeks (4)
Management of acute asthma
ให้การรักษาเช่นเดียวกับในคนปกติ โดยเป้าหมายของการรักษา คือ Po2> 60 mmHg, O2sat ≥95%
1st line therapy คือ β-adrenergic agonist ได้แก่ terbutaline, albuterol, isoetharine,epinephrine, isoproterenol, metaproterenol
สำหรับ corticosteroids ให้เป็น oral หรือ parenteral ก็ได้ เช่น methylprednisolone 40-60 mg, ทุก 6 ชั่วโมง ทั้งหมด 4 dose(2)ซึ่งมีประสิทธิผลเทียบเท่า prednisolone แบบ oral
เป้าหมายในการรักษา คือ
– FEV1หรือ PEFR>70% ของ baselineให้กลับบ้านได้
– FEV1 หรือ PEFR<50%ของ baseline พิจารณานอนโรงพยาบาล
Labor and Delivery
มีหลักการดูแลดังนี้
1. กรณี elective delivery พิจารณาเลื่อนไปหากในขณะนั้นมี exacerbation(4)
2. กลุ่มที่ได้ systemic corticosteroid ภายใน 4 สัปดาห์ก่อนคลอด ให้ Stress dose corticosteroid : Hydrocortisone 100 mg IV ทุก 8 ชั่วโมง ตั้งแต่เจ็บครรภ์คลอดจนถึง 24 ชั่วโมงหลังคลอดเพื่อป้องกันภาวะ adrenal crisis
3. ควรประเมิน FEV1 หรือ PEFR ขณะนอนโรงพยาลและประเมินซ้ำหากมีอาการมากขึ้น
4. Anesthesia มีหลักการดังนี้
- สำหรับ surgical delivery ควรใช้เป็น conduction delivery มากกว่าการทำ tracheal intubation เพราะจะกระตุ้นให้เกิด severe bronchospasm(2)
- พิจารณาให้ ketamine ในการ induction ของการทำ general anesthesia เพราะป้องกัน bronchospasm ได้(4)
- การทำ lumbar anesthesia สามารถลด oxygen consumption, minute ventilation ในระหว่างคลอด (4)
- Regional anesthesia พบว่าเกิด bronchospasm ได้ 2%(3)
5. ยาที่สามารถให้ได้ในระยะคลอด ได้แก่ Prostaglandin E2 or E1, Magnesium sulfate (bronchodilator)
6. ยาที่ห้ามให้ในระยะคลอด ได้แก่(4)
- Carboprost(15-methyl PGF2α), ergonovine, methylergonovine(Methergine) เพราะทำให้เกิดbronchospasm
- Indomethacin ทำให้เกิด bronchospasm ในผู้ป่วยที่เป็น aspirin sensitive ได้
7. Analgesic drug ควรให้เป็น fentanyl มากกว่า meperidine(ทำให้มีการหลั่งของ histamine)
Breast Feeding
ยาที่รักษาหอบหืดทุกตัวสามารถให้ได้ขณะให้นมบุตร ยาผ่านเข้าน้ำนมเพียงเล็กน้อย สำหรับในบางรายพบว่า theophylline เกิด toxic effect ในทารกได้ ซึ่งจะมีอาการดังนี้vomiting, feeding difficulties, jitteriness, cardiac arrhythmia
เอกสารอ้างอิง
- Michael Schatz M M, Steven E Weinberger M. Uptodate :Management of asthma during pregnancy 2015 [updated 17 Feb,2015].
- Cunningham F, Leveno, K., Bloom, S., Spong, C. Y., & Dashe, J. Williams obstetrics. 24th ed: McGraw Hill Professional; 2014.
- Obstetricians ACo, Gynecologists, Obstetricians ACo, Gynecologists. Asthma in pregnancy. ACOG Practice Bulletin No. 90. Obstetrics and Gynecology. 2008;111(2):457-64.
- Creasy RK, Resnik R, Iams JD. Maternal-fetal medicine: principles and practice: Gulf Professional Publishing; 2004.
- Schatz M, Dombrowski MP, Wise R, Thom EA, Landon M, Mabie W, et al. Asthma morbidity during pregnancy can be predicted by severity classification. Journal of allergy and clinical immunology. 2003;112(2):283-8.
- Wendel PJ, Ramin SM, Barnett-Hamm C, Rowe TF, Cunningham FG. Asthma treatment in pregnancy: a randomized controlled study. American journal of obstetrics and gynecology. 1996;175(1):150-4.
- Murphy V, Namazy J, Powell H, Schatz M, Chambers C, Attia J, et al. A meta‐analysis of adverse perinatal outcomes in women with asthma. BJOG: An International Journal of Obstetrics & Gynaecology. 2011;118(11):1314-23.
- Schatz M, Dombrowski MP, Wise R, Momirova V, Landon M, Mabie W, et al. Spirometry is related to perinatal outcomes in pregnant women with asthma. American journal of obstetrics and gynecology. 2006;194(1):120-6.
- Health NIo. National Asthma Education and Prevention Program. Working group report on managing asthma during pregnancy: recommendations for pharmacologic treatment, update 2004. 2006.
- Källén B. Maternal drug use and infant cleft lip/palate with special reference to corticoids. The Cleft palate-craniofacial journal. 2003;40(6):624-8.


