ทารกบวมน้ำที่ไม่เกี่ยวข้องกับปฏิกิริยาอิมมูน
Nonimmune hydrops fetalis (NIHF)
พญ.ณัฏฐา ยศชนะ
รศ.ดร.นพ.ภูดิศ เจต๊ะวรรณ
บทนำ
ทารกบวมน้ำ (hydrops fetalis) คือภาวะที่มีการสะสมของน้ำในชั้นเนื้อเยื่อ (soft tissue) และ ช่องว่างของร่างกาย (serous cavity) สามารถวินิจฉัยได้จากลักษณะที่เห็นจากคลื่นเสียงความถี่สูงคือ ตรวจพบมีน้ำสะสมในช่องว่างของร่างกายอย่างน้อยสองตำแหน่ง ได้แก่ 1.น้ำในช่องท้อง (ascites) 2.น้ำในช่องปอด (pleural effusion) 3.น้ำคั่งในช่องเยื่อหุ้มหัวใจ (pericardial effusion) และ 4.ชั้นใต้ผิวหนังบวมน้ำ(generalized skin edema : skin thickness >5mm)โดยอาจตรวจพบความหนาของรกที่เพิ่มขึ้นกว่าปกติ(placental thickening) โดยวัดความหนาของรกได้มากกว่าหรือเท่ากับ 4 เซนติเมตรในช่วงไตรมาสที่สอง หรือ มากกว่าหรือเท่ากับ 6 เซนติเมตรในช่วงไตรมาสที่สาม และภาวะครรภ์แฝดน้ำ(polyhydramnios) ร่วมด้วยจากการตรวจด้วยเครื่องคลื่นเสียงความถี่สูง (1)
ทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูน (nonimmune hydrops fetalis : NIHF) หมายถึงทารกบวมน้ำที่ไม่ได้เกิดจากภาวะซีดของทารกที่เกิดจากแอนติบอดีของมารดาเข้าไปทำลายเม็ดเลือดแดงของทารก ซึ่งพบเป็นสาเหตุหลักประมาณ90% ของทารกบวมน้ำในปัจจุบัน (2) และมีอุบัติกาณ์อยู่ที่ 1 ต่อ 1700 ถึง 3000 ของการตั้งครรภ์(3) ซึ่งพบมากในประเทศภูมิภาคเอเชียตะวันออกเฉียงใต้ เนื่องจากพบว่ามีความชุกของโรคแอลฟาธาลัสซีเมีย(alpha thalassemia disease)ที่สูงกว่าภูมิภาคอื่น ๆ
ปัจจุบันอุบัติการณ์ของทารกบวมน้ำที่เกิดจากปฏิกิริยาภูมิคุ้มกัน (immune hydrops fetalis) ลดลง ซึ่งที่สาเหตุที่พบได้บ่อยคือภาวะของการไม่เข้ากันของหมู่เลือด Rh ระหว่างมารดากับทารก (Rh incompatibility) เป็นผลจากการพัฒนาของ Rh immunoglobulin ที่ใช้อย่างแพร่หลายมากขึ้น(3)
พยาธิสรีรวิทยาของทารกบวมน้ำ
พยาธิสรีรวิทยาของทารกบวมน้ำ เกิดจากการไม่สมดุลในการแลกเปลี่ยนสารน้ำระหว่าง ภายในหลอดเลือด (intravascular) และช่องว่างระหว่างเซลล์ (interstitial space) โดยมีการผลิตสารน้ำในช่องว่างระหว่างเซลล์ (interstitial space) มากขึ้น หรือมีการไหลเวียนกลับของระบบน้ำเหลือง (lymphatic return)ลดลง อธิบายได้จากหลายกลไก ได้แก่
1. การเพิ่มขึ้นของความดันในหัวใจซีกขวา (right heart pressure) เป็นผลจากการเพิ่มขึ้นของความดันเส้นเลือดดำส่วนกลาง (central venous pressure)
2. การอุดกั้นของการไหลเวียนเลือดดำหรือเลือดแดง (obstruction of venous or arterial blood flow)
3. ภาวะที่มีการบกพร่องของการคลายตัวของหัวใจห้องล่าง (inadequate diastolic ventricular filling)
4. การคั่งของปริมาณเลือดดำในตับ (hepatic venous congestion)ทำให้การทำงานของตับแย่ลงส่งผลให้มีการผลิตโปรตีนอัลบูมินลดลง
5. การเพิ่มขึ้นของปริมาณของเหลวผ่านผนังหลอดเลือด(capillary permeability)
6. ภาวะซีดทำให้เกิดหัวใจล้มเหลวจากการที่ร่างกายต้องการปริมาณเลือดที่ออกจากหัวใจมากกว่าปกติ(high output cardiac failure) และ การสร้างเม็ดเลือดนอกไขกระดูก(extramedullary hematopoiesis)
7. การไหลเวียนน้ำเหลืองอุดตัน (lymphatic obstruction)
8. แรงดันออสโมซิส(osmotic pressure)ลดลงในเส้นเลือด(3)
ลักษณะทางคลินิก
ลักษณะทางคลินิกที่พบในหญิงตั้งครรภ์ สามารถตรวจพบขนาดของมดลูกโตกว่าอายุครรภ์ สตรีตั้งครรภ์มีความรู้สึกว่าลูกดิ้นลดลงหรือมีอาการหายใจลำบากจากการที่มีภาวะครรภ์แฝดน้ำ (polyhydramnios) หรือมีอาการของ Mirror syndrome เช่นตัวบวมขึ้น ความดันโลหิตสูง เป็นต้น
Mirror syndrome เกิดจากรกของทารกที่มีภาวะบวมน้ำผลิต sFlt-1มากขึ้น ทำให้เกิดภาวะครรภ์เป็นพิษ (preeclampsia) ซึ่งสามารถเกิดขึ้นได้ทั้งในช่วงระหว่างการตั้งครรภ์ไปจนถึงหลังคลอด อาการแสดงของภาวะ Mirror syndrome คล้ายกับภาวะครรภ์เป็นพิษได้แก่ หญิงตั้งครรภ์มีน้ำหนักเพิ่มขึ้นมาก มีภาวะตัวบวม มีอาการหายใจเหนื่อย ซึ่งภาวะ Mirror syndrome จะสามารถหายได้เอง เมื่อคลอดทารกที่มีภาวะบวมน้ำ หรือ ทารกบวมน้ำได้รับการรักษาสาเหตุที่ทำให้เกิดภาวะบวมน้ำภายในครรภ์ หรือ ทารกบวมน้ำในครรภ์เสียชีวิต(4)
สาเหตุ
การวินิจฉัยภาวะทารกบวมน้ำสามารถทำการวินิจฉัยได้จากลักษณะที่เห็นจากคลื่นเสียงความถี่สูงดังที่กล่าวไปข้างต้น แต่สิ่งที่ทำได้ยากคือการค้นหาสาเหตุ ซึ่งบางสาเหตุอาจเห็นได้จากคลื่นเสียงความถี่สูงตั้งแต่ครั้งแรกที่ทำการวินิจฉัยภาวะทารกบวมน้ำ ร่วมกับการสืบค้นเพิ่มเติมจากการตรวจทางห้องปฏิบัติการ ทั้งนี้การค้นหาสาเหตุของภาวะบวมน้ำมีความจำเป็น เนื่องจากสามารถบอกพยากรณ์ของโรค แนวทางการดูแลรักษา และ บอกความเสี่ยงของการเป็นซ้ำในครรภ์ถัดไปได้(3)
สาเหตุจากหัวใจและหลอดเลือด (Cardiovascular cause)
เป็นสาเหตุที่พบได้บ่อยของทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูน เกิดจาก โครงสร้างหัวใจของทารกผิดปกติ (cardiac structural abnormality), หัวใจทารกเต้นผิดจังหวะ (arrhythmia), โรคของกล้ามเนื้อหัวใจหนาผิดปกติ (cardiomyopathy), เนื้องอกของกล้ามเนื้อหัวใจ (cardiac tumor), ความผิดปกติของเส้นเลือด (vascular abnormality)โดยภาวะดังกล่าวทำให้เกิดทารกบวมน้ำจากการที่มีความดันเพิ่มขึ้นของระบบเส้นเลือดดำส่วนกลาง(central venous pressure) หรือ มีการบกพร่องของการคลายตัวของหัวใจห้องล่าง (inadequate diastolic ventricular filling)
ทารกบวมน้ำที่เกิดจากโครงสร้างหัวใจทารกผิดปกติ (cardiac structural abnormality) จะมีพยากรณ์โรคที่ไม่ดี เนื่องจากทารกจะมีภาวะหัวใจวายตั้งแต่อยู่ในครรภ์ ซึ่งสามารถเกิดการเสียชีวิตในครรภ์และหลังคลอดได้ และมักสัมพันธ์กับทารกที่มีโครโมโซมผิดปกติ (chromosome abnormality)(3)
ภาวะหัวใจทารกเต้นเร็วผิดจังหวะ (tachyarrhythmia) ที่พบได้บ่อยคือ supraventricular tachycardia รองลงมาคือ atrial flutter, reentry tachycardia, long QT syndrome, ventricular tachycardia ภาวะหัวใจทารกเต้นเร็วผิดจังหวะอาจพบได้ในมารดาที่เป็นไทรอยด์เป็นพิษจาก Graves’ disease เกิดจากการที่มี Thyroid stimulating hormone antibody ผ่านรกไปกระตุ้นต่อมไทรอยด์ของทารกในครรภ์ ทำให้เกิดภาวะ Fetal thyroid goiter, Fetal tachycardia, Advance bone age, Poor growth, Craniosynostosis โดยอาจรุนแรงจนทารกเกิดภาวะหัวใจวายในครรภ์นำไปสู่ภาวะทารกบวมน้ำได้(5)
ภาวะหัวใจทารกเต้นช้าผิดจังหวะ(Bradyarrhythmia) ที่พบได้บ่อยคือ congenital heart block เกิดจากการที่มารดาเป็นโรคภูมิคุ้มกันบกพร่องและมี แอนติบอดีย์ชนิด anti-Ro ส่งผ่านรกไปยังทารกเข้าไปทำลาย fetal bundle of His และ Purkinje fiber โดยตรงทำให้เกิด congenital heart block
นอกจากนี้ congenital heart block อาจเกิดจากโครงสร้างหัวใจทารกผิดปกติ(cardiac structural abnormalities) ที่มีความผิดปกติที่ cardiac conduction บริเวณ AV node เช่น endocardial cushion defect ในโรค Heterotaxy syndrome(5)
ความผิดปกติของโครโมโซม(Chromosome abnormality)
ความผิดปกติของโครโมโซมที่สัมพันธ์กับภาวะทารกบวมน้ำที่พบได้บ่อยที่สุดคือ กลุ่มอาการเทอร์เนอร์ (turner syndrome)เกิดจากความผิดปกติของโครโมโซมเพศหญิง รองลงมาคือ กลุ่มอาการดาวน์ (Down syndrome),กลุ่มอาการพาทัวร์ (Patau’s syndrome),กลุ่มอาการเอ็ดเวิร์ด (Edwards’ syndrome)ซึ่งเกิดจากการเพิ่มขึ้นของจำนวนโครโมโซมร่างกาย(trisomy)คู่ที่ 21,13 และ18 ตามลำดับ โดยมักจะพบภาวะทารกบวมน้ำในช่วงไตรมาสแรกและไตรมาสที่สอง
กลุ่มอาการเทอร์เนอร์(turner syndrome) สัมพันธ์กับ cystic hygroma ได้ 50-80%(6) ซึ่งเกิดจากความผิดปกติของการเชื่อมต่อของระบบน้ำเหลือง(lymphatic system)กับเส้นเลือดดำ(venous drainage)บริเวณส่วนคอของทารกเจริญได้ไม่ดี ทำให้เกิด lymphatic dysplasia และเกิดภาวะทารกบวมน้ำ
Trisomy 13, 18 และ 21 มักสัมพันธ์กับโครงสร้างหัวใจทารกผิดปกติ(cardiac structural abnormality) ทำให้เกิดภาวะทารกบวมน้ำ แต่ใน Trisomy 21 ยังมีกลไกอื่นที่ทำให้เกิดภาวะทารกบวมน้ำได้คือ ภาวะซีดจาก Transient myelopoiesis, Leukemic condition (7)
ดังนั้นภาวะทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูน (nonimmune hydrops fetalis : NIHF) ที่พบหรือไม่พบความผิดปกติของโครงสร้างอวัยวะ มีหรือไม่มีภาวะซีด แนะนำให้สืบค้นเพิ่มเติมเพื่อวินิจฉัยความผิดปกติของโครโมโซมทารกในครรภ์ทุกราย(3)
ภาวะทารกซีด(Fetal anemia)
ภาวะซีดของทารกในครรภ์ทำให้เกิดทารกบวมน้ำได้ทั้งเกี่ยวและไม่เกี่ยวกับปฏิกิริยาอิมมูน โดยสาเหตุของภาวะซีดที่ทำให้เกิดภาวะทารกบวมน้ำไม่เกี่ยวกับปฏิกิริยาอิมมูน ได้แก่ ความผิดปกติของฮีโมโกบิน(hemoglobinopathies) , การสลายของเม็ดเลือดแดง (hemolysis), ภาวะเลือดทารกเข้าสู่ระบบไหลเวียนเลือดของมารดา (feto-maternal hemorrhage), การติดเชื้อพาร์โวไวรัส (parvovirus infection) โดยภาวะซีดทำให้เกิดหัวใจล้มเหลวจากการที่ร่างกายต้องการปริมาณเลือดที่ออกจากหัวใจมากกว่าปกตินำไปสู่ภาวะทารกบวมน้ำ
ภาวะซีดของทารกในครรภ์สามารถตรวจคัดกรองโดยการวัด Doppler fetal MCA PSV โดยเครื่องคลื่นเสียงความถี่สูง หากวัดได้มากกว่าหรือเท่ากับ 1.5 MoM ในอายุครรภ์นั้นๆ แสดงว่าทารกมีภาวะซีดปานกลางถึงสูง จำเป็นต้องเจาะเลือดสายสะดือของทารกเพื่อวินิจฉัยจากค่าความเข้มข้นของเลือด (hematocrit) ทารกโดยตรง โดยจะวินิจฉัยว่าทารกมีภาวะซีดเมื่อความเข้มข้นของเลือดทารกน้อยกว่า 30%
ความผิดปกติของฮีโมโกลบิน(hemoglobinopathies)(8)ที่ทำให้เกิดทารกบวมน้ำที่พบบ่อยที่สุดคือโรคแอลฟาทาลัสซีเมีย(alpha thalassemia disease) พบได้มากในกลุ่มประเทศเอเชียตะวันออกเฉียงใต้ เป็นโรคถ่ายทอดทางพันธุกรรมแบบยีนด้อย(autosomal recessive) หากทารกในครรภ์ขาดยีนควบคุมการสร้างแอลฟ่าโกลบิน 4 ตำแหน่ง ทำให้ไม่มีการสร้าง alpha-globin chain ทารกในครรภ์จะมีฮีโมโกลบินชนิด Hb Bart ซึ่งขนส่งออกซิเจนไปสู่เนื้อเยื่อได้ไม่ดี มีอายุของเม็ดเลือดสั้นกว่าปกติเนื่องจากโครงสร้างเม็ดเลือดที่ผิดปกติ ทำให้ทารกมีภาวะขาดออกซิเจนในครรภ์ หัวใจทำงานมากกว่าปกติจึงเกิดเป็นทารกบวมน้ำ
ภาวะเลือดทารกเข้าสู่ระบบไหลเวียนเลือดของมารดา (feto-maternal hemorrhage) จะทำให้เกิดทารกบวมน้ำได้เมื่อทารกเสียเลือดปริมาณมากทำให้เกิดภาวะซีด แต่ไม่มากพอที่จะทำให้เกิด fetal hypovolemia จนเสียชีวิต ภาวะเลือดทารกเข้าสู่ระบบไหลเวียนเลือดของมารดาสามารถตรวจได้จาก Kleihauer-Betke smear โดยจะเห็น fetal cell ใน maternal peripheral blood นอกจากนี้การตรวจ flow cytometry ยังสามารถบอกปริมาณเลือดของทารกที่เข้าสู่ระบบไหวเวียนเลือดมารดาได้ การที่ทารกซีดจนเกิดทารกบวมน้ำจากภาวะนี้สามารถรักษาได้ด้วยการเติมเลือดให้กับทารกในครรภ์ (intrauterine transfusion)(9)
สาเหตุอื่นๆที่ทำให้เกิดทารกซีดและบวมน้ำ เช่น G-6-PD deficiency, Erythrocyte enzymopathies เช่น pyruvate kinase deficiency ซึ่งตรวจพบได้ยากกว่าจึงมีรายงานน้อยในปัจจุบัน
ภาวะติดเชื้อ(Infection)
การติดเชื้อระหว่างการตั้งครรภ์เป็นสาเหตุของทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูนได้ 5-10% ที่พบได้บ่อยที่สุดคือ การติดเชื้อพาร์โวไวรัส(Parvovirus B19) รองลงมาคือ Cytomegalovirus, Toxoplasmosis, Syphilis การติดเชื้อระหว่างการตั้งครรภ์สามารถทำให้เกิดทารกบวมน้ำได้จาก Anemia, Anoxia, Endothelial cell damage, Increase capillary permeability และ Myocarditis(3)
ลักษณะที่เห็นจากคลื่นเสียงความถี่สูงที่ช่วยบ่งบอกว่าทารกมีภาวะติดเชื้อในครรภ์นอกจากลักษณะของทารกบวมน้ำแล้ว อาจพบว่ามีจุดสีขาวจากการสะสมของหินปูน (calcification) ที่สมอง ตับ หรือ เยื่อหุ้มหัวใจได้ , ทารกศีรษะเล็ก (microcephaly) ,ช่องโพรงน้ำในสมองมีขนาดใหญ่ (ventriculomegaly), ตับม้ามโต(hepatosplenomegaly), ทารกโตช้าในครรภ์ (intrauterine growth restriction) เป็นต้น (10)
การติดเชื้อพาร์โวไวรัส(Parvovirus B19) เป็นสาเหตุที่พบได้บ่อยที่สุดในภาวะติดเชื้อในครรภ์ที่ทำให้ทารกเกิดภาวะซีดและบวมน้ำ เนื่องจากไวรัสมีเซลล์เม็ดเลือดแดงตัวอ่อนที่ไขกระดูกเป็นเป้าหมาย ทำให้เซลล์เม็ดเลือดแดงตัวอ่อนตาย(Apoptosis) จึงไม่สามารถสร้างเซลล์เม็ดเลือดแดงได้ นำมาสู่ภาวะทารกซีดในครรภ์ หากการติดเชื้อเกิดขึ้นในช่วงอายุครรภ์น้อยกว่า 20 สัปดาห์จะนำมาสู่การการพยากรณ์ของโรคที่ไม่ดี หากติดเชื้อที่อายุครรภ์ 13-20 สัปดาห์ทารกจะมีความเสี่ยงที่จะเสียชีวิต 15 % และ 6% หากติดเชื้อที่อายุครรภ์มากกว่า 20 สัปดาห์ ในบางรายภาวะซีดเป็นเพียงชั่วคราวและสามารถดีขึ้นได้จากการเติมเลือดให้ทารกในครรภ์ จึงมีการแนะนำให้ทำการเติมเลือดให้ทารกในครรภ์ที่ซีดและบวมน้ำจากการติดเชื้อพาร์โวไวรัส(11)
ความผิดปกติบริเวณทรวงอกของทารก (fetal thoracic abnormalities)
ความผิดปกติบริเวณทรวงอกของทารกสามารถทำให้เกิดทารกบวมน้ำได้ ไม่ว่าจะเป็น congenital pulmonary airway malformation(CPAM) ที่มีขนาดใหญ่ หรือ pulmonary sequestrationที่อาจพบร่วมกับน้ำในช่องปอด (pleural effusion) ทำให้เกิดการไหลเวียนกลับของเลือดดำในทารกไม่ดี อาจจะทำให้เกิดการกดของหลอดอาหารของทารก ทำให้ขัดขวางการกลืนน้ำคร่ำของทารกลด นำไปสู่ภาวะครรภ์แฝดน้ำได้(12)
congenital pulmonary airway malformation (CPAM) และ pulmonary sequestration เป็นความผิดปกติในปอดที่ทำให้เกิดทารกบวมน้ำได้บ่อย หากมีภาวะบวมน้ำแล้วพยากรณ์โรคจะแย่ลงถ้าทารกไม่ได้รับการรักษา
โรคทั้งสองสามารถเห็นได้จากคลื่นเสียงความถี่สูง CPAM จะเห็นก้อนในทรวงอกหรือถุงน้ำในทรวงอก ส่วน Pulmonary sequestration จะเห็นลักษณะเนื้อตันในทรวงอกเมื่อตรวจ color doppler study อาจเห็นเส้นเลือดที่มาเลี้ยงจาก systemic circulation(12)
น้ำคั่งในช่องปอดที่ทำให้เกิดทารกบวมน้ำได้ คือ chylothorax ที่เกิดจากการอุดกั้นของระบบทางเดินน้ำเหลือง โดยจะวินิจฉัยได้จากการทำคลื่นเสียงความถี่สูงเห็นน้ำคั่งในช่องปอดปริมาณมาก และทำการเจาะน้ำในช่องปอดทารกมาตรวจจะพบว่ามี เม็ดเลือดขาวชนิด lymphocyte มากกว่า 80% และไม่พบว่ามีการติดเชื้อ(3)
Twin-Twin transfusion syndrome (TTTS)
พบในครรภ์แฝดชนิดรกเดียว Monochorionic เกิดจากการเชื่อมต่อกันของเส้นเลือดทารกของแฝดทั้งสอง ทำให้มีการไหลเวียนเลือดที่ไม่สมดุล โดยเลือดจากเส้นเลือดแดงของแฝดผู้ให้(donor) เข้าสู่เส้นเลือดดำของแฝดผู้รับ (recipient) ทำให้ แฝดผู้ให้(donor) มีภาวะซีด โตช้า น้ำคร่ำน้อย ส่วนแฝดผู้รับ (recipient) จะเกิดภาวะน้ำเกิน เลือดข้น น้ำคร่ำมาก และเกิดภาวะทารกบวมน้ำได้ โดยหากเกิดภาวะบวมน้ำแล้วถือว่าพยากรณ์โรคไม่ดี(13)
Twin reversed-arterial-perfusion (TRAP)
พบได้น้อยเกิดจากการที่มีการเชื่อมกันของเส้นเลือดแดงระหว่างแฝดทั้งสองคนโดยไม่ผ่านรก ทำให้ แฝดผู้รับ (recipient) ได้รับเลือดที่ออกซิเจนต่ำและไหลเวียนไปเลี้ยงส่วนล่างของร่างกายทำให้ไม่มีการพัฒนาของหัวใจและอวัยวะส่วนบนเกิดเป็น acardiac twin แฝดผู้รับ (recipient)จะไม่สามารถมีชีวิตรอด และปัญหาจะเกิดกับแฝดผู้ให้(donor) เนื่องจากจะต้องส่งเลือดไปยังแฝดผู้รับ (recipient) ทำให้เกิดภาวะหัวใจล้มเหลวจากการทำงานของหัวใจที่หนักเกินไป ประกอบกับปริมาณน้ำเลือดที่มากจากแฝดผู้ให้ ทำให้เกิดภาวะทารกบวมน้ำได้ในที่สุด(13)
ความผิดปกติของระบบทางเดินปัสสาวะ (genitourinary abnormalities)
พบเป็นสาเหตุของทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูนน้อย ความผิดปกติของระบบทางเดินปัสสาวะที่มีการอุดกั้นจนทำให้เกิด bladder rupture, renal collecting system rupture ทำให้เกิด urinary ascites คล้ายกับการที่มี ascites ในทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูนได้
ส่วนโรคที่ทำให้เกิดทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูนโดยตรงคือ congenital nephrotic syndrome ทารกจะมีภาวะ hypoproteinemia ทำให้เกิดภาวะบวมน้ำจากการลดลงของ oncotic pressure จะสงสัยว่าทารกในครรภ์มีภาวะบวมน้ำจากโรคนี้เมื่อหญิงตั้งครรภ์มีระดับซีรัมอัลฟ่าฟีโตโปรตีน(Alpha fetoprotein : AFP) เพิ่มขึ้น ร่วมกับ พบ hyperechoic fetal kidney จากคลื่นเสียงความถี่สูง(14)
ความผิดปกติของระบบทางเดินอาหาร (gastrointestinal abnormalities)
เป็นสาเหตุของทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูนน้อย เช่นเดียวกับความผิดปกติของระบบทางเดินปัสสาวะ โดยความผิดปกติที่อาจเกี่ยวข้องกับทารกบวมน้ำได้แก่ diaphragmatic hernia, midgut volvulus, jejunal atresia, malrotation of intestine, meconium peritonitis กลไกลที่ทำให้เกิดทารกบวมน้ำอธิบายได้จากการที่มีก้อนในช่องท้องไปขัดขวางการไหลเวียนกลับของเลือดดำ การที่มีลำไส้อุดกั้นหรือขาดเลือดทำให้ colloid osmotic pressure ลดลง นอกจากนี้ความผิดปกติของการทำงานของตับที่ผลิตโปรตีนได้ลดลงก็ยังสามารถทำให้เกิดภาวะทารกบวมน้ำได้(15)
ความผิดปกติของรกและสายสะดือ(Placental and cord lesion)
ความผิดปกติของรกและสายสะดือที่เกี่ยวข้องกับทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูน ได้แก่ chorioangioma, angiomyxoma of the cord, aneurysm of umbilical artery, cord vein thrombosis, umbilical vein torsion, true knot, amniotic band
โดย chorioangioma พบว่าเป็นสาเหตุที่พบได้บ่อยที่สุด พบประมาณ 1% ของการตั้งครรภ์ โดยพยาธิสภาพขนาดเล็กจะไม่ส่งผลทางคลินิกมาก ในขณะที่พยาธิสภาพขนาดใหญ่โดยเฉพาะขนาดมากกว่า 5 เซนติเมตร จะทำให้เกิด high volume AV shunt และทำให้เกิดทารกบวมน้ำจาก หัวใจล้มเหลวจากการที่ร่างกายต้องการปริมาณเลือดที่ออกจากหัวใจมากกว่าปกติ (high output cardiac failure) (15)
เนื้องอกของอวัยวะทารก (fetal tumors)
เนื้องอกที่ผิดปกติของอวัยวะต่างๆของทารกในครรภ์ทำให้เกิดทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิม-มูน อธิบายได้จากกลไกเดียวกันกับ chorioangioma คือ หัวใจล้มเหลวจากการที่ร่างกายต้องการปริมาณเลือดที่ออกจากหัวใจมากกว่าปกติ (high output cardiac failure) โดยเนื้องอกที่พบบ่อยที่ทำให้เกิดภาวะทารกบวมน้ำ ได้แก่ sacrococcygeal teratoma, mediastinal teratoma, pharyngeal teratoma, neuroblastoma, large hemangioma, fetal tuberous sclerosis(15)
กลุ่มโรคกระดูกเจริญผิดปกติ (skeletal dysplasia)
กลุ่มโรคกระดูกเจริญผิดปกติ ได้แก่ achondroplasia, achondrogenesis, osteogenesis imperfecta, osteopetrosis, thanatophoric dysplasia, short-rib polydactyly syndrome, asphyxiating thoracic dysplasia สามารถทำให้เกิดทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูนได้ โดยกลไกอาจเกิดจากการที่ทารกตับโตขึ้นจากการที่ตับต้องทำงานเป็นแหล่งสร้างเม็ดเลือดแทนไขกระดูกที่มีน้อยทำให้กดเส้นเลือดดำส่งผลให้การหมุนเวียนเลือดดำผิดปกติ หรือเกิดจากการขัดขวางของการไหลเวียนเลือดดำหรือระบบน้ำเหลืองจากการที่มีทรวงอกที่เล็กลง(15)
โรคพันธุกรรมเมตาบอลิก (inborn error metabolism)
โรคพันธุกรรมเมตาบอลิกเป็นโรคถ่ายทอดทางพันธุกรรมแบบยีนด้อย (autosomal recessive) ทารกอาจจะมีความผิดปกติตั้งแต่อในครรภ์ พบว่าเป็นสาเหตุของทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูน 1-2 %
lysosomal storage disease ทำให้เกิดภาวะทารกบวมน้ำ ได้แก่ mucopolysaccharidoses, Gaucher disease, Niemann-Pick disease โดยกลไกที่ทำให้เกิดทารกบวมน้ำ คือมีการสะสมของสารในอวัยวะ ทำให้เกิดอวัยวะภายในบางส่วนโต (visceromegaly) กดการไหลเวียนของเลือดดำ การสร้างเม็ดเลือดแดงลดลงทำให้เกิดภาวะซีดในครรภ์
เป็นภาวะที่พบได้ไม่บ่อย แต่มีความสำคัญเนื่องจากเป็นโรคที่ถ่ายทอดทางพันธุกรรม และมีความเสี่ยงเกิดซ้ำได้สูงในครรภ์ถัดไป จึงต้องพิจารณาส่งตรวจเพิ่มเติมเพื่อวินิจฉัยในกรณีที่ทารกมีภาวะบวมน้ำที่มีโครงสร้างอวัยวะปกติจากคลื่นเสียงความถี่สูง และหาสาเหตุอื่นที่ทำให้เกิดภาวะบวมน้ำที่กล่าวไปก่อนหน้านี้ไม่พบ (16)
การประเมินและการสืบค้น(17)
ดังที่ได้กล่าวไปข้างต้นว่าการวินิจฉัยภาวะทารกบวมน้ำในครรภ์ทำได้ไม่ยากเนื่องจากเห็นได้ชัดจากภาพคลื่นเสียงความถี่สูง การค้นหาสาเหตุของภาวะทารกบวมน้ำทำได้ยากและอาจต้องอาศัยผู้เชี่ยวชาญในการทำและแปลผลคลื่นเสียงความถี่สูง รวมไปถึงการทำหัตถการวินิจฉัยก่อนคลอด
ขั้นตอนในการประเมินและสืบค้นหาสาเหตุของทารกบวมน้ำมีความสำคัญ เพื่อค้นหาสาเหตุที่สามารถรักษาหรือทำให้ทารกดีขึ้นได้ในครรภ์ เพื่อค้นหาโรคถ่ายทอดทางพันธุกรรมที่มีความเสี่ยงเป็นซ้ำสูงในครรภ์ถัดไป สาเหตุของทารกบวมน้ำบางสาเหตุสามารถบอกได้จากคลื่นเสียงความถี่สูงในครั้งแรกที่วินิจฉัยภาวะทารกบวมน้ำเช่น twin-to-twin transfusion, cardiac arrhythmia, cardiac structural abnormalities , placental abnormalities , fetal tumors เป็นต้น
การซักประวัติ (history taking)
ซักประวัติมารดาเกี่ยวกับความเสี่ยงและอาการของการติดเชื้อในระหว่างการตั้งครรภ์ และ ประวัติการตั้งครรภ์ทารกบวมน้ำในครอบครัว ประวัติโรคเลือดหรือโรคถ่ายทอดทางพันธุกรรมในครอบครัว หากมีประวัติสงสัยโรคถ่ายทอดทางพันธุกรรมในครอบครัว สามารถนำมาเขียนเป็นพงศาวลี (pedigree chart) เพื่อประเมินลักษณะการถ่ายทอดทางพันธุกรรมได้
คลื่นเสียงความถี่สูง(Ultrasound)
การทำคลื่นเสียงความถี่สูงเพื่อค้นหาความผิดปกติของทารกในครรภ์อย่างละเอียด รวมไปถึงคลื่นเสียงความถี่สูงหัวใจทารกในครรภ์(fetal echocardiography)เพื่อค้นหาความผิดปกติของโครงสร้างหัวใจและการเต้นของหัวใจทารก ดูลักษณะของรกและสายสะดือ วัดปริมาณน้ำคร่ำ คัดกรอง fetal anemia จากการวัด Doppler fetal MCA PSV โดยเครื่องตรวจคลื่นเสียงความถี่สูง
การตรวจทางห้องปฏิบัติการณ์ (laboratory examination)
Complete blood count and red blood cell indices ของหญิงตั้งครรภ์และสามีเพื่อประเมินว่ามีความเสี่ยงเป็นพาหะธาลัสซีเมียที่จะทำให้ทารกในครรภ์บวมน้ำจากภาวะ Hb Bartsหรือไม่ โดยหากหญิงตั้งครรภ์และสามีมี MVC< 80fL โดยไม่มีภาวะขาดธาตุเหล็ก จะต้องสืบค้นเพิ่มเติมด้วย Hb typing และ PCR for alpha thalassemia และนำมาประเมินความเสี่ยงของการเกิด Hb Barts ของทารกในครรภ์
Blood type and antibody screening เพื่อวินิจฉัยภาวะทารกบวมน้ำที่เกิดจากปฏิกิริยาอิมมูนที่เกิดจากการไม่เข้ากันของหมู่เลือด Rh ระหว่างมารดากับทารก (Rh incompatibility)
Kleihauer-Betke acid smear กรณีที่พบว่าทารกมีภาวะซีดและสงสัยว่าสาเหตุเกิดจากภาวะเลือดทารกเข้าสู่ระบบไหลเวียนเลือดของมารดา (fetomaternal hemorrhage)
serology ตรวจหา IgM และ IgG ในเลือดของหญิงตั้งครรภ์เมื่อสงสัยภาวะทารกบวมน้ำจากสาเหตุการติดเชื้อ parvovirus B19, CMV, toxoplasmosis
treponemal or non-treponemal antibody test เพื่อวินิจฉัยโรคซิฟิลิสในหญิงตั้งครรภ์ เนื่องจากภาวะทารกบวมน้ำพบได้ในภาวะ congenital syphilis
การเจาะน้ำคร่ำ (amniocentesis)
การตรวจ karyotyping / microarray จะส่งตรวจในทารกที่พบว่ามีความผิดปกติทางโครงสร้างจากคลื่นเสียงความถี่สูงมีความเสี่ยงสูงที่จะมีโครโมโซมผิดปกติ อย่างไรก็ตามควรส่ง karyotyping หรือ chromosome microarray ในทารกบวมน้ำที่ไม่ได้เกิดจากปฏิกิริยาอิมมูนทุกรายแม้ว่าจะมีความผิดปกติทางโครงสร้างหรือมีภาวะซีดหรือไม่ก็ตาม
testing for infection ภาวะทารกบวมน้ำจากสาเหตุการติดเชื้อสามารถวินิจฉัยโดยใช้ maternal serologyได้ แต่หากได้ทำ amniocentesis เพื่อตรวจโครโมโซมแล้ว แนะนำให้เก็บน้ำคร่ำเพิ่มเพื่อส่งตรวจ PCR หาเชื้อ CMV, parvovirus B19 และ toxoplasmosis ด้วย
amniotic fluid alpha-fetoprotein กรณีที่สงสัย congenital nephrotic syndrome ดังที่ได้กล่าวไปข้างต้น ที่จะเห็น hyperechoic fetal kidney จากคลื่นเสียงความถี่สูงและมีระดับแอลฟาฟีโตโปรตีนสูงในซีรัมของมารดา จะพบว่าระดับแอลฟาฟีโตโปรตีนสูงในน้ำคร่ำเพิ่มขึ้นมากกว่า 10 เท่า
ควรเก็บน้ำคร่ำไว้ 10mL ไว้ในกรณีที่สงสัย lysosomal storage disease และส่งตรวจเพิ่มเติมเมื่อผลตรวจค้นหาสาเหตุอื่นๆของทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูนปกติ
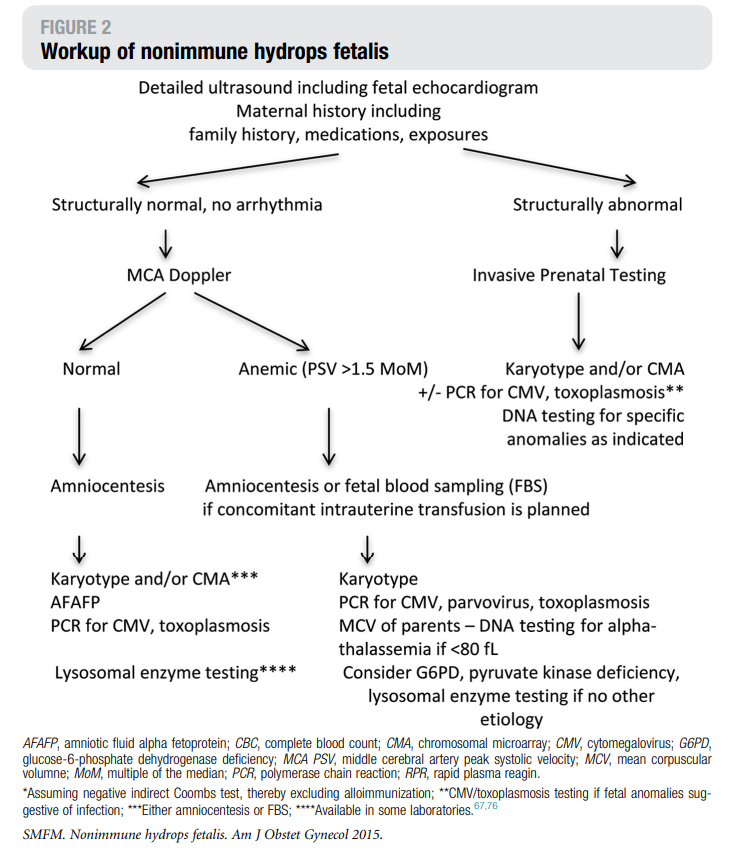 (3)
(3)
แนวทางการรักษา(3)
หลังจากค้นหาสาเหตุทารกบวมน้ำที่ไม่เกี่ยวกับปฏิกิริยาอิมมูนได้แล้ว แนวทางการรักษาและการดูแลขึ้นอยู่กับสาเหตุของภาวะทารกบวมน้ำว่าสามารถรักษาได้ในระหว่างการตั้งครรภ์หรือไม่ และอายุครรภ์ที่พบภาวะทารกบวมน้ำ โดยจะสามารถแบ่งแนวทางการรักษาได้ 3 กลุ่ม คือ 1. กลุ่มที่สามารถรักษาทารกในครรภ์ได้ (fetal therapy) 2. กลุ่มที่พยากรณ์โรคไม่ดี ควรแนะนำให้ยุติการตั้งครรภ์ 3. กลุ่มที่ไม่สามารถบอกพยากรณ์โรคได้และไม่สามารถระบุสาเหตุได้
โดยแนวทางการรักษาจะต้องอธิบายผลที่อาจเกิดขึ้นทั้งหมดแก่หญิงตั้งครรภ์เพื่อพิจารณาร่วมกัน ในกรณีที่พบภาวะทารกบวมน้ำตั้งแต่ก่อนอายุครรภ์ที่ทารกสามารถมีชีวิตรอดควรให้แนวทางยุติการตั้งครรภ์ และกรณีที่หญิงตั้งครรภ์ต้องการตั้งครรภ์ต่อ (expectant management) จะต้องอธิบายถึงผลเสียทั้งหมดที่อาจเกิดขึ้นให้หญิงตั้งครรภ์ทราบ เช่น โอกาสเกิด mirror syndrome ที่อาจรุนแรงถึงขั้นอวัยวะต่างๆในร่างกายล้มเหลวได้ เป็นต้น
กลุ่มที่สามารถรักษาทารกในครรภ์ได้ (fetal therapy)
หัวใจเต้นผิดจังหวะ(Cardiac arrhythmia)
tachyarrhythmia สามารถรักษาด้วยการให้ antiarrhythmic drug แก่หญิงตั้งครรภ์ให้ยาผ่านรกไปสู่ทารกในครรภ์เพื่อหวังผลให้หัวใจทารกกลับมาเต้นเป็นจังหวะปกติหรือช้าลง โดยยาที่ใช้ ได้แก่ digoxin, flecainide, sotalol แต่จะต้องมีการตรวจคลื่นไฟฟ้าหัวใจ (electrocardiography)หญิงตั้งครรภ์ก่อน และหญิงตั้งครรภ์จะต้องไม่มีข้อห้ามในการให้ยา(5)
การให้เลือดแก่ทารกในครรภ์ (Intrauterine transfusion)
กรณีทารกบวมน้ำจากภาวะซีดในครรภ์อันเนื่องมาจากสาเหตุ การติดเชื้อพาร์โวไวรัส (parvovirus B19) หรือ ภาวะเลือดทารกเข้าสู่ระบบไหลเวียนเลือดของมารดา (feto-maternal hemorrhage) ที่คัดกรองจากการวัด MCA-PSV และวินิจฉัยด้วยการเจาะเลือดทารกแล้วพบว่ามีความเข้มข้นของเลือดน้อยกว่า 30 % สามารถพิจารณาทำการเติมเลือดให้กับทารกในครรภ์ โดยแนะนำให้ทำก่อนอายุครรภ์ 34-35 สัปดาห์ จากรายงานพบว่าในทารกที่ซีดและบวมน้ำจากการติดเชื้อ parvovirus B19 พบว่า 94 % ภาวะบวมน้ำดีขึ้นภายใน 6 ถึง 12 เดือนหลังจากการเติมเลือด(10)
CPAM and pulmonary sequestration and pleural effusion (5)
กรณี CPAM ทั้งที่เป็น microcystic form และ macrocystic form ที่ทารกมีภาวะบวมน้ำสามารถรักษาได้ด้วยการให้ corticosteroid ในขนาด Dexamethasone 6.25 mg ทุก 12 ชั่วโมง ทั้งหมด 4 dose หรือ betamethasone 12.5 mg ทุก 24 ชั่วโมง ทั้งหมด 2 dose หลังจากการให้ single course ของ corticosteroid พบว่าภาวะทารกบวมน้ำดีขึ้น 80%
กรณีที่เป็น CPAM ที่มีพยาธิสภาพขนาดใหญ่ (macrocystic)และภาวะทารกบวมน้ำไม่ดีขึ้นหลังจากได้รับการรักษาด้วย corticosteroid แล้ว สามารถพิจาณาทำ drainage หรือ shunt replacement เช่นเดียวกับภาวะ pulmonary sequestration ที่มี pleural effusion ร่วมด้วย และ isolated pleural effusion เพื่อนำน้ำในช่องปอดมาตรวจวินิจฉัยและรักษาไปในตัว
Twin-Twin Transfusion syndrome (5)
เนื่องจาก TTTS เกิดจากการเชื่อมต่อของเส้นเลือดของแฝดทั้งสองทำให้เกิดการไหลเวียนเลือดไม่สมดุล การรักษาจึงทำได้โดยการทำลายเส้นเลือดที่เชื่อมกันระหว่างแฝดทั้งสองโดย fetoscope laser ablation มักจะทำในช่วงอายุครรภ์ 16-26 สัปดาห์ ในครรภ์แฝด monochorionic-diamniotic ที่เป็น TTTS stage II-IV หากไม่ทำการรักษาทารกมีโอกาสเสียชีวิตในครรภ์ 70-100 % และ โอกาสเสียชีวิตในครรภ์ลดลงเหลือ 30-50 % หลังจากทำการรักษา
Twin reversed arterial perfusion sequence (5)
รักษาโดยการใช้ radio frequency ablation ทำลาย acadiac twin แนะนำให้ทำในช่วงอายุครรภ์ 20 สัปดาห์ พบว่าอัตราการอยู่รอดของแฝดที่ปกติอยู่ที่ประมาณ 85% หลังจากการรักษา และหากไม่ได้รับการรักษาอัตราการเสียชีวิตของแฝดที่ปกติอยู่ที่ 50%
การตรวจสุขภาพทารกในครรภ์ (3)
การตรวจสุขภาพทารกในครรภ์ในทารกที่บวมน้ำไม่เพิ่ม perinatal outcome แต่อาจมีประโยชน์ในรายที่ทารกบวมน้ำเกิดจากสาเหตุที่สามารถรักษาทารกในครรภ์ได้ ดังนั้น อาจพิจารณทำการตรวจสุขภาพทารกในครรภ์ในรายต่อไปนี้ 1.สาเหตุของทารกบวมน้ำสามารถรักษาได้ 2.อายุครรภ์ที่วินิจฉัยอยู่ในช่วงที่ทารกสามารถเลี้ยงรอด 3.การตรวจสุขภาพทารกอาจช่วยในการพิจารณาอายุครรภ์ที่ควรจะยุติการตั้งครรภ์
การให้ Antepartum corticosteroid (3)
พิจารณาให้ antepartum corticosteroid ในหญิงตั้งครรภ์ที่มีภาวะทารกบวมน้ำที่อายุครรภ์ 24-34 สัปดาห์ ที่สาเหตุของภาวะทารกบวมน้ำไม่ได้ถึงแก่ชีวิต (nonlethal) และมีแผนที่จะทำการรักษาทารกในครรภ์(fetal intervention) และ การรักษานั้นเพิ่มความเสี่ยงของการคลอดก่อนกำหนดหรือมีโอกาสทำให้ทารกในครรภ์แย่ลงได้
อายุครรภ์ที่เหมาะสมในการให้คลอด (3)
ไม่มีการศึกษาที่ระบุอายุครรภ์ที่ควรให้คลอดแน่ชัดในทารกที่มีภาวะบวมน้ำ และไม่มีหลักฐานว่าการชักนำคลอดทากบวมน้ำที่อายุครรภ์ก่อนกำหนดจะเป็นประโยชน์ แต่หากการดำเนินโรคของภาวะบวมน้ำแย่ลงอาจพิจารณาให้คลอดที่อายุครรภ์ 34 สัปดาห์ได้
หากการดำเนินของโรคไม่แย่ลงสามารถให้คลอดที่อายุครรภ์ครบกำหนดที่อายุครรภ์ 38-39 สัปดาห์ แต่ในกรณีที่หญิงตั้งครรภ์เกิดภาวะ mirror syndrome ควรยุติการตั้งครรภ์ทุกกรณีโดยไม่คำนึงถึงอายุครรภ์
การเลือกช่องทางคลอด (3, 17)
ในรายที่พยากรณ์โรคไม่ดีและไม่มีแนวทางในการรักษาทารกในครรภ์ควรให้คลอดทางช่องคลอด โดยจะต้องเฝ้าระวังการคลอดติดขัด หญิงตั้งครรภ์มีความเสี่ยงในการตกเลือดหลังคลอด จากการบาดเจ็บของช่องทางคลอด มดลูกหดรัดตัวไม่ดี ภาวะรกค้างได้ อาจพิจารณาผ่าตัดคลอดในกรณีที่ทารกภาวะแย่ลงในระหว่างการคลอด และมีแผนที่จะรักษาทารกหลังคลอด การคลอดติดขัดสามารถเกิดได้ทั้งในการคลอดทางช่องคลอดและการผ่าคลอด อาจพิจารณาทำการเจาะระบายน้ำในช่องท้องของทารกเพื่อลดการบาดเจ็บระหว่างคลอด และเพิ่มประสิทธิภาพในการช่วยกู้ชีพทารกแรกคลอดได้ อย่างไรก็ตามควรได้รับการปรึกษาและดูแลร่วมกันระหว่างทีมสูติแพทย์และกุมารแพทย์
คำแนะนำ(3)
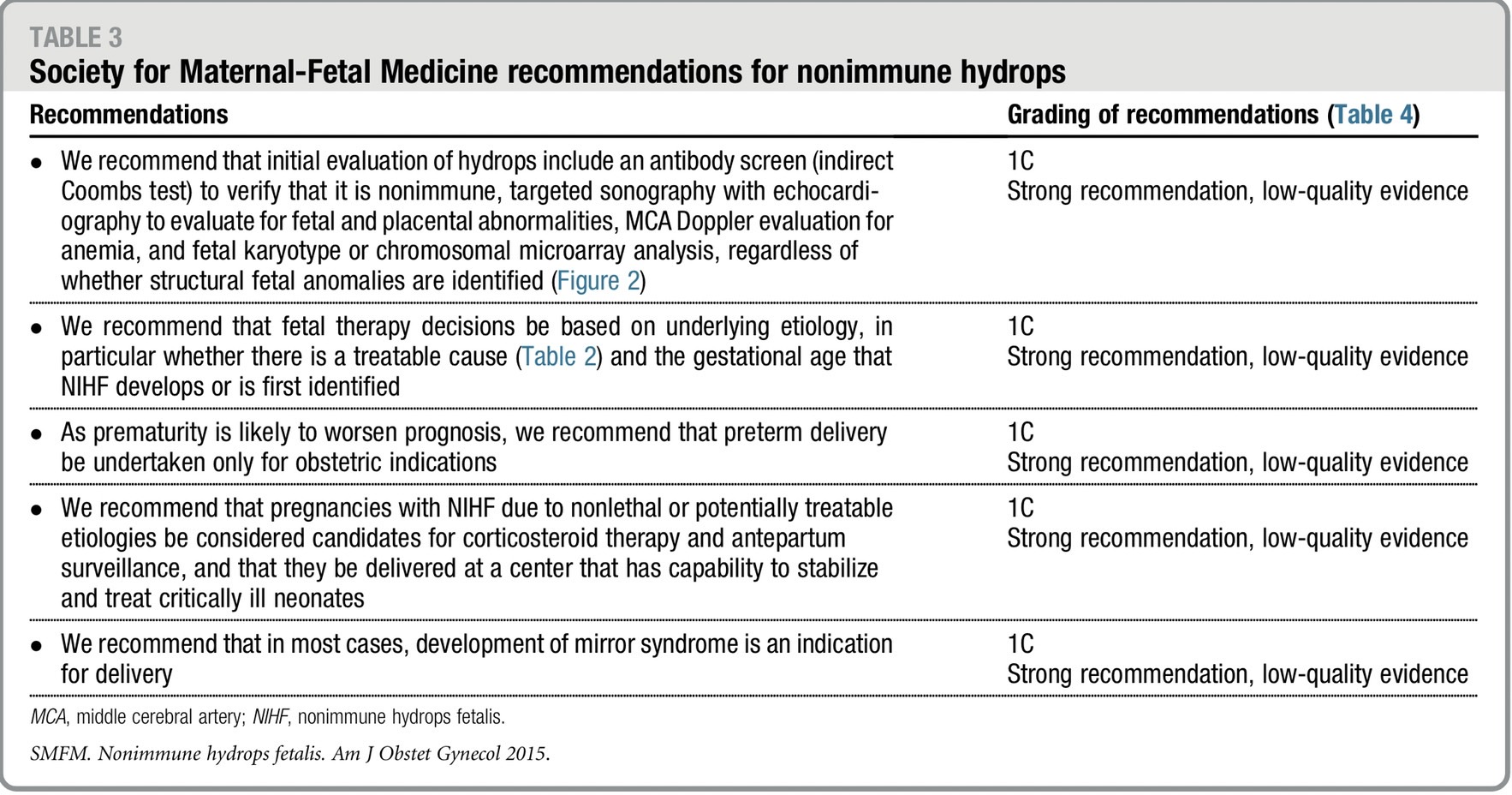
เอกสารอ้างอิง
1. Cunningham FG, Leveno KJ, Dashe JS, Hoffman BL, Spong CY, Casey BM. Williams Obstetrics, 26e. Fetal disorder. New York, NY: McGraw Hill; 2022. p. 360.
2. Santolaya J, Alley D, Jaffe R, Warsof SL. Antenatal classification of hydrops fetalis. Obstetrics and gynecology. 1992;79(2):256-9.
3. Norton ME, Chauhan SP, Dashe JS, Medicine SfM-F. Society for maternal-fetal medicine (SMFM) clinical guideline# 7: nonimmune hydrops fetalis. American journal of obstetrics and gynecology. 2015;212(2):127-39.
4. Resnik R, Lockwood CJ, Moore TR, Greene MF, Copel JA, Silver RM. Creasy and Resnik’s maternal-fetal medicine : principles and practice. Nonimmune Hydrops. Eighth edition. ed. Philadephia, PA: Elsevier; 2019. p. 645.
5. Cunningham FG, Leveno KJ, Dashe JS, Hoffman BL, Spong CY, Casey BM. Williams Obstetrics, 26e. Fetal therapy. New York, NY: McGraw Hill; 2022.
6. Heinonen S, Ryynänen M, Kirkinen P. Etiology and outcome of second trimester non-immunologic fetal hydrops. Acta obstetricia et gynecologica Scandinavica. 2000;79(1):15-8.
7. Malin G, Kilby MD, Velangi M. Transient abnormal myelopoiesis associated with Down syndrome presenting as severe hydrops fetalis: a case report. Fetal diagnosis and therapy. 2010;27(3):171-3.
8. Suwanrath-Kengpol C, Kor-anantakul O, Suntharasaj T, Leetanaporn R. Etiology and outcome of non-immune hydrops fetalis in southern Thailand. Gynecologic and obstetric investigation. 2005;59(3):134-7.
9. Rubod C, Houfflin V, Belot F, Ardiet E, Dufour P, Subtil D, et al. Successful in utero treatment of chronic and massive fetomaternal hemorrhage with fetal hydrops. Fetal diagnosis and therapy. 2006;21(5):410-3.
10. Cunningham FG, Leveno KJ, Dashe JS, Hoffman BL, Spong CY, Casey BM. Williams Obstetrics, 26e. Infectious Diseases. New York, NY: McGraw Hill; 2022. p. 1191.
11. de Jong EP, de Haan TR, Kroes AC, Beersma MF, Oepkes D, Walther FJ. Parvovirus B19 infection in pregnancy. Journal of clinical virology. 2006;36(1):1-7.
12. Cunningham FG, Leveno KJ, Dashe JS, Hoffman BL, Spong CY, Casey BM. Williams Obstetrics, 26e. Normal and Abnormal Fetal Anatomy. New York, NY: McGraw Hill; 2022. p. 287-8.
13. Cunningham FG, Leveno KJ, Dashe JS, Hoffman BL, Spong CY, Casey BM. Williams Obstetrics, 26e. Multifetal Pregnancy. New York, NY: McGraw Hill; 2022. p. 838.
14. Overstreet K, Benirschke K, Scioscia A, Masliah E. Congenital nephrosis of the Finnish type: overview of placental pathology and literature review. Pediatric and Developmental Pathology. 2002;5(2):179-83.
15. Randenberg A. Nonimmune hydrops fetalis part II: does etiology influence mortality? Neonatal Network. 2010;29(6):367-80.
16. Kooper AJ, Janssens PM, de Groot AN, Liebrand-van Sambeek ML, van den Berg CJ, Tan-Sindhunata GB, et al. Lysosomal storage diseases in non-immune hydrops fetalis pregnancies. Clinica chimica acta. 2006;371(1-2):176-82.
17. Lockwood CJ, Julien S, Wilkins-Haug L, Levine D, Garcia-Prats J, Barss V. Nonimmune hydrops fetalis. UpToDate Waltham, MA: UpToDate Inc(In English) URL: https://www uptodate com. 2014.

