การตรวจด้วยคอลโปสโคป (Basic Colposcope)
การตรวจด้วยคอลโปสโคป (Basic Colposcope)
พญ.ชินาภา ณัฐวงค์ศิริ
อาจารย์ที่ปรึกษา อ.น.พ. เศรษฐวัฒก์ เศรษฐเสถียร
บทนำ (Introduction)
การตรวจด้วยคอลโปสโคป (Colposcopy) หมายถึง การตรวจเยื่อบุผิวภายในบริเวณปากมดลูก ช่องคลอด ปากช่องคลอด และทวารหนักด้วยการส่องกล้องขยาย เพื่อการค้นหารอยโรคก่อนมะเร็งและมะเร็ง เพื่อที่จะได้รับการรักษาอย่างรวดเร็วที่สุด (1)
จุดประสงค์ (5)
- เพื่อตรวจแยกว่าไม่มีมะเร็งปากมดลูกในระยะลุกลาม
- เพื่อตรวจหารอยโรคขั้นสูง ได้แก่ CIN2,3 และ adenocarcinoma in situ (AIS) เพื่อรักษาไม่ให้รอยโรคคืบหน้าเป็นมะเร็งระยะลุกลาม
- เพื่อเป็นแนวทางการรักษาที่เหมาะสม เช่น ผล Pap smear เป็น atypical squamous cells of undetermined significance (ASC-US) หรือ low-grade squamous intraepithelial lesion (LSIL) และการตรวจด้วยคอลโปสโคปไม่พบรอยโรคสามารถตรวจติดตามดูการดำเนินโรคได้ทุก 6 เดือน หรือถ้าผล Pap smear เป็น high-grade squamous intraepithelial lesion (HSIL) และการตรวจด้วยคอลโปสโคปไม่เห็น transformation zone หรือเห็นได้ไม่หมด หรือเห็นรอยโรคได้ไม่หมด ควรทำการตัดปากมดลูกเพื่อการวินิจฉัยต่อไป (diagnosis excision)
ข้อบ่งชี้ (Indication)
- ผลการคัดกรองมะเร็งปากมดลูกผิดปกติ (cytology and/or HPV testing)
- อาการหรืออาการแสดงที่สงสัยลักษณะของมะเร็ง เช่น พบลักษณะผิดปกติ เช่น มีแผลหรือมีก้อนเนื้อจากการตรวจภายใน, ภาวะเลือดออกหรือสารคัดหลั่งที่ผิดปกติทางช่องคลอดโดยไม่สามารถหาสาเหตุได้ (2) อย่างไรก็ตามการตรวจด้วยคอลโปสโคปเพียงอย่างเดียว ไม่ใช่การตรวจคัดกรองมะเร็งปากมดลูกที่มีประสิทธิภาพเพียงพอ (3)
- ผลการคัดกรองมะเร็งปากมดลูกวิธีอื่นนอกจาก cytology หรือ HPV testing ให้ผลบวก เช่น การตรวจด้วยน้ำส้มสายชู (visual inspection with acetic acid (VIA)
- ตรวจติดตามผลหลังการรักษารอยโรคด้วยการรักษาเฉพาะที่ เช่น การจี้ด้วยความเย็นและการตัดด้วยห่วงไฟฟ้า (4)
- กรณีอื่น ๆ ที่อาจพิจารณาตรวจด้วยคอลโปสโคป (5)
- การติดเชื้อ high-risk HPV แบบเนิ่นนาน (persistent HPV infection) เช่น ผลการตรวจ HPV DNA testing ให้ผลบวก 2 ครั้ง จากการตรวจห่างกัน 12 เดือน
- รอยโรค CIN 1 ที่คงอยู่นานกว่า12 เดือน
- คู่นอนเป็นเนื้องอกหรือหูดหงอนไก่ที่อวัยวะเพศส่วนล่าง
- ผล Pap smear พบว่ามีการอักเสบหลายครั้งโดยไม่ทราบสาเหตุ
ข้อบ่งห้าม (Contraindication)
โดยทั่วไปไม่มีข้อบ่งห้ามที่ชัดเจน แต่อาจจะพิจารณาเลื่อนการตรวจออกไปก่อนในกรณีดังต่อไปนี้
- มีการติดเชื้อบริเวณปากมดลูกและช่องคลอด โดยจะทำให้การประเมินเยื่อบุผิวทำได้ยากและได้รับความร่วมมือจากการตรวจลดลงจากการเจ็บบริเวณที่อักเสบได้ (6)
- มีเลือดออกผิดปกติทางช่องคลอดหรือประจำเดือนออกปริมาณมาก
การตั้งครรภ์ไม่ได้เป็นข้อบ่งห้าม หากมีข้อบ่งชี้สามารถตรวจได้โดยช่วงอายุครรภ์ที่เหมาะสม คือ 12-15 สัปดาห์ หลีกเลี่ยงการตัดชิ้นเนื้อออกตรวจถ้าไม่สงสัยมะเร็งระยะลุกลามและไม่ควรทำการขุดภายในปากมดลูก (endocervical curettage) เนื่องจากอาจมีผลทำให้ถุงน้ำคร่ำแตกหรือทำให้เลือดออกมากได้
กรณีที่ได้รับยาต้านการแข็งตัวของเลือดหรือมีโรคเกี่ยวกับการแข็งตัวของเลือดผิดปกติ ไม่ได้เป็นข้อบ่งห้าม เนื่องจากเลือดมักออกเพียงเล็กน้อย แต่หากเป็นไปได้ควรหยุดก่อนทำหัตถการ
เยื่อบุปากมดลูกปกติ
เมื่อตรวจด้วยคอลโปสโคปจะพบเยื่อบุปากมดลูกปกติดังนี้
- Squamous epithelium
- Columnar epithelium
- Metaplastic squamous epithelium
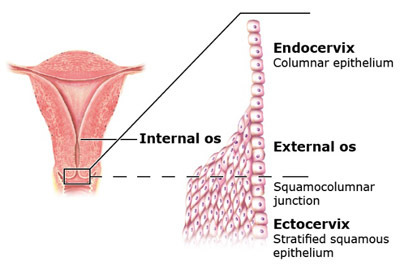
รอยต่อระหว่าง Squamous epithelium เดิม กับ Columnar epithelium เรียกว่า original squamo-columnar junction (original SCJ) เมื่อมีการแปรรูปของเซลล์บริเวณ Columnar epithelium เป็น Squamous epithelium รอยต่อระหว่าง Squamous epithelium ใหม่ กับ Columnar epithelium ด้านบน เรียกว่า new squamo-columnar junction (new SCJ) บริเวณที่อยู่ระหว่างรอยต่อเดิมกับรอยต่อใหม่นี้ คือ เขตเซลล์แปรรูป (transformation zone) การตรวจปากมดลูกด้วยคอลโปสโคปนั้นต้องตรวจดูบริเวณนี้อย่างละเอียด เนื่องจากรอยโรคมักเกิดในบริเวณนี้
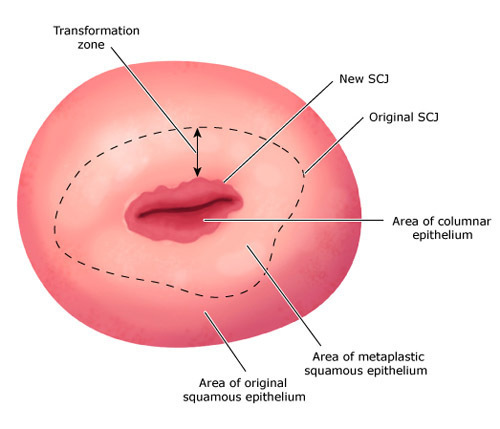
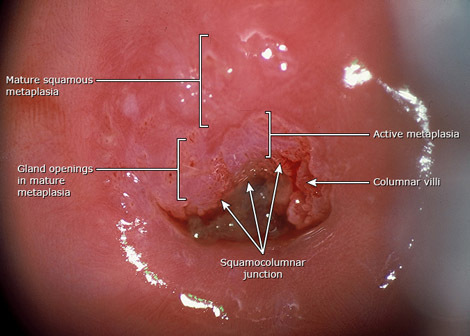
กระบวนการแปรรูป (metaplasia) ของ Columnar epithelium เป็น Squamous epithelium นั้นเกิดไม่พร้อมกันทั้งปากมดลูก มีทั้งที่แปรรูปสมบูรณ์แล้วและยังอยู่ในระยะต่างๆ ของกระบวนการ ทำให้เห็นหย่อมของ Columnar epithelium หลงเหลืออยู่และมี Squamous epithelium ที่แปรรูปแล้วล้อมรอบ ถ้า Columnar epithelium นี้มีรูเปิดออกที่ผิวจะหลั่งมูกออกมาทางรูเปิดเล็กๆนี้เรียกว่า gland openings ถ้ารูเปิดนี้ถูก Squamous epithelium ปกคลุม ทำให้มูกไม่มีทางออก จะกลายเป็นถุงน้ำเล็กๆ เรียกว่า Nabothian cyst ทั้ง gland openings และ Nabothian cyst เป็นร่องรอยที่บ่งบอกว่าบริเวณนี้เดิมเป็น Columnar epithelium แต่มีการแปรรูป (metaplasia) เกิดขึ้น
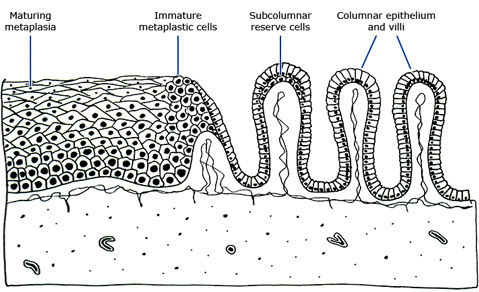
หลังจากชโลมด้วยสารละลาย acetic acid บริเวณ metaplasia squamous epithelium นี้จะขาวกว่า squamous epithelium เดิม มีผิวเรียบ รูปร่างคล้ายลิ้นขนาดต่างๆ กัน โดยสามารถวินิจฉัยแยกจากเยื่อบุสีขาวของรอยโรคภายใน squamous epithelium ได้โดยจะพบว่าบริเวณ metaplasia squamous epithelium จะขาวมากกว่าบริเวณรอยต่อใหม่ และจะค่อยๆจางลง มักพบมีหลายแห่ง รูปร่างคล้ายลิ้น ภายในมี gland openings เป็นรูกลมๆ อาจเห็น Nabothian cyst สีเหลืองใส ขนาดต่างๆกัน หลอดเลือดที่มาเลี้ยงอาจมีจำนวนมากผิดปกติ แต่จะเห็นว่าหลอดเลือดเหล่านี้แตกแขนงปกติและมีขนาดไม่ใหญ่
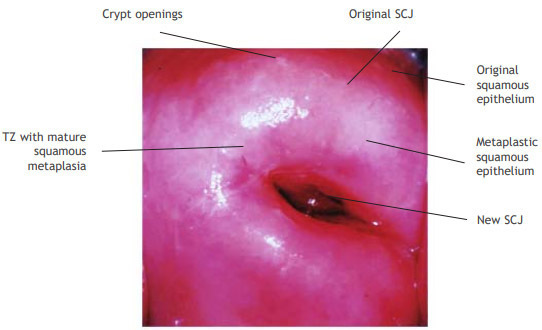
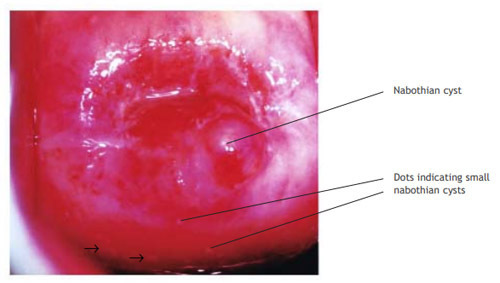
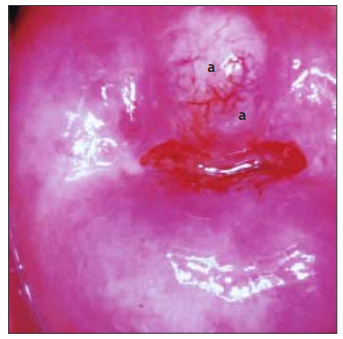
เยื่อบุปากมดลูกผิดปกติ
การแปรรูปของ columnar epithelium เป็นเหตุการณ์ที่เกิดขึ้นตามปกติธรรมชาติ เมื่อเข้าสู่วัยรุ่น มีการสร้างเอสโตรเจนจากรังไข่ทำให้ช่องคลอดมีภาวะเป็นกรด columnar epithelium จึงต้องปรับตัวเป็น squamous epithelium เพื่อให้ทนต่อภาวะกรดในช่องคลอดได้ ในช่วงที่มีการแปรรูปของเซลล์นี้ถ้ามีสารก่อมะเร็ง เช่น การติดเชื้อHPV จะเกิดการแปรรูปเป็น squamous epithelium ที่ผิดปกติในเยื่อบุ จึงเรียกบริเวณนี้ว่า “เขตเซลล์แปรรูปผิดปกติ” หรือ “atypical transformation zone” ซึ่งถ้าไม่ได้รับการรักษาอาจจะดำเนินต่อไปเป็นมะเร็งระยะลุกลามได้ มะเร็งปากมดลูกมักเกิดขึ้นในเขตเซลล์แปรรูปนี้ เนื่องจากประกอบด้วย embryonic cells ที่เชื่อว่าสามารถติดเชื้อ HPV และมี oncogenic transformation ได้มากกว่าบริเวณอื่น (7)
เยื่อบุที่ผิดปกติจะมีความหนาแน่นของนิวเคลียสสูงขึ้น ขนาดของนิวเคลียสใหญ่ขึ้น เมื่อสัมผัสกับสารละลาย acetic acid จะทำให้เกิดการเปลี่ยนแปลงทางออสโมลาริตี ทำให้ความดันออสโมซิสของช่องว่างนอกเซลล์สูงขึ้น น้ำซึมออกนอกเซลล์ เยื่อหุ้มเซลล์ฝ่อยุบลงล้อมรอบนิวเคลียส ทำให้ลำแสงจากคอลโปสโคปผ่านไม่ได้จึงเห็นเป็นสีขาวทึบ ลักษณะเยื่อบุที่มีสีขาวทึบหลังจากชโลมด้วยสารละลาย acetic acid นี้ทางคอลโปสโคป เรียกว่า “เยื่อบุสีขาวจากกรดอะเซติก” หรือ “acetowhite epithelium” กระบวนการนี้ใช้เวลา 1 – 2 นาที เมื่อสารละลาย acetic acid ออกจากเนื้อเยื่อและหมดฤทธิ์ น้ำจะกลับเข้าสู่เซลล์ เยื่อหุ้มเซลล์ขยายพองออก ความขาวจะหายไป ปรากฏการณ์นี้จะเกิดขึ้นชั่วคราวเท่านั้นถ้าต้องการตรวจอีกสามารถชโลมด้วยสารละลาย acetic acid ซ้ำได้ ความรุนแรงของรอยโรคขึ้นกับ (8)
- ระดับความขาวของเยื่อบุ (color tone) ยิ่งขาวทึบมากความรุนแรงยิ่งมากขึ้น
- ระยะเวลาที่เยื่อบุเปลี่ยนเป็นสีขาว (onset & duration) ยิ่งเกิดขึ้นเร็วและคงอยู่นานระดับความรุนแรงของรอยโรคจะยิ่งมากขึ้น
- ขอบหรือรอยต่อกับเนื้อเยื่อปกติที่ล้อมรอบอยู่(margin) ขอบยิ่งคมชัดความรุนแรงยิ่งมากขึ้น ถ้าขอบม้วนขึ้น(rolling) หรือหลุดลอก(peeling) ความรุนแรงของโรคก็มากขึ้นเช่นกัน ดังนั้นในขณะที่ชโลมปากมดลูกด้วยสารละลาย acetic acid ต้องรอประมาณ 1 – 2 นาที เพื่อสังเกตการเปลี่ยนแปลงดังกล่าวก่อนที่จะประเมินความรุนแรงของรอยโรค
เยื่อบุสีขาวจากสารละลาย acetic acid เป็นความผิดปกติที่พบบ่อยที่สุดในเขตเซลล์แปรรูปผิดปกติ ผิวจะเรียบไม่เห็นเส้นเลือดและไม่สามารถมองเห็นได้ด้วยตาเปล่า แต่จะมองเห็นได้หลังจากชโลมด้วยสารละลาย acetic acid ถ้าความผิดปกติรุนแรงขึ้นเซลล์เหล่านี้จะสร้างสารกระตุ้นการสร้างเส้นเลือด (tumor angiogenesis factors)เพื่อให้มีเส้นเลือดมาหล่อเลี้ยงเยื่อบุจึงเรียกสิ่งตรวจพบตามลักษณะของเส้นเลือดเหล่านี้
- Punctation : จากการที่เส้นเลือดฝอยแทรกผ่านเยื่อบุขึ้นมาบนผิว เมื่อตรวจด้วยคอลโปสโคปจะเห็นเป็นจุดสีแดงของปลายเส้นเลือด
- Mosaic : จากการที่เส้นเลือดฝอยแตกแขนงคล้ายตะกร้าหรือรังผึ้งเข้าไปอยู่ระหว่างกลุ่มเซลล์ในเยื่อบุ เมื่อตรวจด้วยคอลโปสโคปจะเห็นเส้นเลือดเรียงกันคล้ายแผ่นกระเบื้อง
- atypical vessels : เส้นเลือดแตกแขนงผิดปกติในแนวระนาบบนเยื่อบุหรือใกล้ผิวเยื่อบุและมีขนาดโตขึ้นร่วมกับการแตกแขนงแปลก ๆ (16)
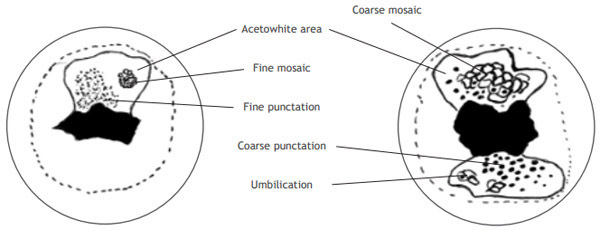
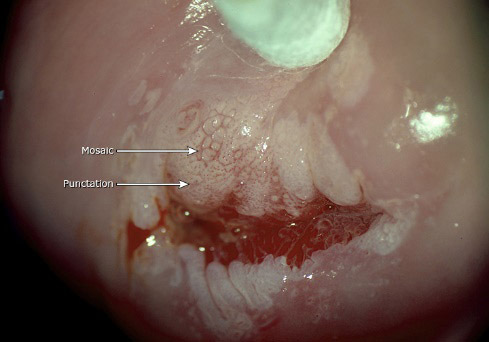
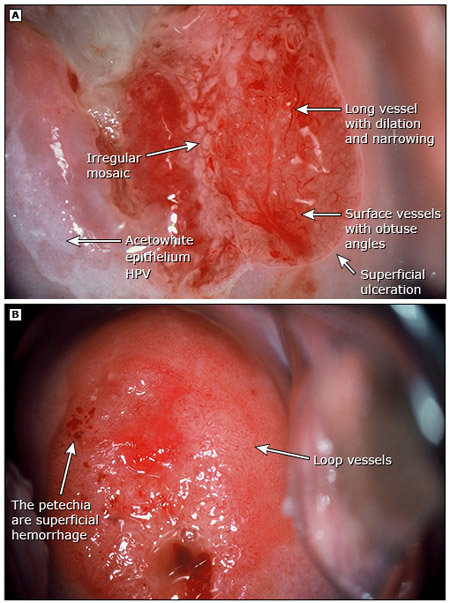
รอยโรคสีขาวที่เห็นด้วยตาเปล่าบนผิวเยื่อบุปากมดลูกก่อนชโลมด้วยกรดอะเซติก เรียกว่า”leukoplakia” หรือ “Hyperkeratosis” มักจะมีขอบเขตชัดเจน เนื่องจากเยื่อบุมีสารเคอราตินเคลือบอยู่จึงทึบแสงและเห็นเป็นสีขาว อาจจะบดบังเส้นเลือดที่อยู่ข้างใต้ ทำให้วินิจฉัยเยื่อบุข้างใต้ไม่ได้ ความสำคัญของ leukoplakia ขึ้นกับตำแหน่งที่เกิด ถ้าอยู่ภายใน squamous epithelium ปกติมักไม่ค่อยมีความสำคัญ อาจเกิดจากการบาดเจ็บ การระคายเคือง หรือการอักเสบเรื้อรัง และการติดเชื้อHPV ถ้าอยู่ภายในเขตเซลล์แปรรูป และมี acetowhite epithelium, punctation หรือ mosaic ล้อมรอบจะมีความสำคัญมาก ซึ่งความสำคัญไม่ได้อยู่ตรงบริเวณที่เป็น leukoplakia แต่อยู่ตรงเยื่อบุที่อยู่ข้างใต้และเยื่อบุที่อยู่ข้างเคียง
เขตเซลล์แปรรูปจะถือว่าผิดปกติเมื่อตรวจพบสิ่งต่อไปนี้ คือ acetowhite epithelium, punctation, mosaic, atypical vessels และ leukoplakia สิ่งตรวจพบเหล่านี้อาจเกิดขึ้นอย่างเดียวหรือร่วมกันหลายอย่างก็ได้ อาจจะมีแห่งเดียวหรือหลายแห่งก็ได้ แต่มักจะเห็นเด่นชัดแยกจากเนื้อเยื่อปกติรอบ ๆ ได้ ภาวะอื่น ๆ ที่ทำให้เซลล์แบ่งตัวมากขึ้นหรือมีการสร้างเส้นเลือดมากขึ้นจนทำให้มองเห็นความผิดปกติเหล่านี้ในเขตเซลล์แปรรูปได้แก่ การติดเชื้อ การอักเสบ การสร้างเนื้อเยื่อใหม่ การซ่อมแซมเยื่อบุ และการตั้งครรภ์ เป็นต้น
โดยสรุปแล้วในการตรวจด้วยคอลโปสโคปให้สังเกตการเปลี่ยนแปลง 2 ประการของปากมดลูก ได้แก่
- การเปลี่ยนแปลงของผิวเยื่อบุ (epithelial changes) เช่น ผิวเรียบหรือขรุขระ ซึ่งบ่งบอกถึงความรุนแรงของรอยโรค ความทึบหรือความขาวหลังจากชโลมด้วยกรดอะเซติก ซึ่งบ่งบอกถึงความหนาแน่นของเซลล์หรือความรุนแรงของรอยโรค และความคมชัดของขอบหรือรอยต่อระหว่างรอยโรคกับเยื่อบุใกล้เคียง
- การเปลี่ยนแปลงของเส้นเลือด (vascular changes) เช่น ลักษณะและขนาดของเส้นเลือดชนิดต่างๆ ระยะห่างระหว่างเส้นเลือด ความเข้มของเส้นเลือดที่ผิดปกติ และตำแหน่งของเส้นเลือด อยู่ภายในรอยโรคหรือทอดอยู่บนผิวของรอยโรค (5)
อุปกรณ์ที่จำเป็นสำหรับการตรวจ ได้แก่
- กล้องคอลโปสโคป
- เครื่องถ่างตรวจช่องคลอด (vaginal speculum) ขนาดต่าง ๆ กันตามความเหมาะสมกับช่องคลอดของผู้ป่วย
- เครื่องถ่างตรวจผนังช่องคลอดด้านข้าง (lateral vaginal wall retractor) ใช้ถ่างผนังช่องคลอดด้านข้างที่ยื่นมาบังการตรวจปากมดลูก
- ตะขอเกี่ยวปากมดลูก (hook) ใช้จับยกเนื้อเยื่อที่มีผิวเรียบเพื่อให้ตัดเนื้อออกตรวจได้ง่ายขึ้น และใช้ดึงผนังช่องคลอดเพื่อตรวจบริเวณรอยย่น
- อุปกรณ์สำหรับการตัดเนื้อออกตรวจ (punch biopsy forceps) ปลายที่ใช้ตัดต้องคมเพื่อไม่ให้ครูดได้แต่เยื่อบุผิว ด้ามต้องยาวประมาณ 20 – 25 ซม. เพื่อใช้ตัดในที่ลึกได้
- เครื่องมือขูดภายในคอมดลูก (endocervical curettes) สำหรับขูดเยื่อบุภายในคอมดลูกมาตรวจทางพยาธิวิทยา ปลายเครื่องมือต้องคมและเล็กพอที่จะสอดเข้าไปภายในคอมดลูกเล็ก ๆ ได้ อาจใช้แปรงขนอ่อน (endocervical brush) หมุนเก็บเซลล์ตัวอย่างภายในคอมดลูกเพื่อตรวจทางเซลล์วิทยา
- เครื่องมือจับยึดปากมดลูก เช่น tenaculum หรือ Allis clampsใช้จับยึดปากมดลูกไม่ให้เลื่อนหนีขณะตัดเนื้อออกตรวจหรือขณะขูดคอมดลูก โดยทั่วไปไม่จำเป็นต้องใช้และอาจทำให้เลือดออกตรงรอยเขี้ยวของเครื่องมือได้
- คีมจับเนื้อเยื่อ (tissue forceps) ยาวอย่างน้อย 20 ซม. ใช้จับสำลีชุบสารละลาย acetic acid เพื่อชโลมปากมดลูก และใช้จับผ้ากอซเพื่อกดห้ามเลือด
- ผ้ากอซพันสำลีพร้อมเชือกรัดหรือผ้ากอซยาวสำหรับประจุช่องคลอด (vaginal packing gauze) ใช้ห้ามเลือดที่ออกจากปากมดลูกหลังจากตัดเนื้อออกตรวจ
- ก้อนสำลี (cotton ball) หรือสำลีพันปลายไม้ (cotton swab) สำหรับชุบสารละลาย acetic acid ชโลมปากมดลูก เช็ดเลือดและกดจุดเลือดออกก่อนที่จะประจุด้วยผ้ากอซ
- สารละลายน้ำเกลือปกติ (normal saline solution) สำหรับเช็ดทำความสะอาดปากมดลูก
- สารละลาย acetic acid ความเข้มข้น 3 – 5 % อาจใส่ไว้ในขวดที่มีหัวฉีดเพื่อใช้ฉีดชโลมปากมดลูกเวลาตรวจปากมดลูกเพื่อดูการเปลี่ยนแปลงของผิวเยื่อบุ
- สารละลายไอโอดีน เช่น Lugol solution หรือ Schiller solution สำหรับการทดสอบชิลเลอร์ (Schiller test) เพื่อตรวจบริเวณที่ติดสีและไม่ติดสีไอโอดีน
- อุปกรณ์ห้ามเลือด เช่น สารละลายมอนเซล (Monsel solution) สำหรับจี้จุดเลือดออกเพื่อห้ามเลือด โดยการประจุปากมดลูกด้วยผ้ากอซยาวก็เพียงพอที่จะห้ามเลือดตรงจุดที่ตัดเนื้อออกตรวจได้
- อุปกรณ์สำหรับเก็บเนื้อเยื่อตัวอย่างจากการตัดเนื้อออกตรวจ ได้แก่ ขวดบรรจุน้ำยาฟอร์มาลิน ไม้จิ้มฟันสำหรับดันเนื้อเยื่อออกจากคีมตัดเนื้อออกตรวจ
- อุปกรณ์สำหรับการทำ Pap smear ได้แก่ Ayre spatula แผ่นกระจก ขวดบรรจุน้ำยาตรึงสภาพเซลล์
- แผ่นบันทึกผลการตรวจและใบคำแนะนำการปฏิบัติตัวภายหลังการตรวจ (5)
การให้คำแนะนำและการเตรียมก่อนการตรวจ
การเตรียมข้อมูลผู้ป่วย เช่น ประวัติการการตรวจ cytology และการทดสอบ HPV, สิ่งตรวจพบหรือผลทางพยาธิวิทยาจากการส่องกล้องครั้งก่อนหน้า, ประวัติการรักษาทางนรีเวช รวมไปถึงประวัติอื่นๆ เช่น ผลการตรวจHIV ประวัติการตั้งครรภ์ ประวัติประจำเดือน การใช้ฮอร์โมน การใช้ยาคุมกำเนิด โรคประจำตัว ประวัติการแพ้ยา ยาที่ใช้ประจำ สูบบุหรี่ เป็นต้น (9)
อธิบายให้ผู้ป่วยเข้าใจถึงความจำเป็นและวิธีการตรวจเพื่อให้ผู้ป่วยคลายความวิตกกังวล และลงนามในเอกสารยินยอมรับการตรวจและการรักษา การชโลมปากมดลูกด้วยสารละลาย acetic acid อาจทำให้มีอาการแสบร้อนเล็กน้อยในช่องคลอด การตัดชิ้นเนื้อ ( biopsy) อาจทำให้มีอาการปวดตึงเล็กน้อย การขูดคอมดลูกอาจทำให้มีอาการปวดคล้ายการปวดประจำเดือนช่วงสั้นๆ ระยะเวลาที่เหมาะสมที่สุดของการตรวจ คือ ช่วงกลางรอบเดือนประมาณวันที่ 8-12 ของรอบเดือน ซึ่งรูปากมดลูกจะเปิดเผยออก มูกจะใสไม่เหนียวข้นมาบังผิวเยื่อบุปากมดลูก แต่อย่างไรก็ตามในช่วงอื่นของรอบเดือนก็สามารถทำการตรวจได้ยกเว้นช่วงที่มีเลือดประจำเดือนไม่ควรตรวจเพราะจะมองเห็นไม่ชัดและอาจมีเลือดออกมาบดบังการตรวจได้ แนะนำให้งดการการสอดยา การสวนล้างช่องคลอด และการมีเพศสัมพันธ์ก่อนการตรวจ 1 วัน
ขั้นตอนการตรวจด้วยกล้องขยายทางช่องคลอด
- จัดท่าผู้ป่วย จัดให้อยู่ในท่าขบนิ่วหรือท่าขึ้นขาหยั่ง วางเท้าบนที่รองรับ งอเข่า และแยกต้นขาออก ปูผ้าคลุม เปิดไว้เฉพาะบริเวณอวัยวะสืบพันธุ์ภายนอก
- สอดเครื่องถ่างตรวจช่องคลอด เปิดให้เห็นปากมดลูกทั้งหมดรวมทั้งผนังช่องคลอดโดยรอบ ตรวจดูปากมดลูก ด้วยตาเปล่า ดูสิ่งคัดหลั่งของปากมดลูกและช่องคลอด รวมทั้งรอยโรคและก้อนเนื้องอกที่เห็นได้ชัดเจนที่ผนังช่องคลอดหรือปากมดลูก ถ้ามีตกขาวให้เก็บส่งตรวจทางจุลชีววิทยา
- ปรับมุมของเครื่องถ่างตรวจช่องคลอดให้ปากมดลูกทำมุมตั้งฉากกับลำแสงของคอลโปสโคป อีกมือหนึ่งจับตัวกล้องคอลโปสโคป ปรับให้ได้ระยะที่คมชัด ถ้าปากมดลูกชี้ลงไปทางด้านหลังให้ใส่ผ้ากอซข้างใต้เพื่อยกปากมดลูกขึ้นมา สังเกตรอยโรคบนปากมดลูก ถ้ามีมูกหรือสิ่งคัดหลั่งปกคลุมให้ใช้สำลีชุบน้ำเกลือเช็ดออกเบา ๆ ถ้ามีเลือดออกให้ใช้สำลีกดไว้ 1–2 นาที ถ้ามีมูกออกมากให้ดูดออกด้วยเครื่องดูดหรือกระบอกฉีดยา ชโลมปากมดลูกด้วยน้ำเกลือแล้วตรวจโดยใช้กำลังขยาย 5 – 10 เท่า ให้สังเกต สี (color)และลักษณะผิว (surface contour)ของเยื่อบุขอบ (margin) ระหว่างรอยโรคกับเนื้อเยื่อปกติ ลักษณะของเส้นเลือด(vasculature) ซึ่งจะเห็นได้ชัดในระยะนี้อาจใช้กระจกกรองแสงสีเขียว(green filter)ช่วยเพื่อให้มองเห็นเส้นเลือดชัดเจนขึ้น
- ชโลมปากมดลูกด้วยสารละลาย acetic acid ความเข้มข้น 3 – 5 % โดยใช้หัวฉีดพ่นสารละลายหรือใช้ก้อน สำลีชุบสารละลาย acetic acid ลงบนปากมดลูก รอประมาณ 1 นาที เพื่อดูการเปลี่ยนแปลงของผิวเยื่อบุ สามารถชโลมซ้ำได้ทุก 2 – 3 นาที ตรวจด้วยกำลังขยาย 5 – 15 เท่า ถ้าเห็นเส้นเลือดผิดปกติอาจตรวจซ้ำด้วยกระจกกรองแสงสีเขียว และใช้กำลังขยายสูงขึ้นเป็น 25–40 เท่า เพื่อที่จะดูลักษณะของเส้นเลือดให้ชัดเจนขึ้น ควรตรวจดูปากมดลูกอย่างเป็นระบบตามเข็มนาฬิกา การตรวจปากมดลูกหลังจากชโลมด้วยสารละลาย acetic acid เป็นขั้นตอนที่สำคัญที่สุด ซึ่งจะเห็นรายละเอียดทั้งหมด ให้สังเกตการเปลี่ยนแปลงของสีและการบวมของเยื่อบุ อาจใช้เวลานานกว่า 1 นาที จึงจะเห็นการเปลี่ยนแปลงอย่างชัดเจนที่สุด ถ้ารอยโรคหรือเขตเซลล์แปรรูปลามเข้าไปในคอมดลูกให้ใส่เครื่องถ่างตรวจภายในคอมดลูกช่วยตรวจบันทึกสิ่งตรวจพบทั้งหมดโดยการถ่ายภาพหรือวาดภาพบรรยายไว้ในใบรายงานผลการตรวจ นิยมบอกตำแหน่งบนปากมดลูกตามตำแหน่งของเข็มนาฬิกาตั้งแต่ 1 – 12 นาฬิกา โดยมีรูปากมดลูกเป็นจุดศูนย์กลาง (10)
- การทดสอบชิลเลอร์ (Schiller test) หรือ การใช้ Lugol solution อาจทำก่อนที่จะทำการตัดเนื้อออกตรวจ เป็นการทดสอบปฏิกิริยาระหว่างไอโอดีนกับไกลโคเจน เยื่อบุช่องคลอดที่เป็น squamous epithelium ปกติจะมีไกลโคเจนจะติดสีไอโอดีนเห็นเป็นสีน้ำตาลเข้มเรียกว่า “ผลลบชิลเลอร์” (Schiller negative) หรือ “ผลบวกไอโอดีน” (iodine positive) เยื่อบุที่ไม่มีไกลโคเจนจะไม่ติดสีไอโอดีนเรียกว่า “ผลบวกชิลเลอร์”(Schiller positive) หรือ “ผลลบไอโอดีน” (iodine negative โดยเยื่อบุที่ไม่มีไกลโคเจนได้แก่ เยื่อบุช่องคลอดที่เป็น columnar epithelium รวมทั้งเยื่อบุที่กำลังแปรรูปซึ่งยังเป็นเซลล์อ่อนอยู่ เยื่อบุที่ติดเชื้อHPV รอยโรคภายใน squamous epithelium และมะเร็งปากมดลูก
- การตัดเนื้อออกตรวจ (punch biopsy)โดยตัดบริเวณที่ผิดปกติมากที่สุดของรอยโรคแต่ละบริเวณเพื่อส่งตรวจทางพยาธิวิทยา และควรตัดให้ได้สโตรมาใต้เยื่อบุด้วยเพื่อประเมินการลุกลาม วิธีการตัดชิ้นเนื้อให้ใช้ปลายคีมตัดเนื้อดันปากมดลูกตรงตำแหน่งที่จะตัดขึ้นไปจนไม่เลื่อนขึ้นไปอีกจึงทำการตัดโดยตัดเนื้อเยื่อให้ตั้งฉากกับผิวเยื่อบุเพื่อไม่ให้เกิดการตัดเฉียง ถ้ามีรอยโรคทั้งด้านบนและด้านล่างของปากมดลูกให้ทำการตัดที่ด้านล่างก่อนด้านบนเพื่อไม่ให้เลือดออกมาบังบริเวณที่จะตัด โดยทั่วไปมักตัดชิ้นเนื้อหลายตำแหน่งเพื่อเพิ่มโอกาสการค้นพบรอยโรคผิดปกติและควรระบุตำแหน่งของเนื้อเยื่อที่ตัดออกมาด้วย (11)
- การสุ่มตรวจภายในปากมดลูก(endocervical sampling) อาจจะตรวจโดยการขูดด้วยเครื่องขูดภายในปากมดลูก (endocervical curettes) เพื่อตรวจทางพยาธิวิทยา หรือใช้แปรงหมุนเก็บเซลล์ภายในปากมดลูก (endocervical brush) เพื่อตรวจทางเซลล์วิทยา บางท่านนิยมทำการสุ่มตรวจคอมดลูกทุกรายเพื่อให้แน่ใจว่าไม่มีรอยโรคอยู่ด้านใน เพราะการตรวจด้วยคอลโปสโคปมีขีดจำกัดคือไม่สามารถมองเห็นภายในปากมดลูก(endocervical canal)ได้ มีการศึกษาพบว่าช่วยเพิ่มความไวของการตรวจในรายที่อายุมาก (12) นอกจากนี้อาจสุ่มเจอเซลล์จาก skip lesions (noncontiguous lesions) ซึ่งพบใน glandular neoplasia (13)
- การห้ามเลือดจากบริเวณที่ตัดเนื้อออกตรวจ โดยทั่วไปแล้วเลือดมักออกเพียงเล็กน้อย สามารถห้ามเลือดได้โดยการกดและประจุด้วยผ้ากอซยาว โผล่ปลายผ้ากอซออกมาด้านนอกเล็กน้อยเพื่อให้ผู้ป่วยดึงออกเอง เลือดมักจะหยุดภายใน 2 – 3 ชั่วโมง อาจใช้สารละลายมอนเซลจี้ห้ามเลือดหลังจากการตัดเนื้อออกตรวจเสร็จแล้ว เพื่อไม่ให้รบกวนการแปลผลทางพยาธิวิทยา ในขณะจี้ห้ามเลือดต้องระวังไม่ให้สารละลายไหลย้อยมาที่ช่องคลอดเพราะจะทำให้ระคายเคือง หากมีต้องเช็ดออกให้หมดก่อนเอาเครื่องถ่างตรวจช่องคลอดออก
- การตรวจผนังช่องคลอดให้สังเกตดูผนังช่องคลอดในขณะที่ถอยเครื่องถ่างตรวจช่องคลอดออก อาจใช้ตะขอเกี่ยวผนังช่องคลอดช่วยตรวจบริเวณรอยย่น การใช้ Lugol solution ป้ายผนังช่องคลอดจะช่วยให้การตรวจหาสิ่งผิดปกติง่ายขึ้น
- การตรวจอวัยวะเพศภายนอกอาจใช้สารละลาย acetic acid ความเข้มข้น 3% ชโลมบาง ๆ เพื่อตรวจการเปลี่ยนแปลงของผิวเยื่อบุ ถ้าพบบริเวณที่สงสัยให้ทำการตัดเนื้อออกตรวจหลังจากฉีดยาชาเฉพาะที่เพื่อระงับปวด
- การตรวจสองมือและการตรวจทางทวารหนัก ควรทำการตรวจภายในหลังจากเสร็จสิ้นการตรวจด้วยคอลโปสโคปแล้วทุกราย ผู้ป่วยบางรายมีผลการตรวจด้วยคอลโปสโคปปกติ แต่มีก้อนมะเร็งที่คลำได้อยู่ที่คอมดลูกด้านใน ผู้ป่วยที่จะทำการสืบค้นต่อโดยการตัดปากมดลูกด้วยห่วงไฟฟ้าหรือการตัดปากมดลูกออกเป็นรูปกรวยควรจะทำการตรวจภายในและตรวจทางทวารหนักเพื่อประเมินเนื้อเยื่อข้างมดลูกหรือพารามีเทรียมไว้ก่อน เพราะหลังการทำผ่าตัดดังกล่าวอาจมีปฏิกิริยาอักเสบของเนื้อเยื่อใกล้เคียงทำให้เนื้อเยื่อตึงขึ้น การกำหนดระยะของมะเร็งยากขึ้น
ระยะเวลาที่ทำการตรวจด้วยคอลโปสโคปโดยทั่วไปใช้เวลาประมาณ 3 – 5 นาที ความแม่นยำของการตรวจด้วยคอลโปสโคปขึ้นกับประสบการณ์และความชำนาญของผู้ตรวจ จากการศึกษาแบบ meta – analysis พบว่าการตรวจด้วยคอลโปสโคปมีความไวในการวินิจฉัยรอยโรคภายใน squamous epithelium มากกว่าร้อยละ 90 แต่ความจำเพาะค่อนข้างต่ำไม่เกินร้อยละ 40 (14)
การบันทึกสิ่งตรวจพบทางคอลโปสโคป
International Federation of Cervical Pathology and Colposcopy (IFCPC) 2011 ได้บัญญัติศัพท์ สิ่งตรวจพบทางคอลโปสโคป และแนะนำให้ใช้สำหรับการวินิจฉัยทางคลินิก การวินิจฉัย และการรักษาเกี่ยวกับมะเร็งปากมดลูก ดังนี้ (15)
1. General assessment
- Adequate / inadequate
- การมองเห็น squamocolumnar junction (completely visible / partially visible / not visible)
- Transformation Zone type 1 / 2 /3
โดยลักษณะที่บ่งบอกว่าเป็น transformation zone ได้แก่ เยื่อบุผิวเรียบมีเส้นเลือดละเอียดขนาดเท่า ๆ กัน, เยื่อบุสีขาวบาง ๆ จากสารละลาย acetic acid , ไม่ติดสีไอโอดีนหรือติดสีบางส่วน
ชนิดของtransformation zone
- Type 1 อยู่ที่ปากมดลูกด้านนอกและมองเห็นได้ทั้งหมด จะมีขนาดเล็กหรือใหญ่ก็ได้
- Type 2 บางส่วนอยู่ในคอมดลูกแต่มองเห็นได้ทั้งหมดและอาจจะมีบางส่วนอยู่ที่ปากมดลูกด้านนอก อาจมีขนาดเล็กหรือใหญ่ก็ได้
- Type 3 อยู่ในคอมดลูกซึ่งมองเห็นได้ไม่หมด อาจจะมีบางส่วนอยู่ที่ปากมดลูกด้านนอก ซึ่งอาจจะมีขนาดเล็กหรือใหญ่ก็ได้
2. Normal colposcopic finding
- Original squamous epithelium : mature / atrophic
- Columnar epithelium : erosion
- Metaplastic squamous epithelium : Nabotian cyst / Crypt (gland) openings
- Deciduosis in pregnancy)
3. Abnormal colposcopic findings
- ทั่วไป (General principles)
- ตำแหน่งของรอยโรค ( inside / outside จาก T-zone, ตำแหน่งรอยโรคตามเข็มนาฬิกา)
- ขนาดของรอยโรค (จำนวน quadrant / percent of cervix)
- Grade 1 (minor change)
- Thin acetowhite epithelium
- Fine mosaic
- Fine punctation
- Irregular, geographic border
- Grade 2 (major change)
- Dense acetowhite epithelium
- Coarse mosaic
- Coarse punctuation
- Prominent excretory duct gland, Cuffed crypt (gland) openings
- Sharp border
- Inner border sign (มีรอยโรคด้านในขาวกว่าด้านนอก)
- Ridge sign (มีรอยโรคที่สันขอบ)
- Rapid acetic reaction (เยื่อบุสีขาวปรากฏขึ้นเร็ว)
- Not specific
- Leukoplakia (keratosis / hyperkeratosis)
- Erosion
- Lugor’s reaction / Schiller test (การติดสีไอโอดีน)
4. Suspected invasion
- Atypical vessel
- ลักษณะอื่นๆ เช่น fragile vessel, irregular surface, exophytic lesion, necrosis, ulceration, tumor/gross neoplasm
5. miscellaneous findings
- Congenital transformation zone
- Condylomas
- Endometriosis
- Polyp (ectocervical / endocervical)
- Inflammation
- Stenosis
- Congenital anomaly
- Postoperative change ( scar / vaginal stump )
การให้คำแนะนำหลังการตรวจ
ภายหลังการตรวจด้วยคอลโปสโคปผู้ป่วยสามารถทำงานได้ตามปกติ แนะนำให้ดึงผ้ากอซที่ใส่ประจุไว้ในช่องคลอดออกหลังการตรวจประมาณ 3 ชั่วโมง สังเกตเลือดออกทางช่องคลอด ภายหลังการตัดเนื้อออกตรวจอาจจะมีเลือดออกมาเล็กน้อยได้ประมาณ 1 – 3 วัน ถ้ามีเลือดออกมากผิดปกติให้กลับมาที่โรงพยาบาลทันทีเพื่อตรวจหาสาเหตุและทำการห้ามเลือด ควรงดการมีเพศสัมพันธ์ประมาณ 2 สัปดาห์เพื่อป้องกันการตกเลือดและการติดเชื้อ ไม่ควรสวนล้างหรือใส่ผ้าอนามัยชนิดสอดในช่องคลอดในช่วง 7 วันแรกหลังการตรวจ และนัดมาฟังผลการตรวจชิ้นเนื้อเพื่อวางแผนการรักษาต่อไป (5)
เอกสารอ้างอิง
- Pierce JG Jr, Bright S. Performance of a colposcopic examination, a loop electrosurgical procedure, and cryotherapy of the cervix. Obstet Gynecol Clin North Am 2013; 40:731.
- Sahu B, Latheef R, Aboel Magd S. Prevalence of pathology in women attending colposcopy for postcoital bleeding with negative cytology. Arch Gynecol Obstet 2007;276:471–3
- Cantor SB, Cárdenas-Turanzas M, Cox DD, et al. Accuracy of colposcopy in the diagnostic setting compared with the screening setting. Obstet Gynecol 2008; 111:7.
- Massad LS, Einstein MH, Huh WK, et al. 2012 updated consensus guidelines for the management of abnormal cervical cancer screening tests and cancer precursors. Obstet Gynecol 2013; 121:829.
- จตุพล ศรีสมบูรณ์ , ชำนาญ เกียรติพีรกุล ,บรรณาธิการ.การตรวจด้วยกล้องขยายทางช่องคลอด.มะเร็งนรีเวชวิทยา. กรุงเทพฯ: ราชวิทยาลัยสูตินรีแพทย์แห่งประเทศไทย; 2554. หน้า60-76.
- Dunlop EM, Garner A, Darougar S, et al. Colposcopy, biopsy, and cytology results in women with chlamydial cervicitis. Genitourin Med 1989; 65:22.
- Herfs M, Yamamoto Y, Laury A, et al. A discrete population of squamocolumnar junction cells implicated in the pathogenesis of cervical cancer. Proc Natl Acad Sci U S A 2012; 109:10516.
- Marina OC, Sanders CK, Mourant JR. Effects of acetic acid on light scattering from cells. J Biomed Opt 2012; 17:085002.
- Chan YM, Lee PW, Ng TY, Ngan HY. Could precolposcopy information and counseling reduce women’s anxiety and improve knowledge and compliance to follow-up? Gynecol Oncol 2004; 95:341.
- MacLean AB. Acetowhite epithelium. Gynecol Oncol 2004; 95:691.
- Wentzensen N, Walker JL, Gold MA, et al. Multiple biopsies and detection of cervical cancer precursors at colposcopy. J Clin Oncol 2015; 33:83.
- Solomon D, Stoler M, Jeronimo J, et al. Diagnostic utility of endocervical curettage in women undergoing colposcopy for equivocal or low-grade cytologic abnormalities. Obstet Gynecol 2007; 110:288.
- Buscema J, Woodruff JD. Significance of neoplastic atypicalities in endocervical epithelium. Gynecol Oncol 1984; 17:356.
- Mitchell MF, Schottenfeld D, Tortolero-Luna G, Cantor SB, Richards-Kortum R. Colposcopy for the diagnosis of squamous intraepithelial lesions : a meta – analysis. Obstet Gynecol 1998 ; 91 : 626 – 3
- Bornstein J, Bentley J, Bösze P, et al. 2011 colposcopic terminology of the International Federation for Cervical Pathology and Colposcopy. Obstet Gynecol 2012; 120:166.
- John W. Sellors and R. Sankaranarayanan. Colposcopy and treatment of cervical intraepithelial neoplasia: a beginners’ manual, 2003