Ectopic Pregnancy
ครรภ์นอกมดลูก
ธีระ ทองสง
Ectopic Pregnancy
ความหมาย
การตั้งครรภ์นอกมดลูก คือ การตั้งครรภ์ที่เกิดจากการที่ไข่ซึ่งถูกผสมแล้ว ไปฝังตัวและเจริญเป็นตัวอ่อนในตำแหน่งอื่น ที่นอกเหนือไปจากภายในโพรงมดลูกปกติ เช่น มีการฝังตัวที่ท่อนำไข่ ปากมดลูก รังไข่ ภายในช่องท้อง หรือใน rudimentary horn ของ anomalous uterus เป็นต้น
อุบัติการณ์
พบได้เกือบร้อยละ 1-2 ของการเกิดมีชีพ พบบ่อยขึ้นในถิ่นที่มีโรคติดเชื้อทางเพศสัมพันธุ์ชุก ในโรงพยาบาลมหาราชนครเชียงใหม่มีอุบัติการณ์ประมาณร้อยละ 1.3 ของการคลอด
ประมาณร้อยละ 10-15 ของครรภ์นอกมดลูกเกิดขึ้นในครรภ์แรก และมากกว่าครึ่งหนึ่งของครรภ์นอกมดลูกเกิดขึ้นในสตรีที่เคยตั้งครรภ์มาก่อนตั้งแต่สามครั้งหรือมากกว่า วัยเจริญพันธุ์ที่อายุมากขึ้น ความเสี่ยงจะสูงขึ้น พบในคนผิวดำมากกว่าผิวขาว 1.6 เท่า
ในปัจจุบันการตั้งครรภ์นอกมดลูกมีแนวโน้มสูงขึ้น เนื่องมาจากสาเหตุหลายประการ ได้แก่
- ความก้าวหน้าในการวินิจฉัย ทำให้ตรวจได้ตั้งแต่ในระยะเริ่มแรก ทำให้ผู้ป่วยบางรายซึ่งเดิมไม่เคยได้รับการวินิจฉัย เพราะอาการของโรคเป็นไม่มากและหายไปเอง ก็ได้รับการวินิจฉัยได้ในปัจจุบัน
- เทคโนโลยีช่วยการเจริญพันธุ์ เช่น IVF มีอัตราการเกิดครรภ์นอกมดลูกได้สูงถึงร้อยละ 3 รวมทั้งเพิ่มชนิดที่พบได้น้อยด้วย เช่น ครรภ์ที่รังไข่ คอร์นู ปากมดลูก เป็นต้น
- มีการผ่าตัดท่อนำไข่มากขึ้น เช่น ผ่าตัดครรภ์นอกมดลูกโดยเก็บท่อนำไข่ไว้ เป็นต้น
- การแต่งงานและมีลูกช้ามีมากขึ้นในปัจจุบัน
ปัจจัยส่งเสริม
ตารางที่ 15.1 ปัจจัยเสี่ยงต่อการเกิดครรภ์นอกมดลูก
| ระดับความเสี่ยง | ปัจจัยเสี่ยง | Odds ratio |
| สูง | Previous ectopic pregnancy | 9.3-47 |
| Previous tubal surgery | 6.0-11.5 | |
| Tubal ligation | 3.0-139 | |
| Tubal pathology | 3.5-25 | |
| In utero DES exposure | 2.4-13 | |
| Current IUD use | 1.1-45 | |
| ปานกลาง | Infertility | 1.1-28 |
| Previous cervicitis (gonorrhea, chlamydia) | 2.8-3.7 | |
| History of pelvic inflammatory disease | 2.1-3.0 | |
| Multiple sexual partners | 1.4-4.8 | |
| Smoking | 2.3-3.9 | |
| ต่ำ | Previous pelvic/abdominal surgery | 0.93-3.8 |
| Vaginal douching | 1.1-3.1 | |
| Early age of intercourse (<18 years) | 1.1-2.5 |
- รอยโรคที่ท่อนำไข่: ประวัติการติดเชื้ออุงเชิงกราน รวมทั้ง salpingitis isthmica nodosa เพิ่มความเสี่ยงอย่างน้อย 3 เท่า ประวัติผ่าตัดท่อนำไข่มาก่อนเพิ่มความเสี่ยงอย่างน้อย 5 เท่า แต่การผ่าตัดอื่นในช่องท้องที่ไม่เกี่ยวกับท่อนำไข่ เช่น ผ่าท้องคลอด ตัดไส้ติ่งที่ไม่แตก ผ่าตัดรังไข่ ทำแท้ง รายที่มี สตรีที่เคยมี exposed ต่อ Diethylstilbestrol ตั้งแต่อยู่ในครรภ์มารดา มักมีความผิดปกติของท่อนำไข่ด้วย และมีความเสี่ยงต่อการเกิดครรภ์นอกมดลูกเพิ่มขึ้น 4-5 เท่า
- ภาวะมีบุตรยากเพิ่มความเสี่ยงประมาณ 2 เท่า ART เพิ่มความเสี่ยงอย่างน้อย 2 เท่า
- การตั้งครรภ์ที่เกิดจากความล้มเหลวในการคุมกำเนิด เช่น ประมาณหนึ่งในสามของการตั้งครรภ์ในรายที่ทำหมันแล้วล้มเหลวจะเป็นครรภ์นอกมดลูก ความเสี่ยงโดยรวมประมาณ 7.1 ต่อ 1000 / 10 ปีโดยความเสี่ยงสูงสุดจากการทำหมันด้วย bipolar และต่ำสุดคือการทำหมันหลังคลอด (Pomeroy) สำหรับ IUD ลดครรภ์นอกมดลูกโดยรวม แต่เมื่อตั้งครรภ์โอกาสเป็นครรภ์นอกมดลูกสูงชัดเจน
- ฤดูกาลอาจมีผลต่อความชุก ในรายงานหนึ่งพบว่าครรภ์นอกมดลูกพบบ่อยที่สุดในช่วงระหว่างเดือนมิถุนายนถึงธันวาคม แต่ยังไม่ทราบเหตุผล
- เคยเป็นครรภ์นอกมดลูกมาก่อน พบว่าเพิ่มความเสี่ยงของการเกิดซ้ำได้อีกราวร้อยละ 10-15
- การสูบบุหรี่เพิ่มความเสี่ยงโดยรวม 2 เท่า
- Ovum transmigration พบคอร์ปัสลูเตียมอยู่ด้านตรงข้ามกับด้านที่มีการตั้งครรภ์นอกมดลูกได้ถึงร้อยละ 15-50 เชื่อว่ามีการตกไข่จากรังไข่ด้านหนึ่งเข้าไปในบริเวณ cul-de-sac และเคลื่อนไปเข้าท่อนำไข่ด้านตรงข้าม ซึ่งไข่ใบดังกล่าวอาจถูกผสมโดยอสุจิแล้ว ดังนั้นเมื่อไข่เข้ามาในท่อนำไข่จึงเกิดการฝังตัวได้เร็ว เพราะอยู่ในระยะที่พัฒนาไปมากแล้ว หรืออาจเป็นเพราะ blastocyst มีขนาดใหญ่เกินไป ไม่สามารถเดินทางผ่านส่วน interstitial ที่แคบของท่อนำไข่ได้ จึงเกิดการตั้งครรภ์นอกมดลูกขึ้น
ตำแหน่งของการตั้งครรภ์นอกมดลูก
ตำแหน่งที่พบบ่อยที่สุดคือ การตั้งครรภ์ที่ท่อนำไข่ คือมากกว่าร้อยละ 90 ของครรภ์นอกมดลูกทั้งหมด ส่วนที่พบบ่อยที่สุดคือ ampulla (ร้อยละ 75) รองลงไปเป็น isthmus (ร้อยละ 12), fimbria (ร้อยละ 11) และ interstitium (หรือคอร์นู) (ร้อยละ 2) การตั้งครรภ์ตำแหน่งอื่น ๆ ได้แก่ การตั้งครรภ์ที่รังไข่ ที่ช่องท้อง ที่ปากมดลูก ใน broad ligament ที่แผลผ่าตัดคลอดที่ตัวมดลูก
พยาธิวิทยา
เมื่อฝังตัวแล้ว conceptus ส่วนใหญ่จะเจริญอยู่ในรูของท่อนำไข่ บางส่วนจะบุกรุกชั้นเยื่อบุ lamina propia และ muscularis จนถึง serosa ได้ การตั้งครรภ์อาจดำเนินไปได้หลายรูปแบบเช่น ฝ่อไปเอง ท่อนำไข่แตก แท้งออกไปทาง fimbria (tubal abortion) ซึ่งพบได้กว่าครึ่งหนึ่งของรายที่มีอาการ หรือแท้งแล้วฝังตัวใหม่กลายเป็น secondary abdominal pregnancy เป็นต้น
มดลูกของผู้ตั้งครรภ์นอกมดลูกอาจจะมีขนาดใหญ่ขึ้น อ่อนนุ่ม เนื่องจากมีการตอบสนองต่อฮอร์โมน และเลือดเลี้ยงมากขึ้น มี decidual reaction ที่เยื่อบุโพรงมดลูกได้ ส่วน decidua อาจหลุดออกมาเป็นชิ้น (decidaul cast) ซึ่งเมื่อนำไปลอยน้ำจะมีลักษณะคล้ายขนนก พบได้ร้อยละ 5-10
เยื่อบุโพรงมดลูกอาจเปลี่ยนเป็นลักษณะ Arias-Stella reaction ซึ่งเซลล์ของต่อมโตขึ้น ติดสีเข้ม มีการแบ่งตัว pleomporphism มี vacuole ในซัยโตพลาสม ขาด polarity และไม่เห็น lumen ของต่อม เพราะเซลล์มี hypertrophy เชื่อว่าเกิดจากการกระตุ้นของฮอร์โมนมากเกินไป แต่ไม่ใช่ลักษณะจำเพาะของการตั้งครรภ์นอกมดลูก
ชิ้นเนื้อจากการขูดมดลูกในผู้ป่วยตั้งครรภ์นอกมดลูก พบว่ามี glandular hypersecretion ร้อยละ 12-60 Arias-Stella reaction ร้อยละ 10-20 proliferative pattern ร้อยละ 10-30
การวินิจฉัยการตั้งครรภ์นอกมดลูก
หลักสำคัญในการวินิจฉัยคือ ต้องนึกถึงโรคนี้เสมอในสตรีวัยเจริญพันธุ์ทุกรายที่มีอาการปวดท้องน้อยเฉียบพลัน โดยเฉพาะอย่างยิ่งรายที่ร่วมกับมีเลือดออกทางช่องคลอด
ไม่มีอาการที่จำเพาะสำหรับครรภ์นอกมดลูก แต่มีอาการหลาย ๆ อย่างร่วมกัน ซึ่ง classical triad ที่สำคัญ คือ การขาดระดู มีเลือดออกผิดปกติทางช่องคลอด และเจ็บที่ปีกมดลูก
อาการ
- ในระยะแรก ๆ ของการตั้งครรภ์มักจะไม่มีอาการอะไร ครรภ์ที่ท่อนำไข่มักจะแตกหรือมีอาการเร็ว โดยเฉพาะที่ isthmus
- ปวดท้องน้อย ประมาณร้อยละ 90-100 ของผู้ป่วย ซึ่งอาจเป็นตั้งแต่ก่อนที่จะมีการแตกของครรภ์นอกมดลูกก็ได้ อาการปวดมักเป็นแบบบิด ๆ อาจเป็นข้างเดียว สองข้าง หรือทั่ว ๆ ไปก็ได้ หรือในบางครั้งอาจปวดด้านตรงข้ามกับที่เป็นก็ได้ ในรายที่มีเลือดออกในช่องท้อง อาจมีอาการปวดร้าวไปที่หัวไหล่ ซึ่งเป็น referred pain จากการที่เลือดไประคายเคืองกะบังลม
- เลือดออกทางช่องคลอด พบได้ประมาณร้อยละ 50-80 ของผู้ป่วย เลือดที่ออกมักมีจำนวนน้อย ลักษณะเป็นแบบเลือดเก่า ๆ และออกกะปริดกะปรอย แต่ในบางรายอาจไม่มีเลือดออกเลยก็ได้ โดยเฉพาะในรายที่ตัวอ่อนยังมีชีวิตอยู่ บางรายอาจให้ประวัติว่ามีชิ้นเนื้อ (decidual cast) ออกทางช่องคลอดด้วย ซึ่งอาจทำให้สับสนกับการตั้งครรภ์ในมดลูก และมีภาวะแท้ง
- ขาดระดู พบได้ประมาณร้อยละ 75-95 ของผู้ป่วย และอาจพบมีอาการแพ้ท้องร่วมด้วย บ่อยครั้งอาจพบว่าผู้ป่วยบอกว่าไม่มีการขาดระดู แต่เมื่อซักประวัติประจำเดือนโดยละเอียด จะพบว่ารอบเดือนครั้งสุดท้ายมาน้อยกว่าปกติ หรือมาล่าช้ากว่าที่ควรเป็น ซึ่งอันที่จริงเป็นเลือดออกผิดปกติ ซึ่งผู้ป่วยคิดว่าเป็นระดูครั้งสุดท้าย
- อาการหน้ามืด เป็นลม พบได้ประมาณหนึ่งในสามของผู้ป่วย
- ช็อคจากการเสียเลือด ซึ่งเป็นสาเหตุสำคัญของการตาย ส่วนใหญ่ของการตายจากครรภ์นอกมดลูกเกิดขึ้นก่อนถึงโรงพยาบาล หรือช็อคมากแล้ว
อาการแสดง
- ผู้ป่วยส่วนใหญ่จะไม่มีไข้ มีน้อยกว่าร้อยละ 10 เท่านั้นที่มีอุณหภูมิกายสูงกว่า 38 องศา
- อาการกดเจ็บบริเวณหน้าท้องพบได้ในร้อยละ 80-95 ของผู้ป่วย ในรายที่มีเลือดออกในช่องท้องมักมี rebound tenderness จาก peritoneal irritation
- รายที่มีเลือดออกในช่องท้องอาจพบมี orthostatic hypotension และชีพจรเร็ว ถ้ามีการเสียเลือดมากอาจมีอาการช็อค ความดันโลหิตต่ำ pulse pressure แคบ และชีพจรเร็วเบา
- การตรวจภายในอาจพบ
- อาการแสดงของการตั้งครรภ์ เช่นปากมดลูกมีสีคล้ำ มดลูกนุ่ม แต่อาจไม่พบก็ได้โดยเฉพาะในรายที่มีการเสียเลือดมากจนซีด
- เจ็บเมื่อโยกปากมดลูก พบได้ประมาณร้อยละ 50 ของผู้ป่วย
- cul-de-sac โป่งและกดเจ็บ ในรายที่มีเลือดออกในช่องท้อง
- ส่วนใหญ่มดลูกขนาดปกติ (ร้อยละ 71) ประมาณหนึ่งในสี่มีมดลูกโตขนาด 6 ถึง 8 สัปดาห์ และมีเพียงร้อยละ 3 เท่านั้นที่มีขนาดมดลูกโต 9-12 สัปดาห์อายุครรภ์
- คลำได้ก้อนที่ปีกมดลูกด้านใดด้านหนึ่ง ประมาณร้อยละ 20 ของผู้ป่วย และกดเจ็บ พบได้ร้อยละ 50 ของผู้ป่วย
- Alder sign ผู้ป่วยจะมีอาการกดเจ็บที่เดิม (fixed abdominal tenderness) ในขณะที่เปลี่ยนท่าไปต่าง ๆ แต่อาการแสดงนี้พบได้น้อย
การพยากรณ์โรคจะดีในรายที่ได้รับการวินิจฉัยและรักษาตั้งแต่ระยะแรก ๆ อัตราการตั้งครรภ์โดยเฉลี่ยภายหลังการตั้งครรภ์นอกมดลูกประมาณร้อยละ 60 แต่อาจเป็นครรภ์นอกมดลูกได้สูงถึงหนึ่งในสี่
การวินิจฉัยแยกโรค
ภาวะที่อาจสับสนกับครรภ์นอกมดลูกได้บ่อย ๆ ที่สุดคือเลือดออกจากการแตกของถุงน้ำคอร์ปัสลูเตียม (โดยเฉพาะในรายที่ตั้งครรภ์) นอกจากนั้นอาจสับสนกับ ปีกมดลูกอักเสบ ภาวะแทรกซ้อนจากการแท้ง ไส้ติ่งอักเสบ การบิดขั้วของเนื้องอกรังไข่ การแตกของถุงน้ำฟอลลิเคิล เป็นต้น
การตรวจค้นเพื่อการวินิจฉัย
การตรวจค้นที่มีประโยชน์มากที่สุดคือการตรวจ TVS ร่วมกับ hCG
1. การทดสอบการตั้งครรภ์ มีคุณค่าในการช่วยวินิจฉัยครรภ์นอกมดลูกคือ
- ยืนยันการตั้งครรภ์ (ในรายทดสอบให้ผลบวก) แต่ไม่อาจบอกได้ว่าตั้งครรภ์ในหรือนอกมดลูก
- ตัดปัญหาครรภ์นอกมดลูกออกไปได้ถ้า beta-hCG ให้ผลลบ แต่ในกรณีนี้ต้องทดสอบด้วยวิธีที่มีความไวมากคือ serum radioimmunoassay (RIA)
- การตรวจปัสสาวะด้วยวิธีใหม่ ๆ เช่น ELISA ที่มีความไวระดับ 10-20 มิลลิยูนิต/มล จะให้ผลบวกกว่าร้อยละ 99 ของครรภ์นอกมดลูก
- การตรวจติดตามระดับ hCG มีประโยชน์ในรายที่ไม่แน่ใจในการวินิจฉัยหรือ PUL
3. การตรวจด้วยอัลตราซาวด์ มีประโยชน์มากในการช่วยวินิจฉัยครรภ์นอกมดลูก โดยเฉพาะเมื่อใช้ร่วมกับการตรวจระดับ hCG เครื่องตรวจอัลตราซาวด์ทางช่องคลอด (TVS) ซึ่งอาจมีความไวในการวินิจฉัยถึงร้อยละ 80 สามารถใช้วินิจฉัยการตั้งครรภ์ภายในโพรงมดลูกได้ตั้งแต่ 4-5 สัปดาห์หลัง LMP และสามารถตรวจพบการเต้นของหัวใจเด็กที่อายุครรภ์ 6 สัปดาห์ การใช้คลื่นเสียงดอพเลอร์ดูการไหลเวียนเลือดจะช่วยให้การวินิจฉัยดีขึ้นไปอีก
คุณค่าของการตรวจอัลตราซาวด์ในรายที่ผลทดสอบการตั้งครรภ์ให้ผลบวก และมีอาการหรืออาการแสดงของครรภ์นอกมดลูก หรือมีปัจจัยเสี่ยงต่อการเกิดครรภ์นอกมดลูก จะช่วยตรวจหาตำแหน่งของการตั้งครรภ์ให้ได้ว่าอยู่นอกหรือในมดลูก ซึ่งอาจให้ผลการตรวจดังนี้
1) ตัดปัญหาครรภ์นอกมดลูกออกได้ ถ้าถ้าพบว่ามีหลักฐานครรภ์ในมดลูก อย่างไรก็ตามจะต้องแยกถุงการตั้งครรภ์จริงในโพรงมดลูกต้องแยกจาก pseudogestational sac (PGS) ที่พบได้ราวร้อยละ 10-20 ของครรภ์นอกมดลูก ซึ่ง PGS ทุกรายไม่เห็น yolk sac มักมีรูปร่างผิดปกติ และไม่เห็น chorio-decidual reaction ชัดเจน แยกจากถุงการตั้งครรภ์จริงได้ไม่ยาก
2) วินิจฉัยการตั้งครรภ์นอกมดลูกได้ทันที โดยเห็นถุงการตั้งครรภ์ชัดเจน (yolk sac หรือเห็นตัวอ่อน) อยู่นอกโพรงมดลูก ซึ่งพบได้ประมาณร้อยละ 20
3) ลักษณะแสดงทางอ้อมที่บ่งชี้ว่ามีโอกาสสูงที่จะเป็นครรภ์นอกมดลูก ได้แก่
- มดลูกว่างเปล่า (empty uterus) (หรือเห็น PGS ด้วย) แต่มีโอกาสเป็นครรภ์ผิดปกติหรือครรภ์ปกติในมดลูกที่อายุครรภ์ยังน้อย อย่างไรก็ตามการพบมดลูกว่างโดยไม่พบสารน้ำในอุ้งเชิงกราน และก้อนที่ปีกมดลูก โอกาสจะเป็นครรภ์นอกมดลูกน้อย (ร้อยละ 5-10) แต่ประมาณร้อยละ 20 ของครรภ์นอกมดลูกอาจะไม่พบความผิดปกติใด ๆ ในการตรวจอัลตราซาวด์ครั้งแรก
- ก้อนที่ปีกมดลูก (complex mass) อาจเกิดจากเนื้อเยื่อการตั้งครรภ์ และก้อนเลือดในบริเวณปีกมดลูก หรือ cul-de-sac มีความเข้มเสียงไม่สม่ำเสมอ เกิดจากก้อนครรภ์นอกมดลูก หรือก้อนเลือดซึ่งขอบเขตไม่ค่อยแน่นอน ประมาณร้อยละ 20 เห็นถุงการตั้งครรภ์อยู่นอกมดลูก (bagel sign) และอีกประมาณร้อยละ 20 สามารถเห็น yolk sac และ/หรือตัวอ่อนซึ่งอาจเห็นการเต้นของหัวใจด้วยหรือไม่ก็ได้ ซึ่งกรณีนี้ถือว่าเป็น “definite EP” ส่วนใหญ่มีความเข้มเสียงต่ำและไม่สม่ำเสมอ (inhomogeneous) ของ amorphous materials ไม่เป็นถุงน้ำ (noncystic) บางท่านเรียกว่า blob sign แยกจากก้อนรังไข่ (พบได้บ่อยที่สุด ประมาณร้อยละ 60 ของผู้ป่วย) ถือว่าเป็น “probable EP” บ่อยครั้งที่เห็นเป็นก้อนกลมในภาพตัดขวางของท่อนำไข่ ซึ่งการตรวจอย่างรอบคอบจะเห็นขอบท่อนำไข่ที่โตขึ้น (tubal ring) และอาจเห็นเป็นท่อยาวบวมเมื่อบิดหัวตรวจ ซึ่งเกิดจาก hematosalpinx การตรวจอัลตราซาวด์อาจพบก้อนได้ถึงร้อยละ 60-90 ของครรภ์นอกมดลูก จาก meta-analysis รวบรวมจาก 10 รายงานแสดงให้เห็นว่าก้อนที่ปีกมดลูกดังกล่าวทำนายการเป็นครรภ์นอกมดลูกถูกต้องโดยมีความไวร้อยละ 84 และความจำเพาะร้อยละ 99 ประมาณร้อยละ 25 ของผู้ตั้งครรภ์นอกมดลูกมาตรวจครั้งแรกให้ผลเป็น PUL และประมาณร้อยละ 7-20 ของผู้ที่ได้รับการวินิจฉัยขั้นต้นเป็น PUL ในที่สุดได้รับการพิสูจน์ว่าเป็น PUL
- สารน้ำขุ่นในช่องท้อง (echogenic peritoneal free fluid) หรือมีส่วนที่เป็นก้อนเลือดด้วยหรือไม่ก็ได้ ก้อนเลือดที่เห็นมักมีความเข้มเสียงไม่สม่ำเสมอ รูปร่างแปลก ๆ ขอบเขตไม่ค่อยแน่นอน โอกาสเป็นครรภ์นอกมดลูกจะมากเกินร้อยละ 50 อย่างไรก็ตามการมีสารน้ำขุ่นนี้บ่งชี้ถึง hemoperitoneum แต่ไม่ได้บ่งชี้ว่าครรภ์นอกมดลูกแตกหรือไม่
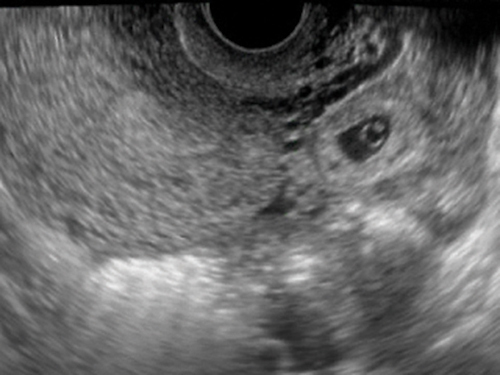
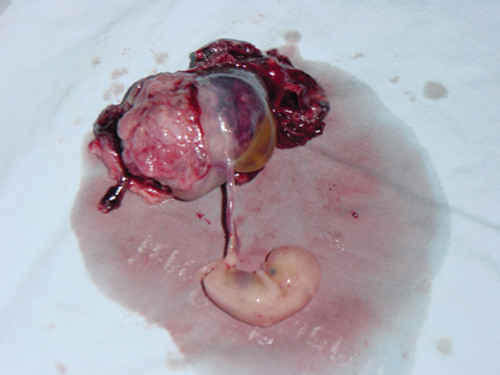
รูปที่ 1 ครรภ์นอกมดลูกที่ท่อนำไข่ ซ้าย: ภาพอัลตราซาวด์แสดงถุงการตั้งครรภ์พร้อมทั้ง yolk sac ที่ท่อนำไข่ข้างซ้าย (ไม่ได้แสดงทารก) ขวา: ท่อนำไข่ที่แตกแล้วขณะผ่าตัด
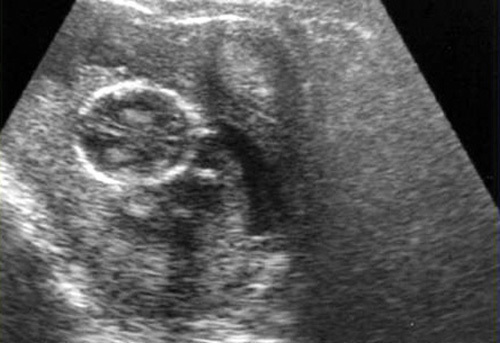
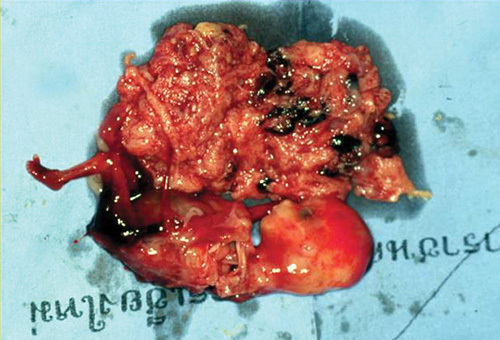
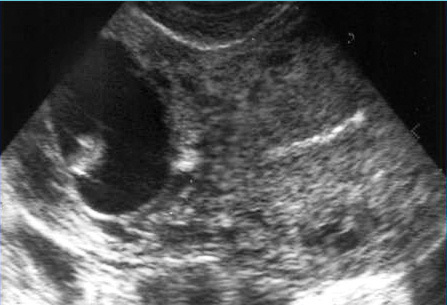
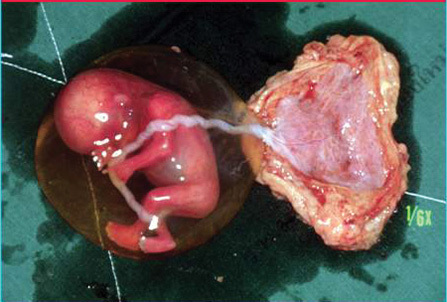
รูปที่ 2 ครรภ์นอกมดลูกในช่องท้อง (abdominal pregnancy) ซ้าย: ภาพอัลตราซาวด์แสดงศีรษะทารกและรกที่อยู่ในช่องท้องหลังตัวมดลูก ขวา: ลักษณะครรภ์ในช่องท้องที่พบขณะผ่าตัด
รูปที่ 3 ครรภ์ที่คอร์นู (cornual pregnancy) ซ้าย: ภาพอัลตราซาวด์ตัดขวางระดับยอดมดลูกแสดงถุงการตั้งครรภ์ที่อยู่บริเวณมุมของยอดมดลูก กล้ามเนื้อมดลูกไม่หุ้มล้อมรอบถุงการตั้งครรภ์ ขวา: ลักษณะครรภ์ในช่องท้องที่พบขณะผ่าตัดเอาคอร์นูและถุงการตั้งครรภ์ออกมา
ข้อสังเกต
- ก้อนการตั้งครรภ์ที่รังไข่มักจะสับสนกับถุงน้ำคอร์ปัสลูเตียมที่มีเลือดออก
- การวัดความหนาของเยื่อบุโพรงมดลูกไม่มีประโยชน์ในการวินิจฉัยครรภ์นอกมดลูก
- ถ้าในมดลูกว่างแบบไม่มี content เลย จะมีโอกาสเป็นครรภ์นอกมดลูกสูงขึ้นเป็น 5 เท่าของการมี content คือ น้ำคั่ง echogenic material ถุงน้ำผิดปกติ
- การเห็น yolk sac หรือตัวอ่อนในโพรงมดลูกทำให้วินิจฉัย IUP ได้ แต่ยังสรุปว่าเป็นครรภ์ปกติไม่ได้
- TVS พบว่า MSD มากกว่า 25 มม โดยไม่เห็นตัวอ่อน หรือ CRL มากกว่า 7 มม แล้วไม่เห็นหัวใจเต้นสรุปได้ว่าเป็นครรภ์ที่ไม่มีชีวิต
- โอกาสเป็นครรภ์นอกมดลูกต่ำ (น้อยกว่าร้อยละ 10) ถ้าระดับ hCG ลงเร็ว (เกินครึ่งใน 1-2 วัน) และโอกาสสูง (เกือบร้อยละ 90) ถ้าลดลงช้ามาก (น้อยกว่าครึ่งในเวลา 7 วัน)
ตารางที่ 15.2 ความไวและความจำเพาะของการตรวจ TVS ในการวินิจฉัย EUP
| ลักษณะทางอัลตราซาวด์ | ความไว | ความจำเพาะ |
| ไม่พบถุงการตั้งครรภ์ในโพรงมดลูก | 100 | 89 |
| ก้อนที่ปีกมดลูก แยกจากรังไข่ (blob / bagel sign) | 93 | 99 |
| ก้อนที่ปีกมดลูก ร่วมกับหัวใจเต้น | 20 | 100 |
| ก้อนที่ปีกมดลูก ร่วมกับเห็น Yolk sac หรือตัวอ่อน | 37 | 100 |
| Tubal ring / yolk sac หรือตัวอ่อน | 65 | 99 |
| น้ำขุ่น (echogenic free fluid) | 56 | 96 |
| Color-flow Doppler | 95 | 98 |
การตรวจอื่น ๆ
การขูดมดลูก: เลือกทำในบางรายที่แน่ใจแล้วว่าเป็นครรภ์ผิดปกติ เช่น ไม่มีการเพิ่มระดับ hCG ที่เหมาะสม หรือระดับโปรเจสเตอโรนต่ำ จะช่วยบอกว่ามีวิลไลในโพรงมดลูกหรือไม่ ถ้าไม่มี โอกาสเป็นครรภ์นอกมดลูกสูงมาก
ส่องแลพพาโรสโคป: ถือเป็นวิธีมาตรฐานในการวินิจฉัยครรภ์นอกมดลูก แต่เป็นเทคนิครุกล้ำ จึงเลือกทำบางราย เฉพาะในรายที่ TVS ร่วมกับ hCG ยังวินิจฉัยได้ไม่แน่ชัด อย่างไรก็ตามการวินิจฉัยครรภ์นอกมดลูกจากแลพพาโรสโคปก็อาจผิดพลาดได้ (ผลบวกหรือลบลวง) ราวร้อยละ 3
การตรวจระดับโปรเจสเตอโรน: ในครรภ์ผิดปกติทั้งในและนอกมดลูกจะมีระดับต่ำ ถ้าค่าเกิน 25 นก/มล.จะเป็นครรภ์ปกติในมดลูกร้อยละ 97.5 แต่ถ้าค่าต่ำกว่า 5 นก./มล. เป็นครรภ์ปกติได้เพียงร้อยละ 0.3 อย่างไรก็ตามผู้ป่วยครรภ์นอกมดลูกจำนวนมากมีค่าที่ระดับ 5-25 นก/มล.ซึ่งมีคุณค่าทางคลินิกน้อย
Culdocentesis: เป็นการเจาะ cul-de-sac ผ่านทางช่องคลอด ใช้วินิจฉัยภาวะเลือดออกในช่องท้อง แต่ไม่ได้บอกว่าเลือดมาจากไหน ขีดจำกัดนี้ทำให้บทบาทของ culdocentesis ลดลงมากในปัจจุบัน
แนวทางในการดูแลรักษาผู้ป่วยที่สงสัยครรภ์นอกมดลูก
กลุ่มที่ vital signs ไม่ดี (unstable) เช่น มีอาการแสดงของช็อคจากการเสียเลือด ควรพิจารณาผ่าตัดทันที โดยไม่ต้องตรวจด้วยอัลตราซาวด์
กลุ่มที่ vital signs ปกติดี แนวทางในการดูแลขึ้นอยู่กับผลจากการตรวจอัลตราซาวด์ ซึ่งจำแนกได้ดังนี้
- Definite EP: เห็นถุงการตั้งครรภ์อยู่นอกมดลูกพร้อมกับเห็น yolk sac และ/หรือตัวอ่อนซึ่งอาจเห็นการเต้นของหัวใจด้วยหรือไม่ก็ได้ กลุ่มนี้ควรได้รับการรักษาทันที
- Probable EP: ก้อนที่ปีกมดลูกแยกจากรังไข่มีลักษณะ inhomogeneous / noncystic (blob sign) หรือคล้ายถุงการตั้งครรภ์นอกมดลูก กลุ่มนี้ควรได้รับการรักษาทันที หรือยืนยันการวินิจฉัยโดยเร็วด้วยแลพพาโรสโคป ขึ้นกับระดับความมั่นใจของผู้ดูแล
- PUL: ไม่พบลักษณะของการตั้งครรภ์ทั้งในและนอกมดลูก ซึ่งพบได้ประมาณไม่เกินร้อยละ 15 ของการตรวจ
- Probable IUP: ลักษณะคล้ายถุงการตั้งครรภ์ในโพรงมดลูก กลุ่มนี้แนะนำให้ตรวจ TVS ติดตามเพื่อยืนยัน
- Definite IUP: เห็นถุงการตั้งครรภ์ในโพรงมดลูกพร้อมกับเห็น yolk sac และ/หรือตัวอ่อนซึ่งอาจเห็นการเต้นของหัวใจด้วยหรือไม่ก็ได้ กลุ่มนี้แนะนำให้ฝากครรภ์
PUL เป็นกลุ่มที่มีความยากในการดูแล ขึ้นกับหลายปัจจัย เช่น ความสะดวกในการตรวจติดตาม การเปลี่ยนแปลของระดับ hCG เป็นต้น ควรให้คำปรึกษาแนะนำผู้ป่วยถึงทางเลือกหลากหลาย เช่น
- ให้ดูลักษณะทางคลินิก ถ้าปวดมากอาจตรวจ hCG หรือส่องแลพพาโรสโคป ถ้าไม่ปวดให้เฝ้าติดตาม (expectant) ร่วมกับตรวจระดับ hCG ที่ 0 และที่ 48 ชั่วโมง แล้วดูแลไปตามผลระดับ hCG: เช่น
- ลดลงมากกว่าร้อยละ 13 คาดว่าเป็น failed PUL ให้ทดสอบการตั้งครรภ์ใน 2 สัปดาห์
- เพิ่มมากกว่าร้อยละ 66 คาดว่าเป็น IUP ปกติ ให้ตรวจ TVS ยืนยันในวันที่ 7
- เพิ่มไม่ถึงร้อยละ 66 อาจเป็น EP ให้ตรวจ TVS ในวันที่ 7 หรือเมื่อคาดว่า hCG เกิน 1000 IU/L
- ลดลงไม่ถึงร้อยละ 13 อาจเป็น failing PUL หรือ EP ให้ตรวจ hCG ซ้ำในวันที่ 7
- ถ้าระดับ hCG สูง เช่น เกินระดับวิกฤติคือประมาณ 2000 IU/L (1,500-2,500) อาจเลือกขูดมดลูกเพื่อตรวจว่ามีวิลไลหรือไม่ หรือส่องแลพพาโรสโคป ซึ่งมีข้อดีข้อเสียต่างไป ถ้าระดับต่ำกว่า 2000 IU/L ตรวจติดตามระดับ hCG ในสองวัน แล้วพิจารณาดูแนวโน้มการเปลี่ยนแปลง ถ้าลงค่อนข้างช้าให้ขูดมดลูกเพื่อดูว่ามีวิลไลหรือไม่ ถ้าลงเร็วแสดงว่าแท้งไปเอง (miscarriage) ถ้าขึ้นปกติให้ตรวจ TVS ซ้ำเมื่อ hCG > 2000 IU/L
การดูแลรักษาต้องชั่งใจหลายประการ เช่น การขูดมดลูกในรายที่ hCG ขึ้นไม่ดี ก็ยังอาจเป็นการทำแท้งโดยไม่ตั้งใจได้ เพราะโอกาสมี IUP ปกติยังคงมีอยู่ แม้จะไม่มากนัก อาจถึงร้อยละ 10 ของ IUP ปกติที่ระดับ hCG ไม่ขึ้นตามปกติ และอาจถึงร้อยละ 15-20 ของ EP ที่ระดับ hCG ขึ้นแบบปกติ รายที่ตรวจติดตามแม้ระดับ hCG บ่งชี้ว่าโอกาสเป็น EP ต่ำมาก ก็ยังอาจเป็นได้อยู่และอาจมีครรภ์นอกมดลูกแตกระหว่างกันติดตาม แม้ว่าโอกาสจะน้อยมากก็ตาม
PUL ควรได้รับการติดตามจนสรุปผลสุดท้าย ซึ่งควรจะจำแนกผลเป็น visualized EP, visualized IUP, spontaneously resolved PUL, และ persisting PUL สำหรับกลุ่มสุดท้ายควรพยายามติดตามและระบุในขั้นสุดท้ายว่าเป็นกลุ่มใดต่อไปนี้ nonvisualized EP, treated persistent PUL, resolved persistent PUL หรือ histologic IUP
วิธีการรักษา
วิธีการรักษามีหลายรูปแบบ ซึ่งเหมาะสมแตกต่างกันไปในแต่ละราย การผ่าตัด salpingostomy ผ่านแลพพาโรสโคป มีค่าใช้จ่ายถูกกว่าการผ่าเปิดหน้าท้อง แต่ประสบความสำเร็จต่ำกว่าเล็กน้อยเนื่องจากอัตราการมี persistent trophoblast สูงกว่า แต่แก้ปัญหานี้ได้ดีด้วยการให้ methotrexate หลังทำแลพพาโรสโคป โดยรวมแล้วการผ่าตัดผ่านแลพพาโรสโคปมีความคุ้มค่าในการรักษาดีกว่าการรักษาด้วยยา methotrexate แต่การรักษาด้วยยามีความความคุ้มกว่าถ้าระดับ hCG ตั้งต้นต่ำกว่า เช่น ต่ำกว่า 3000 มิลลิยูนิต/มล (เหมาะกับยาแบบให้หลายครั้ง) หรือระดับต่ำกว่า 1,500 มิลลิยูนิต/มล (เหมาะกับยาแบบให้ครั้งเดียว)
1. การรักษาด้วยการเฝ้าสังเกต
ครรภ์นอกมดลูกจำนวนหนึ่งฝ่อหายไปเองได้ ในรายเช่นนี้อาจเลือกรักษาด้วยการเฝ้าสังเกต ซึ่งควรเลือกผู้ป่วยที่สามารถตรวจติดตามได้อย่างใกล้ชิด รายที่ระดับ hCG ตั้งต้นต่ำ เช่น < 200 มิลลิยูนิต/มล. หรือ PUL ที่ระดับลดลงเรื่อย ๆ
2. การรักษาด้วยยา
ในทศวรรษที่ผ่านมาการรักษาด้วยยาเข้ามามีบทบาทในการรักษาครรภ์นอกมดลูกจนกลายเป็นวิธีที่ใช้บ่อยที่สุด การให้ methotrexate มี 2 วิธีหลักคือ แบบครั้งเดียว (single dose) หรือแบบหลายครั้ง (multidose) ต่างก็ให้ผลดี (ร้อยละ 75-95) แต่ให้แบบครั้งเดียวมีอัตราล้มเหลวสูงกว่า โดยเฉพาะในรายที่ระดับ hCG สูง หรือตัวอ่อนมีชีวิต ในทางปฏิบัติ มักจะเลือกแบบ single dose กับผู้ป่วยส่วนใหญ่ แต่เลือก multidose ในรายเสี่ยงต่อความล้มเหลวสูง เช่น ตั้งครรภ์ที่คอร์นูหรือที่ปากมดลูก ระดับ hCG สูง หรือตัวอ่อนมีชีวิต
ผู้ป่วยที่เหมาะสมมากในการเลือกรักษาด้วย methotrexate มีดังนี้คือ
- ผู้ป่วยแข็งแรงดี ฮีโมไดนามิคปกติ และให้ความร่วมมือดี
- ไม่มีความบกพร่องของระบบไต ตับ และโลหิต
- ผู้ป่วยให้ความร่วมมือในการตรวจติดตามการรักษา
- ระดับ serum hCG ต่ำกว่า 5000 มิลลิยูนิต/มล
- ขนาดก้อนท่อนำไข่ไม่เกิน 3-4 ซม. และไม่มีหัวใจทารกเต้น
ข้อบ่งห้ามคือ ให้นมบุตร ภูมิคุ้มกันบกพร่อง ติดสุรา โรคตับหรือไต การแข็งตัวของเลือดผิดปกติ โรคปอดที่ตื่นตัวอยู่ แผลในกระเพาะ กรณีที่ระดับ hCG เกิน 5000 มิลลิยูนิต/มล. หรือตัวอ่อนมีชีวิต ไม่ถือเป็นข้อบ่งห้ามโดยเด็ดขาด แต่มีแนวโน้มล้มเหลวและความเสี่ยงต่อการแตกสูงขึ้น
อาการปวดท้องมากขึ้นในช่วงหลาย ๆ วัน (6-7 วัน) หลังได้ยา พบได้บ่อย (ร้อยละ 65-75) ไม่ค่อยรุนแรง มักจะเป็นไม่นาน (1-2 วัน) ให้เฝ้าติดตามอย่างใกล้ชิด ถ้าลักษณะทางคลินิกบ่งชี้ชัดว่าครรภ์นอกมดลูกแตก ให้รีบผ่าตัด
สารน้ำในช่องท้องอาจพบได้เกือบร้อยละ 40 ของครรภ์นอกมดลูกที่ยังไม่แตก การมีหรือไม่มีไม่สามารถทำนายผลการรักษาด้วยยาได้
การรักษาด้วยยาอาจพิจารณาว่าเหมาะสมเป็นพิเศษในกรณีที่มีความเสี่ยงจากการผ่าตัดสูง ได้แก่ การตั้งครรภ์ที่ปากมดลูก หรือที่ cornu ซึ่งปัจจุบันวินิจฉัยก่อนผ่าตัดได้บ่อยขึ้น
การตั้งครรภ์ที่ปากมดลูกที่ตัวอ่อนมีชีวิตแนะนำให้ฉีด KCL ให้เสียชีวิตก่อนจึงให้ methotrexate แบบ multidose
อัตรา tubal patency หลังรักษาสำเร็จพอ ๆ กับผ่าตัดทางแลพพาโรสโคป คือร้อยละ 60-85
โดยทั่วไปแล้ว ร้อยละ 50-80 ของรายที่รักษาด้วย methotrexate กลับมาตั้งครรภ์ในมดลูกปกติ และร้อยละ 10-20 เป็นครรภ์นอกมดลูกซ้ำ
Mifepristone ก็อาจใช้ได้ในการรักษาครรภ์นอกมดลูก แต่ประสิทธิภาพและคุณค่ายังไม่เป็นที่ยอมรับกัน
ตารางที่ 15-3 โปรโตคอลการให้ยา methotrexate ในการรักษาครรภ์นอกมดลูก (การทดสอบก่อนรักษา: ระดับ hCG, TVS, หมู่เลือดซึ่งรวมถึง Rh, CBC การทำงานตับ หยุดให้โฟลิค แนะนำให้หลีกเลี่ยง NSAID งดเพศสัมพันธ์และการออกกำลังหนัก)
| วันที่ | Single dose protocol | Multiple dose protocol |
| 1 | ตรวจวัดระดับ hCG Methotrexate 50 มก/ม2 พื้นผิวร่างกาย IM |
ตรวจวัดระดับ hCG Methotrexate 1 มก/กก น้ำหนักตัว IM หรือ IV |
| 2 | Leucovorin 0.1 มก/กก ☉ | |
| 3 | ตรวจวัดระดับ hCG เทียบกับวันที่ 1 ถ้า ลด <15% ให้ methotrexate 1 มก/กก IM หรือ IV ลด >15% ให้เริ่มตรวจ hCG สัปดาห์ละครั้ง |
|
| 4 | ตรวจวัดระดับ hCG | Leucovorin 0.1 มก/กก ☉* |
| 5 | ตรวจวัดระดับ hCG เทียบกับวันที่ 3 ถ้า ลด <15% ให้ methotrexate 1 มก/กก IM หรือ IV ลด >15% ให้เริ่มตรวจ hCG สัปดาห์ละครั้ง |
|
| 6 | Leucovorin 0.1 มก/กก ☉* | |
| 7 | ตรวจวัดระดับ hCG เทียบกับวันที่ 4 ถ้า ลด <15% ให้ methotrexate 50 มก/ม2 IM ลด >15% ตรวจ hCG สัปดาห์ละครั้ง |
ตรวจวัดระดับ hCG เทียบกับวันที่ 5 ถ้า ลด <15% ให้ methotrexate 1 มก/กก IM หรือ IV ลด >15% ให้เริ่มตรวจ hCG สัปดาห์ละครั้ง |
| 8 | Leucovorin 0.1 มก/กก ☉* | |
| 14 | ตรวจวัดระดับ hCG เทียบกับวันที่ 7 ถ้า ลด <15% ให้ methotrexate 50 มก/ม2 IM ลด >15% ตรวจ hCG สัปดาห์ละครั้ง |
ตรวจวัดระดับ hCG เทียบกับวันที่ 7 ถ้า ลด <15% ให้ methotrexate 1 มก/กก IM (Leucovorin 0.1 มก/กก ☉) ลด >15% ให้เริ่มตรวจ hCG สัปดาห์ละครั้ง |
| 21& 28 | ถ้าให้ครบ 3 ครั้งแล้วลดลงจากวันที่ 21 ถึงวันที่ 18 <15% ให้ผ่าตัด (แลพพาโรสโคป) | ถ้าให้ครบ 5 ครั้งแล้วลดลงจากวันที่ 14 ถึงวันที่ 21 <15% ให้ผ่าตัด (แลพพาโรสโคป) |
ให้ส่องแลพพาโรสโคปถ้าปวดท้องรุนแรงที่บ่งชี้ว่าเกิดจากครรภ์นอกมดลูกแตก หรืออัลตราซาวด์พบว่าน้ำในช่องท้องมากกว่า 300 มล.
ที่มา: 1) Barnhart KT. Clinical practice. Ectopic pregnancy. N Engl J Med 2009; 361:379; 2) American College of Obstetricians and Gynecologists. ACOG Practice Bulletin No. 94: Medical management of ectopic pregnancy. Obstet Gynecol 2008; 111:1479
3. รักษาด้วยการผ่าตัด
ข้อบ่งชี้ในการรักษาด้วยการผ่าตัด ได้แก่ สัญญาณชีพไม่ปกติ เสี่ยงสูงต่อความล้มเหลวจากการรักษาด้วยยา มีข้อบ่งห้ามในการให้ methotrexate หรือให้ยาแล้วล้มเหลว สำหรับรายที่ไม่เห็นก้อนชัดเจนจาก TVS ก็ไม่ควรผ่าตัดเนื่องจากมีโอกาสสูงที่จะผ่าแล้วไม่พบก้อนเช่นเดียวกัน
การผ่าตัดทำได้ทั้งผ่านทางแลพพาโรสโคป (ถือเป็นทางเลือกแรกถ้าสามารถทำได้) หรือผ่าหน้าท้องโดยตรง ซึ่งสามารถผ่าตัดเชิงอนุรักษ์ linear salpingostomy ได้ผลพอ ๆ กัน การผ่าตัดแบบนี้จะต้องติดตาม hCG ซึ่งควรจะให้ผลลบใน 4-6 สัปดาห์ ในรายที่ยังค้างอยู่จะต้องรักษาต่อด้วย methotrexate หรือผ่าตัดซ้ำ ซึ่งกรณีหลังนี้พบได้ประมาณร้อยละ 5
หลังทำ salpingostomy ระดับ b-hCG ลดลงรวดเร็วในไม่กี่วัน หลังจากนั้นลดต่ออย่างช้า ๆ ใช้เวลาในการหายไปโดยเฉลี่ย 20 วัน แต่การให้ methotrexate เข้ากล้าม 1 ครั้ง ระดับจะเพิ่มใน 4 วันแรก แล้วค่อย ๆ ลดลงอย่างช้า ๆ ใช้เวลาในการหายโดยเฉลี่ย 27-34 วัน แต่มีรายที่ยาวนานที่สุดถึง 109 วัน
โดยรวมผลการรักษาจากการผ่าตัด อัตราการตั้งครรภ์ในมดลูกหลังผ่าตัดเชิงอนุรักษ์สูงกว่าการตัดท่อนำไข่ออก โดยอัตราการเกิดครรภ์นอกมดลูกซ้ำภายหลังไม่แตกต่างกัน
การผ่าตัดเอาท่อนำไข่ออก (salpingectomy) ควรพิจารณาทำในรายที่
- มีบุตรเพียงพอแล้ว
- เป็นครรภ์นอกมดลูกซ้ำที่ท่อนำไข่ข้างเดิม
- ควบคุมการเสียเลือดไม่ได้
- ท่อนำไข่แตกหรือถูกทำลายรุนแรง
กลุ่มที่ต้องการมีบุตรอีก มีท่อนำไข่ไม่ตัน (ร้อยละ 80-90) มีครรภ์ในมดลูก (ร้อยละ 55-75) และครรภ์นอกมดลูกซ้ำ (ร้อยละ 10-15) หลังผ่าแบบแลพพาโรสโคป หรือ ผ่าเปิดหน้าท้อง พอ ๆ กัน
การรักษาครรภ์ในช่องท้อง อาศัยการผ่าตัดเป็นหลัก บางครั้งการเอารกออกอาจจะยากและต้องปล่อยทิ้งไว้ให้ค่อย ๆ ถูกดูดซึม หรือใช้ methotrexate หลังผ่าตัดช่วย (พิจารณาเฉพาะบางราย) อาจใช้หลายเทคนิคร่วมกัน เช่น embolization ก่อนผ่าตัด เป็นต้น
Persistent ectopic pregnancy พบบ่อยในรายผ่าเชิงอนุรักษ์ พบในรายผ่าผ่านแลพพาโรสโคปสูงกว่าผ่าเปิดหน้าท้องเล็กน้อย พบบ่อยขึ้นในรายอายุครรภ์น้อยกว่า 6 สัปดาห์ ก้อนครรภ์นอกมดลูกเล็กกว่า 2 ซม. ซึ่งยากที่จะแยกและตัดออกได้สมบูรณ์ วิธีที่จะวินิจฉัยดีที่สุดคือตรวจติดตามระดับ hCG แนะนำให้ตรวจวันแรกหลังผ่าตัด และทุก 3-7 วัน (แล้วแต่ระดับของการลด) ไปจนวัดไม่ได้ ระดับวันแรกหลังผ่าตัดจะบอกทำนายได้ดี ถ้าลดลงมากว่าค่าก่อนผ่าตัดมาก จะมีโอกาส persistent ต่ำ ถ้าลดลงไม่ถึงร้อยละ 50 โอกาส persist สูงเป็น 3 เท่า
การตั้งครรภ์นอกมดลูกที่ไม่ใช่ท่อนำไข่
1. การตั้งครรภ์ในช่องท้อง (abdominal pregnancy) ซึ่งพบได้น้อยคือราวร้อยละ 1.4 ของครรภ์นอกมดลูก แบ่งได้เป็นชนิด primary คือเกิดเมื่อไข่ที่ถูกผสมแล้วมีการฝังตัวในช่องท้องโดยตรง หรือ secondary ซึ่งมีการตั้งครรภ์ที่ท่อนำไข่มาก่อน แล้วหลุดไปเจริญเติบโตต่อในช่องท้อง พบได้บ่อยกว่าแบบแรก
เกณฑ์วินิจฉัยของชนิด primary (Studiford’s criteria) คือการตรวจพบ 1) ท่อนำไข่และรังไข่ปกติ โดยไม่พบร่องรอยของการตั้งครรภ์ทั้งเก่าและใหม่ 2) ไม่มีรูเชื่อมของรกและมดลูก (uteroplacental fistula) และ 3) การตั้งครรภ์ทั้งหมดอยู่ที่ผิวเยื่อบุช่องท้อง และดูใหม่ไม่เหมือนหลุดออกมาฝังต่อจากท่อนำไข่
การตั้งครรภ์ในช่องท้องอาจดำเนินไปถึงครบกำหนดได้ บางรายอาจมีชีวิตรอด แต่โดยทั่วไปจะถูกยุติการตั้งครรภ์เมื่อได้รับการวินิจฉัย เนื่องจากการรอให้ทารกโตเป็นการเพิ่มความเสี่ยงต่อมารดา เมื่อผ่าตัดเอาทารกออกนั้น อาจจะเอารกออกด้วยถ้าคาดว่าทำไม่ยากเกินไปโดยไม่สามารถควบคุมการเสียเลือดได้ หลายรายอาจต้องทิ้งรกไว้และตรวจติดตามรอให้ดูดซึมเอง
2. การตั้งครรภ์ที่รังไข่ (ovarian pregnancy) พบได้น้อย (ร้อยละ 0.5-1 ของครรภ์นอกมดลูก) ไม่สัมพันธ์กับติดเชื้อในอุ้งเชิงกราน และการใส่ห่วงอนามัย เกณฑ์การวินิจฉัย (Spiegelberg’s criteria) คือ
- มีการตั้งครรภ์ในตำแหน่งของรังไข่
- โดยที่ก้อนการตั้งครรภ์มีการติดต่อกับตัวมดลูกด้วย ovarian ligament
- พบเนื้อเยื่อของรังไข่อยู่บริเวณผนังของก้อน
- ท่อนำไข่ข้างเดียวกันกับที่ก้อนการตั้งครรภ์อยู่ต้องมีลักษณะปกติ แยกจากก้อนการตั้งครรภ์ได้ชัดเจน
3. การตั้งครรภ์ที่ปากมดลูก (cervical pregnancy) พบได้น้อยมาก (ร้อยละ 0.2 ของครรภ์นอกมดลูก) แต่พบบ่อยขึ้นจากการตั้งครรภ์เด็กหลอดแก้ว เกิดจากการฝังตัวที่ endocervix ในทางพยาธิวิทยาจะต้องเห็น cervical glands อยู่บริเวณที่มีการฝังตัวของรก รกฝังตัวต่ำกว่าระดับ uterine vessels และไม่มีส่วนของตัวอ่อนอยู่ในโพรงมดลูก
เกณฑ์การวินิจฉัยทางคลินิกได้แก่
- มดลูกมีขนาดเล็กกว่าปากมดลูกที่โป่งขยายตัว
- ปากมดลูกด้านนอก (external os) อาจจะเปิด
- ปากมดลูกมีลักษณะเป็นรอยโรคสีม่วงคล้ำ
- เลือดออกมากเมื่อนวดบีบปากมดลูก
เกณฑ์การวินิจฉัยโดยอัลตราซาวด์
- เห็นถุงการตั้งครรภ์และเนื้อรกอยู่ที่ปากมดลูก
- เยื่อบุโพรงมดลูกปกติ ไม่เห็นส่วนการตั้งครรภ์ในโพรงมดลูก
- มดลูกมีรูปลักษณ์เป็นนาฬิการทราย (hourglass) หรือรูปเลข 8 เนื่องจากปากมดลูกบวมโตออก
- หัวใจทารกเต้นอยู่ใต้ต่อระดับ internal os
- Internal os ปิด
- ถุงการตั้งครรภ์ไม่เขยื้อนเมื่อใช้หัวตรวจกด (TVS) หรือไม่มี sliding sign
ทางเลือกการรักษาอาจเป็นการให้ยา methotrexate แบบหลายครั้ง ถ้าหัวใจเต้นให้พิจารณาฉีด KCL เข้าหัวใจทารกก่อน ถ้าเลือดออกมากควบคุมไม่ได้ให้เลือกวิธีผ่าตัด หรือทำ uterine arterial embolization ก่อนแล้วตามด้วยการ evacuation
5. การตั้งครรภ์ที่แผลผ่าตัดคลอด (cesarean scar) สามารถเกิดขึ้นได้ประมาณ 1 ต่อ 2000 นับเป็นร้อยละ 6 ของครรภ์นอกมดลูกของสตรีที่เคยผ่าตัดคลอดมาก่อน ตัวการตั้งครรภ์ถูกหุ้มล้อมด้วยกล้ามเนื้อมดลูกและเนื้อเยื่อเกี่ยวพัน การวินิฉัยอาศัยภาพอัลตราซาวด์แสดงก้อนการตั้งครรภ์ที่ตำแหน่งแผล โดยปูดยื่นออกนอกแนวผนังด้านหน้าของมดลูก ไม่เห็นส่วนทารกในโพรงมดลูก ในบางรายอาจตรวจ MRI ช่วยเสริมการวินิจฉัย การวินิจฉัยแยกโรคได้แก่ การตั้งครรภ์ที่ปากมดลูก และรกติดแน่น (placenta adherens) การรักษาอาจเลือกตัดเป็นลิ่มออก (อาจผ่านทางการเปิดท้อง กล้องแลพพาโรสโคป หรือกล้องส่องโพรงมดลูก) หรือรักษาด้วยยา หรือ uterine artery embolization ซึ่งยังไม่สามารถระบุวิธีที่ดีที่สุด แต่การวินิจฉัยที่เร็วที่สุดและรักษาโดยเร็วจะมีภาวะแทรกซ้อนน้อยที่สุด ดังนั้นการตรวจอัลตราซาวด์ในระยะแรก ๆ สตรีตั้งครรภ์ที่เคยผ่าตัดคลอดมาก่อน ควรตรวจและระบุตำแหน่งการฝังตัวให้ชัดเจน
8. Heterotropic (combined) pregnancy มีการตั้งครรภ์ทั้งในและนอกมดลูกร่วมกัน พบได้น้อยคือราว 1:4,000-30,000 การตั้งครรภ์ พบบ่อยมากขึ้นในเทคโนโลยีช่วยภาวะเจริญพันธุ์คือพบได้ถึงร้อยละ 1 ของการตั้งครรภ์ที่เกิดขึ้น การรักษาส่วนใหญ่ผ่าตัดท่อนำไข่ออก (แลพพาโรสโคป) การให้ยาแบบ systemic เป็นข้อบ่งห้ามเนื่องจากยาจะไปทำลายครรภ์ปกติที่อยู่โพรงมดลูก บางท่านเลือกที่จะฉีดยาเข้าไปทำลายในถุงการตั้งครรภ์ (salpingocentesis) เช่น KCl, methotrexate เป็นต้น ซึ่งอาจฉีดผ่านทางแลพพาโรสโคป หรือฉีดโดยการชี้นำด้วยอัลตราซาวด์
6. Interstial / cornual pregnancy: การตั้งครรภ์ที่ท่อนำไข่ส่วนที่ฝังอยู่ในกล้ามเนื้อมดลูก พบร้อยละ 2-3 ของครรภ์นอกมดลูก เกณฑ์การวินิจฉัยจากอัลตราซาวด์จะต้องแสดงให้เห็นว่า 1) เห็นถุงการตั้งครรภ์เอียงออกข้าง (eccentric) โพรงมดลูกว่าง (TVS ที่แสดงแนว cervical canal จะไม่เห็นถุงการตั้งครรภ์) 2) ถุงการตั้งครรภ์มีกล้ามเนื้อมดลูกบาง ๆ (น้อยกว่า 5 มม) หุ้มอยู่ และ 3) เห็น Interstitial line (เส้นเข้มเชื่อมจากโพรงมดลูกไปยังถุงการตั้งครรภ์ที่อยู่ขอบ การรักษาในกรณีที่ต้องการเก็บมดลูกไว้ให้พิจารณาการรักษาด้วยยา (multidose) ก่อน เว้นเสียแต่สภาพไม่เหมาะสมเช่นเลือดออกมาจนจำเป็นต้องผ่าตัด ซึ่งอาจผ่าตัดเอาลิ่มคอร์นู (wedge) ที่มีถุงการตั้งครรภ์ออก หรือตัดมดลูกในกรณีที่มีบุตรพอแล้ว
7. Rudimentary horn pregnancy เกิดจากการฝังตัวของตัวอ่อนใน horn ของ bicornuate uterus ซึ่ง ส่วนใหญ่ (ร้อยละ 90) ไม่เชื่อมต่อกับตัวมดลูกปกติ ดังนั้นจึงต้องมี transperitoneal migration ของตัวอสุจิหรือไข่
8. Intraligamentous pregnancy เป็นการตั้งครรภ์ที่อยู่ระหว่าง anterior และ posterior leaves ของ broad ligament การตั้งครรภ์ชนิดนี้เป็นการฝังตัวใหม่ โดยมีการฝังตัวที่อื่นก่อน เช่น ในท่อนำไข่ แล้วต่อมาจึงแตกแทรกเข้าไปใน broad ligament
เอกสารอ้างอิง
- ACOG Practice Bulletin No. 94: Medical management of ectopic pregnancy. Obstet Gynecol 2008 Jun;111(6):1479-85.
- Alkatout I, Honemeyer U, Strauss A, Tinelli A, Malvasi A, Jonat W, et al. Clinical diagnosis and treatment of ectopic pregnancy. Obstet Gynecol Surv 2013 Aug;68(8):571-81.
- Barnhart K, van Mello NM, Bourne T, Kirk E, Van CB, Bottomley C, et al. Pregnancy of unknown location: a consensus statement of nomenclature, definitions, and outcome. Fertil Steril 2011 Mar 1;95(3):857-66.
- Barnhart KT, Gosman G, Ashby R, Sammel M. The medical management of ectopic pregnancy: a meta-analysis comparing “single dose” and “multidose” regimens. Obstet Gynecol 2003 Apr;101(4):778-84.
- Barnhart KT. Clinical practice. Ectopic pregnancy. N Engl J Med 2009 Jul 23;361(4):379-87.
- Brown DL, Doubilet PM. Transvaginal sonography for diagnosing ectopic pregnancy: positivity criteria and performance characteristics. J Ultrasound Med 1994 Apr;13(4):259-66.
- Callahan R, Yacobson I, Halpern V, Nanda K. Ectopic pregnancy with use of progestin-only injectables and contraceptive implants: a systematic review. Contraception 2015 Sep 10.
- Capmas P, Bouyer J, Fernandez H. Treatment of ectopic pregnancies in 2014: new answers to some old questions. Fertil Steril 2014 Mar;101(3):615-20.
- Cole LA. Individual deviations in human chorionic gonadotropin concentrations during pregnancy. Am J Obstet Gynecol 2011 Apr;204(4):349-7.
- Condous G, Timmerman D, Goldstein S, Valentin L, Jurkovic D, Bourne T. Pregnancies of unknown location: consensus statement. Ultrasound Obstet Gynecol 2006 Aug;28(2):121-2.
- Condous G, Kirk E, Lu C, Van CB, Van HS, Timmerman D, et al. There is no role for uterine curettage in the contemporary diagnostic workup of women with a pregnancy of unknown location. Hum Reprod 2006 Oct;21(10):2706-10.
- Doubilet PM, Benson CB, Bourne T, Blaivas M, Barnhart KT, Benacerraf BR, et al. Diagnostic criteria for nonviable pregnancy early in the first trimester. N Engl J Med 2013 Oct 10;369(15):1443-51.
- Feng C, Chen ZY, Zhang J, Xu H, Zhang XM, Huang XF. Clinical utility of serum reproductive hormones for the early diagnosis of ectopic pregnancy in the first trimester. J Obstet Gynaecol Res 2013 Feb;39(2):528-35.
- Fritz MA, Speroff L. Clinical gynecologic endocrinology and infertility. 8 ed. Philadelphia: Wolters Kluwer | Lippincott Williams & Wilkins; 2011.
- Heard MJ, Buster JE. Ectopic pregnancy. In: Scott JR, Gibbs RS, Karlan BY, Haney AF, editors. Danforth’s obstetrics and gynecology. 9th ed. Philadelphia: Lippincott Williams & Wilkins; 2003. p. 89-104.
- Jurkovic D, Hillaby K, Woelfer B, Lawrence A, Salim R, Elson CJ. First-trimester diagnosis and management of pregnancies implanted into the lower uterine segment Cesarean section scar. Ultrasound Obstet Gynecol 2003 Mar;21(3):220-7.
- Kirk E, Papageorghiou AT, Condous G, Tan L, Bora S, Bourne T. The diagnostic effectiveness of an initial transvaginal scan in detecting ectopic pregnancy. Hum Reprod 2007 Nov;22(11):2824-8.
- Kirk E, Bottomley C, Bourne T. Diagnosing ectopic pregnancy and current concepts in the management of pregnancy of unknown location. Hum Reprod Update 2014 Mar;20(2):250-61.
- Ko JK, Cheung VY. Time to revisit the human chorionic gonadotropin discriminatory level in the management of pregnancy of unknown location. J Ultrasound Med 2014 Mar;33(3):465-71.
- Kung FT, Lin H, Hsu TY, Chang CY, Huang HW, Huang LY, et al. Differential diagnosis of suspected cervical pregnancy and conservative treatment with the combination of laparoscopy-assisted uterine artery ligation and hysteroscopic endocervical resection. Fertil Steril 2004 Jun;81(6):1642-9.
- Larrain D, Marengo F, Bourdel N, Jaffeux P, Aublet-Cuvelier B, Pouly JL, et al. Proximal ectopic pregnancy: a descriptive general population-based study and results of different management options in 86 cases. Fertil Steril 2011 Mar 1;95(3):867-71.
- Lobo RA. Ectopic pregnancy. In: Katz VL, Lobo RA, Lentz G, Gershenson D, editors. Comprehensive gynecology. 5th ed. St. Louis, Mo: Mosby; 2007. p. 389-418.
- Moawad NS, Mahajan ST, Moniz MH, Taylor SE, Hurd WW. Current diagnosis and treatment of interstitial pregnancy. Am J Obstet Gynecol 2010 Jan;202(1):15-29.
- Mol F, Mol BW, Ankum WM, van d, V, Hajenius PJ. Current evidence on surgery, systemic methotrexate and expectant management in the treatment of tubal ectopic pregnancy: a systematic review and meta-analysis. Hum Reprod Update 2008 Jul;14(4):309-19.
- Stovall TG. Early pregnancy loss and ectopic pregnancy. In: Berek JS, editor. Berek & Novak’s gynecology. 14th ed. Philadelphia: Lippincott Williams & Wilkins; 2007. p. 601-36.
- Voedisch A, Frederick CE, Nicosia AF, Stovall TG. Early pregnancy loss and ectopic pregnancy. In: Berek JS, editor. Berek & Novak’s gynecology. 15 ed. Philadelphia: Wolters Kluwer Health | Lippincott Williams & Wilkins; 2012. p. 619-45.
- Weibel HS, Alserri A, Reinhold C, Tulandi T. Multidose methotrexate treatment of cervical pregnancy. J Obstet Gynaecol Can 2012 Apr;34(4):359-62.
- Wu G, Yang J, Xu W, Yin T, Zou Y, Wang Y. Serum beta human chorionic gonadotropin levels on day 12 after in vitro fertilization in predicting final type of clinical pregnancy. J Reprod Med 2014 Mar;59(3-4):161-6.
- Xiao-Yan C, Jie L, Dang J, Tao L, Xin-Ru L, Guang-Lun Z. A highly sensitive electrochemiluminescence immunoassay for detecting human embryonic human chorionic gonadotropin in spent embryo culture media during IVF-ET cycle. J Assist Reprod Genet 2013 Mar;30(3):377-82.
- Zee J, Sammel MD, Chung K, Takacs P, Bourne T, Barnhart KT. Ectopic pregnancy prediction in women with a pregnancy of unknown location: data beyond 48 h are necessary. Hum Reprod 2014 Mar;29(3):441-7.

