Common vulvar lesions
พญ.รัศมิ์รวี จันทรศิริ
รศ.พญ.จารุวรรณ แซ่เต็ง
Anatomy of vulva (1,2,3)
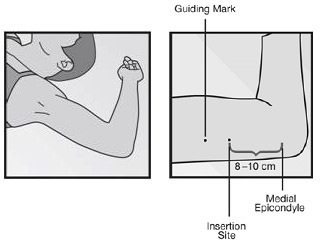
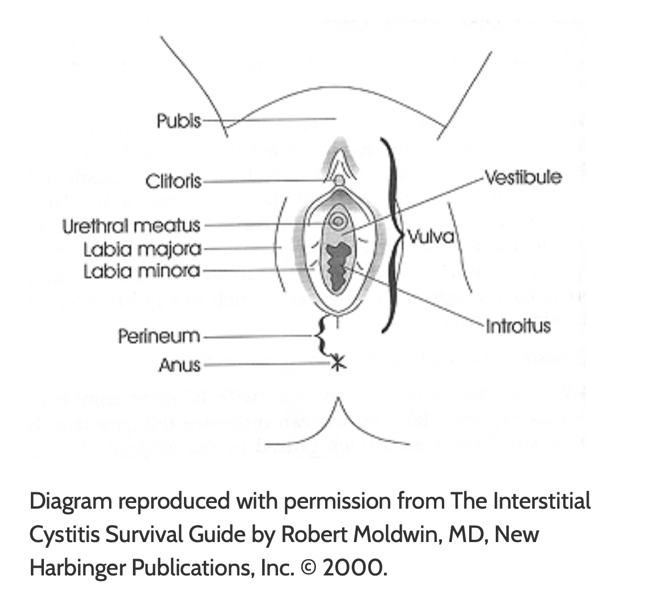
อวัยวะเพศภายนอกของสตรี ซึ่งประกอบด้วย mons pubis, labia majora, labia minora, hymen, clitoris, vestibule, urethra, Skene’s gland, Bartholin’s gland และ vestibular bulbs
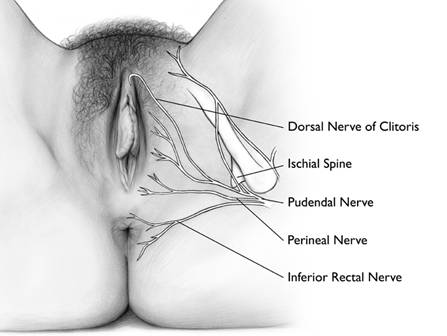
เส้นประสาทที่มาเลี้ยงบริเวณอวัยวะเพศภายนอก ได้แก่ ilioinguinal n., genitofemoral n., femoral cutaneous n., peritoneal n. (แขนงของ pudendal n.)
ในส่วนของ blood supply นั้น หลักๆจะมาจาก internal pudendal a. นอกจากนี้ยังมี external pudendal a. ซึ่งเป็นสาขาของ femoral a.อีกด้วย หลังจากนั้นเลือดจะไหลเวียนกลับโดยผ่าน internal และexternal pudendal v.
Terminology of vulvar lesions (4)
สามารถบรรยายลักษณะของรอยโรคหลักได้ ดังนี้
|
Morphology
|
Definition
|
|
Macule
|
Small (<1 cm) area of color change; no elevation and nonpalpable |
|
Patch
|
Large (>1 cm) area of color change; no elevation and nonpalpable |
|
Papule
|
Small (<1 cm) palpable lesion. |
|
Nodule
|
Large (>1 cm) palpable lesion; usually dome shaped; margins may be distinct (sharp) or slope shouldered. |
|
Plaque
|
Large (>1 cm) flat-topped and palpable lesion. |
|
Vesicle
|
Small (<1 cm) fluid-filled blister; clear fluid. |
|
Bulla
|
Large (>1 cm) fluid-filled blister; clear fluid. |
|
Pustule
|
Small or large pus-filled blister; white or yellow fluid. |
|
Cyst
|
Small or large nodule with epithelial-lined central cavity containing solid, semisolid, or fluid-filled material. |
|
Erosion
|
Shallow defect limited to epidermis; the base of the defect may be red or covered by yellow crust. Erosions heal without scarring. |
|
Ulcer
|
Deep defect into or through the dermis; the base may be red or covered by yellow, blue, or black crust. Ulcers heal with scarring. |
|
Fissure
|
Thin (<2 mm wide), linear erosion into or through the epidermis. |
|
Scale
|
Grey or silver keratin proteins on the tissue surface that become white when moist; usually feels rough on palpation. |
|
Crust
|
Yellow, granular material overlying erosions; develops due to solidification of plasma proteins when the water component of plasma evaporates; crusts overlying ulcers may be blue or black due to heme pigment. |
|
Excoriation
|
Linear or angular erosions due to scratching. |
|
Lichenification
|
Red or skin-colored plaques with exaggerated skin markings due to chronic rubbing; excoriations are usually also present. The surface may be white when moist. |
|
Eczema
|
Erythematous, poorly marginated patches and plaques that demonstrate lichenification and/or evidence of epithelial disruption such as erosions or crust. |
– Size and shape
– Edge: clearly demarcated, poorly defined
– Number, location, distribution of multiple lesions (เช่น scattered, grouped, linear etc.)
– Color
– Consistency (hard, soft, firm, fluctuation)
– feel (tenderness)
– Presence of secondary changes (excoriation, lichenification, edema, scale, crust, fissure, erosion, hypo-/hyperpigmentation, atrophy, scar)
– Acute inflammation (edema, pain,erythema)
Common benign vulvar lesions
Atopic dermatitis/ eczema (5,6)
เป็นผื่นแพ้ของผิวหนัง เกิดจากการสัมผัสโดยตรงกับสิ่งที่ทำให้เกิดการระคายเคือง หรือ สารก่อภูมิแพ้
- Irritant contact dermatitis จะพบในกลุ่มเด็ก หรือผู้สูงอายุ ซึ่งเกิดจากการทำงานของ skin barrier บริเวณปากช่องคลอดไม่ดี จึงทำให้เกิดการระคายเคืองได้จาก direct nonimmunologic cytotoxic effect เวลาสัมผัสกับสิ่งที่ทำให้เกิดการระคายเคือง เช่น ปัสสาวะ สบู่ น้ำหอม ผงซักผ้า สารหล่อลื่น สำหรับกรณีที่มีอาการแพ้เฉียบพลัน หลังจากสัมผัสจะเกิดจาก type I immediate hypersensitivity สารก่อภูมิแพ้ในกลุ่มนี้ ได้แก่ น้ำอสุจิ และยางที่ใช้ทำถุงยางอนามัย นอกจากนี้ยังสามารถเกิดอาการจาก type IV delayed hypersensitivity ที่พบได้จาก ใยผ้าจากเสื้อผ้าที่สวมใส่ ผ้าอนามัย หรือ สารเคมีต่างๆ
อาการแสดง (Clinical presentation) (5,6)
ผู้ป่วยมักจะมาด้วยอาการคันบริเวณปากช่องคลอดหลังจากสัมผัสกับสิ่งที่ทำให้เกิดการระคายเคือง ร่วมกับตรวจร่างกายพบผื่นแดงบริเวณปากช่องคลอด อาการมักจะหายไปหลังได้รับการรักษา แต่หากไม่หลีกเลี่ยงสารก่อภูมิแพ้ ผู้ป่วยจะมีอาการคันเรื้อรัง จะทำให้เกิดการเกาจนกลายเป็น chronic contact dermatitis และมีผิวหนังที่หนาขึ้นได้ (lichenificaiton)
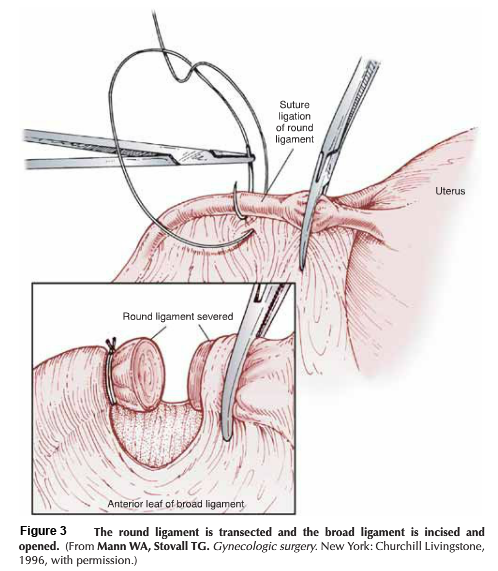
ภาพ Vulva atopic dermatitis ในผู้ป่วยที่เคยมีประวัติเป็น atopic dermatitis (6)
ภาพ Irritant contact dermatitis ในผู้ป่วย urinary inconstinence(6)
การวินิจฉัยโรค (Diagnosis) (5,6)
การวินิจฉัยอาศัยการซักประวัติ และการตรวจร่างกายเป็นหลัก ไม่มีความจำเป็นต้องตัดชิ้นเนื้อเพื่อส่งตรวจทางพยาธิวิทยา การซักประวัติเน้น การซักประวัติเกี่ยวกับการสัมผัสสารที่ก่อให้การระคายเคือง หรือการแพ้
Management (5,6)
หลักการที่สำคัญของการรักษาคือ หาสิ่งที่ทำให้เกิดอาการแพ้ และหลีกเลี่ยงไม่ไปสัมผัสอีก แนะนำให้ใส่เสื้อผ้าหลวม โปร่งสบาย ไม่คับจนเกินไป และงดเพศสัมพันธ์เพื่อลดการเสียดสีของผิวหนังบริเวณดังกล่าว
Acute contact dermatitis
- Burrow solution
- Potassium permanganate
- Emolient
- Steroid
- Antihistamine drug
Chronic contact dermatitis
- Medium strength steroid: 0.1% betamethasone ทา 2-3ครั้ง/วัน นานประมาณ 2 สัปดาห์
- Low strength steroid: 0.1% triamcinolone
Lichen simplex chronicus(5)
เป็น Chronic endogenous eczema ผู้ป่วยมักมาด้วยอาการคันเรื้อรังบริเวณปากช่องคลอด คันตลอดเวลา บ่อยครั้งมักจะมีอาการคันเวลากลางคืน ผู้ป่วยมักจะมีประวัติเป็นผื่นภูมิแพ้ผิวหนัง (atopic dermatitis) ร่วมด้วย
ลักษณะรอยโรคเหมือน atopic dermatitis แต่มี plaque ที่มีสีแดงเข้มอมน้ำตาล แต่หลังจากที่รอยโรคสัมผัสกับความชื้น จากสารคัดหลั่ง ทั้งเหงื่อ ปัสสาวะ และจากช่องคลอด รอยโรคอาจเปลี่ยนไปเป็นสีขาวได้ ส่วนกรณีที่มีการเกามานานสักระยะหนึ่ง ผิวหนังจะหนาตัวขึ้นชัดเจน (lichenification)
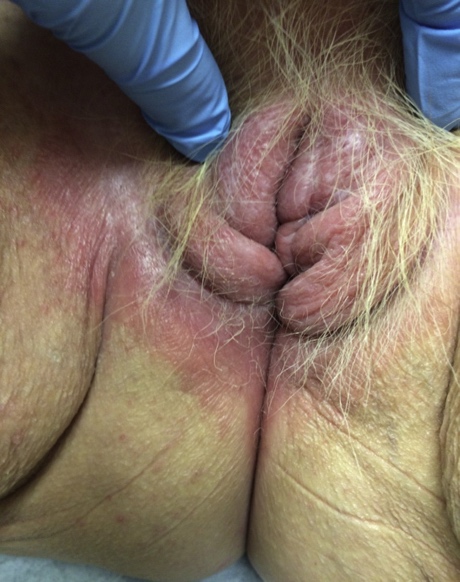
ภาพ lichen simplex chronicus แสดงผิวหนังที่หนาตัวขึ้น (lichenification) Image Courtesy of Dr.Andrew Goldstein
Management (5)
แนะนำให้หยุดการเกา เนื่องจากการเกายิ่งทำให้เกิดการระคายเคืองเรื้อรัง และทำให้เกิดการคันกลับมาอีก นอกจากนี้พยายามสิ่งกระตุ้น หรือสิ่งที่ทำให้เกิดอาการระคายเคือง สำหรับยาทาเฉพาะที่นั้น อาจจะพิจารณาให้เป็น medium strength steroid เช่น 0.1% betamethasone โดยให้ทาบริเวณรอยโรคประมาณ 2-3 ครั้งต่อวัน เป็นเวลา 10-14 วัน จนกว่าอาการคันจะบรรเทาไป หากอาการไม่ดีขึ้น ให้พิจารณาให้เป็น superpotent steroid
Vulvar Lichen planus (7-12)
มีลักษณะคือ มี erosion, papular หรือ hypertrophic lesion บริเวณปากช่องคลอด ซึ่งอาจจะรวมถึงบริเวณช่องคลอดด้วยหรือไม่ก็ได้
อุบัติการณ์ (Epidemiology) (7-9)
พบได้ประมาณร้อยละ 0.5-2 ในประชากรทั่วไป มักพบในหญิงอายุ 50-60 ปี (7-9) แต่อย่างไรก็ตามยังสามารถพบได้ในช่วงอายุที่น้อยกว่า และมากกว่าช่วงอายุดังกล่าว
สาเหตุ (Etiology)
ยังไม่ทราบแน่ชัด แต่เชื่อว่าเกิดจากการที่เซลล์เม็ดเลือดขาว ชนิด T-cell ต่อต้านกับ basal keratinocytes และมักจะสัมพันธ์กับโรคทางภูมิคุ้มกัน (autoimmune disease)
อาการแสดง (Clinical presentation)
มักจะมาด้วยอาการ ดังต่อไปนี้
- vulvar pain
- burning
- pruritus
- soreness
- dyspareunia
- irritating vaginal discharge
โดยอาการเหล่านี้อาจจะเป็นอยู่ตลอด(constant) หรือเป็นๆหายๆ(intermittent) ก็ได้
นอกจากนี้ ยังสามารถพบได้ ร่วมกับ cutaneous lichen planus, oral lichen planus หรือ lichen planopilaris (frontal fibrosing alopecia)
Lichen planus แบ่งออกเป็น 4 กลุ่มตาม clinical varirant ดังนี้
1. Erosive lichen planus
เป็นชนิดที่พบได้บ่อยที่สุด มักพบในลักษณะของการหลุดลอกของเยื่อบุผิว desquamative, erosive, chronic dermatitis โดยรอยโรคมักจะมีขอบเขตชัดเจน (well demacated), glazed, brightly erythematous patches or erosions with white striae, whited border along margin (Wickham striae)
ตำแหน่งของรอยโรค มักพบบริเวณ labia minora, vestibule อาจมี vaginal involvement ได้บ่อย แต่จะไม่ค่อยพบบริเวณ labia majora และ anus
Lichen planus ชนิดนี้สามารถกลับมาเป็นซ้ำได้ รอยโรคหายช้า จึงอาจทำให้เกิดแผลเป็นได้ กล่าวคือ ทำให้ลักษณะทางกายวิภาคบิดเบือนไป รวมถึงทำให้ช่องคลอดตีบแคบ (severe vaginal stenosis) และท่อปัสสาวะอุดกั้น (urethral obstruction)
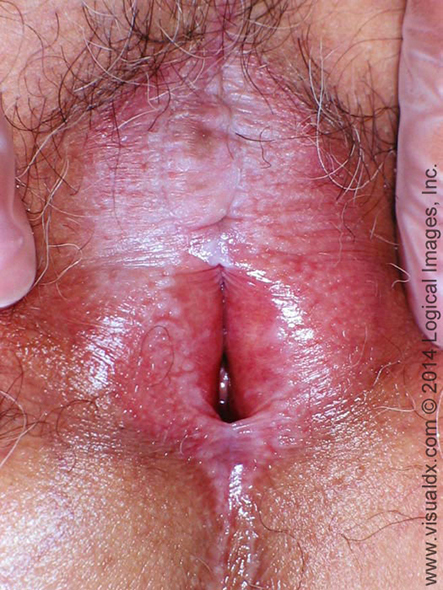
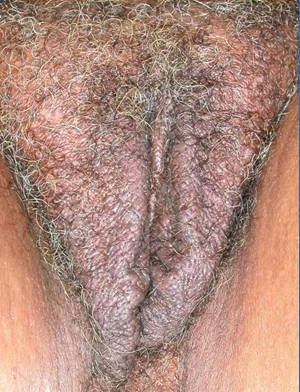
ภาพแสดง Vulvar lichen planus demonstrating loss of architecture, muddy white macules,
and formation of vulvar synechiae causing superior and inferior restriction of the introitus; reference: www.visualdx.com
– Vaginal involvement (12)
Lichen planus สามารถพบ vaginal involvement ร่วมได้ มากถึงร้อยละ 70(12) โดยเยื่อบุผนังช่องคลอดในผู้ป่วยที่เป็น lichen planus จะมีความเปราะบางมา จึงทำให้เลือดออกง่ายหลังการตรวจภายใน หรือหลังมีเพศสัมพันธ์ บางรายอาจพบเป็นการอักเสบรุนแรงได้
สำหรับในรายที่รุนแรงมากๆอาจทำให้เกิดผังผืดในช่องคลอดจนทำให้เกิดการตีบแคบของช่องคลอดตามมา
– Vaginal-gingival syndrome (VVG)
คือ lichen planus ที่สัมพันธ์กับเยื่อบุผิวหนังบริเวณ vulva, vestibule, vagina, mouth ถึงแม้ว่า lichen planus จะสามารถพบได้ในตำแหน่งสำคัญดังกล่าวไปข้างต้น รอยโรคในแต่ละตำแหน่งไม่จำเป็นต้องเกิดขึ้นพร้อมกัน นอกจากนี้ยังอาจจะพบได้ที่บริเวณอื่นๆ ได้แก่ ผิวหนัง, เยื่อบุหลอดอาหาร, เยื่อบุกล่องเสียง, เยื่อบุตา และท่อปัสสาวะ แต่จะพบได้ไม่บ่อยนัก
รอยโรคมักจะพบได้บ่อยที่เยื่อบุช่องปากบริเวณกระพุ้งแก้ม ลิ้น และเพดานปาก ลักษณะเป็น erosion, white plaque, whitish and ice like reticular pattern
เนื่องจาก VVG มักจะไม่ค่อยตอบสนองต่อการรักษา จึงทำให้เกิด long term morbidity ที่สำคัญได้แก่ การเกิดพังผืด แผลเป็น และการตีบแคบของเนื้อเยื่อ (scarring and stricture formation)
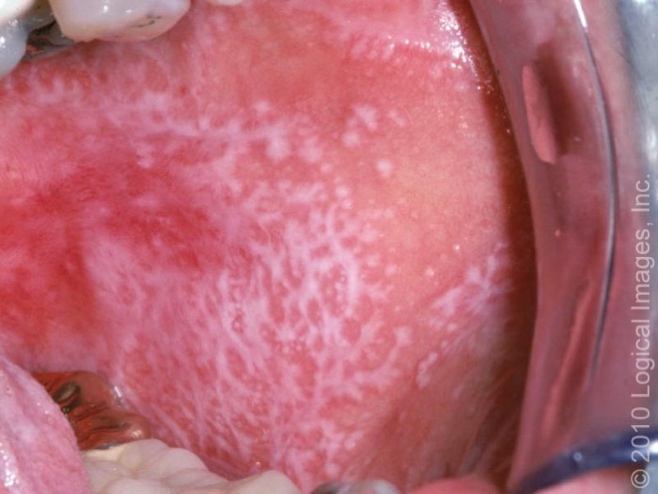
Oral lichen planus “Wickham striae”
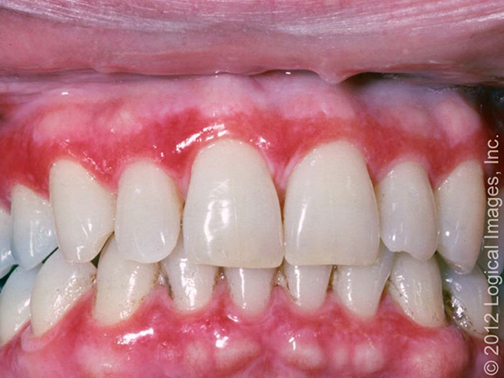
Desquamative gingivitis in oral lichen planus reference: www.visualdx.com
Violaceous, polygonal papules are present on the ventral wrists
2. Papulosquamous lichen planus (classic lichen planus)
รอยโรคจะมีลักษณะเป็น small, intensely pruritic papules โดยหลังจากที่รอยโรคเหล่านี้หายไป มักจะเกิด postinflammatory hyperpigmentation ตามมาได้
Violaceous, polygonal papules are present on the ventral wrists.
3. Hypertrophic lichen planus
เป็นชนิดของ lichen planus ที่พบได้น้อยมาก ลักษณะที่สำคัญคือ มีผิวหนังที่หนา นูน และหยาบมากขึ้น บริเวณ perineum และperianal เนื่องจากลักษณะของรอยโรคดังกล่าว คล้ายคลึงกับ vulvar intraepithelial neoplasia (VIN) , invasive squamous cell carcinoma รวมถึง hypertrophic vulvar lesions อื่นๆ จึงยากที่จะวินิจฉัยจากลักษณะของรอยโรคเพียงอย่างเดียว อาจจะต้องทำการส่งชิ้นเนื้อเพื่อตรวจเพิ่มเติ่ม เพื่อช่วยในการวินิจฉัย
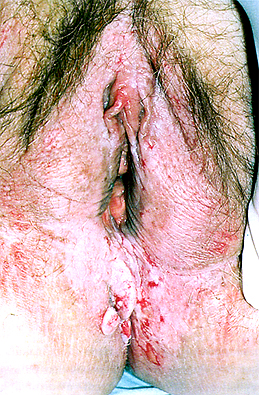
ภาพแสดง hypertrophic lichen planus reference: Ridley CM, Neill SM (Eds),
The Vulva, 2nd ed, Blackwell Science, Oxford 1999. Copyright © 1999 Blackwell Science. http://www.blackwell-science.com.
4. Lichen planopilaris
รอยโรคมักจะมีลักษณะเป็น perifollicular erythema, hyperkeratosis รวมถึง scarring alopecia โดยมากพบที่บริเวณหนังศีรษะ แต่อย่างไรก็ตามเคยมีรายงานที่พบรอยโรคลักษณะดังกล่าว บริเวณ labia majora และ mons pubis ได้เช่นกัน
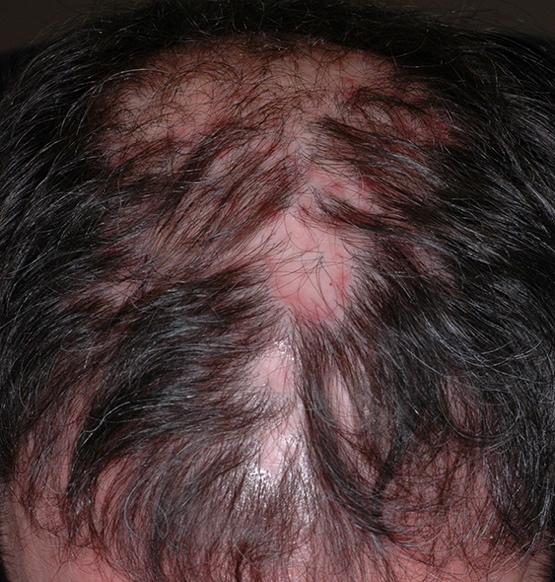
Active classic lichen planopilaris.
การวินิจฉัยโรค (Diagnosis)
ลักษณะทางคลินิก
Erosive lichen planus
- Erythematous erosion with a glazed appearance
- Wickham striae (white striae within involved areas or a serpentine white border)
Papulosquamous lichen planus
- Pruritic violaceous papules
- Postinflammation hyperpigmentation
Diagnostic criteria (International electronic Delphi consensus exercise) (13)
(สามารถช่วยในการวินิจฉัยผู้ป่วยประมาณร้อยละ 75 ที่เป็น lichen planus ได้ โดยจะต้องมีลักษณะดังต่อไปนี้ อย่างน้อย 3หรือ4 ข้อ ขึ้นไป)
- Presence of well-demarcated erosions or glazed erythema at the vaginal introitus
- Presence of a hyperkeratotic white border to erythematous areas or erosions ± Wickham striae in surrounding skin
- Symptoms of pain or burning
- Scarring or loss of normal architecture
- Presence of vaginal inflammation
- Involvement of other mucosal sites
- Presence of a well-defined inflammatory band in the superficial connective tissue that involves the dermoepidermal junction
- Presence of an inflammatory band that consists predominantly of lymphocytes
- Signs of basal cell layer degeneration (eg, Civatte bodies, abnormal keratinocytes, or basal apoptosis)
Biopsy
แนะนำให้ทำใน vulvar lichen planus โดยเฉพาะ erosion, hypertrophic form แต่อย่างไรก็ตาม หากลักษณะของรอยโรคเป็น papulosquamous lichen planus ชัดเจน กล่าวคือ small,violaceous, pruritic papules อาจจะไม่มีความจำเป็นต้องทำการส่งชิ้นเนื้อไปตรวจทางพยาธิวิทยา
Classic histologic features (14) ประกอบด้วย
- Irregular acanthosis of the epidermis (in sites of keratinized skin)
- Vacuolar change of the epidermal basal cell layer
- A band–like dermal infiltrate of lymphocytes in the upper dermis
- Apoptotic keratinocytes scattered within the epidermis
อย่างไรก็ตามลักษณะทางจุลพยาธิวิทยาข้างต้น อาจจะพบได้เพียงร้อยละ 70-80(14) ของผู้ป่วยเท่านั้น
Management (15)
1st line therapy
- Superpotent topical corticosteroid ointment เช่น clobetasol propionate 0.05% ointment or halobetasol propionate 0.05% ointment
ประเมินซ้ำที่ระยะเวลา 2 เดือน ว่าอาการดีขึ้นหรือไม่ หากไม่ พิจารณาเปลี่ยนเป็น systemic glucocorticoid แต่หากกรณีที่ใช้ topical steroid แล้วอาการของโรคดีขึ้น พิจารณาให้ maintainace therapy ต่อ เนื่องจากโรคอาจจะกลับมาเป็นซ้ำได้ง่ายหลังจากที่หยุดให้การรักษาไป
- Maintainance therapy คือการรักษาโดยใช้ potency ของsteroid ให้น้อยที่สุด dose ต่ำสุด ปริมาณน้อยที่สุดเพื่อคงประสิทธิภาพการรักษาโรคไว้ให้ได้ และลดผลข้างเคียงให้เกิดขึ้นน้อยที่สุด
2nd line therapy
- Topical tacrolimus (topical calcineurin inhibitor) จัดเป็น immunosuppressive drug โดยมากนิยมใช้ 0.03- 0.1% ointment วันเว้นวัน หรือบ่อยได้มากที่สุดถึง 2 ครั้งต่อวัน เนื่องจากการใช้ tacrolimus ทำให้เกิด burning sensation ได้มาก จึงแนะนำให้แช่น้ำทุกวันร่วมด้วยในช่วงสัปดาห์แรก หรือทา petrolatum / topical steroid ointment ก่อนที่จะทา tacrolimus ในช่วง 1-2 สัปดาห์แรก
Severe erosive lichen planus
- Oral prednisolone 40-60 มิลลิกรัมต่อวัน เป็นระยะเวลา 4-6 สัปดาห์
- Intramuscular triamcinolone มิลลิกรัมต่อกิโลกรัม เพียงครั้งเดียว หรือให้ทุก1 เดือน
- Intravaginal corticosteroids
- Prednisolone foam 20 มิลลิกรัม ก่อนนอน เป็นเวลา 6 สัปดาห์
- 10% hydrocortisone acetate 125 มิลลิกรัม ก่อนนอน เป็นเวลา 6 สัปดาห์
- Hydrocortisone suppositories 50-100 มิลลิกรัมก่อนนอน เป็นเวลา 14 วัน
Lichen sclerosus (5,16,17,18)
อุบัติการณ์ (Epidemiology)(16)
สามารถพบได้ในทุกช่วงอายุ แต่มักจะมีสองช่วงอายุที่พบได้บ่อย ได้แก่ pre pubertal girls และ perimenopausal/ postmenopausal woman สามารถพบได้ 1 ใน 30 ของผู้หญิงวัยกลางคน แต่ยังไม่ทราบอุบัติการณ์ที่แน่ชัดในเด็ก
สาเหตุ (Etiology)
สาเหตุการเกิดโรคยังไม่ทราบชัดเจน แต่เชื่อว่าเกี่ยวข้องกับปัจจัยต่างๆ ดังนี้ genetic factors, local vulvar factors, immunologic abnormality และ low estrogenic states เป็นต้น
อาการแสดง (Clinical presentation)
- Vulvar pruritus เป็นอาการแสดงที่สำคัญ และพบได้บ่อย
- Anal discomfort เนื่องจาก vulvar lichen sclerosis มักเกิดบริเวณ perianal skin ได้ ดังนั้นจึงทำให้เกิดอาการคันบริเวณรอบๆรูทวาร ท้องผูก ปวดเวลาแบ่งถ่าย เกิด anal fissure และมี rectal bleeding ตามมาได้
- Dyspareunia มักพบในกลุ่ม perimenopausal หรือpostmenopausal woman นอกจากนี้กระบวนการอักเสบของโรค อาจจะทำให้เกิด introital stenosis, fissures หรือ fused labial tissue ตามมาได้
- Dysuria อาการปวดเวลาปัสสาวะ มักมีได้ ในรายที่มีการ fusion of the labia minora over the urethra
Classic vulvar lichen sclerosus
ลักษณะของรอยโรคมักจะมีสีขาว atrophic papules มักจะเกิดที่บริเวณ labia minora, labia majora บางรายอาจจะลุกลามไปถึง perianal area ทำให้มีลักษณะเป็น “Keyhole fashion”
การเกาเพื่อบรรเทาอาการคันบริเวณอวัยวะเพศนั้น อาจจะทำให้เกิดการหลุดลอกของชั้นผิวหนัง (excoriations) จนทำให้เกิดชั้นผิวหนังที่หนาขึ้นตามมา (lichenification) รวมถึงอาจจะทำให้เกิดการบวมของบริเวณ labia minora และ prepuce ได้
ถ้าโรคเป็นมากขึ้น จะทำให้ vulva architecture เปลี่ยนแปลงไป โดยทำให้เกิดการเชื่อมกันของ labia majora และ labia minora clitoris จะถูกหุ้มด้วยlabia ที่เชื่อมติดกัน การหดตัวของบริเวณ introitus และperineum ทำให้เกิดอาการเจ็บเวลามีเพศสัมพันธ์ได้
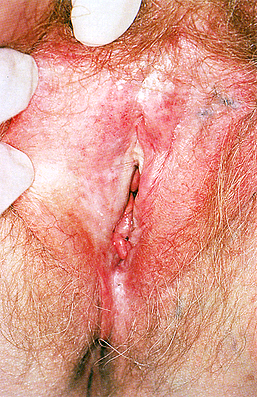
Vulvar lichen sclerosus
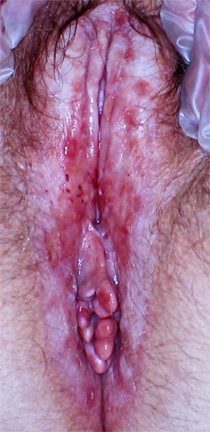
Severely itchy lichen sclerosus in a figure-of-eight pattern around vulva and perianal area with loss of clitoris and labia minora.
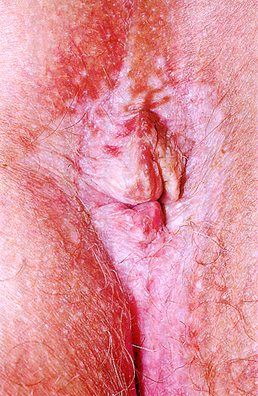
Perianal lichen sclerosus : Keyhole fashion
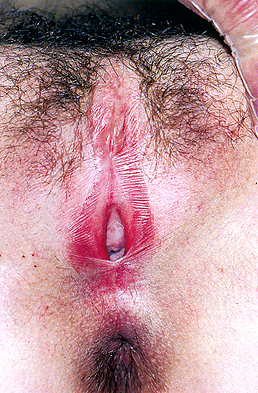
The distinction between labia majora and labia minora is lost and the clitoris becomes buried under the fused prepuce
ภาพอ้างอิงจาก from Ridley CM, Neill SM (Eds), The Vulva, 2nd ed, Blackwell Science, Oxford 1999. Copyright © 1999 Blackwell Science. และ F William Danby, MD, FRCPC, FAAD, and Lynne J Margesson, MD.
การวินิจฉัยโรค (Diagnosis)(17,18)
การวินิจฉัย นั้นสามารถทำได้โดยการดูลักษณะทางคลินิก แต่อย่างไรก็ตาม Gold standard ของการวินิจฉัย คือ ส่งชิ้นเนื้อเพื่อดูทางจุลชีววิทยา (histologic confirmation)
อ้างอิงจาก Evidence based guideline ของ European Academy of dermatology and venereology กล่าวว่า ไม่จำเป็นต้องทำการ biopsy ทุกรายเพื่อยืนยันการวินิจฉัย แต่อย่างไรก็ตาม การทำ biopsy ยังคงมีประโยชน์ในการช่วยวินิจฉัยในรายที่ไม่ตอบสนองต่อการรักษาด้วยยา หรือกรณีที่สงสัยmalignancy
แต่ในแนวทางการปฏิบัติในปัจจุบัน นิยมทำการ biopsy ในรายที่เป็น adult onset lichen sclerosus ตั้งแต่ครั้งแรกที่เริ่มวินิจฉัย เนื่องจากหากได้รับการรักษาด้วย topical steroid อาจจะทำให้หลักฐานทางจุลชีววิทยาขาดหายไป แต่สำหรับในเด็กนั้น จะทำการ biopsy ต่อเมื่อ มีลักษณะอาการผิดปกติหรือ เป็นโรคที่ไม่ตอบสนองต่อการรักษาด้วยยา
ผู้ป่วยที่เป็น Lichen sclerosus มีความเสี่ยงที่รอยโรคจะพัฒนาไปเป็น squamous cell cancer of vulva แต่อย่างไรก็ตาม โอกาสดังกล่าวนั้น มีน้อยกว่าร้อยละ 5
Management (17,18,19)
แนะนำให้ทำการรักษาผู้ป่วย lichen sclerosus ทุกราย แม้ในรายที่ไม่มีอาการ เพื่อป้องกันการดำเนินโรคที่อาจแย่ลงได้ในอนาคต โดยจุดประสงค์ของการรักษาคือ เพื่อรักษาอาการจากโรค ไม่ว่าจะเป็นอาการคัน หรือเจ็บ และรักษารอยโรค ได้แก่ hyperkeratosis, fissuring, ecchymoses
1st line therapy
1. Superpotent corticosteroid
- Clobetasol propionate 0.05% ointment
- Halobetasol proprionate 0.05% ointment
- ใช้ทาทุกวัน วันละ 1 ครั้งก่อนนอนในช่วง 4 สัปดาห์แรก หลังจากนั้น ค่อยๆลดความถี่เป็นวันเว้นวัน และ 2ครั้งต่อสัปดาห์ ตามลำดับ
- ระยะเวลา ประมาณ 6-12 สัปดาห์ หลังจากนั้นให้ค่อยๆลดระยะความถี่ลง (tapering)
2. Intralesional corticosteroids
- เหมาะสำหรับในรายที่มี thickened hypertrophic plaques ที่ไม่ค่อยตอบสนองต่อ topical steroid
2nd line therapy
- Topical calcineurin inhibitors (Tacrolimus) 2 ครั้งต่อวัน เป็นเวลาประมาณ 3 เดือน โดยแนะนำให้นัดติดตามอาการอย่างน้อย 1 ครั้งต่อปี
Vulvar intraepithelial disease
Vulva Intraepithelial Neoplasia (VIN) (2,20)
คือ premalignant conditions of vulva
อุบัติการณ์ (Epidemiology)(21)
พบใน premenopausal มากกว่า post-menopausal woman อายุเฉลี่ยประมาณ 46 ปี
โดย risk factors ที่สำคัญสำหรับ vulva HSIL ได้แก่
- Human papilloma virus (HPV) จากการศึกษาอ้างว่า ร้อยละ 90 ของ VIN นั้นสัมพันธ์กับการติดเชื้อ HPV โดย low grade SIL มักจะสัมพันธ์กับ low risk HPV subtypes (6 และ 11) และ HSIL มักจะสัมพันธ์กับ high risk type (16,18 และ 31)
- Cigarette smoking เชื่อว่าการสูบบุหรี่นั้น สัมพันธ์กับการพัฒนาไปเป็น vulvar SIL แต่ยังไม่ทราบกลไกที่ชัดเจน
- Immunodeficiency vulvar SILs มักจะพบในผู้ป่วยติดเชื้อ HIVs มากกว่าประชากรทั่วไป
สำหรับผู้ป่วย VIN กลุ่ม premenopausal woman มักจะเป็น HPV-associated vulvar HSIL แต่สำหรับกลุ่ม postmenopausal woman นั้นมักจะเป็น non-HPV associated vulvar SIL มากกว่า
คำจำกัดความ (Terminology) (20)
อ้างอิงจาก 2015 Terminology for vulva SILs
- Low-grade squamous intraepithelial lesion (LSIL) of vulva (vulva LSIL, flat condyloma or human papillomavirus [HPV] effect); previously called “VIN1”
- High-grade squamous intraepithelial lesion (HSIL) of the vulva (vulva HSIL, VIN usual type [uVIN]); previously called “VIN2, VIN3”
- Differentiated VIN (dVIN) มักไม่สัมพันธ์กับ HPV แต่มักจะสัมพันธ์กับ vulva dermatoses โดยเฉพาะ lichen sclerosus
ในอดีต VIN เคยถูกแบ่งออกเป็น 3 ระดับ(2) ตาม cellular maturity, nuclear abnormalities, maturation disturbance และ mitotic activity ดังนี้
Grade 1 (mild)
- Immature cells
- Cellular disorganization
- Mitotic activity
Grade 2 (moderate)
- Intermediate between VIN1 and VIN3
Grade 3 (severe or CIS)
- Immature cells with scantly cytoplasm and severe chromatinic alterations occupy most of the epithelium.
- Dyskeratotic cells and mitotic figures occur in superficial layer.
- ** Neoplastic precursor and can be unifocal or multifocal.
โดยมาก multifocal VIN 3 มักจะมาด้วย small hyperpigmented lesions on labia majora
สำหรับ cytopathic changes of HPV infection(2) ประกอบด้วย perinuclear halo with displacement of nuclei by the intracytoplasmic viral protein, thickened cell borders, binucleation and multinucleation มักจะพบใน superficial layer ของ VIN1, VIN2 อย่างไรก็ตามการเปลี่ยนแปลงเหล่านี้ ไม่ได้บ่งบอกถึงการเปลี่ยนแปลงเป็น neoplasia แต่เป็นเพียงสิ่งที่บอกถึง viral exposure เท่านั้น โดยผู้ป่วยที่วินิจฉัย VIN นั้นสัมพันธ์กับ HPV-16 มากถึงร้อยละ 80
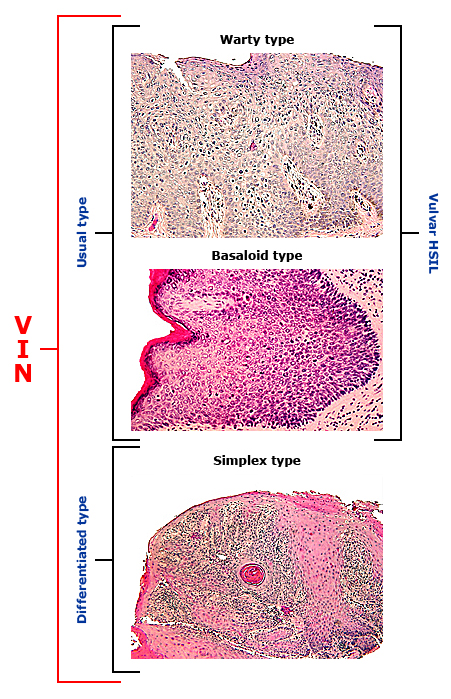
Histopathologic pictures (20)
กลไกการเกิด (Pathogenesis)
เนื่องจาก anogenital epithelium นั้นถูกพัฒนามาจาก embryonic cloaca ที่ประกอบไปด้วย cervix, vagina, vulva, anus และ 3 cm ของ rectal mucosa เหนือต่อ dentate line ดังนั้นเนื้อเยื่อเหล่านี้จึงเปราะบางต่อปัจจัยภายนอกชนิดเดียวกัน โดยเฉพาะอย่างยิ่ง HPV
SILs ในบริเวณเหล่านี้ จะสามารถเกิดได้ 2 แบบ ได้แก่ multifocal (multiple foci of disease within the same organ) และ multicentric (foci of disease involving more than one organ)
สำหรับกลไกการเกิดของ differentiated VIN (dVIN) ยังไม่ทราบแน่ชัด แต่มักจะเป็น unifocal และ unicentric มักจะสัมพันธ์กับ lichen sclerosus ไม่สัมพันธ์กับ HPV infection
อาการแสดง (Clinical presentation)
มักจะไม่มีอาการ (asymptpmatic) หรือ มีอาการดังต่อไปนี้
- Vulvar pruritus: เป็นอาการที่พบได้บ่อยที่สุด อาการอื่นๆที่พบได้เช่นกัน ได้แก่ vulvar pain, burning, dysuria
- Vulvar lesion: มักจะเป็น multifocal และมักจะบริเวณ nonhairy part of vulva ลักษณะรอยโรคไม่ได้มี pathognomonic sign ชัดเจน แต่มักจะยกนูน สีขาว หรือสีอื่นๆ ได้แก่ แดง, ชมพู, เทา หรือน้ำตาล
- Persistent abnormal cervical pathology with no abnormality identified on cervical biopsy
การวินิจฉัยโรค (Diagnosis)(20)
สามารถวินิจฉัยได้จากลักษณะของ histopathology ดังนี้
LSIL of vulva
- Cytologic atypia is most often represented by koilocytosis or basal cell hyperplasia and increased mitotic activity, with squamous maturation occurring in the upper two-third of the epithelium.
HSIL of vulva
- Loss of maturation includes the middle (formerly VIN2) and upper third to full thickness (formerly VIN3) of the squamous epithelium.
- Cytologic changes may be significant with bizarre mitotic figures and significant pleomorphism.
- Stromal invasion is not present.
dVIN
- Differentiated VIN lesions affect the parabasal layer and exhibit keratin formation. The epithelium is generally thickened and parakeratotic with elongated and anastomosing rete ridges.
- The abnormal cells have prominent eosinophilic cytoplasm and are confined to the parabasal and basal portion of the rete pegs with little or no atypia above.
Adapted from: Bornstein J, Bogliatto F, Haefner HK, et al. The 2015 International Society for the Study of Vulvovaginal Disease (ISSVD) Terminology of Vulvar Squamous Intraepithelial Lesions. J Low Genit Tract Dis 2016; 20:11.
Management (2,22)
Vulvar LSILs
- ไม่ถือว่าเป็น precancerous lesion แต่มักจะสัมพันธ์กับ HPV lesion
- เทียบเท่ากับ condyloma acuminata
- รักษาเหมือนกันกับ genital warts
Vulvar HSILs
- Wide excision
- Alternative treatment:
- simple excision
- laser ablation
- superficial or skinning vulvectomy with or without skin grafting;
จุดประสงค์ของการผ่าตัดคือ ป้องกันไม่ให้เกิดการพัฒนาเปลี่ยนแปลงไปเป็น vulvar squamous carcinomaกำจัดรอยโรคออกไปให้มากที่สุด ในขณะที่ต้องรักษา normal vulvar anatomy ให้ได้มากที่สุดเช่นกัน
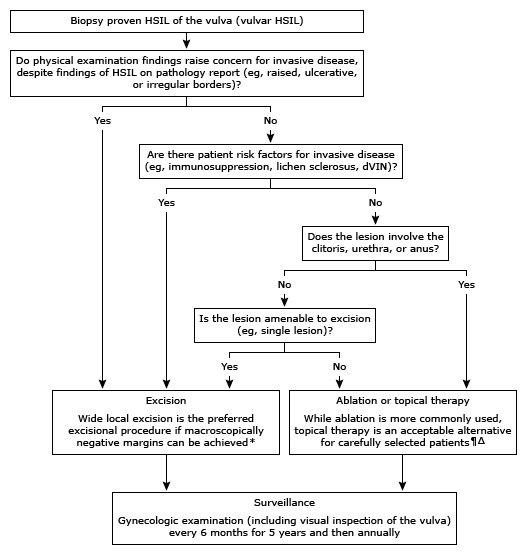
Paget disease (2,5)
Extramammary Paget disease
เป็น intraepithelial adenocarcinoma ที่พบได้น้อยกว่าร้อยละ 1 ในมะเร็งปากช่องคลอด ผู้ป่วยส่วนมากจะอยู่ในช่วงอายุ 60-70 ปี
อาการนำที่สำคัญสำหรับ paget disease มากถึงร้อยละ 70 จะมาด้วยอาการคันบริเวณปากช่องคลอด ลักษณะของรอยโรคจะคล้ายกับที่บริเวณเต้านม เป็นลักษณะของ eczematoid appearance กล่าวคือ มีขอบเขตชัดเจน ขอบยกนูน มักจะมีจุดสีขาวขนาดแตกต่างกันบนพื้นสีแดง
มักพบได้ตั้งแต่บริเวณ vulva, mons, perineum/ perianal area และ inner thigh สามารถพบ underlying invasive adenocarcinoma ร่วมด้วยได้มากถึงร้อยละ 25 นอกจากนี้ในผู้ป่วย paget disease อาจจะพบมะเร็งอื่นร่วมด้วย อีกประมาณ ร้อยละ20-30 ได้แก่ มะเร็งเต้านม, มะเร็งลำไส้ตรง, มะเร็งกระเพาะปัสสาวะและท่อปัสสาวะ, มะเร็งปากมดลูกและ มะเร็งรังไข่
ดังนั้นควรทำการสืบค้นเพิ่มเติมเพื่อหาความผิดปกติของอวัยวะดังกล่าว ด้วยการทำเอกซเรย์คอมพิวเตอร์บริเวณช่องท้อง และอุ้งเชิงกราน การตรวจคัดกรองมะเร็งปากมดลูก และเอกซเรย์เต้านม รวมถึงการตรวจ cystoscopy และ colonoscopy กรณีที่โรคลุกลามเข้าไปบริเวณท่อปัสสาวะ หรือทวารหนัก
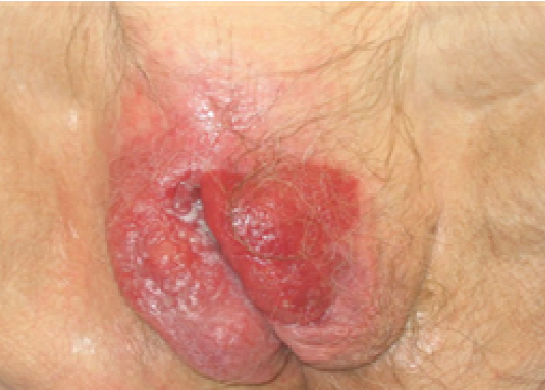
Extramammary Paget’s disease Reference:
www.wikipedia.com
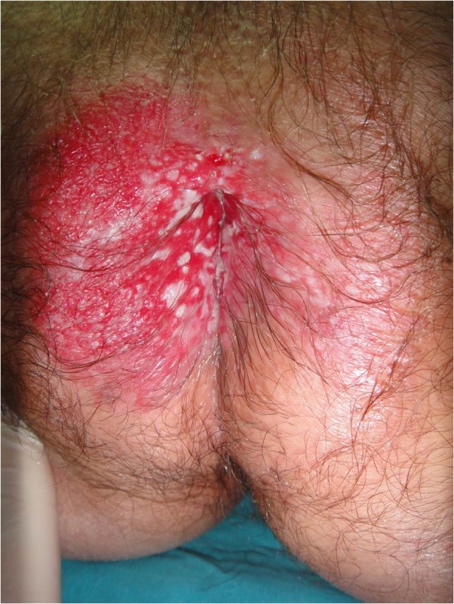
Perianal Paget’s disease Reference:
www.researchgate.net
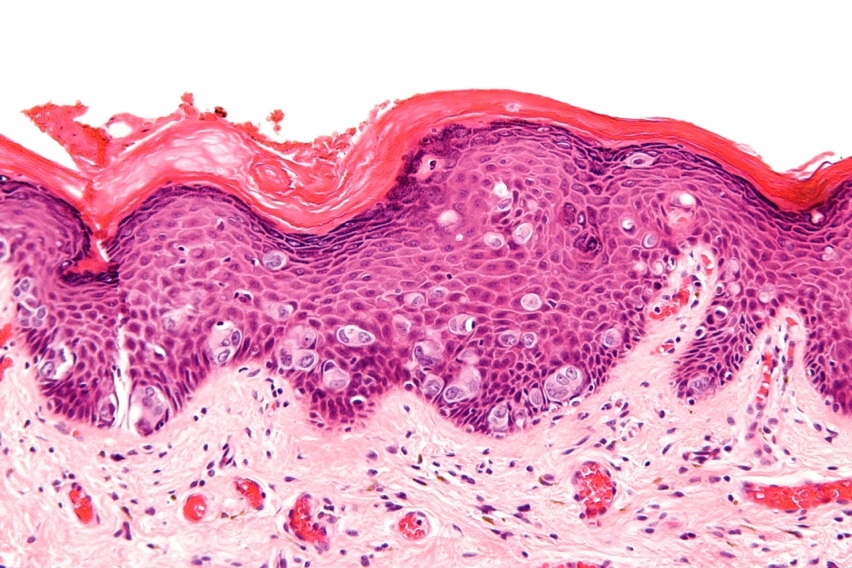
ลักษณะของ histopathology of Paget’s disease Reference: www.wikipedia.com
Behcet’s disease (23,24)
เป็นโรคที่มีการอักเสบเรื้อรังของอวัยวะหลายระบบ ที่ยังไม่ทราบสาเหตุแน่ชัด แต่เชื่อว่าเกิดจากการอักเสบของหลอดเลือด(vasculitis) โดยสามารถกระทบหลอดเลือดทั้งขนาดเล็ก กลาง และใหญ่ มักพบได้บ่อยบริเวณแถบเอเชียตะวันออก ถึงแถบเมดิเตอร์เรเนียน พบได้มากที่สุดที่ประเทศตุรกี มากถึง 80 ถึง 370 รายต่อประชากร 100,000 ราย
อาการแสดงที่สำคัญมักจะเป็น recurrent painful mucocutaneous ulcers เช่น oral ulcerations, urogenital lesions, cutaneous lesions นอกจากนี้ยังมีผลกระทบต่อหลายระบบ ไม่ว่าจะเป็น ocular disease, neurologic disease, vascular disease, pulmonary disease, arthritis, renal disease, cardiac disease และ GI involvement
สำหรับ urogenital lesions เป็นรอยโรคที่ค่อนข้างเฉพาะกับ Behcet’s disease พบได้มากกว่าหรือเท่ากับร้อยละ 75 ในผู้ป่วย Behcet’s disease ทั้งหมด ลักษณะรอยโรคที่พบ จะมีลักษณะคล้าย oral aphthae และเป็น painful lesion โดยรอยโรคมักจะพบที่บริเวณ scrotum ในเพศชาย และบริเวณ vulva ในเพศหญิง
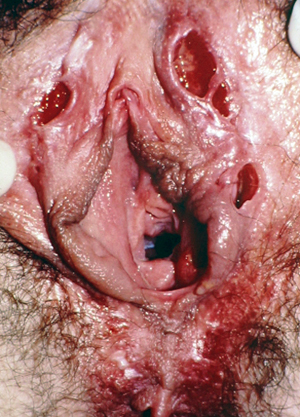
Reference: Lynne J Margesson, MD.
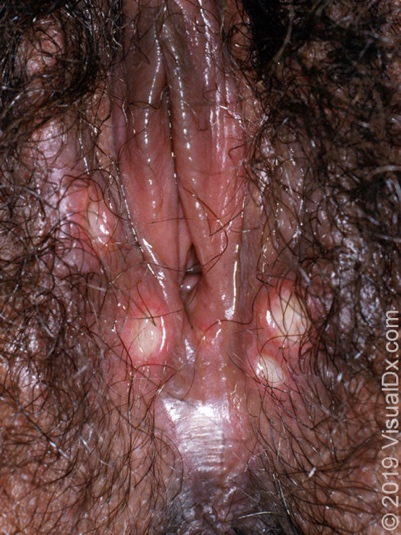
Reference: www.visualdx.com
เอกสารอ้างอิง
- ธีระ ทองสง.นรีเวชวิทยาฉบับสอบบอร์ด .พิมพ์ครั้งที่ 4. เชียงใหม่: ภาควิชาสูติศาสตร์และนรีเวชวิทยา คณะแพทยศาสตร์ มหาวิทยาลัยเชียงใหม่; 2559.
- S.Berek J. Berek & Novak’s Gynecology 16 ed: Wolters Kluwer 2020.
- Association TNV. Vulvar Anatomy: The National Vulvodynia Association; 2020 [Available from: https://www.nva.org/what-is-vulvodynia/vulvar-anatomy/.]
- Lynette J Margesson MD. Vulvar lesions: Differential diagnosis based on morphology.Post TW,ed.UpToDate.Waltham,MA: UpTpDate Inc. http://www.uptodate.com (Accessed on October 10, 2020.)
- manopunya M. vulvar and vaginal lesions. Faculty of medicine, Chiang Mai university 2020.
- Pichardo-Geisinger R. Atopic and Contact Dermatitis of the Vulva. Obstet Gynecol Clin North Am. 2017;44(3):371-8.
- Ball SB, Wojnarowska F. Vulvar dermatoses: lichen sclerosus, lichen planus, and vulval dermatitis/lichen simplex chronicus. Semin Cutan Med Surg. 1998 Sep;17(3):182-8. doi: 10.1016/s1085-5629(98)80012-6.
- Kennedy CM, Galask RP. Erosive vulvar lichen planus: retrospective review of characteristics and outcomes in 113 patients seen in a vulvar specialty clinic. J Reprod Med. 2007 Jan;52(1):43-7.
- Cooper SM, Wojnarowska F. Influence of treatment of erosive lichen planus of the vulva on its prognosis. Arch Dermatol. 2006 Mar;142(3):289-94.
- Cooper SM, Haefner HK, Abrahams-Gessel S, Margesson LJ. Vulvovaginal lichen planus treatment: a survey of current practices. Arch Dermatol. 2008 Nov;144(11):1520-1.
- Simpson RC, Thomas KS, Leighton P, Murphy R. Diagnostic criteria for erosive lichen planus affecting the vulva: an international electronic-Delphi consensus exercise. Br J Dermatol. 2013;169(2):337-43.
- Zendell K, Edwards L. Lichen sclerosus with vaginal involvement: report of 2 cases and review of the literature. JAMA Dermatol. 2013 Oct;149(10):1199-202.
- Simpson RC, Thomas KS, Leighton P, Murphy R. Diagnostic criteria for erosive lichen planus affecting the vulva: an international electronic-Delphi consensus exercise. Br J Dermatol. 2013 Aug;169(2):337-43.
- Belfiore P, Di Fede O, Cabibi D, Campisi G, Amarù GS, De Cantis S, Maresi E. Prevalence of vulval lichen planus in a cohort of women with oral lichen planus: an interdisciplinary study. Br J Dermatol. 2006 Nov;155(5):994-8.
- Bradford J, Fischer G. Management of vulvovaginal lichen planus: a new approach. J Low Genit Tract Dis. 2013 Jan;17(1):28-32.
- Bleeker MC, Visser PJ, Overbeek LI, van Beurden M, Berkhof J. Lichen Sclerosus: Incidence and Risk of Vulvar Squamous Cell Carcinoma. Cancer Epidemiol Biomarkers Prev. 2016 Aug;25(8):1224-30.
- Pérez-López FR, Ceausu I, Depypere H, Erel CT, Lambrinoudaki I, Rees M, et al. EMAS clinical guide: Vulvar lichen sclerosus in peri and postmenopausal women. Maturitas. 2013;74(3):279-82.
- Funaro D. Lichen sclerosus: a review and practical approach. Dermatol Ther. 2004;17(1):28-37. doi: 10.1111/j.1396-0296.2004.04004.x. PMID: 14756888.
- Kirtschig G, Becker K, Günthert A, Jasaitiene D, Cooper S, Chi CC, Kreuter A, Rall KK, Aberer W, Riechardt S, Casabona F, Powell J, Brackenbury F, Erdmann R, Lazzeri M, Barbagli G, Wojnarowska F. Evidence-based (S3) Guideline on (anogenital) Lichen sclerosus. J Eur Acad Dermatol Venereol. 2015 Oct;29(10):e1-43.
- Bornstein J, Bogliatto F, Haefner HK, Stockdale CK, Preti M, Bohl TG, Reutter J; ISSVD Terminology Committee. The 2015 International Society for the Study of Vulvovaginal Disease (ISSVD) Terminology of Vulvar Squamous Intraepithelial Lesions. J Low Genit Tract Dis. 2016 Jan;20(1):11-4.
- van de Nieuwenhof HP, van der Avoort IA, de Hullu JA. Review of squamous premalignant vulvar lesions. Crit Rev Oncol Hematol. 2008 Nov;68(2):131-56.
- Committee on Gynecologic Practice of American College Obstetricians and Gynecologists. ACOG Committee Opinion No. 509: Management of vulvar intraepithelial neoplasia. Obstet Gynecol. 2011 Nov;118(5):1192-4.
- Yazici H, Fresko I, Yurdakul S. Behçet’s syndrome: disease manifestations, management, and advances in treatment. Nat Clin Pract Rheumatol. 2007 Mar;3(3):148-55.
- Criteria for diagnosis of Behçet’s disease. International Study Group for Behçet’s Disease. Lancet. 1990 May 5;335(8697):1078-80.