Combined oral contraceptive pills (COC)
Combined oral contraceptive pills (COC): ยาเม็ดคุมกำเนิดแบบฮอร์โมนรวม
พญ. อมราพร จันทร์กระจ่าง
อาจารย์ที่ปรึกษา ศ.พญ. สายพิณ พงษธา
ยาเม็ดคุมกำเนิดแบบฮอร์โมนรวม ประกอบไปด้วยฮอร์โมน estrogen และ progestin เป็นหนึ่งในวิธีการคุมกำเนิดแบบชั่วคราวที่ใช้กันอย่างแพร่หลาย และเป็นที่นิยมในปัจจุบัน เนื่องจากหาซื้อได้ง่ายและราคาถูก
ประสิทธิภาพในการคุมกำเนิด ขึ้นอยู่กับความสม่ำเสมอในการรับประทานยา โดยพบว่า ผู้หญิงที่ใช้ COC เป็นเวลา 1 ปี พบอัตราการตั้งครรภ์ได้ ประมาณ 9 ใน 100 คน
กลไกการออกฤทธิ์ของ COC
- ยับยั้งการตกไข่ เนื่องจาก estrogen ยับยั้งการหลั่ง follicle stimulating hormone (FSH) ทำให้กดการเจริญของ follicle และ progestin ยับยั้งการหลั่ง luteinizing hormone (LH) ทำให้ไม่มี LH surge จึงไม่เกิดการตกไข่ หากออกฤทธิ์คู่กันจะสามารถยับยั้งการหลั่ง GnRH จาก hypothalamus ได้
- Progestin ทำให้เยื่อบุโพรงมดลูกไม่เหมาะสมแก่การฝังตัวของตัวอ่อน
- Progestin ทำให้มูกบริเวณปากมดลูกข้นเหนียวและทำให้อสุจิผ่านได้ยาก
- Progestin ทำให้ท่อนำไข่เคลื่อนไหวผิดปกติ ซึ่งทำให้ไข่เคลื่อนผ่านได้ยาก
Estrogen ในร่างกาย มี 4 ชนิด ได้แก่
| Estrogen | Production | Process | Potency | Half life |
| E1 (Estrone) | non pregnant woman | peripheral aromatization of androstenedione | 1/10 x of E2 | 10-70 min |
| E2 (Estradiol) | non pregnant woman | ovary, adrenal gland | most potent | 1-2 hrs (17-beta),
10-12 hrs (micronized) |
| E3 (Estriol) | pregnant woman | fetus/placenta | 1/100 x of E2 | 10 – 20 min |
| E4 (Estetrol) | fetal liver in pregnant woman | fetal liver | 1/10 x of E2 | 20 – 28 hrs |
ที่มา: Hugh S. Taylor, Patricia Geraghty, The next generation of oral contraception: Advances in estrogens: OBG management
เนื่องจาก estradiol มี potency มากที่สุด จึงได้รับความนิยม มีการผลิตเป็น hormone สังเคราะห์แบบต่างๆ เช่น mestranol, ethinyl estradiol, estradiol valerate เป็นต้น
Estrogen ที่นิยมใช้ในยาคุมกำเนิดในปัจจุบัน คือ ethinyl estradiol และในปัจจุบัน มีการใช้ estrogen ตัวใหม่ คือ estetrol หรือ E4 ซึ่งมีข้อดีคือ มีการเลือกออกฤทธิ์จําเพาะตามเนื้อเยื่ออวัยวะต่าง ๆ (Natural Estrogen with Selective Tissue activity : NEST) ซึ่งส่งผลดีต่อช่องคลอด เยื่อบุโพรงมดลูก กระดูก และระบบไหลเวียนโลหิต และส่งผลเสียน้อยต่อตับและเต้านม หรือมะเร็งเต้านม นอกจากนี้ยังไม่ค่อยมี drug interaction กับยาในกลุ่มที่ผ่านตับที่เกี่ยวข้องกับ cytochrome 450 enzymes อีกด้วย
Progestin มี 4 generations ได้แก่
| First generation | Estranes derived from testosterone norethindrone, norethynodrel, norethindrone acetate, ethynodiol diacetate
Pregnanes derived from 17-OH progesterone |
| Second generation | Gonanes derived from testosterone levonorgestrel, norgestrel |
| Third generation | Gonane (Levonorgestrel) derivatives desogestrel, gestodene, norgestimate/norelgestromine, etonorgestrel |
| Fourth generation |
Non ethylated estranes dienogest, drospirenone Pregnanes (19-norprogesterones) nestorone, nomegestrol acetate, trimegestone |
ที่มา : Taylor HS, Fritz MA, Pal L, Seli E. Speroff’s clinical gynecologic and endocrinology and infertility. Ninth edition ed. Philadelphia, PA: Wolters Kluwer Philadelphia, PA; 2020.
Progestin รุ่นหลังๆ จะถูกพัฒนาให้ลด androgenicity ของ progestin ทำให้เพิ่ม SHBG และลด free testosterone ทำให้ช่วยลดการเกิดสิวและขนดกได้ดีกว่ารุ่นก่อน โดย progestin บางชนิดจะมีฤทธิ์ anti androgenic effect เช่น drospirenone เป็นต้น
ชนิดของยาคุมกำเนิดชนิดฮอร์โมนรวม
COC มี 2 กลุ่ม ได้แก่ monophasic และ multiphasic pills
Monophasic pills คือ มีปริมาณฮอร์โมน estrogen + progestin ในปริมาณเท่ากันทุกเม็ดหรือมีระดับยาเป็นเป็นระดับเดียวกันในหนึ่งแผง
แบ่งตามปริมาณของ estrogen ซึ่งเป็น ethinyl estradiol (EE) เป็นดังนี้
very low dose EE 15-20 mcg
low dose EE 30-35 mcg
high dose EE > 50 mcg
Multiphasic pills คือ มีปริมาณฮอร์โมนแตกต่างกันเป็นหลายระดับในหนึ่งแผง เช่น 2 ,3 และ 4 ระดับ ใน biphasic, triphasicและ quadriphasic pills ตามลำดับ ฮอร์โมนที่แตกต่างกันเป็นได้ทั้ง estrogen, progestin หรือทั้งคู่ก็ได้ การทำแบบนี้เพื่อให้ระดับฮอร์โมนใกล้เคียงธรรมชาติที่สุด
ตัวอย่างยี่ห้อ COC ที่มีในประเทศไทย
Monophasic pills
| EE | Progestin | Trade name | Active pills |
| 15 mcg | Gestodene 0.06 mg | Minidoz
Minoz |
24 |
| 20 mcg | Gestodene 0.075 mg | Meliane
Onjel 20 Lindynette 20 Annylyn Ciclomex20 |
21 |
| 20 mcg | Desogestrel 0.15 mg | Mercilon Minny
Novynette |
21 |
| 20 mcg | Drospirenone3 mg | Yaz
Herz Synfonia |
24 |
| 30 mcg | LNG 0.15 mg | Anna
Milly R-Den Zarine Microgest Microgynon Microlenyn Cleo Oralcon-F Nordette |
21 |
| 30 mcg | Norgestrel 0.15 mg | Dior
Rigevidon |
21 |
| 30 mcg | Gestodene 0.075 mg | Gynera
Govana Lindynette 30 |
21 |
| 30 mcg | Desogestrel 0.15 mg | Marvelon Daisy
Femine 30 |
21 |
| 30 mcg | Clomadione acetate 2 mg | Belara
Chariva |
21 |
| 30 mcg | Drospirenone 3 mg | Yasmin
Justima Melodia Gveza |
21 |
| 35 mcg | Ciproterone acetate 2 mg | Diane 35 Sucee
Preme Manoane Annie Cypress Helen LadyE35 Sasha B-Lady |
21 |
| 35 mcg | Norgestimate 0.25 mg | Cilest | 21 |
| Estetrol | Progestin | Trade name | Active pills |
| 15 mg | Drospirenone 3 mg | Nextstellis | 24 |
Biphasic pills
Oillezz (22 active pills)
| First | 7 tabs | EE 40 mcg | Desogestrel 0.025 mg |
| Second | 15 tabs | EE 30 mcg | Desogestrel 0.125 mg |
Triphasic pills
Tricilest (21 active pills)
| First | 7 tabs | EE 35 mcg | Norgestimate 0.18 mg |
| Second | 7 tabs | EE 35 mcg | Norgestimate 0.215 mg |
| Third | 7 tabs | EE 35 mcg | Norgestimate 0.25 mg |
Triquilar ED / Trigestrel (21 active pills)
| First | 6 tabs | EE 30 mcg | Levonorgestrel 0.05 mg |
| Second | 5 tabs | EE 40 mcg | Levonorgestrel 0.075 mg |
| Third | 10 tabs | EE 30 mcg | Levonorgestrel 0.125 mg |
Quadriphasic pills
Qlaira (26 active pills)
| First | 2 tabs | EV 3 mg | Dinogest 0 |
| Second | 5 tabs | EV 2 mg | Dinogest 2 mg |
| Third | 17 tabs | EV 2 mg | Dinogest 3 mg |
| Fourth | 2 tabs | EV 1 mg | Dinogest 0 |
EV : estradiol valerate
รูปแบบการรับประทานยา
มีหลายรูปแบบ ได้แก่ 21/7, 24/4, extended cycle และ continuous cycle
ในยา 1 แผง อาจมี 21 เม็ด 24 เม็ด หรือ 28 เม็ด หากเป็นแบบ 21 เม็ด ให้รับประทานวันละ 1 เม็ด เป็นระยะเวลา 3 สัปดาห์และหยุด 1 สัปดาห์ เพื่อให้มีประจำเดือนออกมาเป็นปกติ (withdrawal uterine bleeding) หากเป็นแบบ 28 เม็ด ให้รับประทานติดต่อกันทุกวันเพื่อป้องกันการหลงลืม ซึ่ง 7 เม็ดสุดท้ายจะไม่มีฮอร์โมน อาจเป็นแป้ง วิตามิน หรือธาตุเหล็กแทน (Pill free interval)
ในแผง 28 เม็ด จะมี 2 regimen คือ แบบ 21/7 และ 24/4 โดย จะมีเม็ดที่เป็น active pills 21 และ 24 เม็ดตามลำดับ ซึ่งเม็ดที่เหลือจะเป็นเม็ดแป้ง
21/7 เปรียบเทียบกับ 24/4 regimen คือ 24/4 จะมีช่วงที่มี active pills มากกว่า จะทำมาใน low หรือ very low dose COC เพื่อเพิ่มประสิทธิภาพในการคุมกำเนิดเนื่องจากลด follicular development และลดผลข้างเคียงเลือดออกกะปริบกะปรอย
รูปแบบอื่นๆ ในการรับประทาน เช่น
Extended cycle คือ รับประทาน active pills ต่อเนื่อง 3 เดือน และเว้นให้มีประจำเดือน 1 สัปดาห์
Continuous cycle คือ รับประทาน active pills ต่อเนื่อง 1 ปี หรือมากกว่านั้น
การใช้แบบ extended cycle หรือ continuous cycle เหมาะกับผู้ป่วยที่มีอาการปวดท้องน้อยเรื้อรัง หรือ มีอาการปวดระหว่างรอบเดือนที่ใช้ยาแบบ 28-day cycleแล้วอาการไม่ดีขึ้นหรือยังไม่พึงพอใจ
ข้อดีอื่นๆ ของ COC นอกจากการคุมกำเนิด
ได้แก่ ลดความเสี่ยงในการเป็นมะเร็งเยื่อบุโพรงมดลูก มะเร็งรังไข่ และมะเร็งลำไส้ ช่วยความคุมรอบประจำเดือน ลดปริมาณเลือดประจำเดือน ลดปวดประจำเดือน จึงมีการใช้ COC ในการรักษา endometriosis, dysfunctional uterine bleeding, dysmenorrhea, Mittelschmerz, hypothalamic amenorrhea และอาจช่วยรักษาภาวะ premenstrual syndrome และลดการเกิด functional cyst ได้ นอกจากนี้ยังช่วยเพิ่ม bone density และอาจช่วยลดการเกิด atherosclerosis ได้
หลักการรับประทาน COC ตามแนวทางของ US Selected Practice recommendations for Contraceptive Use, 2016
หญิงทั่วไป : เริ่มวันที่1-5 ของประจำเดือน ถ้าเริ่มวันที่มากกว่า 5 จำเป็นต้อง back up method เช่น งดมีเพศสัมพันธ์ หรือใช้ถุงยางอนามัย เป็นเวลาอีก 1 สัปดาห์
กรณีขาดประจำเดือน (ไม่ใช่หลังคลอด) : สามารถเริ่มได้เลยร่วมกับ back up method 1 อาทิตย์
กรณีหลังคลอด (ให้นมบุตร) : ไม่ควรใช้ในช่วง 4-6 สัปดาห์หลังคลอด เนื่องจากผลข้างเคียงการเกิดลิ่มเลือดอุดตัน และกระทบการหลั่งน้ำนม
กรณีหลังแท้ง : สามารถเริ่มภายใน 7 วันแรกหลังแท้งร่วมกับ back up method 1 สัปดาห์ ยกเว้นเริ่มทันทีหลังการแท้งไม่ต้อง back up method
เมื่อเปลี่ยนจากการคุมกำเนิดแบบอื่นมาเป็น COC
Intrauterine device (IUD) ควรเอาออกหลังจากเริ่มยาแล้ว 7 วันหรือ back up method 1 สัปดาห์
ในกรณีที่ใช้ยาคุมกำเนิดฉุกเฉิน สามารถเริ่มใช้ COC ต่อได้เลย ยกเว้น กรณีที่ยาคุมฉุกเฉินมี UPA (Ulipristal acetate) ควรเริ่มหลังใช้ยาคุมฉุกเฉินมี UPA ไปแล้วอย่างน้อย 5 วัน
การคัดกรองก่อนเริ่ม COC
- CDC แนะนำว่าก่อนเริ่มรับประทานยา ควรมีการตรวจคัดกรองความดันโลหิต
- Genetic testing for VTE
โรค inherited clotting disorder ที่พบได้บ่อยคือ factor V leiden mutation ซึ่งถ่ายทอดแบบ Autosomal dominant ทั้งนี้อุบัติการณ์ในคนเชื้อสายเอเชียพบได้น้อยมาก อาจพิจารณาตรวจแค่ในกลุ่มที่มีประวัติครอบครัวเป็น VTE หรือ เคยมีประวัติ VTE มาก่อน
คำถามที่พบบ่อย ถ้าใช้ COC ขณะตั้งครรภ์ ทารกจะผิดปกติไหม ?
COC ไม่เพิ่มความเสี่ยงความผิดปกติโดยกำเนิดของทารก โดยพบทารกที่มีความผิดปกติได้ 2-3 % เท่ากับ ความเสี่ยงโดยทั่วไปของผู้ที่ไม่ได้ใช้ COC ดังนั้น หากทราบว่าตั้งครรภ์ขณะใช้ COC สามารถหยุดยา แล้วฝากครรภ์ต่อตามปกติ
Flowchart กรณีลืมรับประทาน COC
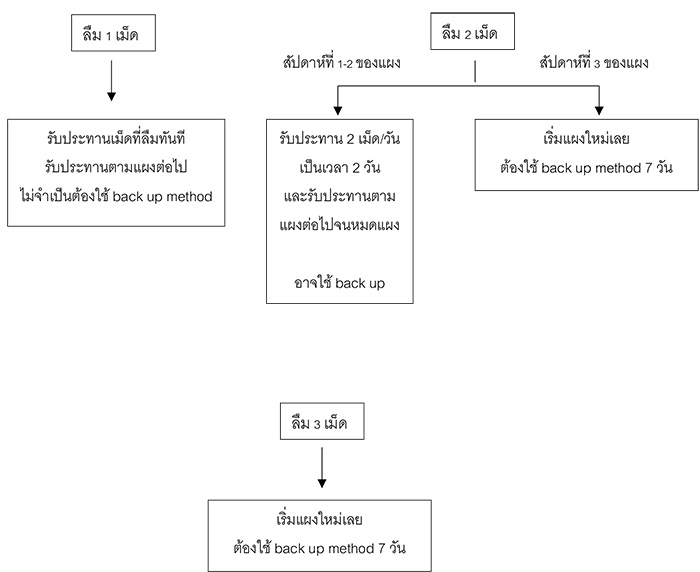
ที่มา: Taylor HS, Fritz MA, Pal L, Seli E. Speroff’s clinical gynecologic and endocrinology and infertility. Ninth edition ed. Philadelphia, PA: Wolters Kluwer Philadelphia, PA; 2020.
ข้อระมัดระวัง การใช้ COC ในกลุ่มเสี่ยง
| Conditions | Recommendations |
| Hypertension | หลีกเลี่ยงการใช้และห้ามใช้ใน Uncontrolled HT |
| Venous thromboembolism | เพิ่มความเสี่ยง 3-5 เท่า
ห้ามใช้ในผู้ป่วยที่มีประวัติ DVT, PE หรือ ได้ Major surgery with prolonged immobilization หรือ known thrombogenic mutations เช่น factor V Leiden; prothrombin mutation; protein S, protein C, and antithrombin deficiencies |
| Migraine | ไม่ควรใช้ในผู้ป่วย Migraine without Aura ที่อายุ 35 ปีขึ้นไป
ห้ามใช้ใน Migraine with aura |
| Metabolic diseases | ไม่เพิ่ม lipid แต่เพิ่ม TG หาก TG > 750 mg/dl ห้ามใช้ COC
ควรติดตาม lipid profile เป็นระยะ |
| Diabetes | ไม่เพิ่มความเสี่ยง แต่ห้ามใช้ในกลุ่มผู้ป่วยที่มีภาวะแทรกซ้อน หรือผู้ป่วยที่เป็นมานานเกิน 20 ปี |
| SLE | เพิ่มความเสี่ยง SLE exacerbation
ห้ามใช้ใน SLE with vascular disease associated or antiphospholipid positive |
| Breast cancer | ห้ามใช้ COC
หลีกเลี่ยงในผู้ที่มีประวัติในครอบครัว |
| Liver disease | ห้ามใช้ใน Acute hepatitis, Decompensated cirrhosis, HCC |
| Epilepsy | ไม่เพิ่มการชัก แต่ยากันชักบางตัว จะลดประสิทธิภาพ COC
เช่น phenytoin, carbamazepine, barbiturates, primidone, topiramate, oxcarbazepine COC จะเพิ่ม clearance ของยา lamotrigine, valproic acid |
| HIV | สามารถใช้ได้ ไม่มี drug interaction with retroviral drugs |
| Smoking | ห้ามใช้คนที่อายุ 35 ขึ้นไปที่สูบบุหรี่
หลีกเลี่ยงในผู้ที่อายุน้อยกว่า 35 ปี แต่สูบบุหรี่มากกว่าวันละ 15มวน หากหยุดสูบบุหรี่ อย่างน้อย 1 ปี = nonsmoker |
ที่มา: Taylor HS, Fritz MA, Pal L, Seli E. Speroff’s clinical gynecologic and endocrinology and infertility. Ninth edition ed. Philadelphia, PA: Wolters Kluwer Philadelphia, PA; 2020.
ผลข้างเคียงที่พบได้บ่อยของ COC
- Breakthrough bleeding
ในช่วงแรก จะมีการปรับตัวของเยื่อบุโพรงมดลูก ทำให้มีเลือดออกกะปริบกะปรอยได้ แต่หากมีเลือดออกหลังจากใช้มานาน โดยเฉพาะในกลุ่ม extended หรือ continuous regimen มักเป็นผลของ endometrial decidualization จาก progestin อาจลองหยุดยาเพื่อปล่อยให้มี withdrawal bleeding หรือใช้ short course estrogen เช่น conjugated estrogen 1.25 mg หรือ estradiol 2 mg ต่อวัน ต่อเนื่องเป็นเวลา 7วัน
- Amenorrhea
ในกรณีที่ใช้ COC เป็นเวลานาน เป็นผลของ endometrial decidualizationจาก progestin
ส่วนผลข้างเคียงที่มักเข้าใจผิดโดยผู้ป่วย คือ น้ำหนักขึ้น สิวขึ้น ซึ่งไม่ได้เกี่ยวข้องกับการใช้ COC และ COC ยังช่วยรักษาสิวและภาวะขนดกได้ด้วย
เมื่อไหร่จะสามารถหยุด COC ได้
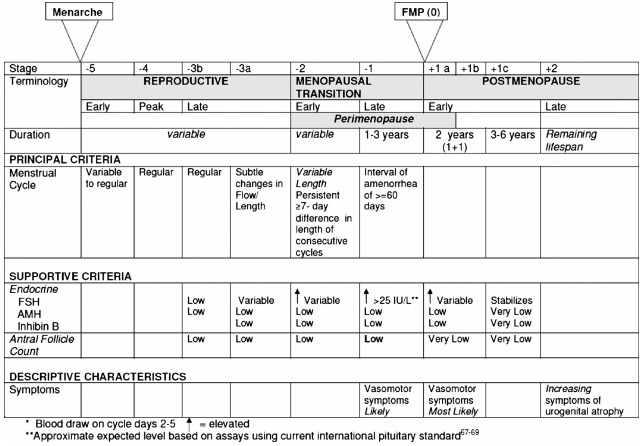
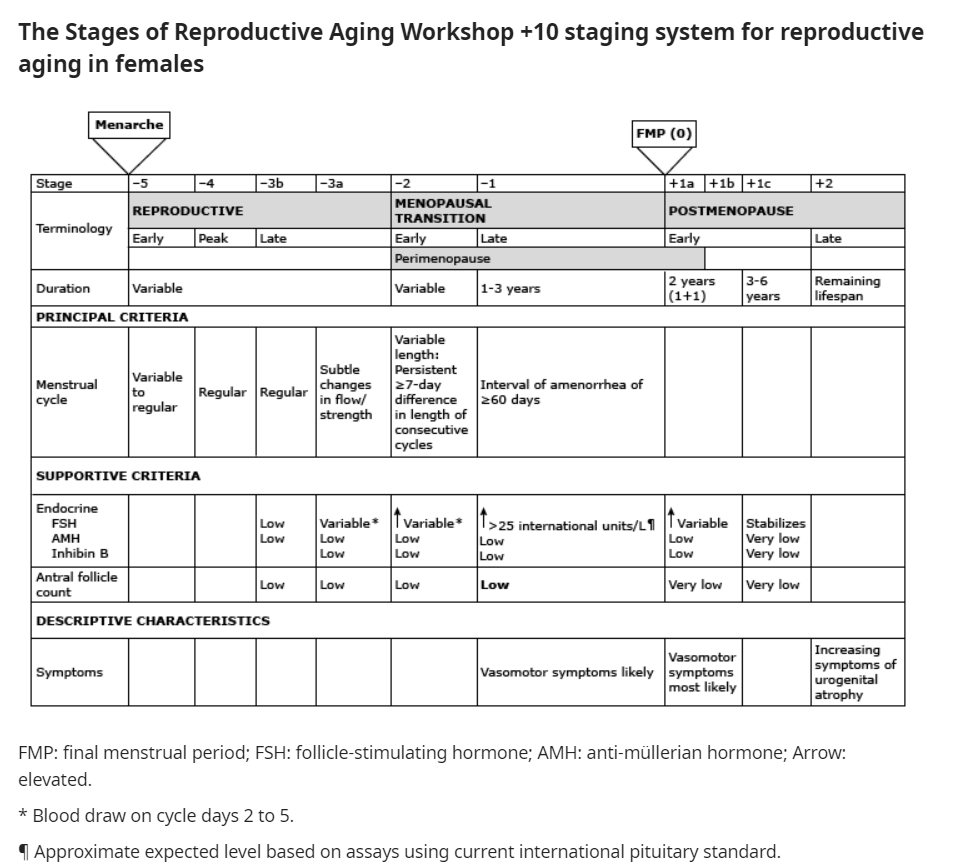
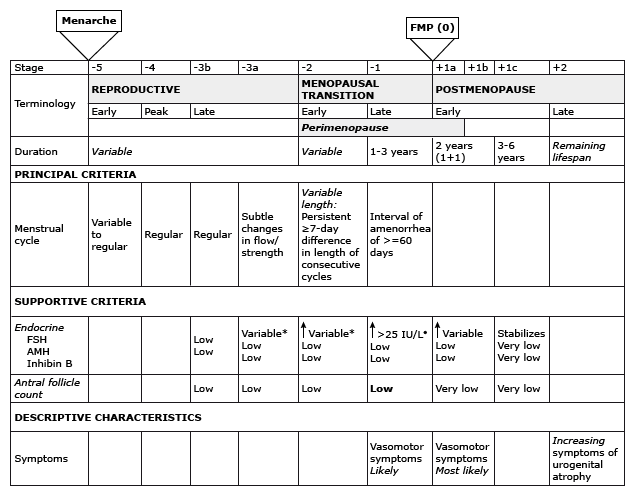
เมื่อเข้าสู่วัยทอง โดยหากอายุ 50ปี อาจลองหยุด COC หรือตรวจ FSH โดยจะตรวจ Day 6 หรือ 7 ของ pill free week หาก FSH > 20 IU/L ถือว่าผู้ป่วยเข้าสู่วัยทองแล้ว อาจพิจารณาใช้ฮอร์โมนตามความเหมาะสม ( menopausal hormone therapy)
เอกสารอ้างอิง
- Taylor HS, Fritz MA, Pal L, Seli E. Speroff’s clinical gynecologic and endocrinology and infertility. Ninth edition ed. Philadelphia, PA: Wolters Kluwer Philadelphia, PA; 2020.
- Cunningham F, Leveno KJ, Bloom SL, Dashe JS, Hoffman BL, Casey BM, Spong CY, et al. Contraception In : Williams Obstetrics. 26th ed. McGraw Hill; 2022. p. 671-673.
- Berek JS, Novak E. Berek & Novak’s gynecology. 16th ed. Philadelphia, PA: Lippincott Williams & Wilkins, 2020.
- P. Kathryn M. Curtis, M. Tara C. Jatlaoui, M. Naomi K. Tepper, P. Lauren B. Zapata, M. Leah G. Horton, M. Denise J. Jamieson, et al. U.S. Selected Practice Recommendations for Contraceptive Use, 2016. MMWR recommendations and reports Vol. 65 p. 22-30.
- Camelia Davtyan, MD, FACP, Clinical Professor of Medicine, UCLA Comprehensive Health Program. Four Generations of Progestins in Oral Contraceptives. Proceedings of UCLA Healthcare -VOLUME 16 (2012)-
- Hugh S. Taylor, Patricia Geraghty, The next generation of oral contraception: Advances in estrogens: OBG management
- เอกสารประกอบบรรยาย เรื่อง Today’s game changer: What’s Novel Native Estrogen E4 with DRSP?
- World Health Organization Medical Eligibility Criteria for Contraceptive Use, 5th edition 2015
- Mathur, Ruchi & Levin, Olga & Azziz, Ricardo. (2008). Use of ethinylestradiol/drospirenone combination in patients with the polycystic ovary syndrome. Therapeutics and clinical risk management. 4. 487-92.
- .Wikipedia contributors. Estrogen. Wikipedia, The Free Encyclopedia. November 9, 2023, 20:12 UTC. Available at: https://en.wikipedia.org/w/index.php?title=Estrogen&oldid=1184336587. Accessed November 11, 2023.